My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Actas Urológicas Españolas
Print version ISSN 0210-4806
Actas Urol Esp vol.34 n.6 Jun. 2010
REVISIÓN - DISFUNCIÓN MICCIONAL
Actualización del síndrome de atrapamiento del nervio pudendo: enfoque anatómico-quirúrgico, diagnóstico y terapéutico
Update in pudendal nerve entrapment syndrome: an approach anatomic-surgical, diagnostic and therapeutic
F. Itza Santosa, J. Salinasb, D. Zarzac, F. Gómez Sanchad y A. Allona Almagroe
aUnidad del Dolor, Clínica del Dolor, Madrid, España
bServicio de Urología, Hospital Clínico San Carlos, Madrid, España
cServicio de Neurofisiología, Hospital NISA Pardo de Aravaca, A Coruña, España
dServicio de Urología, Clínica del Rosario, Madrid, España
eServicio de Urología, Rúber Internacional, Madrid, España
Dirección para correspondencia
RESUMEN
Introducción: El síndrome de atrapamiento del nervio pudendo (SANP) es un gran desconocido y suele ser mal diagnosticado o confundido con otras patologías. Fue descrito por primera vez por Amarenco en 1987. La manifestación clínica clásica es la neuralgia del pudendo, un dolor neuropático del área genital.
Objetivos: Dar a conocer su existencia a los profesionales de la urología a través de una revisión sistemática de la bibliografía existente y sus posibilidades de diagnostico y tratamiento.
Material y método: Realizamos una búsqueda bibliográfica a través de la base de datos «Pubmed» utilizando los términos «Pudendal nerve», «Pudendal nerve entrapment síndrome», «Pelvic floor neuropathic pain», «Pelvic floor myofascial síndrome», «Pudendal nerve decompression». Asimismo, seleccionamos los trabajos en lengua inglesa, española y francesa, revisando también los artículos que dichos trabajos refieren.
Resultados: Se desarrollan los aspectos más destacados del síndrome: anatomía, etiología, fisiopatología, diagnostico clínico, ecodoppler de la arteria pudenda interna, estudios electrofisiológicos, criterios diagnósticos, terapéutica médica, tratamiento con fisioterapia y tratamiento quirúrgico.
Conclusión: Es una causa poco frecuente de dolor en el suelo pélvico y afecta en gran medida la calidad de vida de los pacientes. Hoy, disponemos de herramientas diagnósticas y terapéuticas que nos permiten tratar este síndrome invalidante con buenos resultados.
Palabras clave: Nervio pudendo (NP). Atrapamiento del nervio pudendo (SANP). Dolor neuropático del suelo pélvico. Síndrome miofascial de suelo pélvico. Descompresión del nervio pudendo.
ABSTRACT
Introduction: The syndrome of pudendal nerve entrapment (SANP) is widely unknown and often misdiagnosed or confused with other diseases. It was first described by Amarenco in 1987. The classic clinical manifestation is pudendal neuralgia, a neuropathic pain in the genital area.
Objectives: To make known its existence to the urology professionals through a systematic review of existing literature and its potential for diagnosis and treatment.
Materials and methods: We performed a literature search through the database "Pubmed" using the terms "Pudendal nerve", "Pudendal nerve entrapment syndrome", "Pelvic floor neuropathic pain", "Pelvic floor myofascial syndrome," "Pudendal nerve decompression". Also, selected works in English, Spanish and French, also reviewing the articles relate this work.
Results: We develop the highlights of the syndrome: anatomy, etiology, pathophysiology, clinical diagnosis, ecodoppler of internal pudendal artery, electrophysiological studies, diagnostic criteria, medical therapy, physical therapy treatments and surgery.
Conclusion: It is an uncommon cause of pain in the pelvic floor and greatly affects quality of life of patients. Today, we have diagnostic and therapeutic tools that allow us to treat this disabling syndrome with good results.
Key words: Pudendal nerve. Pudendal nerve entrapment syndrome. Pelvic floor neuropathic pain. Pelvic floor myofascial syndrome. Pudendal nerve decompression.
Introducción
El SANP fue descrito por el neurólogo Dr. Amarenco en al año 1987, cuando acudió a su consulta un ciclista que presentaba una neuralgia en el territorio del nervio pudendo. Utilizó una serie de pruebas electrofisiológicas para determinar la anomalía. En un principio lo denomino síndrome de la parálisis perineal del ciclista1.
Poco después, en el año 1991, el Dr. Shafik describió la técnica para la descompresión del nervio pudendo. La intervención es sencilla y ambulatoria, dura 5-10´ en manos expertas y no se presentan complicaciones salvo infecciones, pequeños hematomas y dolor postoperatorio2.
El principal motivo de consulta es el dolor en zona anal y perineal que aparece característicamente al sentarse, se alivia al levantarse y desaparece al acostarse. Tiene características neuropáticas como sensación de hipoestesia, entumecimiento, hormigueo perianal e incluso fuertes descargas eléctricas3.
En un estudio retrospectivo, Benson pone de manifiesto que estamos ante una entidad en la cual pocos profesionales piensan. Lo que supone un importante peregrinaje de los pacientes antes de ser correctamente diagnosticados e incluso podemos encontrarnos con casos en los que los hallazgos neurofisiológicos presentan valores dentro de la normalidad, aumentando la dificultad del problema4.
La similitud entre los síntomas del SANP y el síndrome de dolor miofascial del suelo pélvico van a ser una constante. Unas veces coexistirán y otras veces cada una de estas entidades llevará a la otra, los dolores característicos de ambas se solapan o destacan unos por encima de los otros haciendo difícil el diagnóstico y posterior tratamiento5.
En cuanto a datos epidemiológicos no se encuentran demasiados en la literatura.
El tiempo medio de diagnóstico es de 4 años, con un rango de 1-15 años. Los médicos visitados antes del diagnostico oscilan entre 10-30. El sexo, cómo no, es importante, afecta más a las féminas. Siete de cada 10 son mujeres.
Se desconoce la incidencia real de la enfermedad.
Objetivos: dar a conocer su existencia a los profesionales de la urología a través de una revisión sistemática de la bibliografía existente y sus posibilidades de diagnóstico y tratamiento.
Material y método: realizamos una búsqueda bibliográfica a través de la base de datos «Pubmed» utilizando los términos «Pudendal nerve», «Pudendal nerve entrapment síndrome», «Pelvic floor neuropathic pain», «Pelvic floor myofascial síndrome», «Pudendal nerve decompression». Asimismo, seleccionamos los trabajos en lengua inglesa, española y francesa, revisando también los artículos que dichos trabajos refieren. Eligiendo finalmente los trabajos que mejor definan el perfil del SANP, descartando los segundos y sucesivos manuscritos de un mismo autor o autores que no añaden relevancia al tema tratado.
Resultados: se desarrollan los aspectos más destacados del síndrome: anatomía, etiología, fisiopatología, diagnóstico clínico, ecodoppler de la arteria pudenda interna, estudios electrofisiológicos, criterios diagnósticos, terapéutica médica, tratamiento con fisioterapia y tratamiento quirúrgico.
Breve recuerdo anatómico-quirúrgico
El nervio pudendo (NP) (figura 1) atraviesa en su recorrido por unos intrincados desfiladeros, por esta circunstancia es fácil que se produzcan atrapamientos6.
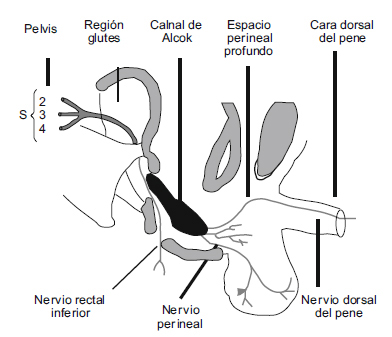
Figura 1. Trayecto del nervio pudendo.
La anatomía del NP ha sido profusamente descrita por importantes anatomistas, pero los datos electrofisiológicos nos muestran que los orígenes de las distintas ramas son bastante diferentes de lo que nos dice la anatomía convencional de acuerdo con las investigaciones anatomo-neurofisiológicas de Bisschop et al7.
La anatomía quirúrgica y sus implicaciones clínicas las informa Shafik en un revelador articulo realizado en 26 cadáveres, siguiendo las vías transperineales y transglúteas que luego veremos en el apartado del tratamiento quirúrgico8.
Robert et al desde la investigación anatómica en cadáveres suponen que los puntos críticos para la producción de un atrapamiento en el NP serian: la pinza entre los ligamentos sacrotuberoso y sacroespinoso, el canal de Alcock y el proceso falciforme9.
Nos encontramos ante una anatomía compleja, sin embargo necesaria para explicar la patología que su atrapamiento provoca. El NP se origina de los segmentos medulares sacros: S2, S3 y S4.
La anatomía de las terminaciones nerviosas es muy compleja y tiene muchas variantes. Sin embargo, el conocimiento de las áreas sensitivas inervadas por el NP, nos va a permitir relacionar el dolor con su posible origen pudendo.
El NP posee 3 ramas terminales: nervio rectal inferior, nervio perineal y nervio dorsal del clítoris/pene.
El NP inerva los músculos bulboespongioso, isquiocavernoso, esfínter anal externo, elevador del ano y el transverso perineal superficial y profundo.
La variabilidad en la inervación del músculo elevador del ano comunicada por Grigoriescu en un estudio en 17 cadáveres, nos debe ser poner en alerta tanto en su repercusión clínica como quirúrgica10.
Las 3 ramas terminales poseen en diferente proporción fibras motoras, sensitivas y autonómicas. Por ello, su atrapamiento puede causar signos y síntomas de expresión en cualquiera de los 3 ámbitos. En total se estima que el 30% es autonómico y el 70% es somático (50 sensitivo y 20% motor).
La inervación del nervio pudendo será6,11:
• Sensitiva: piel del perineo y genitales.
• Motora: esfínter anal externo, músculo elevador del ano, músculos bulbo e isquiocavernoso, esfínter uretral estriado y músculos perineales profundos y superficiales.
• Vegetativa: erección y sensación de necesidad urinaria.
Etiología y mecanismos de producción de la lesión
Bautrant et al analizaron las posibles causa que pueden originar el SANP; encontraron que el parto, caídas, golpes directos y cirugías pélvicas son fuentes frecuentes de esta condición nosológica12.
El ciclismo es motivo clásico descrito por Amarenco para sufrir un atrapamiento y casi podemos deducir otros deportes que lo pueden producir por el mismo mecanismo1; la disfunción eréctil temporal es un frecuente compañero de los ciclistas amateur13.
El estreñimiento crónico y el descenso perineal es una de las primeras causas aportadas como desencadenantes del SANP14.
Shafik hace mención en un interesante artículo sobre la importancia del acompañamiento del prolapso rectal a la incontinencia rectal para la producción del SANP. Se encuentra con valores electromiográficos y electroneurográficos anormales así como una hipoestesia perianal y lo trata con una descompresión, obteniendo resultados alentadores15.
El dolor vulvar asociado al estreñimiento crónico y a la incontinencia podría estar coligado a la compresión del NP de acuerdo con las investigaciones e Shafik en un estudio sobre la vulvodinia de origen idiopático. Tras la descompresión desapareció el dolor a 9 de 11 pacientes16.
La cirugía que involucra la disección de la vagina puede dar lugar a una neuropatía compresiva del NP según comunica Benson17.
La práctica de actividades deportivas durante la juventud puede llevar a un desarrollo inadecuado del proceso espinoso del isquion, que nos lleve a una posterior neuropatía compresiva al paso de los años18.
Con todo lo comentado, es fácilmente comprensible que los microtraumatismos repetidos en zona perineal pueden arrastrarnos a un SANP19.
Solo por atravesar un músculo de cualquier parte del cuerpo, un nervio de ese segmento puede quedar atrapado y producirse una lesión o disfunción nerviosa20. Lien et al describen como posible etiología el estiramiento del nervio durante el parto21.
La episiotomía puede estar en el origen de algunos casos de neuropatía del NP, por tanto, se estará muy vigilante a la hora de realizarla como demuestra un reporte de Soga et al en 15 cadáveres de hembras ancianas22.
Fisiopatología del atrapamiento nervioso
Se pueden identificar 3 factores principales en el desarrollo de una patología del sistema nervioso: vasculares, iónicos y mecánicos. Hay desacuerdo en cuál predomina, especialmente en los estadios tempranos de la compresión; hoy se piensa que predominan los factores vasculares23.
Las fibras nerviosas dependen para su funcionamiento normal de un suministro sanguíneo ininterrumpido. Existen una serie de gradientes de presión en el nervio y en los tejidos y líquidos que rodean el nervio. La importancia de este gradiente de presión en el desarrollo de una neuropatía por atrapamiento es un hecho24.
Sunderland detalló 3 etapas progresivas por aumento de las presiones en la zona atrapada: hipoxia, edema y fibrosis23. Con un estasis venoso, y la hipoxia, se debilita el metabolismo del nervio. La neuroisquemia es una fuente de dolor y otros síntomas como la parestesia. Con una hipoxia continua, la lesión del endotelio capilar provoca una extravasación y edema rico en proteínas.
La isquemia en el nervio se va a traducir en un bloqueo de la transmisión nerviosa. Tres pueden ser las causas:
• tracción excesiva,
• tracciones mínimas en zonas donde hay adherencias y la
• compresión mecánica.
El desarrollo de estas alteraciones sería el siguiente:
• obstrucción del retorno venoso que produce congestión o estasis venoso,
• lesión anóxica directa que incrementa la permeabilidad y
• edema en el tejido endoneural, con aumento de presión en el espacio intrafascicular, que incrementa el efecto de la compresión original.
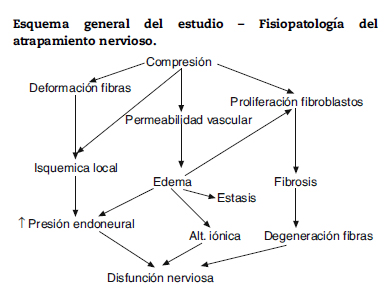
Si se incrementa la compresión o el edema persiste durante u período prolongado tiene lugar una proliferación de fibroblastos dentro del nervio y previamente un proceso de desmielinización. Si la causa persiste, se puede llegar a una fibrosis que origina segmentos nerviosos anóxicos, al estar impedida la circulación y el intercambio de nutrientes entre al plexo vascular y las fibras nerviosas. Cuando una porción de axón sufre isquemia, con una pequeña reducción del flujo sanguíneo del 30-50% de lo normal, la reducción de la fosforilación oxidativa y de la producción de ATP hace que disminuya la eficacia de la bomba de Na, el sistema de transporte axoplásmico y la integridad de la membrana celular y como consecuencia existe una disminución o pérdida en la transmisión a lo largo de la fibra nerviosa.
Los nutrientes son aportados por 2 mecanismos de transporte axoplasmático anterógrados y los catabólicos son recogidos por un mecanismo de transporte axoplasmático retrógrado. La interrupción en la síntesis o las alteraciones en el transporte en ambas direcciones parece ser la explicación del fenómeno de doble o múltiple compresión («double-crash») que significa que un nervio con un trastorno en la conducción en un nivel es más vulnerable a sufrir un trastorno en la conducción en una segunda o tercera localización: Inicialmente se observó que patologías neurales a nivel proximal predisponían el desarrollo de alteraciones dístales; ahora está claro que alteraciones dístales primarias, también favorecen las aparición de trastornos proximales24.
Diagnóstico clínico del atrapamiento
Historia
• Dolor pélvico al sentarse, pudiendo ser menos intenso por la mañana e incrementarse a lo largo del día. Los síntomas pueden disminuir de pie o tumbado. El dolor puede ser perineal, rectal o en el área del clítoris/pene; pudiendo ser unilateral o bilateral.
• Disfunción sexual. En mujeres y hombres, se manifiesta como dolor o disminución de la sensación en los genitales, perineo o recto (hipoestesia). El dolor puede ocurrir con o sin roce. Puede producir anorgasmia. En el hombre, la disfunción se presenta como dolor durante la erección, dificultad para mantenerla o dolor en la eyaculación, así como dolor posteyaculatorio.
• Dificultad al miccionar/defecar. Los pacientes pueden experimentar aumento de la frecuencia y urgencia urinaria. Disconfort postvaciado. Pueden sentir movimientos intestinales dolorosos. Dolor postdefecación. El estreñimiento es frecuente. Sensación de pelota de golf en el recto. También podemos encontrar con cierta frecuencia incontinencia urinaria y fecal en diferentes graduaciones.
• Por otro lado, puede simular una prostatitis crónica, una prostatodinia o una cistitis intersticial.
• Hoy sabemos que la causa más frecuente del viejo concepto de la prostatodinia es la disfunción del suelo pélvico de origen miofascial. Nos encontraríamos según Shafik ante un cuadro caracterizado por dolor perineal persistente acompañado de frecuencia, urgencia, disuria y alteraciones en el flujo urinario. En su artículo propone una descompresión del NP25.
Formas de presentación
Para simplificar y desde el punto de vista clínico y práctico podemos ver las diferentes formas de presentación.
• Solo dolor.
• Dolor con síntomas urinarios.
• Dolor con problemas a la defecación.
• Dolor con disfunción eréctil y eyaculatoria.
• Cualquiera de los anteriores juntos.
• Con alteraciones funcionales sin dolor.
Shafik reporta 2 series de pacientes sin dolor, pero con disfunción eréctil e hipoestesia o anestesia de pene, periné y escroto. Las latencias del nervio pudendo (PNTML) y del bulbocavernoso se encontraron aumentadas. La descompresión del NP se mostró eficaz para el tratamiento de la DE y la sintomatología acompañante. También se sugiere que la causa productora más probable en este caso seria el estreñimiento crónico que conduce a una subluxación del músculo elevador del ano y posteriormente a una compresión del NP en el canal de Alcock26.
Loeser, experto en dolor, comenta que las neuropatías por atrapamiento causan déficit neurológico focal, dolor local e irradiado y parestesias. Pueden presentarse los 3 componentes o no presentarse. Por esto mismo, podemos encontrar una falta de correlación entre los hallazgos clínicos y electrofisiológicos27.
Exploración física
• Normalmente nos vamos a encontrar con músculos doloridos, contracturados, acortados, con puntos gatillo, bandas tensas y con aumento de tono.
• Encontraremos dolorosa a la palpación la salida del conducto de Alcock. Beco et al utilizan una escala para definir si el dolor cuando palpamos a la salida del canal es significativo o no; para ellos es significativo si encuentran dolor moderado-severo con signo de Tinel (reproducción del dolor y parestesias por la presión del tronco nervioso)28.
• El test de la pinza rodada o skin rolling test es positivo a menudo, consiste en desplazar piel y celular subcutáneo desde el ano hacia el pubis, sobre el trayecto de las ramas del nervio pudendo. Al realizar esta maniobra, se reproducirá el dolor en la zona inervada.
• Encontraremos una disminución de la sensibilidad de la región perineal y anal28.
Ecodoppler de los vasos pelviperineales
Esta forma de diagnóstico es muy novedosa, incruenta, fácil de realizar y poco molesta para el paciente. Mollo et al publican un interesante estudio donde comparan la efectividad de del ecodoppler por vía endocavitaria y las tradicionales pruebas electromiográficas y electroneurográficas , criterios diagnósticos y resultados quirúrgicos29.
Estudios electrofisiológicos
Para todos aquellos que quieran entender claramente la neurofisiología del suelo pélvico pueden leer un estudio en español realizado por la Dra. Hernández-Hidalgo32.
Por lo demás, debemos entender que el estudio neurofisiológico del nervio pudendo abarca estructuras nerviosas de tipo motor, sensitivo y vegetativo, en este sentido se aplican técnicas, que intentan objetivar el estado de esta vía desde el punto de vista funcional, informando de la extensión y severidad del daño neuropático, para ello se aplican pruebas específicas para cada uno de los aspectos que deseamos examinar30:
• Estudio de la vía motora (latencia motora distal del nervio pudendo).
Es un test de conducción nerviosa motora. No valora la extensión de la lesión. Para medir el tiempo de conducción se ha desarrollado un electrodo específico desarrollado en el St. Mark's London Hospital (Drs. Kiff y Swash)31 de donde toma su nombre, mide el tiempo que tarda un estímulo eléctrico en desplazarse desde una porción distal del nervio pudendo hasta el esfínter anal externo. Consiste en un sistema, formado por un estimulador bipolar fijado en el extremo distal del dedo índice de un guante y 2 electrodos de registro situados a 3cm aproximadamente. Utilizando la vía rectal se dirige el estimulador hacia la espina isquiática, quedando situado el electrodo de registro sobre el esfínter anal externo. Con este método existe una latencia normal de 2 msg (figura 2).
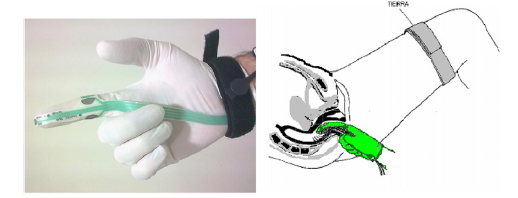
Figura 2. Guante electrodo St. Mark y su introducción anal.
• Estudio de la vía sensitiva somática.
○ Umbrales sensoriales: mediante estimulación eléctrica creciente sobre el nervio dorsal del pene o del clítoris, determinamos el umbral de percepción y el umbral del dolor, comparando los valores de estimulación del paciente, con sujetos normales, podemos determinar si estos se encuentran alterados.
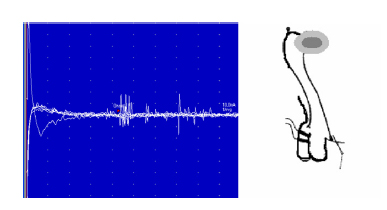
○ Potenciales evocados sensoriales del nervio pudendo: evalúa la vía sensitiva periférica y medular. Mide el tiempo que tarda un estímulo eléctrico en recorrer el nervio periférico, raíces posteriores de la medular cordones posteriores, hasta que recogemos la respuesta cerebral, a nivel parietal, este tiempo se sitúa en sujetos normales en torno a 40 msg (figura 3).
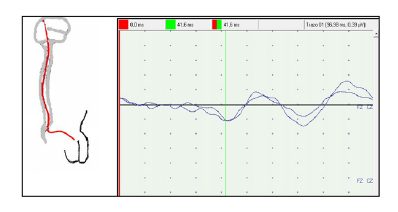
Figura 3. Potenciales evocados sensoriales del nervio pudendo.
• Estudio de la vía autonómica (Respuesta simpático-cutánea).
○ La evaluación de la eferente simpática se realiza mediante la estimulación de reflejos cutáneos, comparando la respuesta a nivel de la mano y los genitales, mediante la respuesta simpático-cutánea (RSC), ésta mide la actividad refleja sudomotora como un cambio transitorio en el potencial eléctrico de la piel (figura 4).
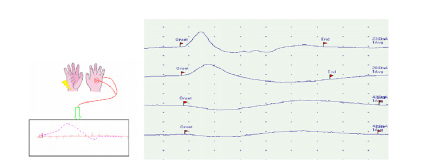
Figura 4. Respuesta Simpático-Cutánea.
• Electromiografía de músculos dependientes del nervio pudendo (bulbocavernoso, esfínter anal externo ).
Esta técnica mediante el análisis de la actividad del músculo en reposo y durante la actividad voluntaria, nos permite determinar si existe denervación sobre la estructura muscular explorada, estableciendo si este suceso se encuentra activo o si se ha cronificado. Mediante el estudio de distintos grupos musculares, podemos determinar la topografía de la lesión y así poder precisar el diagnóstico.
• Reflejos sacros
Mediante esta técnica medimos el tiempo que tarda en desencadenarse una contracción en el músculo bulbo cavernoso, tras estimular eléctricamente el nervio dorsal del pene o del clítoris. Con esta técnica evaluamos las fibras motoras y sensitivas del nervio pudendo, así como las raíces y segmentos medulares situados entre S2-S4. En sujetos normales este arco reflejo tarda entre 30 y 40min (figura 5).
Figura 5. Reflejo sacro. Todas las figuras, diagramas, fotos,
la tabla y el esquema son propios y autorizamos a la revista su publicación.
Bisschop describe a nivel investigativo clínico otros reflejos sacros que nos ayudaran a delimitar el lugar exacto del atrapamiento30.
Criterios diagnósticos
La descripción y determinación de criterios diagnósticos, para una entidad nosológica determinada, permite al clínico una mejor aproximación y abordaje del problema.
Clásicamente se ha utilizado este sistema para la mejor comprensión, enseñanza, diagnóstico y posible tratamiento de síndromes complejos. El SANP no es una excepción y aquí vamos a mostrar dichos criterios11. No obstante, estos criterios deberían ser validados y consensuados en congreso internacional ad hoc.
1. criterio mayor+2 criterios menores.
2. criterios mayores.
• Criterios mayores
1. Área dolorosa en terminación del nervio pudendo.
2. Reproducción del dolor al presionar el tronco del nervio pudendo (equivalente signo de Tinel).
3. Mejoría de al menos 12h tras inyección de lidocaína en lugares anatómicos concretos del recorrido del nervio pudendo.
• Criterios menores
1. Dolor neuropático.
2. Existencia de una posición dolorosa y/o antiálgica (empeora sentado, mejora tumbado).
3. Existencia de un factor etiológico: trauma, cirugía, parto, caída, deporte, etc.
4. Ausencia de otra causa de dolor área pélvica
○ Endometriosis.
○ Miomas uterinos.
○ Fibroma uterino.
Tratamiento
Lógicamente, como ante cualquier condición patológica se puede decir que el tratamiento ha de ser secuencial y se empezará por las medidas menos agresivas.
Tratamiento médico
• Tratamiento sintomático del dolor. Al ser el dolor neuropático el síntoma principal se han utilizado diversos preparados con diferentes grados de respuesta y efectividad. Se utilizan sobre todo los antidepresivos, entre ellos la amitriptilina, los anticomiciales de última generación como la gabapentina o la preglabalina. También se manejan los anestésicos locales tópicos como la lidocaína al 5% en gel33. La amitriptilina suele ser el fármaco de primera elección, ya que ha sido el más utilizado y el que ha obtenido mejores resultados. Durante mucho tiempo se han considerado de primera elección en el tratamiento del dolor neuropático. La mejoría del dolor parece que se debe a la inhibición de la recaptación de noradrenalina y serotonina en los terminales presinápticos, activando de esta forma los sistemas inhibitorios del dolor endógeno en el cerebro que moderan la transmisión del dolor a las células de la médula espinal.
Las benzodiazepinas son usadas en el tratamiento del dolor miofascial y en el SANP. La más útil es el clonazepan.
Se inicia con 0,25mg/d, se aumenta 0,25mg/semana, hasta un máximo de 5-20mg/d. El tratamiento no debe considerarse ineficaz hasta que pasen 4 semanas. En un estudio a 60 días de clonazepan en disfunción temporomandibularcervical (síndrome miofascial), la valoración a 30 días demostró una reducción significativa del dolor con el uso del anticonvulsivante en comparación con placebo (Harkins, 1991)34. De cualquier forma, la respuesta a este tipo de tratamiento conservador es de ligera o moderada mejoría. En una publicación reciente, encontramos que la gabapentina podría producir una mejoría significativa sola o en asociación con la amitriptilina para tratar este tipo de dolor35.
• Tratamiento con infiltraciones corticoideas. Las infiltraciones perineurales con corticoides y lidocaína/bupivacaína, en el espacio interligamentoso y en el canal de Alcock, bajo fluoroscopia o CT scan36, llevan a mejorar los síntomas de forma notable en muchos casos, relajan los esfínteres hipertónicos, suprimen síntomas vesicales y normalizan la disfunción sexual. Su duración va desde horas a semanas y en algunos pacientes hasta la curación. El alivio sintomático depende de la exactitud en la infiltración debido a una anatomía altamente variable. La mejoría sensitiva, motora o autonómica es variable. Se administran cada 4-6 semanas y con un máximo de 3 infiltraciones. Si no hay respuesta adecuada se valora la posibilidad de descompresión quirúrgica32.
• Tratamiento fisioterápico. Una contractura alargada en el tiempo con el consiguiente acortamiento muscular nos lleva a una lesión del paquete vasculonervioso. El grado de lesión y atrapamiento nervioso dependerá de varios factores ya comentados; si se realizan estiramientos musculares por fisioterapeutas especializados en suelo pélvico se pueden obtener resultados sorprendentes. La mejoría no se centrara solo en el dolor, sino que los pacientes encontraran alivio en otros síntomas como frecuencia urinaria, disfunción eréctil, calidad de vida, libido, sensación de pelota de golf en el recto, etc 37.
• Tratamiento con aguja seca o infiltraciones locales de lidocaína. Para la desactivación de los puntos gatillo de los músculos afectados del suelo pélvico, cuando nos encontramos ante una disfunción del sistema nervioso periférico, se pueden utilizar estas técnicas, que nos permitirán la liberación de los puntos gatillo y la disminución de la sintomatología. Al parecer, uno de los fundamentos de estas acciones esta en la desensibilización del sistema nervioso periférico y central38.
Tratamiento quirúrgico
Tiene por objetivo lograr la descompresión del nervio pudendo. Entre los hallazgos que podemos encontrar en la cirugía destacan39:
• Ligamentos hipertróficos a menudo con bordes agudos y prominencias.
• Ligamentos fusionados (funicular). Bandas ligamentosas que atraviesan el nervio.
• Adherencias. Unión y compresión contra el ligamento sacrotuberoso.
• Ramificación proximal: rama rectal inferior que penetra el ligamento sacroespinal.
• Tronco nervioso principal atraviesa el músculo coccígeo. Espina isquiática elongada.
El atrapamiento del NP habitualmente ocurre32:
• Entre el ligamento sacroespinoso y el ligamento sacrotuberoso (pinza interligamentosa, 70% de los casos).
• En el canal de Alcock, 20%.
• En el diafragma urogenital (nervio dorsal).
• En 20% de los casos existe compromiso simultáneo interligamentoso y canal de Alcock.
Las diferentes vías de abordaje quirúrgico pueden ser (tabla 1): la trasperineal, transglútea y transisquiorectal.
• Técnica transperineal.
Descrita por Shafik en1991, es una técnica sencilla en su realización, se comienza con una pequeña incisión paraanal, se entra en la fosa isquiorectal y se sigue el trayecto del nervio rectal inferior hasta la entrada del canal de Alcock, al que tenemos buen acceso, donde con una tijera haremos un pequeño corte en la fascia del músculo obturador interno la cual despegaremos con el dedo índice, liberando todo el trayecto comprometido del nervio pudendo. Sí así lo precisamos podemos proceder a la apertura del espacio interligamentario. El procedimiento quirúrgico es de corta duración (5-10´ por cada lado). No se secciona ningún ligamento.
Se respeta el elevador del ano y se efectúa de forma ambulatoria. Es segura y sin complicaciones significativas. Como principal inconveniente encontramos su dificultad de ser enseñada y aprendida dado que se realiza a ciegas. En algunos casos si persiste el dolor, no hay mejoría y las latencias dístales permanecen elevadas por esta misma técnica operatoria se procede a liberar la pinza entre los ligamentos sacroespinoso y sacrotuberoso, con resultado muy favorables40.
• Técnica transglútea.
Descrita por Robert, es una técnica más cruenta que la anterior y precisa hospitalización. Se práctica una incisión transglútea de unos 10cm. Siendo objetivo fundamental la sección de la pinza producida por los ligamentos sacrotuberoso y sacroespinoso al NP. Este mismo profesional después de 400 intervenciones realizadas asegura no haber tenido complicaciones mayores; luego de un seguimiento de cuatro años obtiene mejorías significativas, aunque reconoce que otros tratamientos rehabilitadores ulteriores, como la fisioterapia, podrían ser necesarios.
Requiere 2 días de hospitalización. La vuelta al trabajo puede requerir entre 10 días a 3 meses. La completa curación puede ocurrir, pero se pueden dar complicaciones como la retención urinaria en el 5% de los pacientes, requiriendo sondaje posterior. La neuropraxia puede necesitar varias semanas para su completa resolución41.
• Técnica transvaginal o transisquiorectal.
Descrita por Bautrant, se realiza por vía transvaginal en las mujeres, y de ahí toma su nombre, pero en los hombres se ejecuta por vía transisquiorectal, denominándose técnica transisquiorectal32.
Se accede a los 3 segmentos del NP a través de la fosa isquiorectal, con la paciente en posición litotómica y a través de la vagina por la cual se alcanza este espacio avascular. Su disección permite exponer la cara medial de cada lado de la pelvis después de rechazar el recto y el elevador del ano. El propósito es la descompresión de los lugares comprometidos, por lo tanto no hay neurolisis ni disección cercana al nervio.
Durante el postoperatorio en un 38% de los casos se produce un dolor intenso en la región glútea, diferente al del ingreso, que puede atribuirse a la sección del ligamento sacroespinoso y la abundancia de la red nerviosa de algunos de ellos. Disminuye progresivamente el primer mes y termina desapareciendo por completo.
La descompresión comienza siempre por abrir el canal bajo el músculo piriforme, en el borde inferior del ligamento sacroespinoso. Una vez que se alcanza el tejido adiposo perineural, se procede a explorar la zona de la compresión. En el 90%, la sección del ligamento sacroespinoso se lleva a cabo para liberar la pinza.
La operación puede proseguir hacia caudal, si es necesario, cortando las fibras del proceso falciforme del ligamento sacrotuberoso hasta penetrar en el canal de Alcock. En esta etapa, se explora digitalmente todo el canal completando la descompresión y asegurándose que todo el canal pudendo está libre.
La formación de hematomas se previene dejando en forma rutinaria con la colocación de un drenaje en la región isquiorectal por 48h.
Hospitalización de 3 o 4 días. Luego quinesioterapia antiálgica y de reeducación perineal. La regeneración nerviosa puede llevar de 6-18 meses.
Las complicaciones descritas en la cirugía de descompresión son menores:
• Infecciosas: ITU (7%), abscesos (2,5%) con evacuación y drenaje.
• Hemorrágicas: 2%, injuria a rama de la arteria pudenda y falso aneurisma secundario en rama de la arteria glútea superior.
La teórica desestabilización y sobrecarga de la articulación sacroilíaca como complicación de la sección de los ligamentos no han sido demostradas hasta ahora en las publicaciones conocidas32.
Series publicadas
Las primeras series publicadas de descompresión quirúrgica comprenden grupos reducidos de pacientes; en la medida que se ha reconocido el diagnóstico, el número de pacientes sometidos a descompresión quirúrgica ha ido progresivamente en aumento y autores como Robert41 han reportado 400 cirugías desde 1989, Bautrant32 reporta 104 descompresiones, Beco28 comunica 74, Mouchel42 192 y Popeney39 58. Podemos observar que la inmensa mayoría de las intervenciones se han realizado a este lado del atlántico, excepto la realizada por el grupo de Popeney.
Persistencia del dolor después de la descompresión
La persistencia del dolor puede tener una serie de causas, Weiss43 destaca:
• Puntos gatillo miofasciales en suelo pélvico que incluso estaban presentes antes de la cirugía y se agravan con el trauma quirúrgico.
• Sensibilidad del tejido celular subcutáneo, que es un importante perpetuador del dolor posquirúrgico.
• Disfunción de la articulación sacroilíaca por la sección de los ligamentos sacrotuberoso y sacroespinoso. Se puede producir una disfunción miofascial generadora de puntos gatillo.
• Patología intrínseca de las ramas del NP. Es la causa algógena más frecuente y la más resistente al tratamiento.
• Otros factores como el estrés, el insomnio, las hormonas y la dieta.
• La sensibilización central.
Conclusión
Se deduce en esta revisión que los atrapamientos del NP son más frecuentes de lo que pensamos y diagnosticados, aunque la frecuencia real se desconoce.
Las especialidades involucradas (urología, ginecología, proctología, neurología, algólogos ) deben hacer un esfuerzo para la difusión de este síndrome tan invalidante y tan poco conocido.
No debemos pasar por alto la importante relación entre el SANP y el síndrome de dolor miofascial, pues muchas veces no sabremos quién llevo a quién.
Los resultados de los tratamientos tanto conservadores como quirúrgicos son más que aceptables, pero siempre tendremos presente comenzar por el menos invasivo.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Amarenco G., Lanoe Y., Perrigot M., Goudal H. A new canal syndrome: compression of the pudendal nerve in alcock's canal or perinal paralysis of cyclists. Presse Med. 1987; 16:399. [ Links ]
2. Shafik A. Pudendal canal syndrome: description of a new syndrome and its treatment. Report of seven cases. Coloproctology. 1991; 13:102-9. [ Links ]
3. Robert, et al. Neuropathic pain: a tunnel syndrome. Surg-Radiol Anat. 1998; 20:93. [ Links ]
4. Benson J.T., Griffis K. Pudendal neuralgia, a severe pain syndrome. Am J Obstet Gynecol. 2005; 192:1663-8. [ Links ]
5. Prendergast S.A., Weiss J.M. Physical therapy and pudendal nerve entrapment. Advance. 2004; 15:47. [ Links ]
6. Rouviere. Anatomia Humana. vol. 2, tronco. Editorial Masson; 2005. [ Links ]
7. Spinosa J.P., De bisschop E., Laurencon J., Kuhn G., Dubuisson J.B., Riederer B.M. Sacral staged reflexes to localize the pudendal compression: an anatomical validation of the concept. Rev Med Suisse. 2006; 2:. 2416-8-2420-1. [ Links ]
8. Shafik A., Doss S.H. Pudendal canal: surgical anatomy and clinical implications. Amer Surg. 1999; 65:176-80. [ Links ]
9. Robert R., Brunet C., Faure A., Lehur P.A., Labat J.J., Bensignor M., et al. Surgery of pudendal nerve in various types of perineal pain: course and results. Chirurgie. 1993-94; 119:535-9. [ Links ]
10. Grigorescu BA, Lazarou G, Olson TR, Downie SA, Powers K, Greston WM, et al. Innervation of the levator ani muscles: description of the nerve branches to the pubococcygeus, iliococcygeus, and puborectalis muscles.int urogynecol. J Pelvic Floor Dysfunct. 2007. [ Links ]
11. Sobotta. Atlas de Anatomía Humana. vol. 2. Putz - Pabst. 2006. Editorial Panamericana. [ Links ]
12. Bautrant E., De Bisschop E., Vaini-elies V., Massonnat J., Aleman I., Buntinx J., et al. La prise en charge moderne des névralgies pudendales. A partir d'une série de 212 patientes et 104 interventions de décompression. J Gynecol Obstet Biol Reprod (Paris). 2003; 32:705-12. [ Links ]
13. Andersen K.V., Bovim G. Impotence and nerve entrapment in long distance amateur cyclists. Acta Neurol Scand. 1997; 95:233-40. [ Links ]
14. Kiff E.S., Barnes P.R., Swash M. Evidence of pudendal neuropathy in patients with perineal descent and chronic straining at stool. Gut. 1984; 25:1279-82. [ Links ]
15. Shafik A. Pudendal canal descompression for the treatment of fecal incontinence in complete rectal prolapse. Am Surg. 1996; 62:339-43. [ Links ]
16. Shafik A. Pudendal canal syndrome as a cause of vulvodynia and its treatment by pudendal nerve decompression. Eur J Obstet Gynecol Reprod. 1998; 80:215-20. [ Links ]
17. Benson J.T., Mcclellan E. The effect of vaginal dissection on the pudendal nerve. Obstet Gynecol. 1993; 82:387-9. [ Links ]
18. Antolak S.J.J., Hough D.M., Pawlina W., Spinner R.J. Anatomical basis of chronic pelvic pain syndrome: the ischial spine and pudendal nerve entrapment. Med Hypotheses. 2002; 59:349-53. [ Links ]
19. Pisani R., Stubinski R., Datti R. Entrapment neuropathy of the internal pudendal nerve. Report of two cases. Scand J Urol Nephrol. 1997; 31:407-10. [ Links ]
20. Pessis E., Drapé J.L., Guérini H., Bach F., Feydy A., Chevrot A. Nerve and vascular entrapment in athletes. J Radiol. 2007; 88(1 pt 2):156-71. [ Links ]
21. Lien K.C., Morgan D.M., Delancey J.O., Ashton-Miller J.A. Pudendal nerve stretch during vaginal birth: a 3-d computer simulation. Am J Obstet Gynecol. 2005; 192:1669-76. [ Links ]
22. Soga H., Nagata I., Murakami G., Yajima T., Takenaka A., Fujisawa M., et al. A histotopographic study of the perineal body in elderly women: the surgical applicability of novel histological findings. Int Urogynecol J Pelvic Floor Dysfunct. 2007. [ Links ]
23. Sunderland S. Nerves and Injuries. Ed. Churchill Livingstone; 1976. [ Links ]
24. Butler D.S. Movilización del sistema nervioso. Ed. Paidotribo; 2002. [ Links ]
25. Shafik A. Pudendal canal syndrome. A new etiological factor in prostatodynia and its treatment by pudendal canal decompression. Pain Digest. 1998; 8:32-6. [ Links ]
26. Shafik A. Pudendal canal decompression in the treatment of erectile dysfunction. Arch Androl. 1994; 32:141-9. [ Links ]
27. Loeser J. Terapeutica del dolor. Bonica. vol. II. Ed. Mcgraw-Hill; 2003. p. 1858. [ Links ]
28. Beco J., Climov D., Bex M. Pudendal nerve decompression in perineology: a case series. Bmc Surg. 2004; 30:15. [ Links ]
29. Mollo M., Bautrant E., Rossi-Seignert A.-K., Collet S., Boyer R., Thiers-Bautrant D. Evaluation of diagnostic accuracy of colour duplex scanning, compared to electromyography, diagnostic score and surgical outcomes, in pudendal neuralgia by entrapment: a prospective study on 96 patients. Pain. 2009; 142:159-63. [ Links ]
30. Bisschop E, Bautrant E. EMG: which one and why? Considerations regarding pudendal nerve terminal motor latencies (pntml). 31 Meeting Annual of the International Urogynecological Association (IUGA 2006). Encontrado en internet: www.perineology.com/files/de-bisschop-athens2006.pdf. [ Links ]
31. Kiff E., Swash M. Slowed conduction in the pudendal nerves in idiopathic (neurogenic) faecal incontinence. Br J Surg. 1984; 71:614-6. [ Links ]
32. González-Hidalgo M. Exploración neurofisiológica del suelo de la pelvis. Rev Neurol. 1998; 26:432-8. [ Links ]
33. Wallace J.M. Update on pharmacotherapy guidelines for treatment of neuropathic pain. Curr Pain Headache Rep. 2007; 11:208-14. [ Links ]
34. Harkins S., Linford J., Cohen J., Kramer T., Cueva L. Administration of clonazepam in the treatment of tmd and associated myofascial pain: a double-blind pilot study. J Craniomandib Disord. 1991; 5:179-86. [ Links ]
35. Sator-katzenschlager S.M., Scharbert G., Kress H.G., Frickey N., Ellend A., Gleiss A., et al. Chronic pelvic pain treated with gabapentin and amitriptyline: a randomized controlled pilot study. Wien klin wochenschr. 2005; 117:761-8. [ Links ]
36. Kovacs P., Gruber H., Piegger J., Bodner G. New, simple, ultrasound-guided infiltration of the pudendal nerve: ultrasonographic technique. Dis Colon Rectum. 2001; 44:1381-5. [ Links ]
37. Anderson R.U., Wise D., Sawyer T., Chan Ca. Sexual dysfunction in men with chronic prostatitis/chronic pelvic pain syndrome: improvement after trigger point release and paradoxical relaxation training. J Urol. 2006; 176(4 pt 1):. 1534-8; discussion 1538-9. [ Links ]
38. Hsieh Y.L., Kao M.J., Kuan T.S., Chen S.M., Chen J.T., Hong C.Z. Dry needling to a key myofascial trigger point may reduce the irritability of satellite mtrps. Am J Phys Med Rehabil. 2007; 86:397-403. [ Links ]
39. Popeney C., Ansell V., Renney K. Pudendal entrapment as an etiology of chronic perineal pain: diagnosis and treatment. Neurourol Urodyn. 2007. [ Links ]
40. Shafik A. Pudendal canal syndrome: description of a new syndrome and its treatment. Report of seven cases. Coloproctology. 1991; 13:102-9. [ Links ]
41. Robert R., Labat J.J., Bensignor M., Glemain P., Deschamps C., Raoul S., et al. Decompression and transposition of the pudendal nerve in pudendal neuralgia: a randomized controlled trial and long-term evaluation. Eur Urol. 2005; 47:403-8. [ Links ]
42. Mouchel J, Mouchel T, Zaka P.Trans-perineal pudendal nerve decompression. 31 Meeting Annual of the International Urogynecological Association (IUGA 2006). Disponible en: www.perineology.com/files/mouchel-athens2006.pdf. [ Links ]
43. Weiss J. Treatment options for persistent pain following pudendal nerve decompression surgery. 31 Meeting annual of the international urogynecological association (iuga 2006). Disponible en: www.perineology.com/files/weiss-athens2006.pdf. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico:fitza@arrakis.es
(F. Itza Santos)
Recibido 21 Febrero 2010
Aceptado 11 Marzo 2010