My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Nutrición Hospitalaria
On-line version ISSN 1699-5198Print version ISSN 0212-1611
Nutr. Hosp. vol.19 n.2 Madrid Mar./Apr. 2004
Original
La práctica de la nutrición artificial domiciliaria en Europa
J. M. Moreno Villares
Pediatra. Médico adjunto de la Unidad de Nutrición Clínica. Hospital 12 de Octubre. Madrid.
| Resumen La nutrición artificial fuera del ámbito hospitalario es una práctica muy extendida pero realizada con gran variabilidad. La tasa de prevalencia de nutrición parenteral domiciliaria (NPD) varía desde los 120 pacientes por millón de habitantes en Estados Unidos hasta los 2-4 en Europa o los 1,5 en España. La indicación más frecuente es el síndrome de intestino corto y el cáncer activo. El grupo mayor de pacientes tienen entre 40 y 60 años; sólo el 10 a 20% son niños. Casi 2/3 de los pacientes infunden la nutrición parenteral a través de un catéter tunelizado. La tasa de incidencia complicaciones en España es superior a la del registro europeo o el norteamericano. Las más frecuentes son las complicaciones infecciosas. En el momento actual, el pronóstico y la supervivencia a medio y largo plazo son superiores con la NPD que con el trasplante intestinal. Este debe reservarse para aquellos pacientes que presentan complicaciones graves con la NPD. La estandarización de los cuidados y el desarrollo de buenos programas de educación pueden contribuir a mejorar los resultados. Aunque la nutrición enteral domiciliaria se desarrolló con posterioridad a la NPD su crecimiento ha sido mucho mayor. Es difícil conocer la incidencia exacta, que oscila entre 460 (Estados Unidos) y 40 (España) pacientes/millón de habitantes y año. Las enfermedades neurológicas y el cáncer son las indicaciones más frecuentes. Mientras que en otros países europeos la principal vía de acceso es una gastrostomía, en España sólo ocurre en el 25%. La tasa de complicaciones es alrededor de 0,16 complicaciones por paciente y año. El pronóstico depende fundamentalmente de la enfermedad de base. Su uso creciente en pacientes con progresivo deterioro neurológico plantea interrogantes éticos. La legislación y el sistema de organización varía entre países. En España sólo la nutrición enteral domiciliaria está regulada por ley. (Nutr Hosp 2004, 19:59-67) Palabras clave: Nutrición parenteral. Nutrición enteral. Atención domiciliaria. Legislación. Epidemiología. | THE PRACTICE OF HOME ARTIFICIAL NUTRITION IN EUROPE Abstract Artificial nutrition outside hospital settings is a widespread practice but with great variability. The prevalence of home parenteral nutrition (HPN) ranges from 120 patients per million inhabitants in the United States to 2-4 in Europe or 1.5 in Spain. The most frequent indication is the short intestine syndrome and active cancer. The largest group of patients is aged between 40 and 60, with only 10%-20% of children. Almost 2/3 of patients apply parenteral nutrition through a tunnelled catheter. In Spain, the incidence of complications is higher than that registered in Europe or North America. The most frequent are infection-related complication. At the present time, prognosis and survival in the medium and long term are higher with HPN than with intestinal transplant. This must be reserved for those patients presenting severe complications with HPN. The standardization of care and the development of good education programmes may contribute to an improvement in the results. Although home enteral nutrition was developed after HPN, it has grown much faster. It is difficult to determine the real incidence, which varies from 460 (United States) and 40 (Spain) patients per million inhabitants and year. Neurological diseases and cancer are the most frequent indications. Whereas in other countries of Europe, the main access route is gastrostomy, this only occurs in 25% of cases in Spain. The rate of complications is around 0.16 complications per patient and year. The prognosis basically depends on the underlying disease. Its increasing use in patients with progressive neurological deterioration raises ethical questions. The legislation and the organizational system varies from one country to another. In Spain, only home enteral nutrition is regulated by law. (Nutr Hosp 2004, 19:59-67) Key words: Parenteral nutrition. Enteral nutrition. Home care. Legislation. Epidemiology. |
Correspondencia: José Manuel Moreno Villares.
Unidad de Nutrición Clínica. - Hospital 12 de Octubre.
Carretera de Andalucía, Km. 5,400. - 28041 Madrid.
Tel. y Fax: 91 390 83 18. e-mail: jmoreno.hdoc@salud.madrid.org
Recibido: 3-XI-2003.
Aceptado: 20-I-2004.
El soporte nutricional en el domicilio ha permitido el tratamiento con éxito en pacientes con enfermedades que, de otra manera, hubieran precisado ingresos prolongados o repetidos para la corrección de las alteraciones nutricionales. Se engloba dentro del desarrollo de los programas de hospitalización a domicilio que están estrechamente ligados a la humanización de la enfermedad, al desarrollo de las nuevas tecnologías y al mejor aprovechamiento de todos los recursos de los distintos niveles asistenciales1. Los avances tecnológicos en catéteres venosos centrales, sondas de nutrición enteral, formulaciones específicas y bombas de infusión en los últimos treinta años han permitido este desarrollo. Estos avances acompañados de programas de seguimiento adecuados y de guías de cuidados actualizadas han hecho posible que la nutrición artificial a domicilio (NAD) constituya una vía para la promoción de la salud y el bienestar de aquellos que precisan tratamiento nutricional altamente cualificado2.
Aunque existen protocolos de actuación o guías elaboradas a nivel local o nacional es difícil encontrar recomendaciones universalmente aceptadas. En las guías de práctica clínica publicadas por la Sociedad Americana de Nutrición Parenteral y Enteral en 2002 sólo encontramos las siguientes recomendaciones para la NAD: 1) debe reservarse para aquellos pacientes que no pueden cubrir sus necesidades con la ingesta oral y que no precisan hospitalización; 2) siempre que sea posible es preferible la nutrición enteral (NE), y 3) La nutrición parenteral domiciliaria (NPD) sólo estará indicada cuando el tracto gastrointestinal no funciona y el soporte enteral no es suficiente. Estas recomendaciones las categoriza como basadas en una evidencia científica suficiente (estudios bien diseñados sin aleatorización)3. Por su parte, la Asociación Norteamericana de Gastroenterología en su actualización del año 2001 sobre nutrición parenteral (NP) realiza las siguientes afirmaciones sobre la NPD: 1) está indicada en pacientes con fracaso intestinal prolongado que impide una absorción adecuada de los nutrientes, y 2) no deberá proporcionarse a pacientes con una esperanza de vida limitada (inferior a 3 meses). Señala además que estas conclusiones están basadas en datos que no proceden de estudios prospectivos, controlados y aleatorizados4,5. Es, por tanto, una práctica extendida pero realizada con una gran variabilidad. Desarrollaremos a continuación la descripción del uso de la NAD en Europa en comparación con la práctica en España.
Nutrición parenteral domiciliaria
1. Datos históricos y epidemiológicos
La NPD se utilizó por primera vez en 1967 en Estados Unidos de Norteamérica 6. Los primeros pacientes europeos datan de principios de los años 1970 en Dinamarca; mientras que hay que esperar hasta 1984 para encontrar los primeros casos en España.
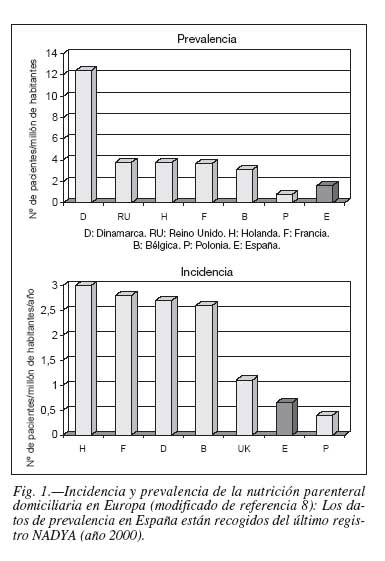
Aunque ninguno de los registros nacionales recoge todos los casos con NPD, la tasa de prevalencia en Estados Unidos para el período 1989-1992 fue de 120 pacientes por millón de habitantes7, mientras que las cifras en Europa oscilan entre 0,3 y 12 pacientes por millón de habitantes8 (fig. 1). En España las tasas de prevalencia del último registro publicado son de 1,6 casos por millón de habitantes9. Estas enormes diferencias a uno y otro lado del Atlántico tienen varias posibles explicaciones: diferente prevalencia de enfermedad de Crohn, uso más extendido de la NPD en el paciente con cáncer activo, diferente sistema de financiación, falta de equipos experimentados en la técnica, escasa presión para acortar las estancias medias, asistencia domiciliaria especializada deficiente y escasa coordinación entre la atención primaria y el hospital. Las diferencias entre países europeos tienen una explicación más difícil, pues la financiación es a través del Sistema público de salud en todos los casos y la provisión tanto de las bolsas de NP como del resto de servicios es similar.
2. Indicaciones y aspectos técnicos
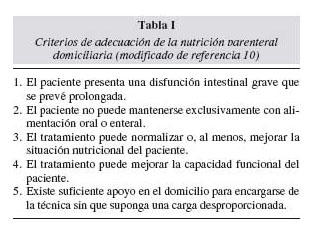
La NPD está indicada en pacientes con fracaso intestinal transitorio o permanente que presentan déficits nutricionales y/o alteraciones hidroelectrolíticas que no pueden corregirse por vía enteral. Sin embargo, sólo podemos considerar que la NPD es un tratamiento adecuado cuando exista una posibilidad razonable de que la técnica añada calidad y duración a la vida del paciente10 (tabla I).
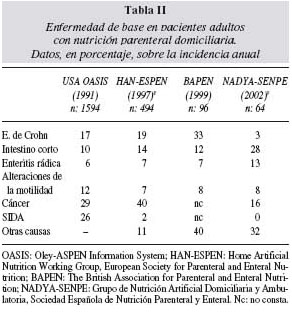
Las indicaciones más frecuentes de NPD son el síndrome de intestino corto y otras causas que produzcan una disminución efectiva de la superficie de absorción: fístulas entéricas, enfermedad inflamatoria intestinal, enteritis por radiación y los trastornos graves de la motilidad. Como puede verse en la tabla II, es más controvertido y, por tanto, existe más variabilidad en la práctica clínica en el uso de la NPD en pacientes con cáncer activo (sobre todo en situaciones de obstrucción intestinal no solucionables con cirugía), o previamente en pacientes con SIDA.
Refiriéndonos exclusivamente a los datos europeos, la NPD en adultos es más frecuente es el grupo de edad entre 41 y 60 años (44%) seguido de los edad comprendida entre 16 y 40 años (28%), Sólo el 10% de los pacientes es mayor de 70 años. Existe un discreto predominio de mujeres. Entre el 10 y el 20% de los pacientes con NPD son niños. La causa principal para recibir NPD en este grupo de edad es el síndrome de intestino corto, bien secundario a malformaciones congénitas o a enterocolitis necrosante.
Alrededor de 2/3 de los pacientes se infunden la nutrición parenteral a través de un catéter tunelizado tipo Broviac® o Hickman®; seguido de los reservorios subcutáneos (30%), la mayoría en pacientes oncológicos. Los catéteres venosos centrales transitorios son excepcionales. En el reciente estudio multicéntrico de Bozzetti y cols.11, de 447 pacientes que iniciaron la NPD entre 1995 y 2001, el 90,6% usaron un catéter tunelizado.
La forma de administración es cíclica nocturna en la mayoría de casos (93%). La mitad de los pacientes con NPD siguen una dieta libre, y otra cuarta parte una dieta restringida. Sólo en algo menos del 25% la NPD constituye la única fuente de alimentación. Los datos para los pacientes españoles son muy similares.
El sistema de financiación difiere enormemente entre Estados Unidos y Europa. La cobertura financiera en Estados Unidos procede de compañías de seguros, libres o concertados, o de programas gubernamentales (Medicaid y Medicare). En Europa la financiación corre a cargo de los Sistemas Nacionales de Salud12. La provisión de las soluciones de nutrición parenteral y del resto del material es, sin embargo, muy variable. Puede depender de la farmacia hospitalaria, de farmacias privadas o a través de empresas de atención domiciliaria (Home Care companies) en función de la regulación de cada país. En España mayoritariamente la elaboración de la NPD se realiza en la Farmacia Hospitalaria; existe un escaso desarrollo de las empresas de atención domiciliaria. Un aspecto importante se refiere al hecho de que esta posibilidad de tratamiento no está contemplada actualmente dentro de las prestaciones del sistema público de salud y permanece en el ámbito de las prestaciones hospitalarias. Es preciso, pues, que como ha ocurrido con la nutrición enteral domiciliaria (NED) se proceda al desarrollo de la legislación pertinente.
3. Complicaciones
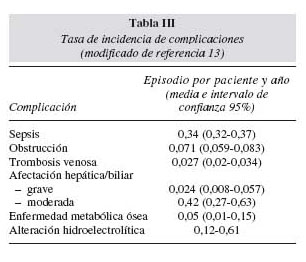
La incidencia de complicaciones es inversamente proporcional a la experiencia del equipo que atiende a estos pacientes, por lo que parece deseable la concentración de enfermos en unos cuantos centros. Las complicaciones se agrupan bajo tres epígrafes: infecciosas, mecánicas y metabólicas. En el año 1997, Richards y cols. publicaron una revisión sistemática en la que apuntan las tasas promedio de complicaciones a partir de lo publicado hasta la fecha (tabla III) 13
3.1. Complicaciones infecciosas
La bacteriemia o la sepsis asociada a catéter es la complicación más frecuente y la más temida. Su frecuencia varía según las series, desde un episodio cada 11 meses de NPD hasta 1 cada 113 meses. Por término medio la tasa de incidencia es de 1 episodio/paciente y año de NPD. Los gérmenes más habituales son parte de la flora saprofita de la piel (S. Epidermidis, S. Aureus y más ocasionalmente Candida) y, en segundo lugar, la flora entérica. Parece existir una mayor tendencia en algunos pacientes para desarrollar episodios repetidos de infección, mientras que otros no desarrollan ninguna complicación. Se ha intentado conocer qué factores pueden predisponer a infección en pacientes con NPD. O'Keefe y cols. mostraron que la enfermedad de Crohn, una yeyunostomía de alto débito, una mala técnica de cuidado del catéter, la existencia de trombosis venosa o el hábito tabáquico predisponían a la infección 14. No se ha comprobado que los reservorios subcutáneos tengan una menor tasa de infección. Tampoco está claro el papel de los apósitos cutáneos o la aplicación de distintos antisépticos en el lugar de salida del catéter a través de la piel.
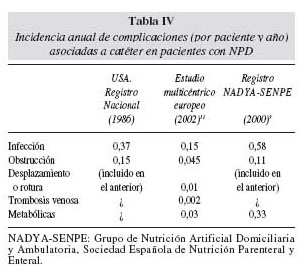
Aunque las prácticas de cuidados son muy similares en toda Europa, la tasa de incidencia de complicaciones es superior en nuestro país a las del registro europeo o norteamericano (tabla IV), sin encontrar ninguna explicación plausible. Aunque se están desarrollando nuevas estrategias para la prevención de las infecciones asociadas a catéter (catéteres impregnados en plata o en antibióticos; infusión de nuevos antisépticos como taurolidina) la mejor prevención consiste en el estricto seguimiento del protocolo de cuidados del catéter. Conviene insistir en el cumplimiento del protocolo para vencer la tendencia a la simplificación que acompaña cualquier tratamiento laborioso que se prolonga en el tiempo.
3.2. Complicaciones mecánicas
La mayoría ocurren durante la inserción del catéter y son las mismas que la técnica conlleva en cualquier otro paciente. Complicaciones más tardías son el desplazamiento o la rotura del catéter, pero sin duda, las que más preocupan son la obstrucción del catéter, con una incidencia anual de alrededor de 0,2 episodios/ paciente y año, generalmente debidas a precipitados de sales minerales en la luz o a coágulos de sangre o fibrina. También es motivo de preocupación la trombosis de una o varias venas centrales, sobre todo en el territorio de la vena cava superior. Al igual que ocurre con las complicaciones infecciosas, nuestros datos cuando menos duplican la tasa de otros países.
3.3. Complicaciones metabólicas
Las dos más importantes son la enfermedad hepática y la enfermedad ósea relacionadas con NPD. No disponemos de datos generales de incidencia.
4. Pronóstico y resultados
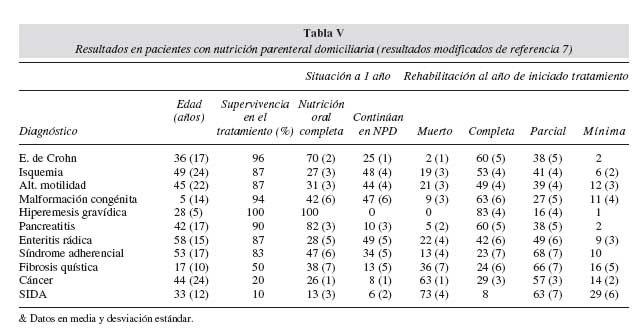
El tipo de enfermedad primaria y la edad repercuten profundamente en la evolución de los pacientes con NPD, como puede observarse en la tabla V (datos referidos a una muestra de 5.000 pacientes en Estados Unidos, entre 1989 y 1992). La mejor supervivencia y rehabilitación corresponde a pacientes con enfermedad de Crohn. Los pacientes con enfermedad vascular, trastornos de la motilidad, enteritis por radiación y alteraciones intestinales congénitas tienen también una evolución satisfactoria. Por el contrario, los que presentan una enfermedad progresiva, principalmente cáncer y SIDA, tienen una supervivencia muy corta. La supervivencia media a los 3 años es para el conjunto de enfermedades no malignas del 68%, que baja al 64% a los 5 años.
El 95% de las muertes en pacientes con NPD se atribuyen a la enfermedad de base. En general el grado de rehabilitación se correlaciona bien con la super-vivencia, excepto en la enteritis por radiación y en los trastornos de la motilidad.
En un estudio europeo reciente en pacientes con NPD de larga duración, la media de hospitalizaciones a lo largo de una año fue de 2,7 (rango, 0 a 12) correspondiendo a una media de 23 días de hospitalización, siendo aproximadamente la mitad por complicaciones de la NPD, sobre todo infecciosas 15. En niños la frecuencia de complicaciones es casi el doble.
Entre un 65 y un 75% de los pacientes con NPD mantienen una calidad de vida aceptable, que les permite mantener un empleo o su actividad habitual 16. Sin embargo, aquellos pacientes con mala situación funcional al inicio de la NPD son los que peor grado de rehabilitación consiguen. En el caso de los niños, además de los problemas psicológicos que pueden presentar los niños17, sus familias experimentan una notable modificación de sus costumbres con la NPD, en especial las referentes a su vida social18. Capítulo importante lo constituye el soporte familiar. El paciente y sus allegados pasan a hacerse cargo de la técnica de infusión, e implica un alto grado de compromiso. Por parte del equipo de Nutrición clínica debe garantizarse un adecuado programa de enseñanza, ayudados por los medios de aprendizaje más idóneos (manuales, vídeos, etc.) y una vía de acceso permanente a alguno de los miembros del equipo con el fin de resolver las dudas o complicaciones que pudieran surgir. El uso de material interactivo se ha mostrado eficaz en la capacidad de resolución de problemas y en la disminución de las escalas de ansiedad y depresión19. Poco desarrolladas en España, las asociaciones de enfermos en Estados Unidos y algunos países europeos, como la Oley Foundation, juegan no sólo un papel importante de apoyo familiar sino que además condicionan un menor número de complicaciones, con independencia de la experiencia del equipo encargado del caso 20,21.
En los últimos años el trasplante intestinal se ha convertido en una opción terapéutica para pacientes con fracaso intestinal permanente22. Sin embargo, si consideramos los resultados comunicados hasta fecha (supervivencia a 3 años con NPD, 70-90% frente a 58% en trasplante intestinal) 23, 24, la opinión más generalizada es que el trasplante debe reservarse para los pacientes con NPD que presenten enfermedad hepática progresiva o en aquellos en los que se carezca de accesos venosos para la NPD25. Las indicaciones para el trasplante intestinal son, hoy por hoy, limitadas.
Como conclusión podemos decir que la NPD es una técnica claramente adecuada para aquellos pacientes con fracaso intestinal en los que se pueda esperar una rehabilitación completa o parcial y una supervivencia prolongada. En palabras de L. Howard, "la NPD es una técnica invasiva y que requiere tiempo y esfuerzos por parte del paciente. Por lo tanto, sólo la aceptará el paciente cuando le reporte beneficios. Así, mientras que sea éste quien se responsabilice de su propio cuidado, el uso excesivo o inadecuado pare-ce poco probable"26. Sigue siendo objeto de consideración el papel de la NPD en enfermedades progresivas, sobre todo en pacientes con cáncer. Una visión panorámica del problema puede encontrarse en revisiones recientes27,28.
En los últimos años hemos asistido también a un debate sobre el modelo de asistencia médica del que las técnicas de nutrición artificial a domicilio no se han visto libres. Frente al modelo francés tradicional
La práctica de la nutrición artificial domiciliaria en Europa donde un grupo pequeño de centros lleva la atención de todos los pacientes con NPD, otros países han potenciado una atención más descentralizada o incluso han puesto en manos de compañías de infusión a domicilio gran parte del programa de NPD. Con el fin de mantener un alto nivel de calidad en la asistencia -y esto va ligado a una experiencia mayor- evitando desplazamientos largos de los pacientes en Escocia se está desarrollando una red de centros conectados mediante telemedicina, incluyendo un portal en Internet que posibilita la comunicación entre clínicos y pacientes29,30.
Nutrición enteral domiciliaria
El desarrollo de la nutrición enteral a domicilio (NED) es posterior al de la NPD, aunque su crecimiento ha sido mucho mayor. La aparición de nuevas formas de acceso al tubo digestivo y la disponibilidad de un gran número de nuevas dietas de nutrición enteral explican, en parte, su gran difusión.
1. Epidemiología
Es difícil conocer la incidencia exacta de la NED en España o en otros países, ya que los pacientes con NED son controlados por múltiples hospitales y médicos. Otra cuestión no menos importante es la definición de NED; mientras que para algunos registros sólo la consideran en caso de recibir alimentación a través de una sonda u ostomía en otros también se consideran las dietas enterales recibidas vía oral cuando superan un determinado porcentaje de las calorías de la dieta. Se estima que la prevalencia de NED en Estados Unidos es de 460 pacientes/millón de habitantes, mientras que en Gran Bretaña es de 280 casos. De los últimos datos publicados del registro NADYA (2000) si recogemos exclusivamente los datos de pacientes con sonda, la prevalencia es de 37 casos por millón de habitantes 31, cifra que aumenta hasta los 74,6 casos si se tiene en cuenta el total del registro. Estos datos son similares a los publicados en algunas Comunidades Autónomas32. Sin embargo, en otro estudio reciente referido exclusivamente a Galicia, la prevalencia fue de 10,34 casos/10.000 habitantes33, lo que hace suponer que los datos comunicados al registro no recogen la totalidad de la práctica clínica.
2. ¿Qué pacientes reciben NED?
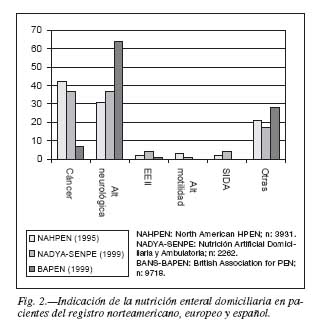
La distribución de enfermedades de base en la NED difiere en gran medida respecto a la NPD34. Las enfermedades neurológicas seguidas del cáncer de cabeza y cuello son las indicaciones más frecuentes (fig. 2). Las diferencias entre países se deben más al sistema de registro (sólo NED por sonda frente a cualquier vía de administración) que a diferencias en la indicación.
La distribución de los pacientes muestra un perfil bimodal, con mayor frecuencia en la infancia y en la ancianidad. Alrededor del 30% de los pacientes tienen menos de 20 años y algo más del 50% tienen más de 60 años.
3. Aspectos técnicos
Mientras que la administración a través de una gastrostomía es el método más frecuentemente utilizado en la mayoría de países35; en el registro español alrededor del 50% reciben la dieta enteral por vía oral31. De los que utilizan una vía distinta a la oral sólo algo menos de la mitad lo hacen a través de una gastrostomía.
Al igual que en la NPD es preciso contar con un programa de enseñanza de la técnica, donde junto al manejo de la vía de acceso se instruya al paciente y/o la familia sobre la detección, prevención y tratamiento de las complicaciones, aunque, como es lógico, es menos prolijo que en el caso de la NPD 36,37. El seguimiento por unidades especializadas facilita la posibilidad de contacto entre el paciente y el equipo responsable, lo que redunda en una mejora del servicio. Desde la publicación de la Orden Ministerial que regula la financiación de la NED, se ha facilitado la indicación y la provisión de los productos de nutrición enteral, aunque todavía quedan algunos aspectos por resolver como son la provisión a domicilio del material necesario para la NE, y la inclusión de algunas patologías, en especial referentes a la edad infantil. La situación en otros países europeos es muy variable, tanto en lo relativo a la financiación como a la provisión del material de la NED 12.
4. Complicaciones
Aunque la NED es una técnica segura no está exenta de complicaciones. Las elevadas tasas de mortalidad en pacientes con NED hacen referencia más a la enfermedad de base y a la edad avanzada que a la técnica en sí. Pueden presentarse complicaciones en relación con la administración de los nutrientes, p.ej. problemas para conseguir la fórmula o el material, obstrucción o rotura de la sonda; problemas gastrointestinales: vómitos, diarrea, estreñimiento, etc. o alteraciones nutricionales o metabólicas. En un estudio prospectivo reciente, un 42% de los pacientes tuvo alguna complicación; de ellas las digestivas fueron las más frecuentes seguidas de las mecánicas. La tasa media de complicaciones fue de 0,16 complicaciones por paciente y año 38. Estas cifras son inferiores a las comunicadas en el último registro español (2000)31.
5. Resultados clínicos
La NED es una forma de tratamiento eficaz: consigue el mantenimiento del peso o la recuperación del peso perdido. Favorece el crecimiento en niños y adolescentes con deterioro del crecimiento de origen nutricional y favorece su actividad habitual39. Es un método idóneo para mejorar y mantener el estado nutricional, más barato y con menos complicaciones que la NPD.
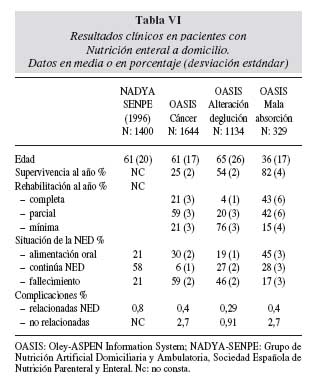
El principal factor que determina los resultados clínicos es la enfermedad de base (tabla VI) De modo global se puede decir que los resultados son peores en pacientes que iniciaron la NED por un cáncer, que en aquellos en los que la indicación fue un trastorno de la deglución. Los datos relativos a la rehabilitación corren paralelos a los referidos a mortalidad, aunque los pacientes que reciben NED a causa de una alteración neurológica que dificulte la deglución tienen una pobre capacidad de rehabilitación. Para el mismo problema clínico una edad menor supone mejor pronóstico40. En personas atendidas en residencias asistidas, la NE a través de gastrostomía en personas con demencia es motivo de controversia; la mayoría de resultados publicados o no muestran cambios o son clínicamente poco relevantes tanto en el estado funcional como en el nutricional; además en este grupo de pacientes el porcentaje de complicaciones no es despreciable. La indicación de NED en la infancia es muy distinta de la población adulta, siendo las enfermedades benignas la principal indicación, con unos porcentajes de supervivencia y de rehabilitación muy superiores a los encontrados en las series de adultos.
Cuando se considera la capacidad de rehabilitación y la mejora de situación vital los resultados varían en función de la enfermedad de base y de la edad de los pacientes, aunque en general experimentan una mejoría de la misma en relación con el momento del inicio de la NED41-43.
Tanto el inicio como la retirada de la alimentación artificial en pacientes con un pésimo pronóstico o con una situación de grave deterioro, como p.ej. los estados de demencia, deben ser valorados juiciosamente tomando en consideración los valores del paciente y su familia, los resultados esperables y la carga que la nutrición artificial a domicilio pueda suponer.
Como resumen de lo expuesto:
1. Existe gran variabilidad en la práctica clínica entre los diferentes países europeos. No existen guías de actuación común y son escasos los estudios multicéntricos.
2. La prevalencia de NPD varía entre 0,9 y 12 pacientes por millón de habitantes. La tasa de prevalencia en España es aproximadamente la mitad de la de los países de nuestro entorno.
3. Los mejores resultados se obtienen en los centros que reúnen mayor experiencia. Algunas variables como los programas de enseñanza de la técnica o la existencia de organizaciones de apoyo pueden influir favorablemente en los resultados.
4. La NPD está financiada por los sistemas públicos de salud en todos los países.
5. A la vista de los datos publicados en pacientes con enfermedad benigna, los resultados a medio y largo plazo son mejores con la NPD que con el trasplante intestinal. El trasplante intestinal es la mejor opción para pacientes que presenten complicaciones graves asociadas al uso de la NPD.
6. La variabilidad en el uso de la nutrición enteral domiciliaria es todavía mayor con el inconveniente de la dificultad que entraña carecer de datos de registros nacionales. En general, la NED se refiere a pacientes con alimentación a través de una sonda u ostomía.
7. La prevalencia de la NED en España es alrededor de 5 veces inferior a la de otros países o áreas europeas.
8. Los aspectos administrativos: financiación, provisión, etc. varían considerablemente entre países.
9. El uso de la NED en algunas situaciones clínicas p.ej. demencia progresiva plantea interrogantes éticos.
Referencias
1. González Ramallo VJ, Valdivieso Martínez B, Ruiz García V: Hospitalización a domicilio. Med Clin (Barc), 2002, 118:659-664. [ Links ]
2. ASPEN Board of Directors: Standards for home nutrition support. Nutr Clin Pract, 1999, 13:157-166. [ Links ]
3. ASPEN Board of Directors and the Clinical Guidelines Task Force: Guidelines for the use of parenteral and enteral nutrition in adult and pediatric patients. J Parent Ent Nutr, 2002, 26 (Supl):1SA-138SA. [ Links ]
4. Koretz RL, Lipman TO, Klein S: AGA Technical review on parenteral nutrition. Gastroenterology, 2001, 121:970-1001. [ Links ]
5. American Gastroenterological Association Medical Position Statement: Parenteral Nutrition. Gastroenterology, 2001, 121: 966-969. [ Links ]
6. Shils ME, Wright WL, Turnbull A y cols.: Long term parenteral nutrition through external arteriovenous shunt. N Engl J Med, 1970, 283:341-344. [ Links ]
7. Howard L, Ament M, Fleming CR, Shike M, Steiger E: Current use and clinical outcome of home parenteral and enteral nutrition therapies in the United States. Gastroenterology, 1995, 109:355-365. [ Links ]
8. Van Gossum A, Bakker H, Bozzetti F y cols.: Home parenteral nutrition in adults: a European multicentre survey in 1997. Clin Nutr, 1999, 18:135-140. [ Links ]
9. Planas M, Castellá M, León M y cols.: Nutrición parenteral domiciliaria (NPD): registro NADYA. Año 2000. Nutr Hosp, 2003, 18:29-33. [ Links ]
10. Howard L, Hassan N: Home parenteral nutrition. 25 years later. Gastroenterol Clin North Amer, 1998, 27:481-512. [ Links ]
11. Bozzetti F, Mariani L, Boggio Bertinet D y cols.: Central venous catheter complications in 447 patients on home parenteral nutrition: an analysis of over 100,000 catheter days. Clin Nutr, 2002, 21:475-485. [ Links ]
12. Moreno JM, Shaffer J, Staun M y cols.: Survey on legislation and funding of Home Artificial Nutrition in different european countries. Clin Nutr, 2001, 20:117-123. [ Links ]
13. Richards DM, Deeks JJ, Sheldon TA, Shaffer JL: Home parenteral nutrition: a systematic review. Health Technol Assess, 1997, 1:1-59. [ Links ]
14. O'Keefe SJD, Burnes JU, Thompson RL: Recurrent sepsis in home parenteral nutrition patients: an analysis of risk factors. J Parent Enteral Nutr, 1994, 18:256-263. [ Links ]
15. Van Gossum A, Vahedi K, Abdel-Malik y cols.: Clinical, social and rehabilitation status of long-term home parenteral nutrition patients: results of a European multicentre survey. Clin Nutr, 2001, 20:205-210. [ Links ]
16. Howard L, Ashley C: Management of complications in patients receiving home parenteral nutrition. Gastroenterology, 2003, 124:1561-1661. [ Links ]
17. Engström I, Björnestram B, Finkel Y: Psychological distress associated with home parenteral nutrition in Swedish children, adolescents, and their parents: preliminary results. JPGN, 2003, 37:246-251. [ Links ]
18. Holden CE: Enteral and parenteral nutrition feeding at home. Impact on family life and the implications for home care. MSc thesis. Wolverhampton University, 1994. [ Links ]
19. Smith CE, Curtas S, Kleinbeck SVM, Werkowitch M, Mosier M, Seidner DL, Steiger E: Clinical trial of interactive and videotaped educational interventions reduce infection, reactive depression, and rehospitalizations for sepsis in patients on Home Parenteral Nutrition. J Parent Ent Nutr, 2003, 27:137-145. [ Links ]
20. Smith CE, Curtas S, Werkowitch M, Kleinbeck SVM, Howard L: Home parenteral nutrition: does affiliation with a national support and educational organization improve patient outcomes? J Parent Ent Nutr, 2002, 26:159-163. [ Links ]
21. Kindle R: Life with Fred: 12 years of home parenteral nutrition. Nutr Clin Pract, 2003, 18:235-237. [ Links ]
22. Fishbein TM, Gondolesi GE, Kaufman SS: Intestinal transplantation for gut failure. Gastroenterology, 2003, 124:1615-1628. [ Links ]
23. Messing B, Crenn P, Beau P, Boutron-Ruault MC, Rambaud JC, Matuchansky C: Long-term survival and parenteral nutrition dependence in adult patients with the short bowel syndrome. Gastroenterology, 1999, 117:1043-1050. [ Links ]
24. Abu-Élmag K, Reyes J, Bond G y cols.: Clinical intestinal transplantation: a decade of experience at a single center. Ann Surg, 2001, 234:404-417. [ Links ]
25. Buchman AL, Scolapio J, Fryer J: AGA Technical review on short bowel syndrome and intestinal trasplantation. Gastroenterology, 2003, 124:111-1134. [ Links ]
26. Howard L: Home parenteral nutrition: a transatlantic review. Clin Nutr, 1999, 18:131-133. [ Links ]
27. Bozzetti F, Bozzetti V: Home artificial nutrition in incurable cancer patients: rationale and ethics. Clin Nutr, 2001, 20 (Supl 2):23-27. [ Links ]
28. Fédération nationale des centres de lutte contre le cancer: Standards, options et recommandations pour la nutrition artificielle à domicile du malade cancereux adulte (rapport intégral). Nutr Clin Métab, 2003, 17:97-110. [ Links ]
29. Baxter JP, McKee RF: The Scottish Home Parenteral Nutrition Manged Clinical Network: one year on. Clin Nutr, 2003, 22:501-504. [ Links ]
30. Jones BJM: Recent developments in the delivery of home parenteral nutrition in the UK. Proceed Nutr Soc, 2003, 62:719-725. [ Links ]
31. Planas M, Castellá M, García Luna PP y cols.: Nutrición enteral domiciliaria (NED): registro Nacional del año 2000. Nutr Hosp, 2003, 18:33-37. [ Links ]
32. De Luis DA, Aller R, De Luis J, Izaola O, Romero E, Terroba MC, Cuellar LA: Clinical and biochemical characteristics of patients with home enteral nutrition in an area of Spain. Eur J Clin Nutr, 2003, 57:612-615. [ Links ]
33. Pérez Méndez LF, García-Mayor RV y Grupo de trabajo de la Sociedad gallega de Nutrición y Dietética: situación actual de la nutrición enteral domiciliaria en Galicia. Estudio multicéntrico. Nutr Hosp, 2001, 16:257-261. [ Links ]
34. Consejo Interterritorial del Sistema Nacional de Salud: Guía de práctica clínica de nutrición enteral domiciliaria. Ministerio de Sanidad y Consumo, Madrid, 1998, 3-42. [ Links ]
35. Hebuterne X, Bozzetti F, Moreno-Villares JM y cols.: Home enteral nutrition in adults: a European multicentre survey. Clin Nutr, 2003, 22:261-266. [ Links ]
36. García Luna PP, Parejo Campos J, Fenoy Macías JL: Actualización de la nutrición enteral en el domicilio del paciente. Nutr Hosp, 1999, 14 (Supl 2):120(s)-128(s). [ Links ]
37. Colomb V: Nutrition artificiel à domicile chez l'enfant. Indications et organization. Arch Pédiatr, 2001, 8:79-85. [ Links ]
38. Gómez Candela C, Cos Blanco A, García Luna PP y cols.: Complicaciones de la nutrición enteral domiciliaria. Resultados de un estudio multicéntrico. Nutr Hosp, 2003, 18:167-173. [ Links ]
39. Vanderhoof JA, Young RJ: Overview of considerations for the pediatric patient receiving home parenteral and enteral nutrition. Nutr Clin Pract, 2003, 18:221-226. [ Links ]
40. Elia M: Home enteral tube feeding following cerebrovascular accident. Clin Nutr, 2001, 20:27-30. [ Links ]
41. Schneider SM, Pouget I, Staccini P, Rampal P, Hebuterne X: Quality of life in long-term home enteral nutrition patients. Clin Nutr, 2000, 19:23-28. [ Links ]
42. Mackie E: Home enteral feeding. III. A patient's perspective. Clin Nutr, 2001, 20 (Supl 1):77-79. [ Links ]
43. Loeser C, Von Herz U, Küchler T, Rzehak P, Müller MJ: Quality of life and nutritional state in patients on home enteral tube feeding. Nutrition, 2003, 19:605-611. [ Links ]