Introducción
El osteosarcoma es un tipo de neoplasia ósea que se desarrolla en las células osteoblásticas formadoras de hueso. Su incidencia es más frecuente en niños, adolescentes y adultos jóvenes, su presentación es agresiva y en muchas ocasiones mortal. Generalmente representa el 1% de los tumores malignos, siendo en esencia un tipo de tumor muy raro(1) aunque existe literatura que reporta una incidencia que abarca de 1.8-5 por cada 100.000 personas al año.(2)
El tratamiento más frecuente en la actualidad para este tipo de pacientes es un tratamiento radical con amputación de la extremidad afectada, lo que condiciona una serie de afectaciones psicológicas, físicas y funcionales severas en las personas con esta patología.(3) Desde hace ya varios años están descritas múltiples técnicas de reconstrucción para mejorar la calidad de vida de los pacientes que sufren secuelas de osteosarcoma,(4,5) por lo que gracias a los avances desarrollados por la Cirugía Plástica Reconstructiva y los avances en técnicas microquirúrgicas, en la actualidad la reconstrucción mediante colgajos tiene cada vez más aceptación como tratamiento quirúrgico definitivo y que al mismo tiempo satisface los objetivos oncológicos.(6)
Cabe recordar, que el colgajo de dorsal ancho fue introducido por Tansini en el año 1896, utilizándose para la cobertura de defectos secundarios a mastectomía con grandes áreas de extensión. El colgajo de músculo dorsal ancho, como transferencia pediculada o de tejido libre microvascular, es uno de los más frecuentemente utilizados en Cirugía Reparadora por aportar vasos de gran diámetro y un largo pedículo fiable. Puede elevarse como colgajo muscular, musculocutáneo y/o osteomiocutáneo. Como injerto compuesto, incluyendo cantidades variables de músculo, piel y tejido subcutáneo, puede utilizarse en cualquier variedad de reconstrucción y en cualquier área del cuerpo.(7,8)
Un algoritmo propuesto por Panattoni afronta el trauma de la extremidad superior de manera sistemática de acuerdo con prioridades y con las respectivas opciones disponibles en cada etapa del tratamiento: a) evaluación, b) hueso, c) contracción de tendones, d) denervación con reparación nerviosa primaria y e) cobertura.(9) De acuerdo con lo anterior, una vez resueltas las prioridades, dentro de las opciones de colgajos pediculados para brindar un manejo definitivo de la cubierta cutánea, contamos con el colgajo dorso-epigástrico descrito por Haddad, que es una variante del colgajo de músculo dorsal ancho basado en la rama descendente de la arteria tóracodorsal, rama de la arteria subescapular.(10)
Cabe señalar que el índice de recurrencia de este tipo de tumores es muy elevado. Están descritas en la literatura tasas de recurrencia que llegan hasta un 25%,(11,12) sin que hasta la actualidad se haya llegado a un consenso para disminuirlas pese a los avances científicos. Sin embargo, existen opciones terapéuticas como la radioterapia en caso de recurrencia local.(13)
En este artículo presentamos un caso clínico exitoso en el que empleamos el colgajo dorso-epigástrico como opción de tratamiento quirúrgico viable y de preservación de una extremidad afectada por osteosarcoma, lo cual permitió conservar un área mayor de músculo con un resultado más estético y funcional que facilita la integración del paciente a la vida diaria, evitando las repercusiones que conlleva el desarrollo psicosocial de un niño que carece de una extremidad torácica.
Caso clínico
El presente caso fue tratado en el año 2022 en el Servicio de Cirugía Plástica, Estética y Reconstructiva del Hospital para el Niño con la colaboración del Instituto de Salud del Estado de México en la Ciudad de Toluca, Estado de México (México).
Paciente femenina de 9 años y 3 meses de edad, hermana de 2 varones aparentemente sanos y sin otros antecedentes heredofamiliares de importancia. Nació por parto eutócico a las 42 semanas de gestación, sin agregados patológicos. Cursa cuarto año de primaria y cuenta con condiciones higiénico-dietéticas regulares y esquema de vacunación completo.
Inicia su patología el 1 de diciembre de 2020 al sufrir caída de su propia altura mientras subía un escalón en su domicilio, sufriendo contusión directa en brazo izquierdo con un trazo de fractura (Fig. 1).
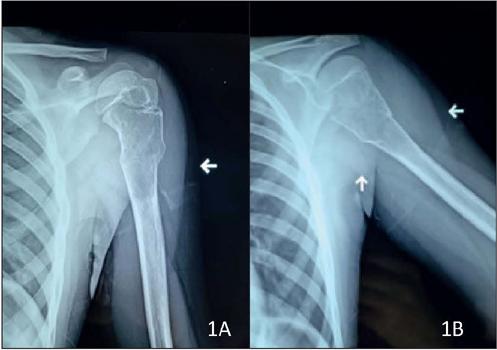
Figura 1 A. Radiografía anteroposterior de miembro torácico izquierdo: pérdida de solución de continuidad transversal metafisiaria con afección de ambas cortezas a nivel proximal entra el cuello anatómico y el cuello quirúrgico del húmero izquierdo. B. Radiografía anteroposterior que muestra la misma lesión sin desplazamiento.
La paciente fue valorada en el Hospital General de Tejupilco, Estado de México (México) donde se visualiza fractura metafisaria proximal de húmero izquierdo que fue tratada de forma conservadora con colocación de inmovilizador de hombro durante 30 días.
El 15 de enero de 2021 sufre nuevamente caída de su propia altura al resbalar con agua en su domicilio, sufriendo nueva contusión directa en el brazo izquierdo. Acude nuevamente a Hospital Tejupilco donde visualizan nueva fractura diafisaria de húmero y deciden tratamiento quirúrgico con colocación de clavo de Kirschner (Fig. 2A).
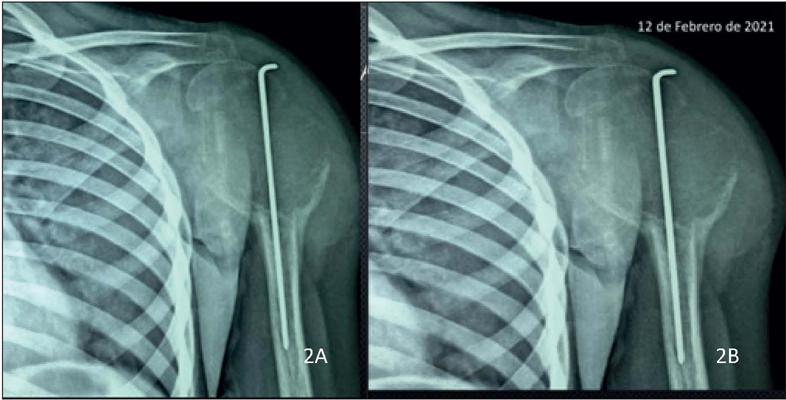
Figura 2 A. Radiografía anteroposterior de hombro izquierdo con fractura diafisiaria de húmero tras reducción con colocación de clavo de Kirschner, con cambios radiológicos a nivel de la cabeza humeral. B. Radiografía anteroposterior de humero izquierdo un més después de la colocación del clavo en la que se visualiza tumoración ósea de mayor tamaño a nivel de cabeza y metáfisis humeral.
Sin embargo, en los controles radiográficos realizados 1 mes después se visualiza tumoración ósea a nivel de cabeza y metáfisis humeral, motivo por el cual se solicitan marcadores tumorales que presentan los siguientes parámetros: antígeno carcinoembrionario (CEA): 0.866U/ml, hormona gonadotrofina coriónica humana (HCG): 0U/ml, CA 19-9: 3.34U/ml, CA 125: 4.75U/ml, CA 15.3: 13.9U/ml. Se realiza biopsia tumoral en el mismo hospital con informe histopatológico compatible con sarcoma osteogénico con patrón osteoblástico, motivo por el cual se refiere a la paciente al Hospital para el Niño del Instituto Materno Infantil del Estado de México en la ciudad de Toluca, Estado de México (México), donde se procede a tratamiento con 9 sesiones de quimioterapia con metrotexato y posteriormente se inicia protocolo para realización de tratamiento quirúrgico con los siguientes procedimientos.
En junio de 2021 se realiza retirada del clavo centro-medular de Kirschner. De noviembre a diciembre de 2021 se practican 4 aseos quirúrgicos con desbridamiento y colocación de sistema de presión negativa. Un mes después se realiza resección de la tumoración ósea con colocación de un espaciador óseo con cemento medicado y sistema de presión negativa. Se valora la posibilidad de cirugía radical con desarticulación de extremidad torácica izquierda, por lo que se solicita tratamiento conjunto entre el Servicio de Traumatología y Ortopedia y el Servicio de Cirugía Plástica para realización de artroplastia tumoral de hombro izquierdo y posterior cobertura cutánea con colgajo dorso-epigástrico de rama transversal superior de arteria tóracodorsal izquierda.
Los exámenes de laboratorio preoperatorios mostraron anemia grado II de la OMS y trombocitopenia leve sin otras alteraciones en la analítica sanguínea. Tras el protocolo prequirúrgico, la paciente fue programada para realización del plan quirúrgico programado, intervención que se llevó a cabo 6 meses después de la resección del tumor y en 2 tiempos quirúrgicos.
Técnica quirúrgica
Primer tiempo quirúrgico: artroplastia tumoral de hombro izquierdo. Se rima canal medular hasta llegar a 9, se coloca copa en la glena fijada con 4 tornillos de 3.5 cm, y de vástago con 2 tornillos distales 3.5 cm. Este tiempo tuvo una duración de 2 horas y media; al terminar, se hizo cambio de campos quirúrgicos, se colocó a la paciente en decúbito lateral, antisepsia y se procedió al segundo tiempo quirúrgico.
Segundo tiempo quirúrgico: confección del colgajo dorso-epigástrico. Marcamos una isla cutánea de 20 x 10 cm, levantamos isla cutánea, disección hasta localización de arteria tóracodorsal hasta bifurcación, posteriormente levantamos el colgajo miocutáneo incluyendo rama transversal bajo visión directa, disección anterior de la superficie a nivel de la línea axilar anterior y colocamos sobre área cruenta en zona de deltoides izquierda y superficie anterior de brazo izquierdo sin tunelizar pedículo vascular; fijamos el colgajo sobre el área cruenta y sobre la endoprótesis, sin complicaciones ni cambios en el colgajo dorso-epigástrico (Fig. 3 y 4). Este segundo tiempo tuvo una duración de 3 horas.
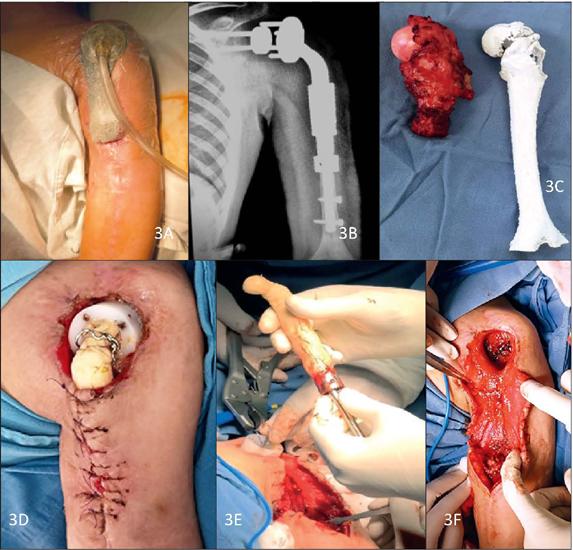
Figura 3 A. Imagen clínica de hombro izquierdo con sistema de presión negativa antes del procedimiento quirúrgico. B. Radiografía anteroposterior de hombro izquierdo antes del procedimiento quirúrgico con espaciador óseo cementado después de retirar la tumoración ósea. C. Tumoración ósea resecada y espaciador óseo con cemento medicado antes de la colocación. D. Área cruenta en superficie de hombro izquierdo con exposición de espaciador con cemento medicado. E. Espaciador con cemento medicado tras su retirada, superficie articular a articulación de hombro izquierdo y área cruenta antes del tratamiento definitivo. F. Área cruenta en hombro izquierdo: articulación glenohumeral y cabo humeral antes del tratamiento quirúrgico definitivo.
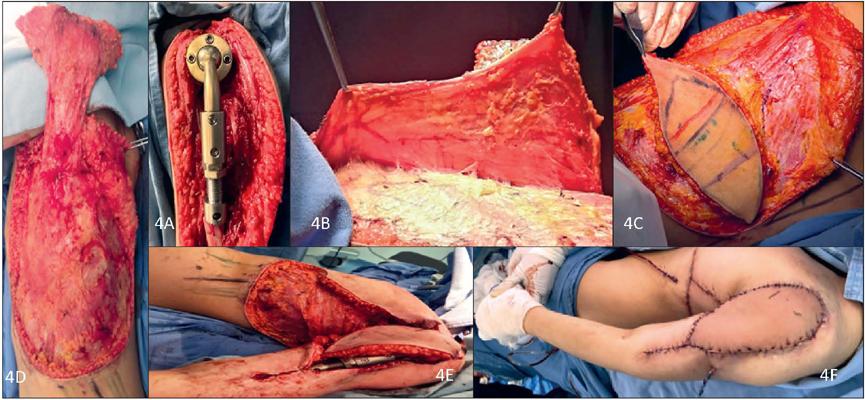
Figura 4 A. Imagen posterior a la retirada del espaciador cementado y desbridamiento del tejido desvitalizado con colocación de endoprótesis tumoral izquierda fija y funcional. B. Exposición de colgajo dorso-epigástrico con pedículo dominante (rama transversal de arteria tóracodorsal). C. Isla cutánea y colgajo miocutáneo completamente disecado. D. Colgajo miocutáneo completamente levantado; se observa área donadora antes del cierre de la misma. E. Colocación del colgajo sobre el área receptora y área donante antes de la fijación del colgajo y cierre primario. F. Colgajo dorso-epigástrico sobre área receptora, con cobertura total del defecto y endoprótesis tumoral; área donadora cerrada con cierre primario
Tras la recuperación del procedimiento quirúrgico, la paciente egresó sin complicaciones a los 7 días y continúo seguimiento a través de la consulta externa de Traumatología y Ortopedia y de Cirugía Plástica.
En total, desde la detección del tumor hasta el egreso hospitalario tras la intervención transcurrieron 18 meses.
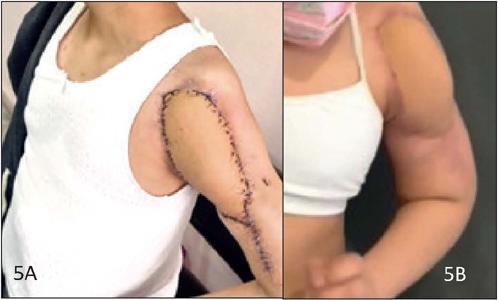
En cuanto a la recuperación de actividad y movimientos, la paciente tuvo limitación de movimiento durante 2 semanas tras la intervención y luego siguió tratamiento por Rehabilitación que le permitió recuperar arcos de movilidad: a las 2 semanas inició movimientos pasivos y a la tercera semana inició movimientos activos. Realizamos valoración con grados de movilidad a las 8 y a las 12 semanas de postoperatorio, obteniendo los siguientes resultados: elevación del hombro rango de 15 a 20 grados; depresión del hombro 5 a 10 grados; abducción 90 grados por pérdida del deltoides 20 a 40°, rotación externa 70°, rotación interna 70° y circunduccion con limitación a movimientos de elevación. En cuanto a las actividades de la vida diaria que realiza de manera independiente registramos: vestimenta personal, aseo personal, toma de objetos, movimientos finos con la mano y elevación del hombro limitada por pérdida del deltoides (Fig. 5).
Discusión
El colgajo dorso-epigástrico es un colgajo de reciente descripción(10) que proporciona una opción viable para preservar extremidades afectadas por tumores óseos como el osteosarcoma.(14) Dispone de una menor tasa de complicaciones(15) además de ser una técnica quirúrgica fácilmente reproducible, lo que le hace ser una opción viable y eficaz en este tipo de pacientes,(16) permitiendo la disminución de secuelas psicológicas y funcionales con resultados estéticamente satisfactorios.(17,18,19)
El colgajo dorso-epigástrico tiene como ventaja respecto a otro tipo de colgajos el que permite recobrar la función de la extremidad casi en su totalidad, con integración y reincorporación de los pacientes a su vida cotidiana con resultados estéticos ampliamente placenteros.(20,21) Permite reducir la estancia hospitalaria y la recuperación postoperatoria en comparación a los colgajos libres o abdominales, y puede utilizarse de manera ideal para reconstrucción con tejidos autólogos permitiendo, además, la utilización de mayor tejido disponible con una menor morbilidad del sitio donante, con colgajos más seguros y extensos al poseer una mayor y mejor irrigación sanguínea.
Conclusiones
En el caso clínico presentado, la artroplastia tumoral de hombro con posterior cobertura cutánea con colgajo dorso-epigástrico de rama transversal de arteria tóracodorsal izquierda fue una opción terapéutica multidisciplinaria, válida y eficaz, ante la presentación de un tumor óseo maligno en extremidad superior. Permitió evitar un tratamiento radical en paciente pediátrico, hecho que afectaría a su desarrollo global, su apariencia y autoestima.
Consideramos que este procedimiento ofrece preservar la extremidad superior con resultado exitoso, baja tasa de complicaciones y buena calidad de vida para los pacientes. De esta forma es posible extirpar tumores en áreas anatómicas complicadas y realizar una reconstrucción con colgajo que satisface los objetivos oncológicos y que permite la utilización de mayor tejido autólogo al poseer mayor irrigación sanguínea.