My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Española de Enfermedades Digestivas
Print version ISSN 1130-0108
Rev. esp. enferm. dig. vol.107 n.3 Madrid Mar. 2015
Estándares de calidad en 480 resecciones pancreáticas: estudio prospectivo observacional
Quality standards in 480 pancreatic resections: a prospective observational study
Francisco Javier Herrera-Cabezón, Pablo Sánchez-Acedo, Cruz Zazpe-Ripa, Antonio Tarifa-Castilla y José Miguel Lera-Tricas
Unidad de Cirugía Hepato-bilio-pancreática. Complejo Hospitalario de Navarra. Pamplona, Navarra
Dirección para correspondencia
RESUMEN
Introducción: la resección pancreática es un procedimiento estándar para el tratamiento de los tumores periampulares. La morbimortalidad es elevada y los estándares de calidad en nuestro medio son escasos. Las clasificaciones internacionales de las complicaciones Clavien-Dindo y las específicas de las pancreatectomías (ISGPS) permiten una adecuada comparación de casuísticas.
Objetivos: los objetivos de nuestro trabajo son describir la morbimortalidad de 480 pancreatectomías utilizando las clasificaciones internacionales ISGPS y Clavien-Dindo para contribuir al establecimiento de un estándar de calidad en nuestro medio, y comparar los resultados de la DPC con reconstrucción mediante pancreaticogastrostomía (1.55) frente a la pancreaticoyeyunostomía (177).
Métodos: presentamos 480 resecciones que incluyen 337 duodenopancreatectomías, 116 pancreatectomías distales, 11 pancreatectomías totales, 10 pancreatectomías centrales y 6 enucleaciones.
Resultados: los resultados en la duodenopancreatectomía son: 62 % de morbilidad (Clavien ≥ III 25,9 %), 12,3 % de reintervenciones y 3,3 % de mortalidad global. En las reconstrucción con pancreaticoyeyunostomía: 71,2 % de morbilidad (Clavien ≥ III 34,4 %), 17,5 % de reintervenciones y 3,3 % de mortalidad. En la reconstrucción con pancreaticogastrostomía: 51 % de morbilidad (Clavien ≥ III 15,4 %), 6,4 % de reintervenciones y 3,2 % de mortalidad, las diferencias son significativas, excepto en la mortalidad.
Conclusiones: concluimos que nuestra serie cumple criterios de calidad en comparación con la experiencia de otros grupos. La reconstrucción con pancreaticogastrostomía disminuye significativamente el número de complicaciones, su gravedad, la tasa de fístula pancreática y las reintervenciones.
Palabras clave: Pancreaticoduodenectomía. Pancreatectomía. Morbilidad. Mortalidad. Indicadores de calidad. Sistema sanitario.
ABSTRACT
Background: Pancreatic resection is a standard procedure for the treatment of periampullary tumors. Morbidity and mortality are high, and quality standards are scarce in our setting. International classifications of complications (Clavien-Dindo) and those specific for pancreatectomies (ISGPS) allow adequate case comparisons.
Objectives: The goals of our work are to describe the morbidity and mortality of 480 pancreatectomies using the international classifications ISGPS and Clavien-Dindo to help establish a quality standard in our setting and to compare the results of CPD with reconstruction by pancreaticogastrostomy (1,559 versus 177 pancreaticojejunostomy).
Methods: We report 480 resections including 337 duodenopancreatectomies, 116 distal pancreatectomies, 11 total pancreatectomies, 10 central pancreatectomies, and 6 enucleations.
Results:Results for duodenopancreatectomy include: 62 % morbidity (Clavien ≥ III 25.9 %), 12.3 % reinterventions, and 3.3 % overall mortality. For reconstruction by pancreaticojejunostomy: 71.2 % morbidity (Clavien ≥ III 34.4 %), 17.5 % reinterventions, and 3.3 % mortality. For reconstruction by pancreaticogastrostomy: 51 % morbidity (Clavien ≥ III 15.4%), 6.4 % reinterventions, and 3.2 % mortality. Differences are significant except for mortality.
Conclusions: We conclude that our series meets quality criteria as compared to other groups. Reconstruction with pancreaticogastrostomy significantly reduces complication number and severity, as well as pancreatic fistula and reintervention rates.
Key words: Pancreaticoduodenectomy. Pancreatectomy. Morbidity. Mortality. Quality Indicators. Health Care.
Lista de abreviaturas:
ISGPS: International Study Group of Pancreatic Surgery;
DPC: duodenopancreatectomía cefálica;
PD: pancreatectomía distal;
ASA: American Society of Anesthesiologists;
IMC: índice de masa corporal;
FP: fístula pancreática;
RVG: retraso de vaciamiento gástrico;
PY: pancreaticoyeyunostomía;
PG: pancreaticogastrostomía;
PT: duodenopancreatectomía total;
ERAS: enhanced recovery after surgery;
PC: pancreatectomía central;
GIST: gastrointestinal stromal tumors;
UCI: unidad cuidados intensivos.
Introducción
El aumento del número de resecciones pancreáticas en unidades especializadas ha permitido una mejora de la morbilidad y mortalidad. Pese a ello, en nuestro sistema sanitario, carecemos de estándares de calidad postoperatorios, específicos para los dos procedimientos más frecuentes: duodenopancreatectomía cefálica (DPC) y pancreatectomía corporocaudal o distal (PD). Se ha demostrado que en la duodenopancreatectomía la morbimortalidad desciende a medida que aumenta el número de procedimientos por cirujano y centro hospitalario, si bien los límites son imprecisos (1-4). Por otra parte, las referencias a la calidad de que disponemos, proceden mayoritariamente de series de entornos sanitarios en los que predominan los centros de referencia de alto volumen (5). La descripción de las complicaciones recientemente estandarizada gracias a las clasificaciones ISGPS (6-8) y Clavien-Dindo (9,10) (Tabla I), ha sido muy poco utilizada en las publicaciones españolas (5,11-14). Este hecho impide una adecuada comparación de las casuísticas y complica el establecimiento de estándares de calidad adaptados a nuestra realidad sanitaria.
Los objetivos de nuestro trabajo son describir la morbimortalidad de 480 pancreatectomías utilizando las clasificaciones internacionales ISGPS y Clavien-Dindo para contribuir al establecimiento de un estándar de calidad en nuestro medio, y comparar los resultados de la DPC con reconstrucción mediante pancreaticogastrostomía frente a la pancreaticoyeyunostomía.
Pacientes y métodos
Se incluyeron todos los pacientes sometidos a una resección pancreática en el periodo junio de 1994 a junio de 2014. Los datos fueron incluidos prospectivamente en una base de datos FileMaker Pro 3.0 de diseño propio al alta del paciente y también se incluyeron los reingresos a los 30 días del alta. Se estudiaron 17 variables: datos demográficos, clasificación ASA, índice de masa corporal (IMC), diagnóstico, procedimientos quirúrgicos, fecha de la intervención, complicaciones quirúrgicas según la clasificación ISGPS, fístula pancreática (FP), retraso de vaciamiento gástrico (RVG), hemorragia y Clavien-Dindo, reintervenciones, infecciones, ingreso en cuidados intensivos, necesidad de procedimientos radiológicos/endoscópicos o transfusión, mortalidad, y su causa, a 30 días o en cualquier periodo si permanecía ingresado y estancia hospitalaria. Las complicaciones de los reingresos han sido añadidas a los resultados generales. Los datos anteriores a 2008 fueron adaptados a las clasificaciones internacionales caso a caso y revisadas por el primer autor. Se consideraron complicaciones menores a las Clavien I-II y mayores a las Clavien ≥ III-A, incluyendo la mortalidad. Todos los pacientes firmaron un consentimiento informado cumpliendo las directrices éticas de la declaración de Helsinki de 1975.
Los pacientes fueron agrupados según el tipo de resección pancreática en: DPC con dos periodos, el que va desde junio de 1994 hasta abril de 2008 en el que se utilizó la reconstrucción pancreática mediante pancreaticoyeyunostomía ducto-mucosa con tutor de silicona perdido (PY) (15); y el comprendido entre abril de 2008 hasta junio de 2014 en el que la reconstrucción de elección fue la pancreaticogastrostomía invaginada doble plano según técnica de Delcore (PG) (16). Ambas cohortes se utilizaron para comparar la morbimortalidad y la estancia postoperatoria.
Duodenopancreatectomía total (PT) cuando se extirpa la totalidad del páncreas junto con el duodeno y el bazo, por lo que no existe sutura ni borde de sección del páncreas.
Pancreatectomía distal, corporocaudal o subtotal agrupándolas como pancreatectomías (PD); dentro de ellas se clasifican en dos grupos: cirugía urgente (pancreatitis y trauma) o programada.
Pancreatectomía central (PC) cuando existe una sección del páncreas proximal y una extirpación de parte del cuerpo del páncreas con una anastomosis al yeyuno o estómago del páncreas distal. Enucleación pancreática referida a la extirpación de un fragmento mínimo del páncreas alrededor de la lesión. Los datos se presentarán según la técnica de resección pancreática y comparando el grupo de PY versus PG.
El estudio preoperatorio, técnica y cuidados postoperatorios se estandarizaron y a partir de 2008 se utilizó una vía clínica basada en un protocolo de rehabilitación multimodal postoperatoria (17) para la DPC.
Estudio estadístico
Para el análisis descriptivo se utilizaron la media con la desviación típica y la mediana con el rango. Se realizó un estudio comparativo de cohortes entre el grupo PY versus PG. Para las variables cualitativas se realizaron los test de Chi-cuadrado o Fisher y para las variables cuantitativas el test de t de Student o U de Mann Whitney. Los datos fueron analizados con un paquete estadístico SPPS 22.0s y el valor estadísticamente significativo considerado fue de p-valor 0,05 en todos los casos.
Resultados
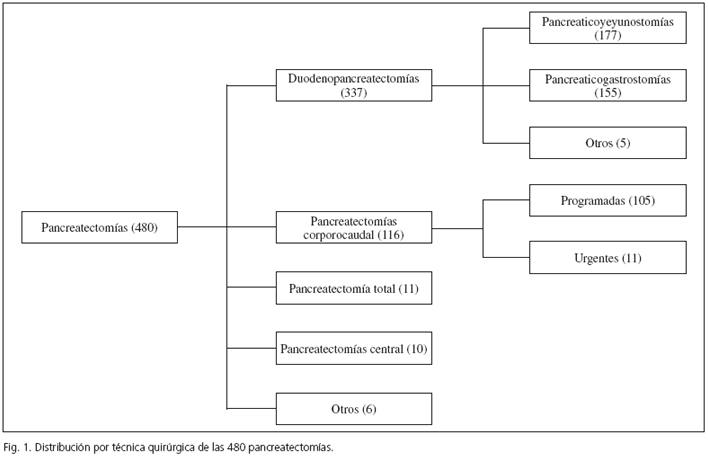
Se incluyeron 480 pacientes de los cuales se obtuvieron 5.893 datos de las 17 variables estudiadas con 207 (3,2 %) datos perdidos (128 IMC y 53 sobre grado del RVG). La técnica quirúrgica fue: 337 DPC (177 PY, 155 PG, 5 excluidos), 116 PD (11 urgentes-105 programadas), 11 PT, 10 PC y 6 enucleaciones (Fig. 1).
DPC
De las 337 DPC 5 se excluyeron del estudio por cirugía mayor asociada (2 gastrectomías totales, 2 hepatectomías mayores) y 1 por una herida por arma de fuego (Tabla II).
Los diagnósticos fueron: 119 adenocarcinomas de páncreas, 60 de papila, 34 colangiocarcinomas, 34 pancreatitis crónicas, 19 neoplasias papilares mucinosas intraductales, 17 adenomas de papila, 15 tumores neuroendocrinos, 8 adenocarcinomas de duodeno, 5 cistoadenomas serosos, 3 metástasis (2 de carcinoma renal, 1 de hemangiopericitoma), 2 cistoadenomas mucinosos, 2 cistoadenocarcinomas, 14 miscelánea (3 estenosis ampulares, 3 cánceres de colon, 2 estenosis biliares, 1 enfermedad de Castleman, 1 cáncer de vesícula, 1 cáncer gástrico, 1 linfoma, 1 hamartoma, 1 GIST duodenal).
De todas las DPC 289 (87 %) fueron por tumores: 251 (75,6 %) malignos, 33 (10 %) premalignos y 5 (1,5 %) benignos; el resto fue patología inflamatoria 43 (13 %).
Complicaciones
En 206 pacientes (62 %) hubo al menos una complicación. Las complicaciones menores fueron 121 (36,4 %) y las mayores 85 (25,5 %). De los pacientes con complicaciones mayores: 25 (7,5 %) fueron III-A (22 drenajes percutáneos, 3 embolizaciones de aneurismas de arteria visceral); 19 (5,7 %) fueron III-B (17 casos por reintervenciones y 2 procedimientos radiológicos con anestesia general); 18 (5,4 %) pacientes fueron IV-A (11 hemorragias con fallo hemodinámico -5 digestivas, 5 de arteria visceral, 1 hemoperitoneo-, 7 reintervenciones que requirieron ingreso en UCI); 12 (3,6 %) fueron IV-B (12 pacientes reintervenidos con fallo orgánico).
La mortalidad (Clavien V) fue de 11 pacientes (3,3 %) cuyas causas fueron: 5 sepsis abdominales, 3 hemorragias de arteria visceral, 1 hemoperitoneo, 1 broncoaspiración y 1 parada cardiaca por fibrilación ventricular. De los fallecidos 4 fueron reintervenidos y 4 tuvieron una fístula pancreática.
Fístula pancreática
Las FP se describen con dos clasificaciones: la ISGFP y la de Clavien. En 76 pacientes (22,9 %) se detectó una FP según la ISGPF: A 18 (5,4 %), B 27 (8,1 %), C 31 (9,4 %). Según la clasificación de Clavien: grado I-II 28 (8,4 %), III 25 (7,5 %) y IV-V 25 (6,9 %). De los 76 pacientes con FP 27 (35,5 %) fueron reintervenidos frente a 14 (5,7 %) de los que no desarrollaron FP (p < 0,001), 4 pacientes fallecieron con FP (5,2 %) frente a 7 (2,7 %) sin FP (p = 0,27), 7 pacientes con FP (9,2 %) desarrollaron una hemorragia de arteria visceral, 4 (1,5 %) sin FP (p < 0,001).
Retraso del vaciamiento gástrico
Nuestros datos anteriores a la publicación de la clasificación ISGPS fueron adaptados a la misma. En este proceso pudo estimarse en el 100 % la incidencia de RVG pero sólo en 53 casos (15,9 %) el grado. La incidencia global de RVG fue del 114 (34,3 %), siendo la complicación más frecuente. La asociación con otras complicaciones abdominales fue: FP 47 (64 %) con RVG y 67 (35,4 %) FP sin RVG (p < 0,001), 41 (36 %) abscesos intraabdominales con RVG y 27 (12,3 %) sin RVG (p < 0,001), 27 (23,6 %) reintervenciones con RVG y 14 (12,2 %) sin RVG (p < 0,001).
Reintervenciones
Hubo 41 pacientes reintervenidos (12,3 %), incluyendo las de los reingresos en los primeros 30 días, que requirieron 59 reintervenciones (28 una, 8 dos y 5 tres). Las causas, en ocasiones múltiples, fueron: 26 fístulas pancreáticas grado C, 25 hemorragias, 22 infecciones intraabdominales y 1 evisceración. La mortalidad de las reintervenciones fue de 4 pacientes (9,7 %).
Reingresos
Las causas de los 30 (9 %) reingresos fueron: 10 intolerancias digestivas, 9 hemorragias, 8 por fiebre y 3 abscesos que requirieron drenaje percutáneo.
Estancia
La estancia media fue de 20 (17,14) días con una mediana de 15 (6-144) días. En los pacientes no complicados la media fue de 10 (3,84) días, en Clavien < III 19,7 (9,03) días (p < 0,001), en Clavien ≥ III 36 (24,68) días (p < 0,001). En pacientes con FP 33,6 (23,51) días frente a 16,2 (12,3) días sin FP (p < 0,001).
Comparación entre PY y PG
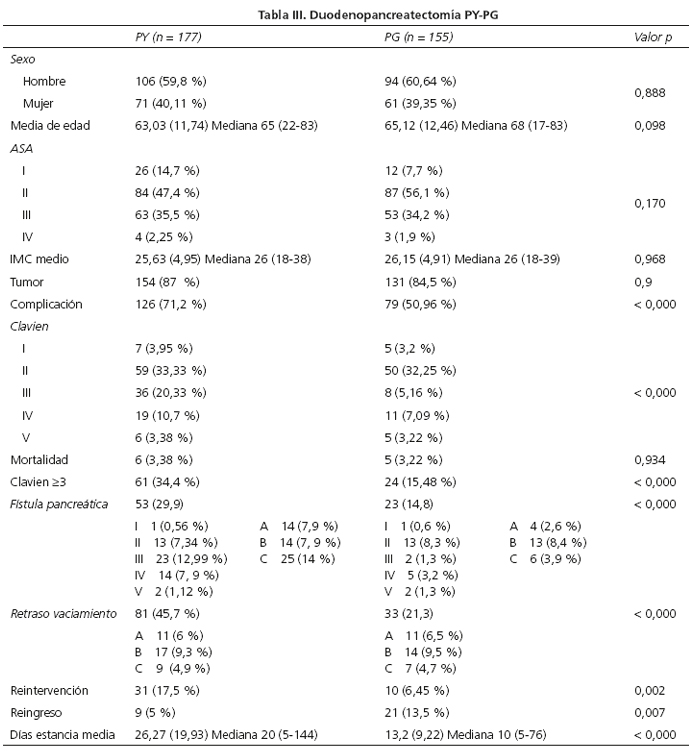
Las dos cohortes no presentan diferencias significativas en los datos demográficos, de riesgo operatorio ni de diagnóstico. Las intervenciones se realizaron por los mismos cirujanos y hubo dos diferencias en la técnica: la anastomosis pancreática (PG vs. PY), y en 87 casos (49,1 %) de pacientes con PY se realizó una preservación pilórica. En todas la PG se realizó una antrectomía (Tabla III).
La incidencia global de complicaciones fue significativamente mayor en la PY 71,2 % frente a 50,9 % en la PG (p < 0,000). Las diferencias no fueron significativas en las leves 37,2 % en la PY y un 35,5 % en la PG. Por el contrario, en las graves las diferencias sí fueron significativas; 34,4 % en la PY y 15,5 % en la PG (p < 0,000). Esta reducción en las complicaciones graves va pareja a la incidencia de FP 29,9 % en la PY y 14,8 % en la PG (p < 0,000). Las diferencias no sólo son globales sino también de gravedad de la FP (Clavien ≥ III) 22 % en PY y 5,8 % en la PG.
En cuanto al RVG las diferencias son 45,7 % en la PY y 21,3 en la PG (p < 0,000) reflejando la relación entre complicaciones abdominales y el RVG.
La mortalidad fue similar en ambos grupos 3,3 % en PY y 3,2 % en PG. La única variable en la que el grupo de las PG tiene peores resultados es en el índice de reingresos en los primeros 30 días, 13,5 % frente a 5 % en la PY (p < 0,007).
Pancreatectomías distales
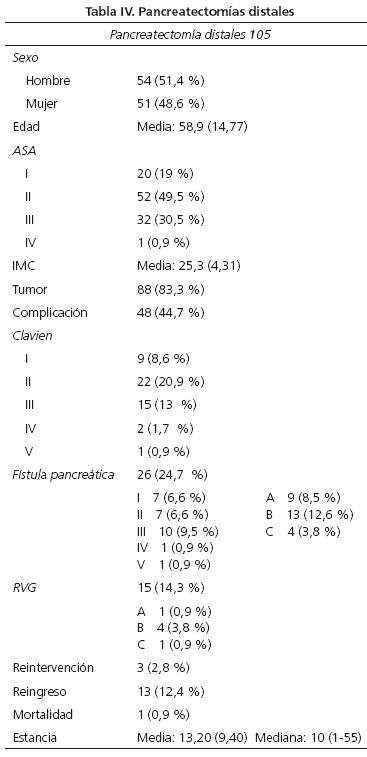
Se realizaron 116 PD: 105 programadas y 11 urgentes (Tabla IV).
Los diagnósticos fueron: 25 tumores quísticos, 22 tumores neuroendocrinos, 20 adenocarcinomas de páncreas, 17 pancreatitis crónicas complicadas, 11 asociadas a gastrectomía total, 4 asociadas a colectomía, 3 metástasis de carcinoma renal, 2 tumores sólido-papilares y 1 paraganglioma.
Complicaciones
Se incluyeron sólo las complicaciones derivadas de la PD, en 48 pacientes (44,7 %) se produjo al menos una complicación, 31 (29,5 %) fueron leves y 17 (14,7 %) fueron graves. De estas, 11 (10,4 %) fueron drenajes percutáneos de fístulas o abscesos intraabdominales. En 3 casos fue necesaria la reintervención (1 hemoperitoneo precoz, 1 absceso, 1 perforación isquémica de ciego). Hubo un caso de mortalidad por infarto de miocardio.
Fístula pancreática
Desarrollaron una FP según la clasificación ISGPF 26 pacientes -26 (24,8 %), en 4 (22 %) fue grado A o B y en 4 (3,8 %) grado C. Según la clasificación de Clavien 14 (13,2 %) desarrollaron complicaciones leves y 12 (11,3 %) graves. Siete (6,6 %) requirieron drenaje percutáneo, 3 (2,8 %) fueron reintervenidos. La fístula pancreática supuso la mitad de las complicaciones.
Hubo 13 (12,4 %) reingresos: 9 colecciones intraabdominales, 1 hemorragia de arteria visceral, 1 infarto esplénico, 1 hemorragia digestiva y 1 pancreatitis.
Se realizaron 11 (10,4 %) abordajes laparoscópicos con una conversión y 10 PD laparoscópicas: 3 con preservación esplénica y 1 con preservación de vasos. Hubo dos complicaciones: 1 FP y 1 infección de herida.
Pancreatectomía total
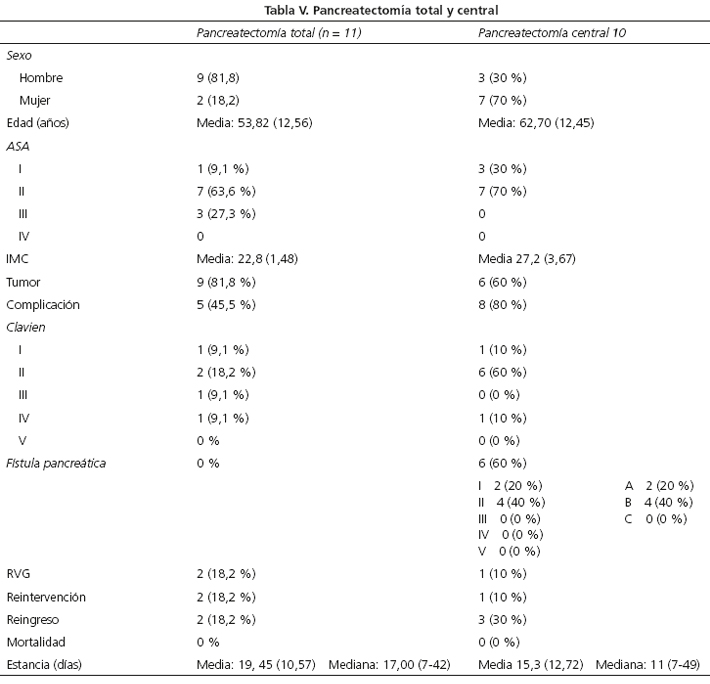
Se realizaron 11 casos: 8 por adenocarcinoma, 2 por pancreatitis crónica y 1 por un tumor neuroendocrino. La morbilidad fue inferior a la DPC y no hubo mortalidad (Tabla V).
Pancreatectomía central
Se realizaron 10 PC: 3 tumores papilares mucinosos intraductales tipo II, 4 tumores quísticos, 3 tumores neuroendocrinos. La anastomosis del páncreas distal se realizó al yeyuno en 5 ocasiones y en el resto se realizó una PG. En el 80 % hubo complicaciones, 70 % leves (Clavien I-II) todas fístulas pancreáticas o infecciones intraabdominales resueltas con tratamiento antibiótico. En 1 caso hubo una hemorragia de arteria visceral que requirió reintervención y completar la pancreatectomía distal. No hubo mortalidad. En el 30 % se requirió un reingreso por fiebre y colección intraabdominal (Tabla V).
Discusión
Esta revisión de 480 pancreatectomías, en nuestro conocimiento, es la más numerosa de las publicadas en la literatura por grupos españoles, en cuanto a número total y de DPC.
La mortalidad global de nuestra serie fue de 12 pacientes (2,5 %) y de 11 (3,3 %) en 332 DPC, datos comparables a las de otras series españolas (12,13,18,19) y extranjeras (2,20,21).
El Hospital de Bellvitge (19) publicó una serie de 204 DPC por adenocarcinoma de páncreas. En ella se utilizó la clarificación IGSPF para la FP pero no la de Clavien para el resto de complicaciones lo que dificulta las comparaciones con nuestra serie. El índice de FP fue de 10 % utilizando PY, mejor que el de nuestra serie, aunque hay que tener en cuenta que el adenocarcinoma ductal de páncreas se suele asociar a páncreas de consistencia dura y Wirsung dilatado, con menos riesgo de FP. El número de reintervenciones y la mortalidad fueron de 13 % y 7 % frente a 9,2 % y 1,5 %, en nuestra serie.
En cuanto a las DPC, la serie de Figueras y cols. (11) compara los resultados de 58 PY con 65 PG, en un estudio prospectivo randomizado utilizando la misma técnica en los dos tipos de reconstrucción pancreática que en nuestra serie. Sus conclusiones son que la PG disminuye significativamente la incidencia y severidad de la FP. Las complicaciones graves, incluyendo las dos técnicas, fueron 38,9 % frente a 25,6 % en nuestra serie. Si comparamos solo las PG 63 % y 50,9 % en nuestros casos.
La incidencia global de FP fue de 24,4 % -34 % en la PY y 15 % en la PG- (p = 0,014). En nuestra serie, 22,9 % -29,9 % en la PY y 14,8 % en la PG- (p < 0,000). En cuanto a la severidad de la FP los resultados fueron: 33 % grado B-C en la PY y 11 % en la PG (p = 0,006). En nuestra serie, 22 % en la PY y 12,3 % en la PG (p = 0,000). En ambas series coincidimos en que la PG presenta menor incidencia y severidad de FP.
En el citado trabajo, el RVG fue de 27,6 % similar entre PY y PG, a diferencia de nuestra serie, con un global de 34,3 % pero con diferencias entre PY 45,7 % y PG 21,3 % (p < 0,000). Esta diferencia puede explicarse por la relación entre las complicaciones abdominales y el RVG demostrada por otros autores (22).
El segundo estudio que puede ser comparable con nuestra serie es un ensayo clínico prospectivo randomizado multicéntrico belga de 329 DPC (23), mitad PG y mitad PG estratificado por diámetro del Wirsung (≥ 3 mm). La media de complicaciones fue de 62 %, similar a la nuestra, sin que hubiera diferencias entre los dos tipos de reconstrucción. Tampoco hubo diferencias en las reintervenciones ni en la mortalidad. La estancia hospitalaria media fue de 18,5 días sin diferencias entre grupos: en nuestra experiencia 26,7 días (19,93) para la PY y 13,2 días (9,22) para la PG (p < 0,000).
Las conclusiones del estudio belga son que la PG es más eficiente en la prevención de la fístula pancreática y en la severidad de las complicaciones aunque no en su incidencia global. Las diferencias de los resultados de la PY con nuestros resultados pueden deberse a la diferente técnica utilizada: ducto-mucosa en nuestra serie e invaginada en la belga. En un estudio randomizado se demostró que la PY invaginada era superior a la ducto-mucosa (24) lo que puede explicar las diferencias con los resultados de la serie de Figueras y cols. (11) y con la nuestra.
La FP está relacionada con la textura del páncreas y el diámetro del Wirsung y es la principal causa la morbilidad y la mortalidad postoperatoria. En la serie belga (26) la FP cuadruplica el riesgo de mortalidad y en la de Figueras y cols. (11) presenta un HR de (7,29) para complicaciones graves. En nuestra experiencia la FP está relacionada significativamente con las complicaciones graves pero no con la mortalidad.
En el estudio prospectivo randomizado de Fernández Cruz y cols. (25) los resultados son mejores que los antes citados pero la comparación puede estar sesgada por la diferencia en la técnica de la PG. Un metaanálisis de 2014 (26) resume los 7 estudios prospectivos randomizados de PY versus PG, 4 de los cuales utilizan la clasificación ISGPF. Las conclusiones coinciden con las de nuestro estudio: la PG presenta menos FP que la PY (p < 0,001).
En cuanto a los estándares de calidad, Sabater y cols. (5) realizan una elegante estudio de revisión sobre 6.336 DPC en el periodo (2000-2010) en neoplasias periampulares aplicando la clasificación ISGPS concluyendo que los límites de calidad aceptables son: < 55 % de morbilidad (no se explica según que clasificación), < 31 % de FP según la ISGPF, señalando que existen 12 definiciones diferentes de FP, y mortalidad < 5 %.
Las cuatro series citadas anteriormente (11,19,23,25), y la nuestra, cumplen los criterios de calidad exigibles si bien hay que tener en cuenta que la morbilidad total no se obtuvo de la clasificación de Clavien. Grupos españoles han publicado sus propios estándares el primero en 2002 por Figueras y cols. (27) que señala como límites una mortalidad del 10 % y morbilidad del 50 % para la DPC. En 2011 Fernández Cruz y cols. (28) hacen una revisión sobre las complicaciones de la DPC. En 2013 Domínguez-Comesaña (12) presenta la morbilidad de una serie de 117 pancreatectomías (61 DPC -58 PY-, 15 PT y 40 PD) con 59 % de morbilidad en la DPC: FP 9,83 %, RVG 9,8 %, hemorragia 16,4 %, reintervenciones 23 %, mortalidad 6,5 %. Otros dos grupos españoles han presentado series con resultados similares Sabater y cols. en 2009 (18) y Montiel y cols. 2010 (29).
En cuanto a la PD nuestra serie cumple los criterios de calidad publicados por Sabater y cols. (5) que revisa 11 series con más de 100 pacientes con unos límites de calidad aceptable de < 53 % de morbilidad, < 31 % de FP y < 1 % de mortalidad.
Una serie comprable es la de Goh (21) que en 21 años presenta 232 PD abiertas con una morbilidad de 47 %, mortalidad de 3 % y FP de 31 % (18 % A, 6 % B, 8 % C) similar a nuestros resultados.
La PC es una intervención cuyo objetivo fundamental es la preservación del páncreas en lesiones benignas o borderline. En ella se asocia la morbilidad de la PD con la de una anastomosis pancreático-entérica; esto explica nuestra elevada morbilidad 80 % (Clavien ≥ III 10 %), si bien sin mortalidad. En un estudio multicéntrico francés (30) de 100 PC con reconstrucción con PG la morbilidad fue de 72 % (Clavien ≥ III del 18 %), con 6 % de reintervenciones y una mortalidad del 3%.
Las limitaciones de nuestro estudio están relacionadas con una serie histórica en la que alguna complicación leve puede no haberse contabilizado ya que hubo que traducir las complicaciones registradas a las clasificaciones internacionales. Por otra parte, en la comparación de PY versus PG no se realizó un cálculo del volumen muestral aunque creemos que puede ser suficiente para los objetivos planteados.
Conclusiones
La serie de DPC y PG descrita es la más numerosa de las publicadas por centros españoles. Nuestros resultados cumplen con los criterios de calidad exigibles en morbimortalidad comparándolos con series actuales y con los estándares publicados. Coincidimos con los metaanálisis publicados en que la reconstrucción pancreática mediante PG presenta mejores resultados que la PY (ducto-mucosa) en cuanto a FP -frecuencia y gravedad-, complicaciones abdominales, morbilidad grave y estancia hospitalaria, aunque no mejora la mortalidad. En las PD los resultados están dentro de los estándares publicados, aunque el abordaje laparoscópico probablemente los mejorará. En cuanto a la PC coincidimos con otros grupos en que siendo una cirugía conservadora de la función pancreática presenta una elevada morbilidad por lo se debe de reservar para pacientes jóvenes y con bajo riesgo quirúrgico.
![]() Dirección para correspondencia:
Dirección para correspondencia:
Francisco Javier Herrera Cabezón
Secretaria de Cirugía General (Pabellón H-3o)
Complejo Hospitalario de Navarra-A. Irunlarrea, s/n
31008 Pamplona, Navarra
e-mail: javierherrera2004@gmail.com
Recibido: 07-10-2014
Aceptado: 23-12-2014
Bibliografía
1. Eppsteiner RW, Csikesz NG, McPhee JT, Tseng JF, Shah SA. Surgeon volume impacts hospital mortality for pancreatic resection. Ann Surg. 2009;249:635-40. [ Links ]
2. Orr RK. Outcomes in pancreatic cancer surgery. Surg Clin North Am. 2010;90:219-34. [ Links ]
3. Hartwig W, Werner J, Jäger D, Debus J, Büchler MW. Improvement of surgical results for pancreatic cancer. Lancet Oncol. 2013;14:e476-85. [ Links ]
4. Yoshioka R, Yasunaga H, Hasegawa K, Horiguchi H, Fushimi K, Aoki T, et al. Impact of hospital volume on hospital mortality, length of stay and total costs after pancreaticoduodenectomy. Br J Surg. 2014;101:523-9. [ Links ]
5. Sabater L, García-Granero A, Escrig-Sos J, Gómez-Mateo MDC, Sastre J, Ferrández A, et al. Outcome quality standards in pancreatic oncologic surgery. Ann Surg Oncol. 2014;21:1138-46. [ Links ]
6. Bassi C, Dervenis C, Butturini G, Fingerhut A, Yeo C, Izbicki J, et al. Postoperative pancreatic fistula: an international study group (ISGPF) definition. Surgery. 2005;138:8-13. [ Links ]
7. Wente MN, Bassi C, Dervenis C, Fingerhut A, Gouma DJ, Izbicki JR, et al. Delayed gastric emptying (DGE) after pancreatic surgery: a suggested definition by the International Study Group of Pancreatic Surgery (ISGPS). Surgery. 2007;142:761-8. [ Links ]
8. Wente MN, Veit JA, Bassi C, Dervenis C, Fingerhut A, Gouma DJ, et al. Postpancreatectomy hemorrhage (PPH): an International Study Group of Pancreatic Surgery (ISGPS) definition. Surgery. 2007;142:20-5. [ Links ]
9. Dindo D, Demartines N, Clavien P-A. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg. 2004;240:205-13. [ Links ]
10. Strasberg SM, Linehan DC, Clavien P-A, Barkun JS. Proposal for definition and severity grading of pancreatic anastomosis failure and pancreatic occlusion failure. Surgery. 2007;141:420-6. [ Links ]
11. Figueras J, Sabater L, Planellas P, Muñoz-Forner E, Lopez-Ben S, Falgueras L, et al. Randomized clinical trial of pancreaticogastrostomy versus pancreaticojejunostomy on the rate and severity of pancreatic fistula after pancreaticoduodenectomy. Br J Surg. 2013;100:1597-605. [ Links ]
12. Dominguez-Comesaña E, Gonzalez-Rodriguez FJ, Ulla-Rocha JL, Lede-Fernandez A, Portela-Serra JL, Piñon-Cimadevila MÁ. Morbimortalidad de la reseccion pancreatica.. Cir Esp. 2013;91:651-8. [ Links ]
13. Fernández-Cruz L, Sabater L, Fabregat J, Boggi U. Complicaciones despues de una pancreaticoduodenectomia. Cir Esp. 2012;90:222-32. [ Links ]
14. Fabregat J, Busquets J, Peláez N, Jorba R, García-Borobia F, Masuet C, et al. Tratamiento quirúrgico del adenocarcinoma pancreático mediante duodenopancreatectomía cefálica (parte 2). Seguimiento a largo plazo tras 204 casos. Cir Esp. 2010;88:374-82. [ Links ]
15. Kimura W. Pancreaticojejunal anastomosis, using a stent tube, in pancreaticoduodenectomy. J Hepatobiliary Pancreat Surg. 2009;16:305-9. [ Links ]
16. Delcore R, Thomas JH, Pierce GE, Hermreck AS. Pancreatogastrostomy: a safe drainage procedure after pancreatoduodenectomy. Surgery. 1990;108:641-5; discussion 645-7. [ Links ]
17. Lassen K, Coolsen MME, Slim K, Carli F, de Aguilar-Nascimento JE, Schäfer M, et al. Guidelines for perioperative care for pancreaticoduodenectomy: Enhanced Recovery After Surgery (ERAS®) Society recommendations. World J Surg. 2013;37:240-58. [ Links ]
18. Sabater L, Calvete J, Aparisi L, Cánovas R, Muñoz E, Añón R, et al. Neoplasias de pancreas y periampulares: morbimortalidad, resultados funcionales y supervivencia a largo plazo. Cir Esp. 2009; 86:159-66. [ Links ]
19. Busquets J, Fabregat J, Jorba R, Peláez N, García-Borobia F, Masuet C, et al. Tratamiento quirurgico del adenocarcinoma pancreatico mediante duodenopancreatectomia cefalica (Parte 1). Complicaciones postoperatorias en 204 casos en un centro de referencia. Cir Esp. 2010;88:299-307. [ Links ]
20. Van Buren G 2nd, Bloomston M, Hughes SJ, Winter J, Behrman SW, Zyromski NJ, et al. A randomized prospective multicenter trial of pancreaticoduodenectomy with and without routine intraperitoneal drainage. Ann Surg. 2014;259:605-12. [ Links ]
21. Goh BKP, Tan Y-M, Chung Y-FA, Cheow P-C, Ong H-S, Chan W-H, et al. Critical appraisal of 232 consecutive distal pancreatectomies with emphasis on risk factors, outcome, and management of the postoperative pancreatic fistula: a 21-year experience at a single institution. Arch Surg Chic Ill 1960. 2008;143:956-65. [ Links ]
22. Park JS, Hwang HK, Kim JK, Cho SI, Yoon D-S, Lee WJ, et al. Clinical validation and risk factors for delayed gastric emptying based on the International Study Group of Pancreatic Surgery (ISGPS) Classification. Surgery. 2009;146:882-7. [ Links ]
23. Topal B, Fieuws S, Aerts R, Weerts J, Feryn T, Roeyen G, et al. Pancreaticojejunostomy versus pancreaticogastrostomy reconstruction after pancreaticoduodenectomy for pancreatic or periampullary tumours: a multicentre randomised trial. Lancet Oncol. 2013;14:655-62. [ Links ]
24. Berger AC, Howard TJ, Kennedy EP, Sauter PK, Bower-Cherry M, Dutkevitch S, et al. Does type of pancreaticojejunostomy after pancreaticoduodenectomy decrease rate of pancreatic fistula? A randomized, prospective, dual-institution trial. J Am Coll Surg. 2009;208:738-47. [ Links ]
25. Fernández-Cruz L, Cosa R, Blanco L, López-Boado MA, Astudillo E. Pancreatogastrostomy with gastric partition after pylorus-preserving pancreatoduodenectomy versus conventional pancreatojejunostomy: a prospective randomized study. Ann Surg. 2008;248:930-8. [ Links ]
26. Chen Z, Song X, Yang D, Li Y, Xu K, He Y. Pancreaticogastrostomy versus pancreaticojejunostomy after pancreaticoduodenectomy: A meta-analysis of randomized control trials. Eur J Surg Oncol 2014;40:1177-85. [ Links ]
27. Figueras Joan J, Valls C, Fabregat J, Serrano T, Jaurrieta E. Equipamiento, experiencia mínima y estándares en la cirugía hepatobiliopancreática (HBP). Cir Esp. 2002;71:201-6. [ Links ]
28. Fernández-Cruz L. Pancreaticojejunostomy versus pancreaticogastrostomy. J Hepato-Biliary-Pancreat Sci. 2011; 18: 762-8. [ Links ]
29. Montiel Casado MC, Pardo Sánchez F, Rotellar Sastre F, Martí Cruchaga P, Alvarez Cienfuegos FJ. Experiencia de un programa de fast-track en la duodenopancreatectomia cefalica. Cir Esp. 2010;87:378-84. [ Links ]
30. Goudard Y, Gaujoux S, Dokmak S, Cros J, Couvelard A, Palazzo M, et al. Reappraisal of central pancreatectomy a 12-year single-center experience. JAMA Surg. 2014;149:356-63. [ Links ]











 text in
text in