INTRODUCCIÓN
Las mordeduras de animales representan un riesgo y un serio problema de salud pública para los humanos.
La Organización Mundial de la Salud1 afirma que las mordeduras de perro son de las que más riesgo y gravedad revisten, en función del tamaño del animal, lesiones producidas, estado de salud de la víctima y de la accesibilidad a la red sanitaria.
Los más vulnerables a sufrir una mordedura de perro son los niños y los ancianos. Palacio et al.2 afirman que, aunque exista variabilidad en los rangos de edad, actualmente en España los menores de 14 años tienen 4 veces más riesgo de padecer este tipo de mordeduras que el resto de población estudiada. El mayor riesgo de muerte por mordeduras lo sufren los neonatos, los bebés y los ancianos, debido a sus características específicas y a una menor capacidad de defensa3.
Para el manejo de estas lesiones, es muy importante controlar el riesgo de infección -ya que entre el 3% y el 18% contraen infecciones1- y la posible necrosis de colgajo. Williamson et al.4 recomiendan realizar un seguimiento en 24-72 horas para reevaluar la herida y valorar conjuntamente las enfermedades del paciente, la ubicación de la mordida, su complejidad y los riesgos de infección (si es bajo, la OMS1 aconseja la práctica de una sutura primaria). Asimismo, si compromete una extremidad y existe riesgo potencial de infección y/o edema5, debemos inmovilizarla y elevarla.
Actualmente, una de las opciones recomendadas para acelerar el proceso de cicatrización en las heridas agudas o crónicas es la terapia de presión negativa. En el caso descrito por Saku et al.6, este tratamiento resultó ser eficaz a la hora de combatir la infección postoperatoria después de la reparación del tendón de Aquiles de un paciente.
El objetivo principal de este caso es lograr la epitelización total de la lesión. Los objetivos específicos son: controlar la infección y carga bacteriana; evitar los efectos adversos que puedan afectar a la viabilidad del tendón expuesto; conseguir la adhesión al tratamiento y evaluar la relación coste-consecuente del tratamiento.
HISTORIA CLÍNICA
Mujer de 84 años, bien nutrida. Demencia senil y Alzheimer diagnosticada en 2017. Sin otras patologías de interés.
EXPLORACIÓN
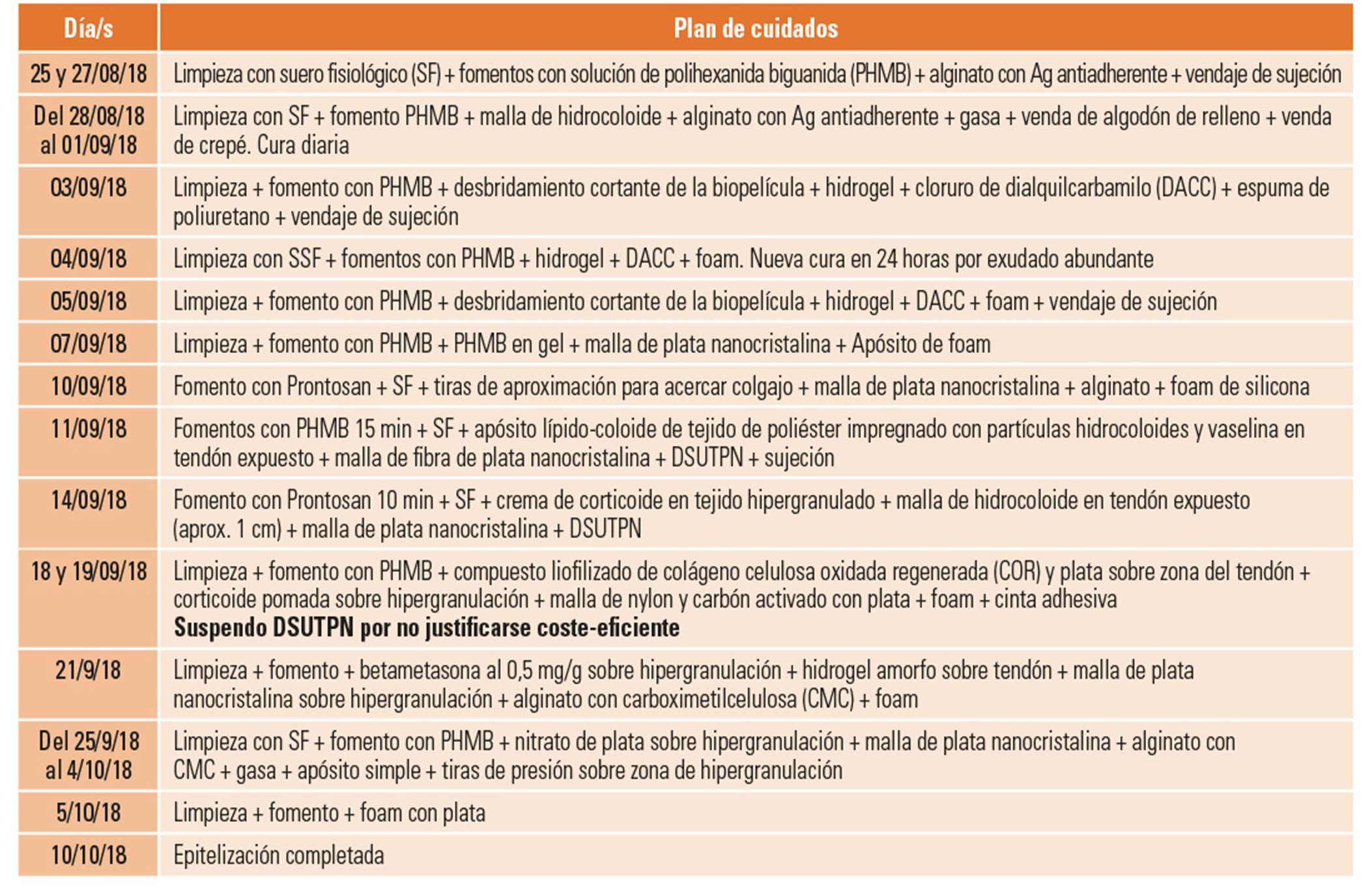
Herida avulsiva en tercio proximal de antebrazo producida por mordedura de perro, con tendón expuesto. No constan dimensiones ni profundidad en la primera valoración. En la décima cura se registra medición con hoja de evolución RESVECH 2.0 de 14 (fig. 1 A-D)7 8-9.

Figura 1. A) Lesión el primer día que abordamos la cura (03/09/2018). Se observa la presencia de tejido de granulación con un exudado abundante de aspecto serohemático, además de una biopelícula madura. Aunque los bordes están relativamente definidos, la parte inferior de la lesión es un colgajo totalmente retraído, el cual rehidratamos mediante un fomento con solución de polihexanida biguanida (PHMB) y reinsertamos definitivamente a la piel con tiras de aproximación durante 24 horas. B). En ausencia de film de poliuretano estéril, utilizamos la cara interna de la cobertura de plástico transparente de un paquete de gasas estériles. C). Con un rotulador indeleble se perfila el perímetro de la herida. D). Este mismo día, se evalúa mediante la escala RESVECH 2.0 la herida obteniendo un resultado de 14. En la imagen se muestra cómo, colocando el plástico sobre el papel milimetrado de electrocardiograma, se mide el área en cm2.
DIAGNÓSTICO
La primera visita fue del 24 de agosto de 2018, y únicamente se registró la consulta del médico de atención continuada (tabla 1).
PLAN DE ACTUACIÓN
Se puede observar la evolución de la lesión, conforme a los cuidados, en la tabla 2:
Manejo de la infección con antibiótico sistémico.
Eliminación de la biopelícula con desbridamiento seriado cada 3-4 días y apósitos antimicrobianos.
Adecuación de los apósitos secundarios a las necesidades del exudado.
Protección del tendón con apósitos de gel o gelificantes para evitar la desecación del paretenón.
Utilización del dispositivo de un solo uso de terapia de presión negativa (DSUTPN) PICO 7® tras descarga bacteriana.
Prevención y/o resolución de eventos adversos.
Educación para la salud para fomentar la adhesión al tratamiento.
TRATAMIENTO
Tratamiento inicial: limpieza con suero salino fisiológico + fomento de la herida con solución de polihexanida biguanida (PHMB) (Prontosan solución®) durante 10 minutos + alginato antiadherente con plata (Silvercell®). Entre la 4.ª y 8.ª cura se añadió malla de hidrocoloides con lípidos (Urgotul®) como apósito principal.
Abordaje de la biopelícula: limpieza + fomento con PHMB + desbridamiento cortante + hidrogel amorfo sobre tendón + apósitos bactericidas (plata nanoctristalina, Acticoat®) y/o bacteriostáticos como el cloruro de dialquilcarbamilo (DACC, Sorbact®) (fig. 2 A y B), o apósito de malla de carbón activado con plata (Actisorb®) + espuma de poliuretano + vendaje.
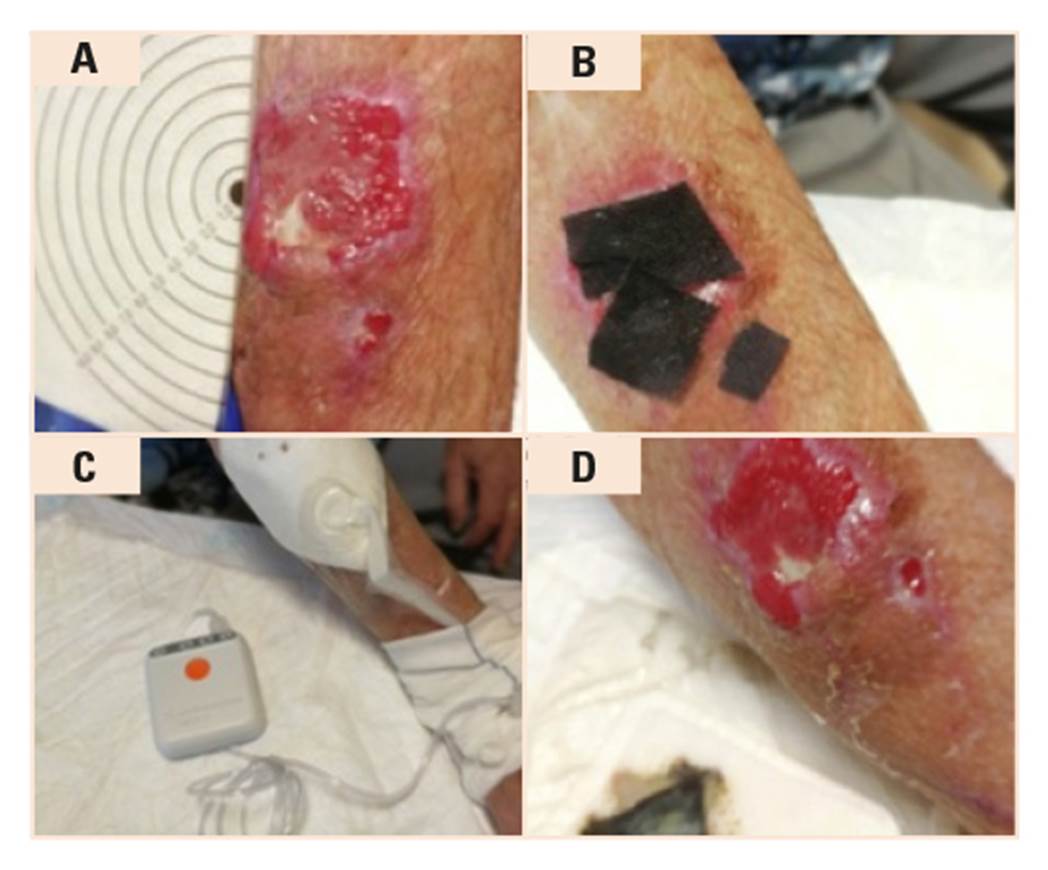
Figura 2. A) Colgajo ya reinsertado a la piel, reduciendo así la zona de tendón expuesto. B) Aplicamos apósito lípido-coloide de tejido de poliéster impregnado con partículas hidrocoloides y vaselina sobre el tendón expuesto y malla de fibra de plata nanocristalina en el resto de la lesión para evitar el crecimiento del biofilm. C) Aplicación del dispositivo de un solo uso de terapia de presión negativa (DSUTPN) para acelerar el crecimiento del tejido de granulación. D) Lesión tras 8 días de aplicación de terapia de presión negativa. Se suspende entonces el uso del DSUTPN por la aparición de tejido hipergranulado en la herida, que no se logró controlar con crema de corticoide.
Ayuda a la reparación tisular: limpieza + fomento + malla de hidrocoloide con lípidos sobre tendón + apósitos bactericidas + DSUTPN (fig. 2 C y D).
Resolución de la hipergranulación (fig. 3 A y B): se suspende la cura húmeda y se asocian apósitos bacteriostáticos a la crema de corticoide y apósito de gasa.
Ayuda a la regeneración epitelial (fig. 3 C y D): limpieza + desbridamiento cortante de la hiperqueratosis del borde + apósito de espuma con plata.

Figura 3. A y B) Evolución de la lesión tras retirar el dispositivo de un solo uso de terapia de presión negativa. La cura a partir de este momento consistió en aplicar sobre el tejido hipergranulado nitrato de plata y tiras de presión. En el resto de la lesión, utilizamos malla de plata nanocristalina y alginato con CMC. C y D) Completa epitelización de la herida.
EVOLUCIÓN
La utilización del colgajo como apósito biológico y la aplicación del tratamiento para la eliminación de la biopelícula favorecieron la epitelización total de la herida en menos de 30 días. El evento adverso fue la hipergranulación del lecho, que con la actuación llevada a cabo no llegó a comprometer la viabilidad del tendón.
DISCUSIÓN
El abordaje inicial de las mordeduras es fundamental para lograr una buena evolución. Tal como se describe en la literatura disponible, un tratamiento inicial mediante un lavado intenso con las soluciones bactericidas adecuadas5 hubiese permitido una primera cura con sutura y cierre por tercera intención que hubiese protegido el tendón expuesto y facilitado la limpieza del resto del lecho. Una temprana instauración del tratamiento antibiótico por vía sistémica habría evitado el riesgo de infección10.
El tratamiento tópico inicial (tabla 2), con mucha probabilidad, retrasó la cicatrización de la herida, pues se omitió el desbridamiento seriado de la biopelícula que recubría el lecho de la herida. La utilización de una malla de hidrocoloides con lípidos como interfase entre el lecho de la herida y el apósito antiadherente de alginato con plata, además de carecer de evidencia, pudo entorpecer el intercambio iónico de la plata con el lecho de la herida y, por lo tanto, aumentar el tamaño y virulencia de la biopelícula11.
A partir de la 9.ª cura se interrumpió tanto la variabilidad de los profesionales que realizaban la cura como de los tratamientos aplicados. Utilizar diferentes criterios de cura en un espacio de tiempo muy corto tiende a empeorar la evolución, ya que puede producirse una imitación reiterada de la pauta anterior o bien una modificación sistemática de la cura sin criterio de eficiencia12. Eliminar la variabilidad y establecer un plan de actuación de enfermería basado en la evidencia13,14 nos permitió marcar las mejores pautas clínicas para la resolución del caso.
El desbridamiento cortante de los detritos del lecho de la herida, para eliminar la biopelícula y facilitar la acción de los apósitos bactericidas, ayudó a recuperar el equilibrio bacteriano. Junto al desbridamiento, el empleo de malla de plata nanocristalina impide la reproducción de la biopelícula bacteriana11,15. En cuanto a la retracción del colgajo en la zona distal de la herida, se resolvió rehidratándolo con fomento de solución de PHMB durante 10 minutos, lo que dotó al colgajo retraído y enrollado sobre sí mismo de la flexibilidad suficiente como para poder traccionarlo y fijarlo a la epidermis sana con una tira de aproximación16. Esta operación permitió cubrir parcialmente el tendón expuesto y facilitó la aplicación del DSUTPN.
En este caso, la utilización en la herida del DSUTPN en formato de PICO 7®17, pese a las contraindicaciones incluidas en el prospecto de no aplicar sobre estructuras nobles o heridas infectadas, estuvo precedida por la descarga bacteriana. Cuando se utiliza el DSUTPN en grandes cavidades y se rellena el defecto cutáneo con espuma18,19, se protege el lecho de la herida con apósitos de malla de hidrocoloide. Aunque el dispositivo lleva incorporada una malla de silicona que impide la adherencia al lecho de la herida20, no encontramos bibliografía de su uso sobre estructuras nobles. Por el contrario, en los dispositivos portátiles de VAC, al utilizar una espuma de alcohol de polivinilo, sí que estaría descrito e indicado19. Por eso, y por evitar el riesgo de desecación excesiva del paratenón, optamos por cubrir la zona tendinosa expuesta con una malla de hidrocoloide con lípidos.
Al retirar el DSUTPN, se apreció hipergranulación en los bordes. Como coincidió con el fin de semana, se optó por aplicar una sola dosis de crema de betametasona con una concentración de 0,5 mg/g para reducir el factor inflamatorio de la hipergranulación, y se cubrió con apósitos bactericidas en combinación con otros de cura en ambiente húmedo. Esto reveló ser una mala decisión, ya que dicha combinación produjo la hipergranulación de todo el lecho. Este efecto adverso se resolvió con la utilización conjunta de crema de betametasona 0,5 mg/g y apósitos bactericidas de plata y apósitos de alginato21. En este segundo tratamiento, como apósito secundario, se evitó la cura en ambiente húmedo y se optó por la fijación con cinta adhesiva quirúrgica o apósitos simples.
La justificación de la utilización de DSUTPN en este caso viene dada por el acortamiento del tratamiento y por una mejora en la calidad de vida de la paciente22.
Existe el sesgo de que, en algunos registros, el personal de enfermería no deja constancia de la exploración de la herida. Eso dificulta la valoración de los primeros días de evolución de la lesión. Una futura línea de investigación podría ser la utilización de los DSUTPN como apósito de elección tras el estiramiento y recolocación de un colgajo de una herida avulsiva sobre el lecho de la herida.
CONCLUSIONES
El correcto abordaje inicial de la herida producida por mordedura de perro es crucial para una rápida resolución de la misma.
La variabilidad en los tratamientos aplicados ha entorpecido la correcta evolución del proceso de cicatrización. La utilización del DSUTPN ha sido coste-consecuente al disminuir el número de curas, favorecer la correcta evolución de la estructura noble expuesta y reducirle la ansiedad a la paciente.
El único efecto adverso fue la hipergranulación, que retrasó la cicatrización una semana.