INTRODUCCIÓN
La causa más frecuente de AME es debida a la alteración del gen SMN1 que codifica para la proteína de la neurona motora de supervivencia (SMN), fundamental para el mantenimiento de la neurona motora. Por otro lado, la proteína SMN puede ser sintetizada a partir de otro gen, el SMN2. El gen SMN1 está alterado en todos los pacientes siendo determinante en la enfermedad, mientras que el gen SMN2 está siempre presente en número de una a cinco copias4.
La AME se clasifica clínicamente en cuatro grandes grupos según la gravedad de los síntomas, edad de aparición yevolución2,3. En su forma más frecuente y severa denominada AME tipo I, los pacientes presentan hipotonía generalizada, nunca consiguen sedestación pasiva y fallecen antes de cumplir dos años en más del 80% de los casos, la mayoría como consecuencia de complicaciones respiratorias3,5;este grupo se divide a su vez en tipo IA, IB y IC en función del tiempo de aparición de los síntomas5.
Nusinersen es un oligonucleótido antisentido que permite al gen SMN2 producir la proteína SMN completa funcional, lo que se relaciona con la eficacia terapéutica6. Este fármaco se administra por vía intratecal siendo la dosis recomendada 12 mg por administración. Se debe iniciar lo antes posible tras el diagnóstico con cuatro dosis de carga los días 0, 14, 28 y 63, a partir de entonces se administra una dosis de mantenimiento cada cuatro meses5,6.
DESCRIPCIÓN DEL CASO
Paciente de un año y onces meses con problemas de frialdad acra desde el nacimiento.
A los cuatro meses, en la exploración neurológica, se observa debilidad generalizada; eleva los miembros superiores pero no los inferiores y no presenta reflejos osteotendinosos. La analítica presenta valores normales y el electromiograma, fibrilaciones y escasas fasciculaciones con reconfiguraciones neurógenas de unidades motoras, por lo que se solicita estudio genético objetivándose la deleción homocigota de SMN1 y la presencia de dos copias de SMN2, confirmándose el diagnóstico de AME tipo IB.
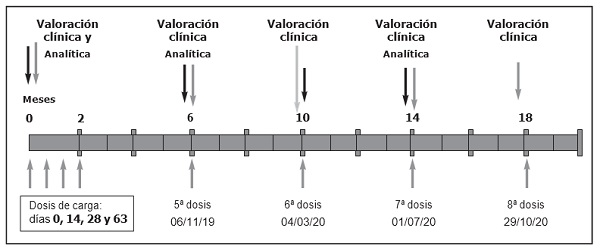
Se solicita inicio de nusinersen y, tras comprobar que cumple los criterios del protocolo farmacoclínico7, en mayo de 2019 se administra la primera dosis. A los catorce días se administra la segunda y se recomienda la colocación de dispositivo BIPAP durante la noche, comenzando durante una hora y aumentando de forma paulatina. El paciente recibe dos dosis más hasta finalizar las dosis de carga.
Continúa con la administración de nusinersen cada cuatro meses hasta que el día previo a la octava administración se detecta PCR positiva para SARS-CoV-2 en test de control, requiriendo ingreso hospitalario por presentar clínica respiratoria con aumento del diestrés y pico febril de 38,6ºC.
Al ingreso requiere aumento de soporte de BIPAP domiciliario. En radiografía de tórax se objetiva infiltrado retrocardiaco y elevación de reactantes de fase aguda, por lo que se decide antibioterapia empírica con azitromicina y ceftriaxona, previa extracción de hemocultivos. Dado el empeoramiento en su mecánica respiratoria, se determina administrar la dosis de nusinersen programada (figura 1) considerando que podría beneficiarse del mismo.
Al segundo día precisa oxígeno por lo que ante el empeoramiento de la función respiratoria, se inicia tratamiento con metilprednisolona. El día siguiente se objetiva mejoría respiratoria, alternando BIPAP y gafas nasales, en ocasiones sin soporte respiratorio, presentando estabilidad hemodinámica, buen ritmo de diuresis y manteniéndose afebril.
Al cuarto día, en hemocultivo se aísla Staphylococcus epidermidis, se cambia ceftriaxona por amoxicilina-clavulánico y se mantiene azitromicina hasta el día siguiente. El paciente permanece afebril y se retira oxígeno sin incidencias. Dada la buena evolución se decide alta a domicilio.
Actualmente el paciente tiene dos años, continúa con mejoría a nivel motor, se voltea hacia ambos lados, puede arrodillarse, sentarse y alcanza objetos. Tras el último ingreso no ha presentado infecciones, comienza la deambulación siendo capaz de mantenerse de pie con apoyo.
DISCUSIÓN Y CONCLUSIONES
En las AME tipo I nusinersen ha demostrado un efecto positivo sobre la función motora, respiratoria y la supervivencia. Sin embargo, existe una alta variabilidad en la respuesta al medicamento y no hay información sobre la eficacia a largo plazo5. Además, es uno de los fármacos con mayor coste, por ello, la financiación por el sistema nacional de sanidad se restringe para pacientes diagnosticados de AME, excluyéndose los tipos 0, IA y IV, siendo supeditado al cumplimiento de criterios de inicio, seguimiento y discontinuación de un protocolo farmacoclínico5,7.
De acuerdo al protocolo, es necesaria la valoración clínica y el cumplimiento de criterios al iniciar el tratamiento y cada cuatro meses previa administración. Estas valoraciones deben realizarse en condiciones estables del paciente, sin enfermedades intercurrentes, reflejando la situación motora y respiratoria real9. Se debe continuar administrando mientras resulte beneficioso, considerando su suspensión si se cumplen los criterios incluidos en el protocolo6,7. La tabla 1 recoge los datos de las valoraciones clínicas.
Tabla 1. Datos de valoraciones clínicas antes de iniciar el tratamiento con nusinersen y antes de cada administración.
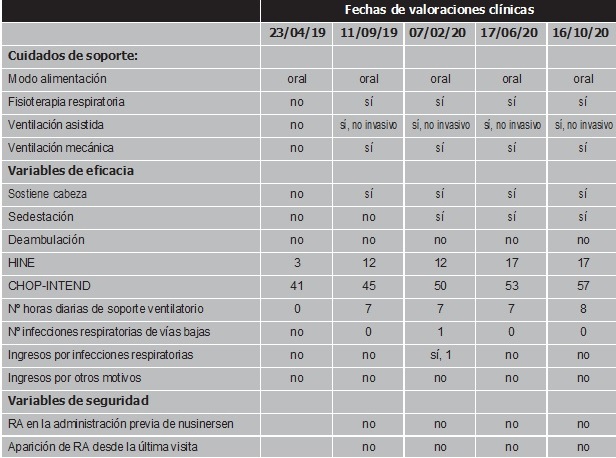
CHOP-INTEND: Children's Hospital of Philadelphia Infant Test of Neuromuscular Disorders; HINE: Hammersmith Infant Neurological Examination
El paciente ha manifestado una mejoría desde el inicio de tratamiento. La puntuación de las escalas HINE y CHOPINTEND, que evalúan la función física en pacientes con AME tipo I, han aumentado progresivamente, mantiene el número de horas con soporte ventilatorio y refiere buena tolerancia al fármaco.
En cuanto al tratamiento de SARS-COV-2 no existe evidencia para recomendar un tratamiento específico en niños.
Remdesivir ha mostrado un beneficio discreto, estando indicado en niños mayores de 12 años8,9; tocilizumab se puede plantear en pacientes graves con progresión clínica y con valores elevados de IL-6, pero no hay datos en niños menores de dos años y los corticoides sistémicos se pueden valorar en caso de shock séptico, encefalitis o fallo respiratorio agudo con necesidad de ventilación mecánica, entre otros8,10. En este caso clínico no se pauta ni remdesivir ni tocilizumab ya que no cumple los criterios de edad y se decide asociar me-tilprednisolona a dosis de 1 mg/kg/día dada la insuficiencia respiratoria, con buena resolución del cuadro infeccioso.
En nuestra experiencia, nusinersen ha mostrado un claro beneficio en la patología de base del paciente, motivo por el que se decide su administración durante el cuadro clínico por COVID-19, sin que haya supuesto un perjuicio en la evolución del cuadro infeccioso ni en su resolución positiva.