INTRODUCCCIÓN Y OBJETIVOS
El traumatismo craneoencefálico (TCE) ocasiona una elevada morbimortalidad y discapacidad neurológica entre los jóvenes1. Desafortunadamente, no se dispone de un tratamiento neuroprotector eficaz y dada la variedad de lesiones y complicaciones asociadas, la atención precoz, la monitorización multimodal en la Unidad de Cuidados Intensivos (UCI) y el manejo multidisciplinar son los pilares fundamentales para mejorar su pronóstico. El presente trabajo pretende describir la fisiopatología del TCE, los principales sistemas de neuromonitorización y el manejo terapéutico actualizado.
FUENTES UTILIZADAS Y ESTUDIOS SELECCIONADOS
Se realizó una revisión sistemática de la bibliografía publicada en los últimos diez años sobre hipertensión intracraneal (HTIC) tras sufrir un TCE y neuromonitorización en pacientes críticos. Se consultó Medline (en su versión PUBMED) y Cochrane Library, a partir de combinaciones de palabras clave y, por supuesto, las principales y más actualizadas Guías de Práctica Clínica.
SÍNTESIS DE DATOS
Fisiopatología
El daño neurológico producido por un TCE es gradual y dinámico con una fisiopatología cambiante. Tras el impacto se genera la lesión primaria, directamente relacionada con el mecanismo y la energía transferida. La cascada bioquímica inflamatoria posterior es la responsable de la lesión secundaria (LCS), la cual puede agravarse por fenómenos de isquemia, la disfunción mitocondrial y la inflamación que provoca la alteración del funcionamiento cerebral2-4.
Clasificación
La clasificación del coma de Glasgow (GCS) se utiliza para catalogar la gravedad de los TCE (tabla 1). También se utiliza la de Marshall, basada en seis hallazgos de la Tomografía Computarizada (TC)5 (tabla 2).
Tabla 1. Escala Coma Glasgow.
| DESCRIPCIÓN | VALOR | |
|---|---|---|
| APERTURA OCULAR | Espontánea | 4 |
| Al estímulo verbal | 3 | |
| Al estímulo doloroso | 2 | |
| Sin respuesta | 1 | |
| RESPUESTA VERBAL | Orientada | 5 |
| Confusa | 4 | |
| Inapropiada | 3 | |
| Sonidos incomprensibles | 2 | |
| Sin respuesta | 1 | |
| RESPUESTA MOTORA | Obedece órdenes | 6 |
| Localiza el dolor | 5 | |
| Retira al dolor | 4 | |
| Flexión anómala (decorticación) | 3 | |
| Extensión anómala (descerebración) | 2 | |
| Sin respuesta | 1 |
Fuente: elaboración propia.
Tabla 2. Clasificación de Marshall.
| Clasificación tomográfica de Marshall | |
|---|---|
| Categoría | Características |
| Lesión difusa I | No patología intracraneal visible en el TAC |
| Lesión difusa II | Cisternas presentes, pero con desviación de la línea media <0-5 mm y/o lesiones de densidad alta o mixta mayores a >25 cm3 |
| Lesión difusa III | Cisternas comprimidas o ausentes, con desviación de línea media de 0-5 mm sin lesiones de densidad alta o mixta >25 cm3 |
| Lesión difusa IV | Desviación de línea media >5 mm sin lesiones de densidad alta o mixta >25 cm3 |
| Lesión evacuada con efecto de masa V | Cualquier lesión evacuada quirúrgicamente |
| Lesión no evacuada con efecto de masa VI | Lesiones de densidad alta o mixta >25 cm3 |
Fuente: Modificado de Acad Radiol. 2014; 21(5): 605-11.
Presión intracraneal y neuromonitorización
En condiciones normales, el contenido craneal mantiene un volumen constante y se divide en tres compartimentos (teoría de Monro-Kellie): parénquima cerebral (80%), líquido cefalorraquídeo (LCR) (10%) y sangre (10%)6. Si estos compartimentos sufren un aumento brusco de su volumen, los sistemas tampón evitan, en la fase inicial, el aumento de la presión intracraneal (PIC) desplazando LCR a la cisterna lumbar y en menor cantidad, sangre a venas yugulares extracraneales. Cuando la autorregulación falla, pequeños cambios de volumen condicionan grandes cambios de PIC (figura 1). La elevación de la PIC es el primer fenómeno indicativo de la falta de perfusión cerebral.
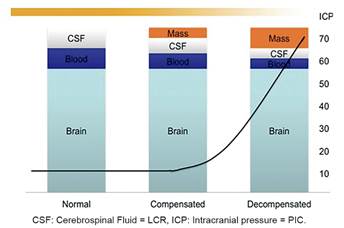
Fuente: Principle Monro-Kellie. Memorial Hermann. Misher Neurosiciences Institute. Houston.
Figura 1. Relación PIC - Volumen intracraneal.
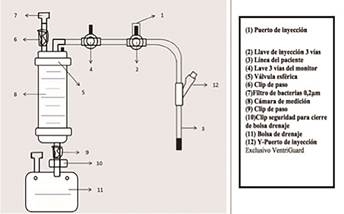
El tratamiento de esa elevación de la PIC es fundamental para reducir la mortalidad tras un TCE grave. El método de monitorización estándar es la colocación de un catéter intraventricular asociado o no a un sistema de drenaje de LCR6 (figuras 2- 4). El objetivo es mantener la PIC <20 mmHg y la PPC en torno a 60 mmHg para evitar tanto los fenómenos isquémicos como de edema cerebral. Según las Guías para el manejo del TCE grave3 (nivel recomendación IIB), la PIC debería monitorizarse en pacientes con TCE grave y TC craneal patológico (hematomas, contusiones, edema, herniación o compresión de cisternas basales) o TC craneal normal y al menos dos de las siguientes: edad >40 años, descerebración uni o bilateral o Tensión Arterial Sistólica (TAS) <90 mmHg.

Fuente: UCI Traumatología H.U. Miguel Servet.
Figura 3. Colocación y del sistema de DVE. Nivel cero y cámara de drenaje.
El valor, la morfología y los cambios de las ondas de PIC pueden alertarnos del fracaso de la autorregulación (figura 5).
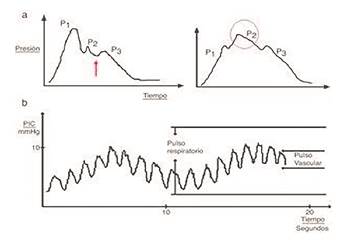
Fuente: Conceptos básicos sobre la fisiología cerebral y la monitorización de la presión intracraneal. Neurología. 2015; 30(1): 16-22.
Figura 5. Registro PIC. A. Ondas cardíacas. Elevación de P2. B. Ondas respiratorias.
El registro de las llamadas ondas cardíacas (transmisión del latido de vasos cerebrales) distingue tres improntas:
P1 (onda de percusión) representa el latido arterial sobre los plexos coroideos y refleja el flujo cerebral.
P2 (onda de Tidal) representa el LCR + Parénquima. El cambio de P2 puede alertar del fallo de la autorregulación siendo un indicador precoz de HIC.
P3 (onda dícrota) representa el latido venoso retrógrado de las venas yugulares sobre corticales.
Las ondas respiratorias (Lundberg) confieren la forma sinusoidal al registro. Se distinguen:
Ondas A o en «plateau» representan la elevación de PIC mantenida (5-20 min), de gran amplitud (50-100mmHg; pueden verse en el paciente sano, pero de forma mantenida suponen compromiso de PPC e isquemia global.
Ondas B: representan PIC <20 mmHg durante <2 min, casi siempre son variaciones reactivas del FSC (dolor puntual, aspiración de secreciones…), de amplitud 20-50 mmHg; pueden progresar a ondas A.
-
Ondas C: no patológicas (transmisión onda presión arterial)
La exploración neurológica, junto al TC y la medición de PIC, se consideran la monitorización básica y mínima. Sin embargo, aunque el registro de la PIC ofrece una visión global intracraneal, también presenta limitaciones, entre ellas, la valoración de la fosa posterior; por ello, actualmente se recomienda complementar la monitorización de la PIC (nivel recomendación III)3 con otras técnicas más específicas que ayuden a detectar el daño neurológico precozmente contribuyendo a un manejo óptimo e individualizado del TCE2-4,6-7.
Entre ellas:
-
– Medidas de flujo: regional
-
Doppler transcraneal: estudia la velocidad del flujo sanguíneo cerebral (a través de sus ventanas temporal, orbitaria, basilar/suboccipital, submandibular) permitiendo distinguir 4 estadios evolutivos o patrones de flujo:
-
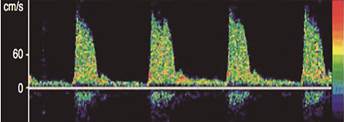
Patrón 1: PIC > TAD
La velocidad del FSC al final de la diástole es cero, persistiendo flujo solo durante la sístole. Corresponde a una situación de HTIC, considerándose un patrón de pre-paro circulatorio cerebral (figura 6).
-
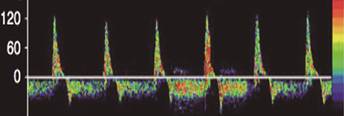
Patrón 2: PIC ≥ TAS
Flujo reverberante, oscilante bifásico o diastólico invertido. Aparece un flujo anterógrado en sístole y diastólico retrógrado o invertido, siendo el flujo neto cerebral cero. Corresponde al cese de la PPC (figura 7).
-
Patrón 3: PIC>TAS
Espigas sistólicas: pequeñas ondas sistólicas anterógradas, cortas, puntiagudas, sin flujo en sístole ni diástole. Corresponde también al paro circulatorio cerebral (figura 8).
-
Patrón 4. PIC muy elevada con obstrucción de segmento proximal de arterias de la base del cráneo o ausencia de ventana sónica. Ausencia total de señal de flujo.
Entre sus ventajas destaca ser una técnica portátil, no invasiva, a pie de cama, de alta disponibilidad, barata, no afectada por depresores del SNC ni por la hipotermia. Sin embargo, requiere una curva de aprendizaje y debería realizarse en las mismas condiciones clínicas y por el mismo experto explorador, conociendo la posibilidad de falsos positivos (HSA inicial) y negativos (craniectomía descompresiva, drenaje ventricular, fracturas base de cráneo o anoxia cerebral)8.
-
-
– Medidas de oxigenación: regional
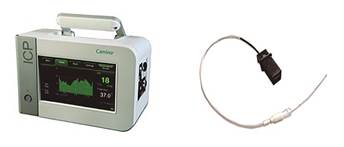
NIRS (near infrared spectroscopy) medida de saturación cerebral de O2 mediante haces luz cercanos a los infrarrojos en la piel de la línea media frontal (región arteria cerebral media ACM y anterior ACA). Consta de dos detectores, para discriminar hueso y partes blandas de tejido cerebral. La intensidad de la luz que recibe cada uno de ellos se convierte en una señal eléctrica que se procesa y digitaliza, obteniendo valores de saturación (predominantemente del lecho vascular venoso) de los dos hemisferios cerebrales actualizados cada cuatro segundos. El valor normal oscila entre 60-80% (<50% o 20% basal se considera desaturación y >85% hiperaflujo), siendo más valorable la tendencia que un valor absoluto9,10 (figura 9).
-
PtiO2 (presión tisular de oxígeno) cuantificación directa y continua de la presión tisular de O2 mediante un electrodo de Clark inmerso en una solución electrolítica y envuelto en una membrana semipermeable que puede óxido-reducir el O2 disuelto generando una corriente eléctrica proporcional (y cuantificable) a la pO2 del medio. Representa el balance entre liberación-difusión-consumo O2. Incrementa la capacidad diagnóstica de la hipoxia cerebral (PIC solo detecta hipoxia isquémica). El catéter debe ubicarse en la sustancia blanca frontal a 2 cm de la línea media entre la ACA y ACM, preferiblemente en tejido no lesionado o área de penumbra próxima a la lesión encefálica, evitando áreas contundidas y hemorrágicas, comprobando, posteriormente, la correcta colocación y ausencia de complicación con un TC.
Tras la inserción del catéter, se precisa un tiempo de adaptación (aproximadamente dos horas) para evitar mediciones artefactualmente bajas tras el microtraumatismo. La calibración del catéter del sistema Licox® es automática y precisa la temperatura, manual o de forma continua, mediante un sensor cerebral conectado al monitor. Es un sistema de fácil manejo y mantenimiento, exacto y fiable sin complicaciones relevantes en la inserción y con capacidad para detectar casi todos los tipos de hipoxia cerebral (dudosa la que bloquea la cadena mitocondrial). Se aproxima por tanto al patrón oro de monitorización de hipoxia a pie de cama; sin embargo, se trata de una medida regional, invasiva, cara, con falta de evidencia y que requiere una adecuada interpretación, en contexto de monitorización multiparamétrica y de variables fisiológicas.
Los valores normales oscilan entre 30-50 mmHg. Existe correlación entre valores bajos y mal pronóstico neurológico: hipoxia leve-moderada ≤10 y severa <5 mmHg. Una PtiO2 baja inicial no es sinónimo de isquemia, se debe comprobar la ubicación correcta, completar el periodo de adaptación y descartar malfunción del catéter con la «prueba de hiperoxia» o «de reacitividad O2» (FiO2 al 100% durante 10 minutos, incrementa rápida y notablemente la PtiO2; si no es así, considerar mal funcionamiento o microhematoma no visible en TC)6,10-12.
En caso de confirmar hipoxia, el objetivo es optimizar la liberación de O2 y disminuir su consumo: FiO2, hematocrito, viscosidad de la sangre, gasto cardíaco, normotermia, sedo-analgesia, posición a 30º, PIC… (figura 10).
-
– Medidas de oxigenación: global
-
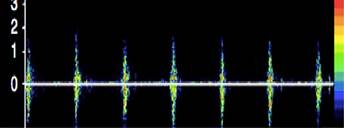
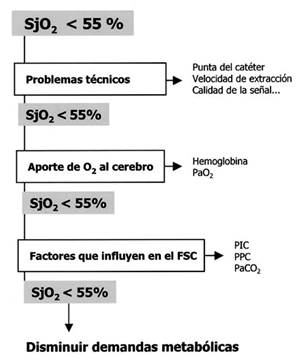
SvjO2 (saturación venosa O2 en el bulbo yugular) determina el equilibrio entre el aporte cerebral de O2 (flujo sanguíneo cerebral, FSC) y la tasa metabólica. La medición se realiza a través de un catéter de fibra óptica de doble luz, colocado en el bulbo de la vena yugular, de forma retrógrada por técnica de Seldinger. En caso de lesión focal se coloca ipsilateral a la lesión y, si es difusa, en el lado de flujo dominante (predominantemente derecho). Cuantifica el porcentaje de oxihemoglobina mediante espectrofotometría y, por tanto, el riesgo de isquemia o hiperemia cerebral permitiendo optimizar la ventilación así como otras terapias. SjvO2 es directamente proporcional al flujo FSC e inversamente proporcional consumo metabólico de O2.
El rango normal de flujo sanguíneo adaptado al consumo oscila entre 55-75%, considerándose riesgo de isquemia <55% (menor flujo, mayor consumo) y de hiperemia >75% (exceso de flujo, bajo consumo). Requiere experiencia en la técnica para obtener valores fiables y calibraciones periódicas10,13 (figura 11 y tabla 3).
-
-
– Medidas de metabolismo cerebral: regional
Microdiálisis cerebral: analiza los metabolitos (lactato, piruvato, glucosa, glutamato, glicerol…) detectados en el intersticio tisular cerebral, permitiendo conocer la eficiencia energética de ciertas rutas metabólicas y los productos de desecho de la lesión tisular. Valora la repercusión e intensidad de las alteraciones hemodinámicas y disponibilidad de oxígeno cerebral descritas anteriormente. Se compone de una sonda de doble luz, revestida con una membrana semipermeable de diálisis, por la que se perfunde una solución isotónica que permite el intercambio de sustancias a través de la membrana semipermeable, obteniéndose el microdializado. Corresponde también a una monitorización local, con implantación del catéter en zonas de riesgo de lesión secundaria y en el hemisferio no dominante en caso de lesión difusa. El incremento del ratio lactato-piruvato hace sospechar disfunción mitocondrial local y se asocia a peor pronóstico neurológico. El elevado coste de catéteres y reactivos, los recursos de personal para las mediciones y la falta de resultados de forma inmediata y continua (ofrece valores horarios) son las principales limitaciones de la técnica10,14.
-
– Medidas electrofisiológicas: global
Electroencefalograma (EEG): medida de la actividad bioeléctrica y hemodinámica cerebral. Recientemente se ha demostrado que cambios en los patrones del EEG (bandas espectrales delta, theta y alfa) se correlacionan con cambios en la PPC, es decir existe una relación entre la actividad eléctrica medida por EEG, quizá incluso más precoz, y la PIC. Es una opción de monitorización no invasiva, que a pesar de sus limitaciones y necesidad de mayor evidencia, abre puertas para futuras investigaciones15.
Otras: potenciales evocados, Resonancia Magnética, BIS, termodifusión…
-
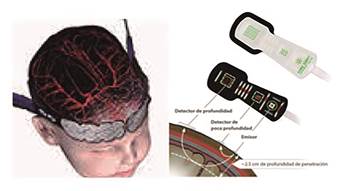
Fuente: oximetría cerebral no invasiva. Introducción y principios. Grupoaran. Sistema de oximetría tisular foresight. Edwards.
Figura 9. NIRS.
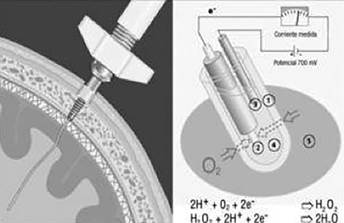
Fuente: Monitorización de la presión tisular de oxígeno (PtiO2) en la hipoxia cerebral: aproximación diagnóstica y terapéutica. Medicina Intensiva 2008; 32 (2): 81-90.
Figura 10. PtiO2. Véase el sensor insertado en sustancia blanca del lóbulo frontal. El electrodo de Clark consta de una membrana semipermeable al oxígeno (1) que recubre un cátodo (2) y un ánodo (3) bañados en una solución electrolítica (4), que a un potencial determinado genera una corriente proporcional a la p)2 del tejido (5).
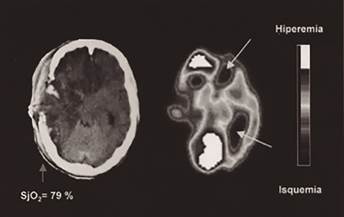
Figura 11. SatjO2. Paciente con valores de SjO2 elevados en el contexto de una lesión cerebral postraumática.
Manejo inicial del TCE
La asistencia inicial al politraumatizado comienza a nivel extrahospitalario aplicando los estándares establecidos de soporte vital avanzado al traumatismo (ATLS) y medidas de neuroprotección precoz, que continuarán durante el traslado hasta el hospital más útil (salvo lesiones de riesgo vital que será hasta el hospital más cercano). Aunque inicialmente no precisen tratamiento neuroquirúrgico, los pacientes que han sufrido TCE deben ser manejados en hospitales con capacidad neuroquirúrgica y de neuromonitorización en UCI4,6,7.
Medidas
Generales
Las principales medidas generales en las que hacer hincapié son:
– Soporte hemodinámico. Se desaconseja la hipotensión permisiva tras TCE grave o lesión medular aguda por influencia deletérea sobre la LCS. Valorar la necesidad de vasopresores y/o inótropos si persiste TA media < 80 mmHg y/o compromiso de la contractilidad cardíaca16.
– Soporte respiratorio. Se recomienda intubación y ventilación mecánica invasiva. Normalizar la oxigenación (SaO2> 90%, PaO2> 80mmHg), evitando hipoxemia e hiperoxia y la ventilación (ph 7,35-7,45 y pCO2 35-40 mmHg).
– Control metabólico: normoglucemia (110-180gr/dl), normonatremia. Mantener normovolemia. Preferibles soluciones salinas fisiológicas frente a coloides. Se desaconsejan soluciones hipotónicas en la resucitación16.
-
– Evitar los corticoides. Estudio CRASH 1.
Ácido tranexámico (ATX). El reciente Estudio CRASH 3 proporciona evidencia de que el ATX (bolo intravenoso de 1 gramo en 10 minutos y perfusión de 1 gramo en 8 horas) es seguro en pacientes con TCE y que su administración dentro de las 3 horas de la lesión reduce las muertes relacionadas con lesiones craneales, principalmente lesiones leves y moderadas, sin reducción aparente en aquellos con lesiones graves17,18,19.
Nutrición enteral precoz tras resucitación inicial y estabilización clínica a razón de 25-30 kcal/día con aporte de 1,2-2 gr/kg de proteínas20.
Protección ocular.
Higiene cavidad oral.
Profilaxis del sangrado digestivo con inhibidores de la bomba de protones.
Primer nivel6
Optimizar el retorno venoso yugular
– Cabecero de la cama a 30-45º y posición neutra cabeza. Si embarazada, decúbito lateral izquierdo.
– Evitar maniobras que aumenten la presión torácica (más si PEEP elevada) y abdominal: permeabilidad de sonda vesical, nasogástrica, uso de relajantes musculares, laxantes o descompresión si se sospecha hipertensión abdominal.
Disminuir el consumo metabólico cerebral
– Sedación y analgesia óptimas, asociada a relajación muscular si precisa20.
– Normotermia.
Mejorar la oxigenación cerebral
– Hiperventilación moderada pCO2 25-30 mmHg (hiperventilación intensa pCO2≤25 mmHg contraindicada las primeras 24h por riesgo de isquemia cerebral; si es posible monitorizar la oxigenación cerebral con SvjO2 o PtiO2).
– Saturación O2 > 90% y PaO2 > 80 mmHg.
– Normoperfusión: mantener Hto 30-33% y Hb 8-10g/dl, con necesidad de trasfusión si sangrado masivo o Hb <7-8gr/dl. Descartadas otras causas de hipoxia, la neuromonitorización avanzada (PtiO2 <15 mmHg, SvjO2<55-60%), las comorbilidades y la situación extracraneal podrían contribuir a la toma de decisiones en caso de incertidumbre transfusional y controversia por falta de evidencia, como es el caso de niveles de Hb 8-10g/dl21.
Disminuir el edema cerebral
-
– Solución hiperosmolar (osmoterapia): recomendado en bolos intermitentes durante 20’ si HTIC, signos herniación transtentorial o deterioro neurológico progresivo no extracraneal, manteniendo una osmolalidad plasmática < 320 mOsm/kg y la natremia <155 mEq/l.
Manitol 20% iv: 0,5-1 g/Kg iv en 15 minutos. Expansor del plasma y diurético osmótico. Riesgo de hipovolemia por poliuria e hipernatremia; edema cerebral de rebote, insuficiencia cardíaca y nefropatía osmótica son menos frecuentes.
Suero salino hipertónico (SSH) iv al 3%, 7,2%, 20% o 23,4%: 0,5 ml/kg. Riesgo de hipervolemia e hipernatremia. Los últimos metaanálisis revelan mayor efectividad de SSH en HTIC refractaria por su efecto más sostenido sobre PIC y mayor efectividad sobre PPC22-23.
Drenaje ventricular externo: permite monitorización de PIC y drenaje de LCR si precisa.
Profilaxis anticonvulsiva precoz: durante los primeros 7 días (p.e.j: Levetiracetam)4,6.
Segundo nivel6
Medidas de rescate que deben ser individualizadas y monitorizadas. No son medidas profilácticas de neuroprotección precoz ni deben plantearse como medidas de rutina; solo valorar en casos de HTIC refractaria a tratamiento médico y quirúrgico máximos (tabla 5).
Tabla 4. Nivel de lesión cerebral y su expresión neurológica (reflejo fotomotor, oculocefálico y respuesta motora).
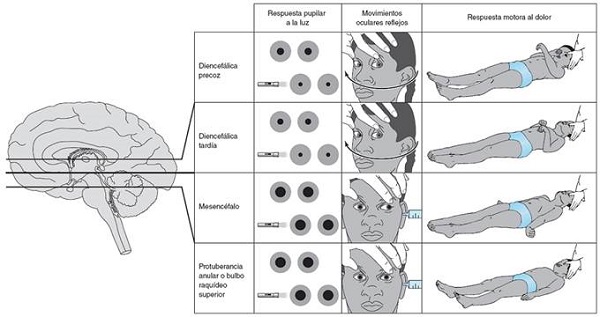
Fuente: Roger P et al. Neurología clínica, 7e.
Tabla 5. Medidas de primer y segundo nivel en el TCE.
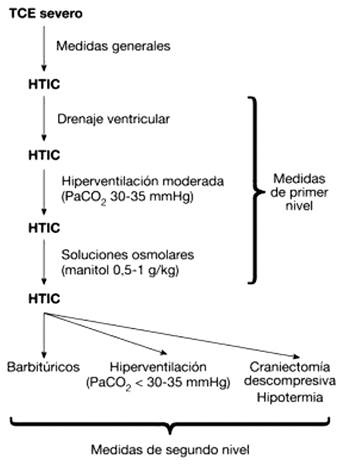
Fuente: Actualizaciones en el manejo del traumatismo craneoencefálico grave. Med Intensiva. 2009; 33(1): 16-30.
Coma barbitúrico: depresor del SNC por estímulo del inhibidor GABA que protege al cerebro de isquemia optimizando el consumo O2, FSC y PIC. Riesgo de hipotensión arterial, inmunodepresión e infección.
Hiperventilación intensa: PaCO2 <30 mmHg. Solo en una situación crítica de herniación cerebral.
Hipotermia moderada (32-35 °C): Controversia. Los últimos estudios revelan que los TCE graves con PIC elevada podrían beneficiarse de la hipotermia terapéutica en las primeras 24 h, sin embargo, se requiere más investigación para recomendar estos resultados24,25.
Cirugía: Craniectomía descompresiva (CD) promete reducir la mortalidad pero, desgraciadamente, en muchos casos a costa del incremento de la discapacidad y un pronóstico neurológico controvertido o desfavorable. Es fundamental valorar de forma individual a cada paciente mediante una adecuada exploración (edad, comorbilidades, presentación clínica, signos neurológicos al inicio y progresivos), pruebas de neuroimagen (presencia de lesión evacuable, localización y tamaño de la lesión, signos de HTIC, deslizamiento de línea media, edema cerebral) y, por supuesto, la neuromonitorización multimodal. Todo ello ayudaría a predecir los candidatos con mayor probabilidad de beneficio y calidad de vida tras CD y el momento óptimo para realizarla.
En caso de estar indicada, debería realizarse de forma precoz. Se recomienda CD frontotemporoparietal grande (no menos 12 × 15 cm o 15 cm de diámetro) sobre frontotemporoparietal pequeña para reducir la mortalidad y mejorar los resultados neurológicos2,4,26-28.
Se espera que el ensayo randomizado RESCUE-ASDH (Randomised Evaluation of Surgery with Craniectomy for patients Undergoing Evacuation of Acute SubDural Haematoma), en curso, ofrezca nuevos resultados.
Hematomas extraparenquimatosos (tabla 6 y figura 12)
Tabla 6. Hematoma subdural y epidural.
| HEMATOMA SUBDURAL | HEMATOMA EPIDURAL | |
|---|---|---|
| FRECUENCIA | +++ | + |
| LOCALIZACIÓN | Entre duramadre y cerebro | Entre cráneo y duramadre |
| EDAD | Ancianos | Joven |
| PRONÓSTICO | Mal pronóstico por edema Elevada mortalidad y limitación fx | Mejor pronóstico |
| MECANISMO LESIÓN | Caídas | Traumatismos de alta energía (fractura temporal frecuente) |
| LESIÓN VASCULAR | Vena seno sagital superior | Arteria meníngea media |
| DETERIORO NEUROLÓGICO | Rápido desde inicio | Intervalo lúcido tras pérdida de conciencia |
| TC CEREBRAL |
Colección media luna Cruza suturas (no confinado) No pasa hoz ni tentorio |
Masa biconvexa bien definida No cruza suturas (confinado) Pasa hoz cerebral y tentorio |
| TRATAMIENTO | Craneotomía y evacuación urgente (según GCS, tamaño hematoma y desplazamiento línea media) | |
Fuente: elaboración propia.
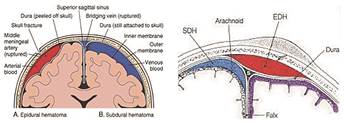
Fuente: Radiology department Abd Fares epidural and subdural hematomas.
Figura 12. Hematoma epidural (rojo) y subdural (azul).
Con frecuencia, el TCE grave conlleva la aparición de hematomas extra (subdural, epidural) o intraparenquimatosos que causan elevada morbimortalidad por el impacto de la lesión secundaria. A pesar de los avances, sigue sin haber consenso universal ni, por tanto, grandes cambios en el manejo de estos hematomas en los últimos años, por lo que la decisión de tratamiento conservador inicial o evacuación quirúrgica urgente, bien sea mediante craneotomía o craniectomía, y el momento siguen siendo controvertidos y dependientes de factores clínicos, neurológicos y radiológicos.
La neurocirugía urgente precoz se realiza, fundamentalmente, en hematomas epidurales y subdurales agudos; la tardía se relaciona más con el deterioro clínico, crecimiento de los hematomas durante el seguimiento en UCI o la PIC refractaria a medidas iniciales.
Se recomienda intervención quirúrgica urgente (craneotomía + evacuación) de los hematomas subdurales de grosor >10mm o desviación de línea media >5 mm, deterioro neurológico o GCS<9 y/o HTIC (PIC>20 mmHg)29-31. En el caso de los epidurales si el volumen del hematoma >30 ml, independientemente del GCS, deterioro neurológico o GCS <9 y/o anisocoria32.
CONCLUSIONES
La morbimortalidad que generan las lesiones neurológicas derivadas de un TCE grave suponen un importante problema a nivel mundial, sobre todo entre los más jóvenes.
El manejo de la HTIC requiere una valoración individualizada multidisciplinar y dinámica, clave para prevenir nuevas lesiones cerebrales. Desafortunadamente, no se han experimentado grandes cambios, a pesar de los numerosos ensayos clínicos, llevados a cabo en los últimos años.
Conocer en profundidad la fisiopatología de la lesión cerebral y aplicar la neuromonitorización multimodal específica puede guiar en la instauración del tratamiento adecuado a tiempo y mejorar el pronóstico neurológico del paciente crítico.