INTRODUCCIÓN
El tejido óseo tiene la capacidad de adaptarse a los estímulos del entorno mediante la alteración de su morfología y de su metabolismo1.
La formación, la remodelación y la reparación del tejido óseo son procesos dinámicos regulados por la acción conjunta de las células óseas (osteocitos, osteoblastos y osteoclastos). Los osteocitos son el tipo celular más abundante en el hueso. Se localizan en la matriz ósea mineralizada, formando una extensa red de intercomunicación celular, denominada sistema lacuno-canalicular osteocitario (SLCO). Los osteocitos son las principales células mecanosensoras del hueso2, es decir, son capaces de detectar los estímulos mecánicos de su entorno y comunicar dicha señal a las células efectoras (osteoblastos y osteoclastos). Presentan diferentes estructuras mecanosensoras: los canales iónicos, las integrinas3, el ligando del receptor de la parathormona tipo 1 (PTH1R), las conexinas4 y el cilio primario. Se ha constatado que algunos de estos mecanosensores interactúan entre sí, permitiendo la integración de las múltiples señales extracelulares3.
El estímulo mecánico regula la remodelación ósea. La desregulación de este proceso produce osteoporosis, una patología que se caracteriza por la disminución de la masa ósea y el aumento de su fragilidad5.
Los osteocitos responden al estímulo mecánico gracias a la activación de diversas vías de señalización, como la proteína tipo Wingless (Wnt)/β-catenina, y las proteínas quinasas activadas por mitógenos (MAPK) y Hedghog (HH). En este trabajo se analizan algunas moléculas que intervienen en estas vías de señalización, específicamente la P-ERK y la ERK.
Para el mantenimiento de la homeostasis del tejido óseo es fundamental la interacción entre las células que lo conforman6. La comunicación celular a través de uniones comunicantes (UCs) es una de las más importantes, permitiendo la interacción entre los citoplasmas de células adyacentes y, por tanto, la difusión intercelular de moléculas pequeñas7. Las UCs no solo sirven como canales pasivos, también intervienen en la regulación de diferentes rutas de señalización8.
Las Cxs son proteínas transmembrana que se denominan por su peso molecular, de 26 a 59 kDa. La Cx43 es la proteína más abundante en las UCs de las células óseas. Las conexinas, en particular la Cx43, interactúan con las moléculas estructurales y de señalización, regulando las funciones celulares9,10.
El cilio primario es una estructura basada en microtúbulos; en el que se localizan numerosos canales y proteínas receptoras, que permiten la actuación del cilio como mecanosensor11,12. El PTH1R es un receptor acoplado a proteínas G (GPCR), que se expresa en los cilios primarios y tiene un papel fundamental en la transducción de señales mecánicas en células MLO-Y413. Este receptor presenta dos ligandos ampliamente caracterizados: la PTH y la PTHrP (proteína relacionada con la parathormona). Tanto la PTH como la PTHrP tienen efectos en la formación ósea y son utilizados como agentes anabólicos en el tratamiento de la osteoporosis13,14.
También se ha demostrado que la estimulación por PTHrP y la estimulación mecánica por flujo de fluido inducen la activación de ERK, impidiendo así el aumento de la apoptosis de células osteocíticas15.
En el presente estudio se hipotetizó que el cilio primario y la Cx43 actúan de manera conjunta en la regulación de vías de señalización implicadas en la supervivencia celular y en la capacidad de adhesión celular. Se determinó la expresión del cilio primario, tanto en células Cx43+/+ como en Cx43-/- y la no colocalización de estos dos mecanosensores. Por tanto, se sugiere que la deficiencia en Cx43 no está involucrada en el desarrollo del cilio primario, pero sí podría influir en otros aspectos, como su funcionalidad, longitud o en el transporte intraflagelar.
Asimismo, se analizó la respuesta celular de los osteocitos (fosforilación de ERK) tras estimular el PTH1R, tanto con PTHrP, obteniéndose un mayor aumento de P-ERK en las células Cx43-/- respecto a Cx43+/+, como mecánicamente, que produjo un aumento de la expresión de P-ERK independiente de la deficiencia en Cx43.
MATERIALES Y MÉTODOS
1. Cultivos celulares
En este proyecto se trabajó con la línea continua de osteocitos MLO-Y4 de huesos largos murinos Cx43+/+, utilizadas como control, y deficientes en Cx43 (Cx43-/-), que fueron cedidas amablemente por la Dra. L. I Plotkin. Dichas células se sembraron a una concentración de 24.000 células/cm2. Se cultivaron con el medio ɑ-Modified Eagle´s Medium (ɑ-MEM) (GibcoTM, Thermo Fisher Scientfic, España), suplementado con 2,5% de suero de ternero (Calf Serum; CS), 2,5% de suero fetal bovino (Fetal Bovine Serum; FBS), 1% de L-Glutamina, 1% de Penicilina/Estreptomicina y Puromicina (de Streptomyces alboniger, Sigma Aldrich, BioReagent, Merck, España) a una concentración 10 μg/ml.
Para favorecer el desarrollo del cilio primario, las células se cultivaban en medio de depleción, compuesto por ɑ-MEM (GibcoTM) suplementado con 1% de penicilina/estreptomicina y puromicina a una concentración de 10 μg/ml, durante 24 h.
Todas las superficies sobre las que se sembraron estas células debían estar previamente colagenizadas, con colágeno tipo I al 0,01% de ácido acético, para simular la matriz de colágeno donde se encuentran embebidos los osteocitos in vivo. Las células se mantuvieron a 37ºC y 5% de CO2.
2. Western blot
Se extrajo la proteína total de las células empleando el buffer RIPA (Sigma-Aldrich, Merck, España), suplementado con inhibidores de proteasas y fosfatasas (Calbiochem, Merck, España).
Posteriormente, se procedió a la cuantificación de proteínas mediante el ensayo de ácido bicinconínico (BCA) (PierceTM BCA Protein Assay Kit, Thermo Fisher Scientfic, España), que genera una reacción colorimétrica detectable a 562 nanómetros (nm). Para realizar la lectura se utilizó el lector de placas Varioskan Flash (Thermo Fisher Scientfic), mediante el programa SkanIt Software 2.4.3 RE.
Los extractos de proteína (20 μg) se separaron mediante un gel de poliacrilamida al 10%, en condiciones reductoras; posteriormente se transfirieron a una membrana de nitrocelulosa (Bio-Rad, Hercules, California, EE.UU.). El bloqueo se realizó con leche en polvo al 5%, en tampón Tris salino con Tween20 (TTBS) al 0,05%, durante 1 h en agitación a temperatura ambiente. A continuación, se pusieron en agitación entre 15-18 h y 4ºC los siguientes anticuerpos primarios: anti-Phospho-p44/42 MAPK (Erk1/2) (Cell Signaling, Beverly, Massachusetts, EE.UU.), anti-p44/42 MAPK (Erk1/2) y anti-Cx43 (Sigma Aldrich, ST. Louis, Misuri, EE.UU.) y anti-tubulina (Sigma Aldrich). Todos son anticuerpos policlonales producidos en conejo, menos la anti-tubulina que es monoclonal producido en ratón. Después se incubó durante una hora a temperatura ambiente, con la correspondiente IgG acoplada a peroxidasa, y se reveló la membrana mediante quimioluminiscencia con el sustrato ClarityTM Western ECL (Bio-Rad, Life Science Research, España). La intensidad de las bandas se cuantificó por densitometría, usando DNR Bio Imaging System MF ChemiBIS3.2 y los programas Gelcapture y QuantityOneTM (Bio-Rad).
3. Inmunofluorescencia
Se sembraron 30.000 células/pocillo de las placas multipocillo (Falcon®, Thermo Fisher Scientfic, España). Las células se crecieron hasta que alcanzaron una confluencia del 80%; y posteriormente se añadió medio de depleción durante 24 h para inducir la formación del cilio primario. Después, las células se fijaron con paraformaldehído (PFA) al 4% y se permeabilizaron con Tritón X-100 al 0,5%. Seguidamente, se añadió la solución de bloqueo, compuesta por albumina de suero bovino (BSA) al 10%, suplementado con suero de cabra al 5%, durante 1 h. Posteriormente, se mantuvieron en agitación durante 15-18 h a 4ºC los siguientes anticuerpos primarios: anti-Cx43 policlonal producido en conejo (Sigma Aldrich) y anti-ɑ tubulina acetilada monoclonal producido en ratón (Sigma Aldrich), para observar así el cilio primario. A continuación, se dispusieron los anticuerpos secundarios: para cilio Alexa fluor® 488 de cabra anti-ratón (Invitrogen Molecular probes, Thermo Fisher ScientificTM, España), y para Cx43, Alexa fluor® 568 anti-conejo IgG (Life technologies, Thermo ScientificTM, España) (dilución 1:1000 en BSA al 10% y suero de cabra al 5%). Tras 1 h de incubación, se añadió 4´-6-diamidino2-fenilindol (DAPI). Los núcleos, el cilio primario y la Cx43 se visualizaron con el microscopio de fluorescencia (Leica CTR 6000). La fusión (merged) de las imágenes individuales del cilio primario, la Cx43 y núcleos celulares en una sola se realizó con el programa ImageJ.
4. Estimulación mecánica mediante flujo de fluido (fluid flow) y por PTHrP
Para realizar la estimulación mediante flujo de fluido (FF) y PTHrP, las células se sembraron en portaobjetos de cristal delimitados con teflón a una densidad de 25.000 células/cm2. La técnica del FF se basa en bombear medio de cultivo de forma constante sobre la monocapa celular, en un circuito cerrado herméticamente, a 10 dinas/cm2 durante 10 min, mediante una bomba peristáltica (Flexcell International Corp., Hillsborough, Carolina del Norte, EE.UU.). Las configuraciones del tiempo y frecuencia se establecieron a través del programa Master Flex Peristaltic Pump 2010. Por otro lado, se realizó la estimulación con PTHrP (1-36) (Bachem, Bubendorf, Switzerland) a una concentración de 10-7 molar (M), durante 10 min. El mismo número de portaobjetos se cultivó con células que no fueron sometidas a ningún estímulo, constituyendo los controles estáticos (CE).
5. Análisis estadístico
En el análisis estadístico de los resultados, los datos se expresan como media ± desviación estándar de al menos dos experimentos llevados a cabo por triplicado. Se realizó utilizando el programa GraphPad Prism 8 (software GraphPad, La Jolla, California, EE.UU.). Para comparar medias entre dos grupos se llevó a cabo el test no paramétrico Mann-Whitney, y para comparar medias de más de dos grupos se empleó el test no paramétrico Kruskal-Wallis. Los análisis múltiples se llevaron a cabo mediante el test de Dunn. En todos los test estadísticos el intervalo de confianza establecido fue del 95%. Por tanto, se consideraron estadísticamente significativos los resultados con un valor de p<0,05.
RESULTADOS
1. Efecto de la Cx43 en el desarrollo del cilio primario en células Cx43+/+ y Cx43-/-
Los resultados obtenidos mediante Western blot nos indican que en las células deficientes en Cx43 la expresión de esta proteína disminuye significativamente con respecto a las células control Cx43+/+ (W=0, p=0,029), lo que nos permite corroborar la deficiencia de esta proteína (Figura 1). Además, se caracterizó la presencia del cilio primario mediante el análisis de expresión de la proteína IFT88. Se empleó IFT88 como marcador de la presencia de cilio primario, dado que es una proteína que se expresa de manera muy abundante en este orgánulo, debido a que está involucrada en el transporte intraflagelar, necesario para la ciliogénesis18. Se observó que la proteína IFT88 se expresa de forma similar, independientemente de la deficiencia en Cx43 (W=4, p=0,343).
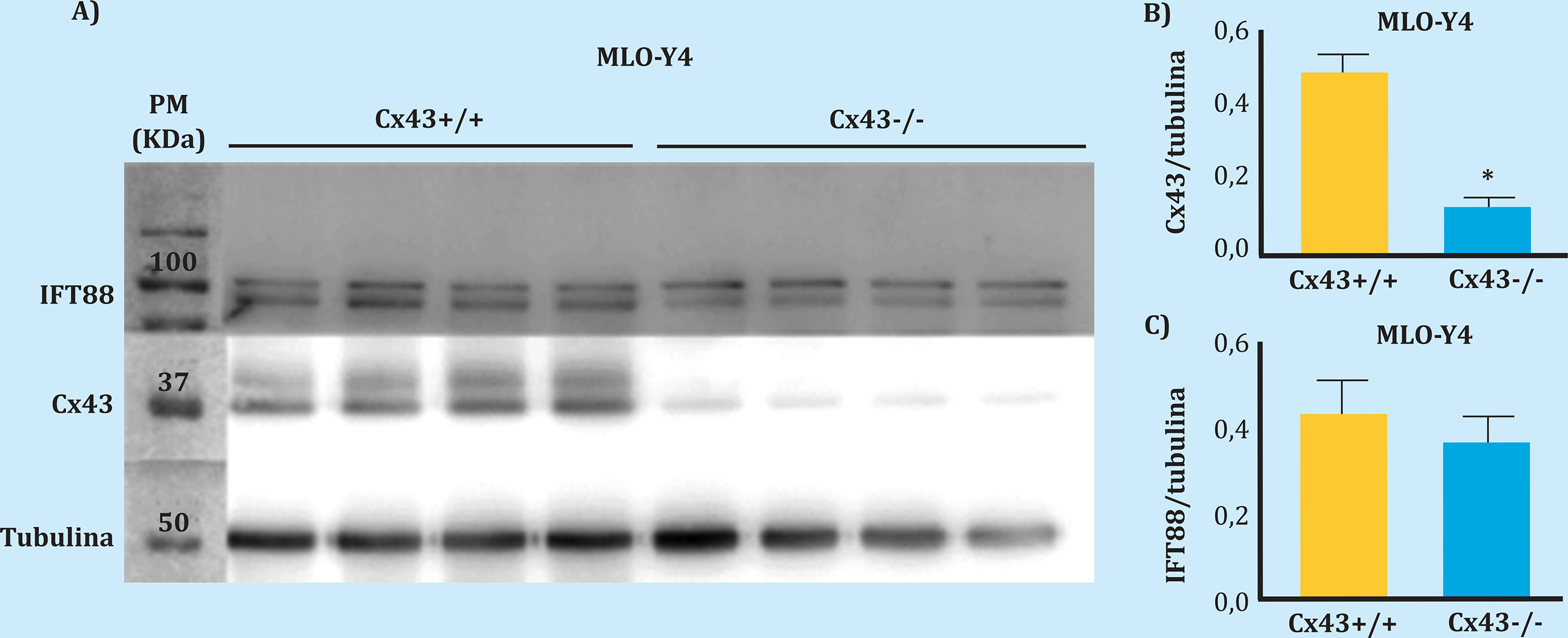
Figura 1. Expresión de Cx43 e IFT88. A) Resultado del revelado de la membrana de nitrocelulosa para el análisis de Cx43, IFT88 y tubulina como control de carga, se utilizaron extractos de proteínas celulares totales (25 µg). En el primer carril se dispuso el marcador de peso molecular (PM); los cuatro carriles siguientes pertenecen a cuatro réplicas de células MLO-Y4 control (Cx43+/+) y los cuatro últimos corresponden a cuatro réplicas de células MLO-Y4 deficientes en Cx43 (Cx43-/-). B) Promedio ± desviación estándar de Cx43/tubulina. C) Promedio ± desviación estándar de IFT88/tubulina. Los niveles proteicos se normalizaron frente a tubulina *p<0,05
Asimismo, se analizó la Cx43 y el cilio primario mediante inmunofluorescencia para intentar determinar la posible interacción entre estos dos mecanosensores. La figura 2 muestra que tanto las células Cx43+/+ como las Cx43-/- desarrollan cilio primario, que se evidencia por la presencia del anticuerpo primario anti α-tubulina acetilada, y que este orgánulo se origina desde la superficie celular. También, se puede ver que la Cx43 se expresa fundamentalmente en la membrana celular, por lo que posiblemente se encuentre formando UCs. Además, parece observarse que el cilio primario no colocaliza con la Cx43. Por otra parte, se realizaron contajes de las células que presentaban cilio primario, a partir de nueve fotografías tomadas en distintos campos, con el microscopio de fluorescencia. En cada imagen se cuantificó el número (Nº) de células (cel.) totales y el número de células que presentaban cilio primario, y se calculó el cociente (Nº de cel. con cilio/Nº de cel. totales), tanto para la línea celular Cx43+/+ como para Cx43-/- (Tabla 1 y figura 3). En estos resultados se constató que el número de cilios formados no difería significativamente (p=0,089) entre las dos líneas celulares (Cx43+/+ y Cx43-/-).
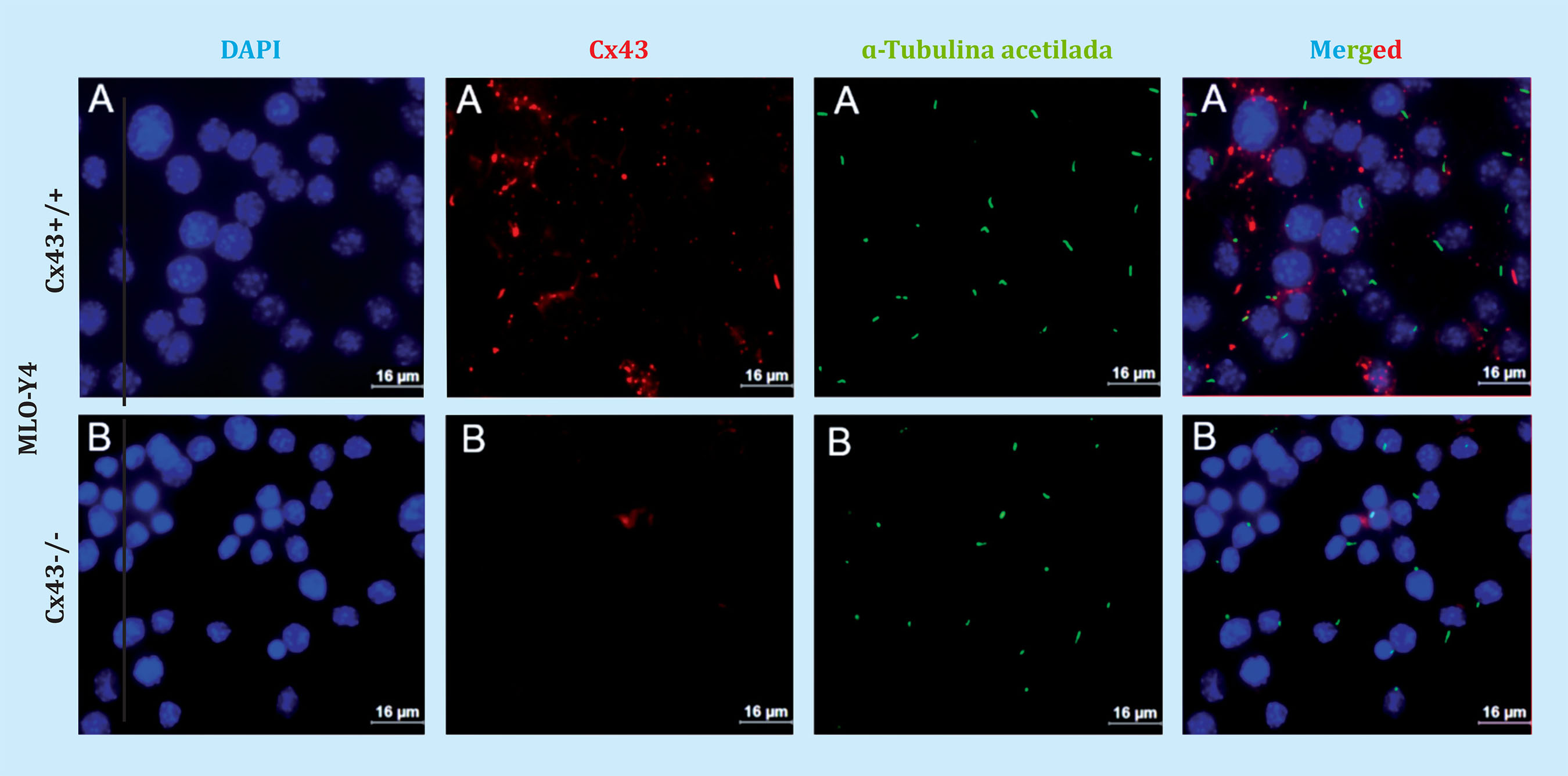
Figura 2. Inmunofluorescencia realizada con osteocitos de la línea MLO-Y4 (A) Cx43+/+ y (B) Cx43-/-. Los núcleos celulares se tiñeron con DAPI (azul), se utilizó anticuerpo anti ɑ-tubulina acetilada para marcar el cilio primario (verde), anticuerpo anti Cx43 para marcar la Cx43 (rojo) y el merged. Las imágenes fueron realizadas con el objetivo de inmersión a 63X. Barra de escala = 16 μm
Tabla 1. Contajes de las células (cel.) que presentan cilio primario en las líneas MLO-Y4 Cx43+/+ y Cx43
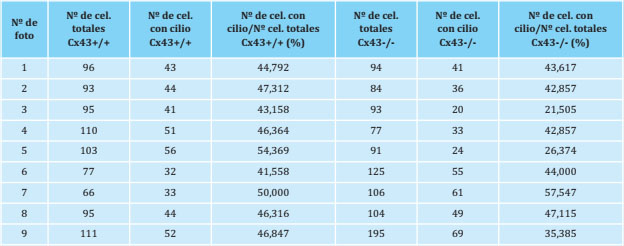
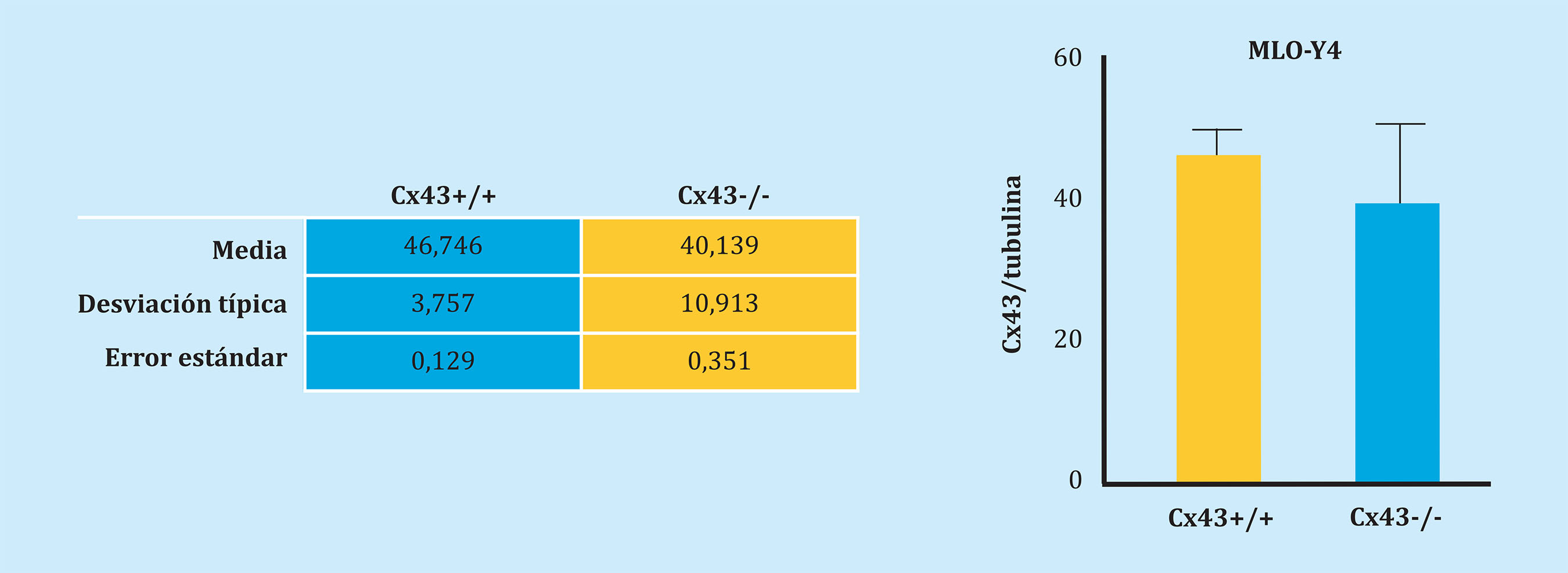
Figura 3. Nº de células con cilio/Nº de células totales (%) en las líneas Cx43+/+ y Cx43-/-. Los resultados se expresan como media ± desviación estándar
2. Efecto del estímulo mecánico y de PTHrP en células Cx43+/+ y Cx43-/-
En varios estudios se ha determinado que la estimulación mecánica inhibe la apoptosis de los osteocitos, mediante un mecanismo que implica la fosforilación de MAPK como ERKs16. Con este experimento se pretendía analizar si la deficiencia en Cx43 alteraba el efecto que tiene el estímulo mecánico en los osteocitos y determinar si la Cx43 interviene en la activación del receptor PTH1R, tras estimularlo con uno de sus ligandos, PTHrP. Para caracterizar los efectos que desencadenan la estimulación mecánica y la estimulación con PTHrP en las células MLO-Y4, se analizó mediante Western blot la expresión de P-ERK.
Se aplicó el test Kruskal-Wallis para determinar si existían diferencias entre los grupos Cx43+/+ y Cx43-/para las condiciones: CE, FF y PTHrP. El resultado del test indicó que había diferencias entre algunos de los grupos (p=0,0005). Para determinar entre qué grupos, se realizó el test de comparaciones múltiples Dunn, que mostró que tanto el estímulo mecánico (FF) (p=0,049) como el estímulo con PTHrP (p=0,017) inducen el aumento significativo de la fosforilación de ERK respecto a las células no estimuladas (control estático, CE); en la línea celular MLO-Y4 Cx43+/+. Este resultado evidencia que los estímulos extracelulares favorecen la activación de la vía de señalización Src/ERK, que promueve la supervivencia celular. En el caso de las MLO-Y4 Cx43-/- se observa que tras la estimulación mecánica (FF), P-ERK no aumenta significativamente respecto a CE (p=0,955). Sin embargo, cuando estimulamos con PTHrP la fosforilación de ERK aumenta significativamente (p=0,025) (Figura 4).
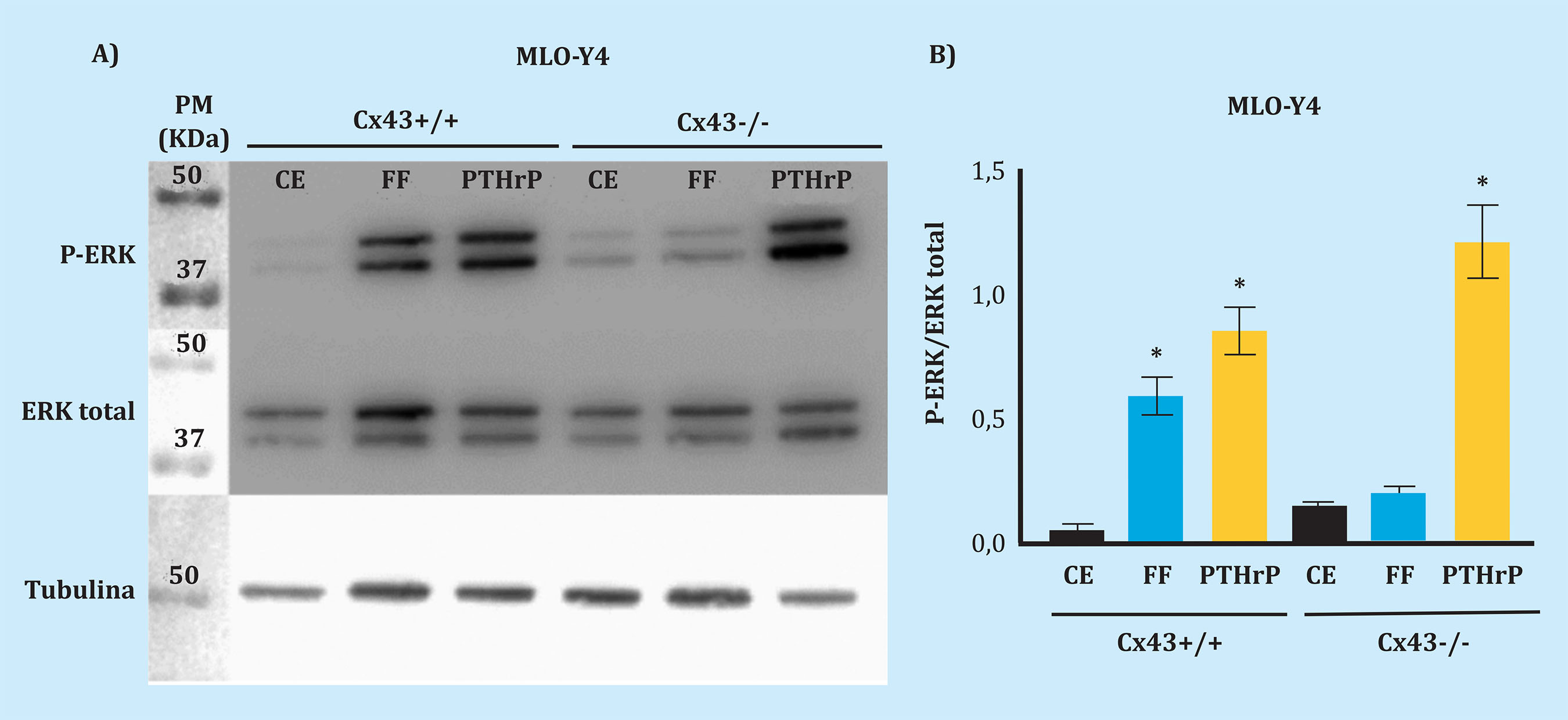
Figura 4. Análisis de P-ERK tras la estimulación mecánica y con PTHrP. Tras la estimulación mecánica y la estimulación con PTHrP, se evaluaron los cambios en los niveles proteicos, mediante Western blot, de P-ERK en extractos de proteína celular total, de las líneas celulares Cx43+/+ y Cx43-/-, que se estimularon o no (control estático, CE). Se utilizaron ERK total y tubulina para normalizar. Los resultados se expresan como media ± desviación estándar de un experimento por duplicado de cada condición experimental vs. CE
DISCUSIÓN
Las conexinas y el cilio primario son elementos mecanosensores de las células óseas, desempeñando un papel fundamental en la detección de estímulos y transmisión de señales3.
Los resultados obtenidos mediante Western blot confirman que la línea celular Cx43-/- utilizada en el experimento era deficiente en esta proteína, pues el nivel de expresión de Cx43 disminuía significativamente en comparación con la línea Cx43+/+. También se analizó la expresión de la proteína IFT88, ya que en estudios previos se empleaba como marcador de la presencia del cilio primario17. Según los resultados obtenidos, se puede concluir que no existen diferencias significativas en la expresión de la proteína IFT88 entre las líneas Cx43+/+ y Cx43-/-. Los resultados del análisis de IFT88 mediante Western blot, por sí solos, no permiten asegurar que el cilio primario se esté desarrollando correctamente, debido a que la proteína IFT88 podría estar expresándose en otro compartimento celular distinto al cilio primario. Por tanto, para comprobar si la deficiencia en Cx43 influye en la formación del cilio primario, se analizó la expresión de este orgánulo y de la Cx43 mediante inmunofluorescencia. Se observó que tanto las células Cx43+/+ como las células Cx43-/desarrollaron cilio primario; asimismo, se constató que el número de cilios formados no difería significativamente entre las dos líneas celulares. Además, parece observarse que la Cx43 y el cilio primario no colocalizan; y que en las células Cx43+/+, la Cx43 se encuentra en la membrana plasmática de la célula, que sería la localización esperada, pues es donde forma las UCs.
Investigaciones previas han demostrado que las células MLO-Y4 son un modelo óptimo para realizar estudios de estimulación mecánica16. No obstante, para poder extrapolar los resultados obtenidos en estos estudios in vitro a las auténticas condiciones in vivo, es necesario trabajar con estímulos mecánicos que reproduzcan y generen respuestas similares a las que se producen en la situación fisiológica. Actualmente, el flujo de fluido (FF) sobre una monocapa de células osteocíticas es la técnica que más se aproxima a esta situación18.
La diana molecular elegida como indicador de la viabilidad de la línea MLO-Y4 fue P-ERK, porque su activación tras la estimulación mecánica es un indicador de supervivencia en células osteocíticas16,18. De acuerdo con las investigaciones mencionadas, se observó que el estímulo mecánico mediante FF induce el aumento en la expresión de P-ERK16,18. Por tanto, se interpreta que el FF promueve la supervivencia de las células MLO-Y4.
Por otro lado, el sistema PTHrP/PTH1R también es fundamental en la regulación del remodelado óseo. Resultados preliminares sugieren que el PTH1R es clave en la respuesta anabólica ósea en respuesta a la estimulación mecánica in vivo. Se ha demostrado que este receptor actúa como mecanorreceptor en células osteoblásticas13. Los resultados del estudio efectuado indican que la administración exógena de PTHrP (1-36) (ligando del PTH1R) protege de la apoptosis de modo similar al de la estimulación mecánica en los osteocitos, debido a que induce el aumento de la expresión de P-ERK. De manera similar, estudios anteriores constataron que la PTHrP, al igual que la PTH, posee propiedades anti-apoptóticas en osteocitos16.
CONCLUSIONES
El número de células con cilio primario no varía por la expresión de Cx43.
El cilio primario y la Cx43 actúan como mecanosensores de los osteocitos.
El estímulo mecánico inducido mediante flujo de fluido (FF) promueve la supervivencia de las células MLO-Y4, independientemente de la deficiencia en Cx43, pues provoca un aumento en la expresión de P-ERK, tanto en células Cx43+/+ como en Cx43-/-.
La administración exógena de PTHrP (1-36) (ligando del PTH1R) produce un aumento de P-ERK en las células Cx43+/+ y Cx43-/-. No obstante, este aumento es mucho mayor en las células Cx43-/-. Por tanto, se sugiere que la Cx43 está inhibiendo al receptor PTH1R, lo que provoca que, tras la unión de su ligando PTHrP, la ruta de activación en la que interviene P-ERK no se active completamente.











 text in
text in 


