1. Introducción
Introducción a la edición de 2004
El líquido de diálisis (LD) es un elemento fundamental de la hemodiálisis (HD). Es un medio líquido que se pone en contacto con la sangre a través de la membrana semipermeable del dializador durante la sesión de HD. Permite el intercambio de sustancias, fundamentalmente solutos, con la sangre de forma bidireccional.
Se trata de una solución electrolítica preparada extemporáneamente por el monitor de hemodiálisis a partir de agua purificada y solutos proporcionados en forma de concentrados electrolíticos o sales no disueltas. La composición del LD así formada es prácticamente isotónica y tiene una composición electrolítica parecida al plasma. Las diferencias de sus concentraciones están en función de los gradientes necesarios para lograr los balances adecuados de cada sustancia, en función de las necesidades del paciente.
La calidad y pureza del LD es uno de los principales requisitos de la técnica de HD. De hecho, la presencia de contaminantes en el LD expone al paciente a un riesgo de acumular sustancias tóxicas, dando lugar a complicaciones tanto agudas como crónicas. Algunos contaminantes pueden interaccionar con células o proteínas, desencadenando fenómenos de bioincompatibilidad, que se añaden a los producidos por otros componentes del circuito sanguíneo extracorpóreo de la HD.
La pureza y calidad del LD es la consecuencia de una compleja cadena de procesos en la que cualquier error tiene un gran impacto en el producto final. Es por tanto necesario cuidar todos los elementos y pasos necesarios para la producción del LD. Las condiciones de preparación, distribución y almacenamiento deben estar diseñadas para minimizar el riesgo de contaminación química y microbiológica.
Para facilitar su compresión, esta guía se desarrolla en 6 puntos fundamentales:
La guía comprende: un glosario de la terminología con referencia a los apartados (2); una guía rápida con las normas, en negrilla, y recomendaciones fundamentales, divididas en 6 apartados (4-9); un texto con los razonamientos y evidencias que sustentan las recomendaciones (apartado 10) y unos anexos donde se detallan los componentes de equipos y metodología (A.1-A.6).
Introducción a la edición de 2015
El objetivo de esta primera revisión de la Guía de gestión de calidad del líquido de diálisis (GGCLD) de la Sociedad Española de Nefrología (SEN), publicada en Nefrología 2004; 24 Suppl 2: 1-42, es adecuar su contenido a la hemodiálisis (HD) actual.
Han pasado 11 años desde esa primera edición de la GGCLD, y la HD y sus características han evolucionado:
La mayoría de las HD en nuestro entorno son de alto flujo (80-90%) y la proporción de pacientes en hemodiafiltración en línea ha aumentado considerablemente (20-30%). La HD actual precisa de un líquido de diálisis (LD) de características ultrapuras.
La tecnología de tratamiento del agua para HD también ha evolucionado. Los buenos tratamientos del agua para HD actuales mantienen unos estándares bastante uniformes.
Aunque muchos de los tratamientos de agua para HD se han renovado y mejorado en España, se siguen produciendo contaminaciones por encima de los límites establecidos: fundamentalmente en relación a contaminaciones microbiológicas, aluminio y cloraminas. Su prevención debe ser un objetivo.
El mantenimiento del estándar de agua ultrapura sigue creando problemas técnicos en bastantes unidades de HD. Algunos requisitos del agua ultrapura se deben matizar o modificar, sin que afecten a la calidad exigida.
Se quieren incluir aspectos relacionados con la calidad del LD no incluidos en la primera edición, como son características del agua de aporte, metodología de la determinación de algunos contaminantes, tratamientos del agua portátiles y domiciliarios, control de los sistemas centralizados de concentrados.
La GGCLD ha marcado la pauta a seguir en cuanto a la calidad del agua y del LD para HD en España y otros países. Las comunidades autónomas españolas la han trasladado, en muchas ocasiones, a sus pliegos técnicos y conciertos de HD. El Ministerio de Sanidad, Política Social e Igualdad la incluyó como referencia en sus Estándares y Recomendaciones para las Unidades de Depuración Extrarrenal, en el año 2011. La GGCLD ha servido para crear una cultura sobre la importancia clínica de un LD ultrapuro, avalada posteriormente por numerosas evidencias científicas. En varios aspectos ha sido pionera. A nivel microbiológico, la metodología propuesta en la GGCLD de 2004 es similar a la de la ISO13959 del 2014.
Se ha intentado que los términos de esta Guía sean más fácilmente entendibles e interpretables, para ello las formas gramaticales empleadas se atienen a los significados explicados en los métodos, punto 3.3.
La GGCLD es un encargo de la Sociedad Española de Nefrología a un grupo de expertos. Esta renovación vuelve a ser un encargo de la actual Junta Directiva de la SEN, presidida por la Dra. M. Dolores del Pino, a un grupo renovado de expertos.
2. Glosario de terminología y definiciones
AAMI |
- (Asociación para el Avance de la Instrumentación Médica) Recomienda estándares para procedimientos médicos en Estados Unidos. www.aami.org. Ver anexo 6. |
Agua de aporte o bruta |
- Se entiende como agua de aporte el agua que se va a tratar, bien si procede de la red municipal, se capta de un pozo o se recibe en camiones cisterna. En general se trata de agua potable sujeta en España a la normativa correspondiente. Ver anexos 1 y 5. |
Agua de rechazo o «concentrado» |
- Es el agua que no ha pasado a través de las membranas de ósmosis y que lleva la práctica totalidad de las sales y de los contaminantes. Ver anexo 2. |
Agua estéril apirógena |
- Es el agua libre de organismos vivos y esporas. La esterilidad viene definida como la presencia de un número de bacterias viables inferior a 1 × 10-6 UFC/ml y <0,03 UE/ml. Ver anexo 3. |
Agua pretratada |
- Es el agua sometida a todos los procesos previos a su llegada al equipo de ósmosis o tratamiento. Ver anexo 2. |
Agua purificada |
- Es el agua destinada a la preparación de medicamentos o de líquidos de diálisis que no deben ser necesariamente estériles y exentos de pirógenos. Ver apartado 4.1 de esta Guía. |
Agua ultrapura |
- Se define como agua ultrapura o altamente purificada la que se ajusta a un contenido de contaminantes químicos de acuerdo con lo recomendado en el apartado 4.1.2. Su conductividad máxima es 5 μS·cm−1, medida a 25 °C; tiene menos contaminación bacteriana de 0,1 UFC/ml (10 UFC/100ml) y el nivel de endotoxinas debe ser inferior a 0,03 UE/ml. Ver apartado 4.2. |
Ao |
- Ao es una manera de calcular la «dosis de energía térmica necesaria» para desinfectar, en base a diferentes combinaciones de tiempo y temperatura. Un Ao es igual a un segundo de 80 °C (1 Ao = 1segundo a 80 °C). Ao = ∑10 (T-80)/z • Δt, donde T es la temperatura en °C, z es igual a 10 °C y Δt es el tiempo en segundos. Ver apartado 8. |
Bacterias heterótrofas |
- Bacterias que desde el punto de vista metabólico dependen para su desarrollo de la utilización de compuestos orgánicos. Este es un grupo muy amplio y diverso que incluye especies simbiontes, saprofitas y patógenas. El término heterótrofo se utiliza comúnmente como nombre genérico para las bacterias del agua con escasos requerimientos nutricionales. Ver anexo 3. |
Bacterias quimiosintéticas |
- Aquellas capaces de sintetizar sus nutrientes y de obtener energía a partir de compuestos inorgánicos. Ver anexo 3. |
Bidón tampón |
- Bidón instalado al inicio de una planta de tratamiento de agua para facilitar su control. Su función no es la de almacenar agua, sino la de estabilizar el proceso y no depender de la presión de alimentación del agua de aporte. Ver anexo 2. |
Biofilm |
- Colonias de bacterias asentadas sobre las superficies de los circuitos hidráulicos, protegidas por un ecosistema de precipitados minerales y una matriz polisacárida mucosa extracelular, que se reproducen y generan en lugares de estancamiento. Su presencia se asocia a contaminación bacteriana persistente. Es fuente activa de endotoxinas y otros derivados bacterianos biológicamente activos. Es resistente a la mayoría de los desinfectantes. Ver anexo 3. |
Caudal nominal |
- Es el caudal que produce un equipo de ósmosis inversa en condiciones ideales. Ver anexo 2. |
Concentrados para diálisis |
- Concentrados o sales que, mezclados con el agua purificada o ultrapura, en el monitor de hemodiálisis, van a formar el líquido de diálisis. Estos concentrados o sales están manufacturados, empaquetados y etiquetados según el marcado CE y deberán estar de acuerdo con la ISO 13958. Ver apartado 5. |
Conductividad |
- Es la densidad de corriente dividida por la amplitud del campo eléctrico e inversa de la resistividad. La concentración de electrólitos en el agua se relaciona de forma directa en la conductividad eléctrica de la solución. Se mide en S·cm-1. Ver apartado 10.8. |
Cloraminas |
- Productos formados por la combinación del cloro libre con amonio. El amonio puede proceder de la descomposición vegetal, otros contaminantes orgánicos o aportado por los responsables de la potabilidad del agua para desinfectarla. Son extremadamente oxidantes y tóxicas para los pacientes en hemodiálisis. Ver anexo 5. |
Cloro combinado |
- Cloro químicamente unido a otros compuestos, como es el caso de las cloraminas. El cloro total es igual al libre más el combinado. Ver anexo 5. |
Cloro libre |
- Cloro molecular disuelto. Ver anexo 5. |
Descalcificador o «ablandador» |
- Dispositivo para reducir la dureza del agua mediante la eliminación del calcio y del magnesio por intercambio iónico con cationes ligados a resinas. Ver anexo 2. |
Desinfección |
- Proceso de destrucción de microorganismos que reduce su número pero no los elimina. La esterilización reduce el número hasta un nivel seguro, dado que la eliminación total es virtualmente imposible. Puede ser química o térmica. Ver apartado 8. |
Desionizador |
- Dispositivo para reducir los iones libres en el agua mediante lechos dobles o mixtos de resinas catiónicas y aniónicas. Ver anexo 2. |
Desionizador eléctrico continuo o electrodesionizador |
- Dispositivo para reducir la concentración de iones libres en el agua, cationes y aniones, mediante un campo eléctrico. Ver anexo 2. |
Dializador |
- Elemento de la hemodiálisis donde se realiza la diálisis, mediante trasporte difusivo, convectivo y adsorción. En su interior se ponen en contacto la sangre y el líquido de diálisis a través de una membrana semipermeable. También se denomina filtro. |
Endotoxina |
- Sustancia pirógena y biológicamente activa, lipopolisacárida, liberada de la pared celular externa bacteriana gramnegativa. Se miden en unidades de endotoxina (UE)/ml o en unidades internacionales (UI)/ml, que actualmente son equivalentes. Ver anexo 3. |
Equipo electromédico |
- Es un producto sanitario activo no implantable y, como tal, sujeto a normativas europeas y nacionales, como RD1591/2009, Medical Devices Directive, 93/42/CEE, ISO13485, IEC 60601.1:2015. Ver anexo 6. |
Esponjamiento de un lecho |
- Es el incremento de volumen aparente de un lecho al ser sometido a un lavado a contracorriente. Ver anexo 2. |
Exotoxina |
- Proteínas con capacidad pirogénica secretadas por los microorganismos. Ver anexo 3. |
Filtro de carbón activado |
- Filtro empleado para eliminar del agua cloro, cloraminas y sustancias orgánicas por medio de la adsorción de la estructura microporosa del carbón activado. Ver anexo 2. |
Filtro de cartucho |
- Está formado por un cilindro de material poroso que, al pasar el agua a través de él, retiene las partículas de menor tamaño que el del poro. Ver anexo 2. |
Filtro de cartucho bobinado |
- Filtro de cartucho formado por un alma rígida perforada en el que el material poroso está formado por un cordón que puede ser de algodón, polipropileno u otro similar y que, dependiendo del tipo de hilo, del número de hilos por vuelta y de la presión del bobinado, se obtiene mayor o menor capacidad de filtrado. Pueden retener partículas entre 1 y 100 μm. Ver anexo 2. |
Filtro de cartucho plisado |
- Filtro de cartucho formado por un alma rígida perforada en el que el material poroso es de poco espesor y mucha superficie, «una especie de papel» y doblado en zigzag, sellado por ambos extremos y unidos al alma. La capacidad de filtrado la determina la porosidad del material filtrante. Pueden retener partículas y bacterias de hasta 0,2 μm. Ver anexo 2. |
Filtro de lecho |
- Filtro compuesto por un recipiente lleno de un material rígido granulado de tamaño homogéneo que retiene las partículas en los espacios libres. Para eliminar las partículas retenidas hay que hacerle lavados a contracorriente. Ver anexo 2. |
Hemodiafiltración |
- Forma de hemodiálisis en la que, junto al transporte difusivo, el transporte convectivo juega un papel importante en la eliminación de solutos. |
Hemodiálisis |
- Forma de tratamiento renal sustitutivo que consiste en la eliminación e intercambio de solutos desde/entre la sangre y el líquido de diálisis. Estos solutos son eliminados preferentemente por difusión. |
ISO |
- International Standardization Organization. Ver anexo 6. |
LAL |
- Limulus amebocito lisado (análisis de lisado de amebocito de Limulus). Ensayo específico de detección de endotoxinas basado en el lisado de amebocitos del cangrejo Limulus polyphemus. Ver anexo 3. |
Lavado a contracorriente |
- Proceso a que se somete un filtro de lecho consistente en introducir el agua por la parte inferior a un caudal ascendente para esponjar el lecho y permitir la eliminación de las partículas retenidas. Para el correcto lavado la velocidad del agua debe ser ligeramente superior a la velocidad de fluidificación a fin de conseguir un esponjamiento del lecho en un 10% al menos. Ver anexo 2. |
Lavado a corriente |
- Proceso a que se somete un filtro de lecho consistente en introducir el agua por la parte superior y eliminar el agua utilizada en el lavado a contracorriente que no ha sido filtrada. Ver anexo 2. |
Líquido de diálisis |
- Fluido acuoso que contiene electrólitos, tampones y habitualmente glucosa, que se forma por la unión del agua para diálisis y los concentrados y sales en el monitor de diálisis. Son sinónimos: dializado, solución de diálisis o baño. Ver apartado 6. |
Líquido de diálisis ultrapuro |
- Líquido de diálisis producido preferentemente con agua ultrapura, con menos de 0,1 UFC/ml y menos de 0,03 UE/ml de endotoxinas y que ha pasado por un ultrafiltro inmediatamente antes del dializador. Ver apartado 6. |
Líquido de sustitución |
- Líquido o fluido de diálisis que se utiliza en las técnicas de hemodiafiltración y hemofiltración para reponer el ultrafiltrado, infundiéndolo en el circuito sanguíneo. Es mandatario que corresponda a líquido de diálisis ultrapuro y que pase por un segundo ultrafiltro de endotoxinas. También se puede utilizar para el cebado o purgado del circuito sanguíneo, en bolos como infusión durante la sesión o en el retorno de la sangre. También se denomina líquido de infusión. Ver apartado 6. |
Lipopolisacáridos |
- Endotoxinas compuestas por lípidos y azúcares (polisacáridos). Ver anexo 3. |
Microfiltro |
- Filtro que es capaz de eliminar partículas mayores de 1μm de diámetro. (0,1-0,3 μm según la AAMI). Ver anexo 2. |
Monitor de hemodiálisis |
- Máquina o sistema que realiza el proceso de hemodiálisis. El proceso de diálisis se produce en un dializador, donde se unen el circuito de sangre y el circuito hidráulico, capaz de producir líquido de diálisis. Estos 2 circuitos son controlados por el monitor con la máxima eficacia y seguridad para el paciente. |
Nanofiltración |
- Retiene compuestos orgánicos con pesos moleculares entre 300 y 1.000 D. Retiene algunas sales y trabaja a menos presión que la OI. Ver anexo 2. |
Nivel de actuación |
- Grado de contaminación con el que se recomienda iniciar medidas correctoras para evitar alcanzar los límites de contaminaciones no aceptables. Ver apartado 4.1.1. |
Ósmosis inversa |
- Proceso de purificación del agua mediante el tamizado a través de una membrana y rechazo del concentrado iónico. Elimina iones y contaminantes orgánicos de peso molecular >100 D. Ver anexo 2. |
Permeado o «filtrado» |
- Fluido que ha pasado a través de una membrana de ósmosis inversa. Ver anexo 2. |
Pirógeno |
- Sustancia que induce fiebre e inflamación. Los pirógenos externos (endotoxinas/exotoxinas, ADN bacteriano) inducen citoquinas, como IL-6, IL-1 o TNFα, que son mediadores en la inducción de fiebre e inflamación. Sustancias capaces de activar a las células mononucleares de la sangre. Ver anexo 3. |
Prefiltro o «filtro de sedimentación o de arena |
- Filtro de lecho que elimina grandes partículas, entre 500-20 μm, y se coloca en el agua de entrada al tratamiento. Permite contralavados. Ver anexo 2. |
R2A |
- Medio de cultivo para bacterias especialmente indicado para contaminantes del agua, por su alta sensibilidad. Ver composición en anexo 3. |
Resina |
- Cationes, aniones o mezcla fijada a gránulos, en los lechos de intercambio iónico como los de los descalcificadores y desionizadores. Ver anexo 2. |
Resistividad |
- Resistencia de un medio al paso eléctrico. Es la inversa de la conductividad. A menor número de electrólitos, mayor resistividad. Una resistividad de 1 MΩ/cm es lo mismo que una conductividad de 1 microS/cm. Ver apartado 10.8. |
SDI |
- Silt Density Index. Parámetro que mide la densidad de sedimentos o la suciedad del agua. La ASTM International (anteriormente American Society for Testing and Materials) regula la forma de medir este índice. Ver apartado 10.5. |
TGEA |
- Medio de cultivo para bacterias, recomendado por la ISO y las Guías Europeas, junto al R2A. Composición: agar triptona glucosa extracto de levadura. Ver anexo 3. |
Tiempo de contacto |
- En inglés Empty Bed Contact Time (EBCT). Tiempo de contacto del agua con el lecho de carbón activado. Se calcula con la siguiente ecuación EBCT=(7,48 · V)/Q, donde V es el volumen aparente del lecho y Q el flujo del agua expresado en galones/min. Ver anexo 2. |
TDS |
- Sólidos totales disueltos. Suma de todos los iones disueltos. Guarda relación con la conductividad eléctrica y sirve para controlar el funcionamiento de la ósmosis inversa. Ver apartado 10.8. |
TSA |
- Medio de cultivo para bacterias. Ver composición en anexo 3. |
Unidades de endotoxinas por ml (UE/ml) |
- Unidades de endotoxinas (ET) tituladas mediante una prueba basada en la activación de un lisado de amebocitos Limulus (LAL). Las ET varían en su actividad según su composición, por lo que su actividad se refiere al estándar de E. coli. (O: 113: H10). La relación de la actividad y la masa varía con el lote de LAL y el lote de ET estándar. En general, 0,012 unidades de endotoxinas equivalen aproximadamente a un picogramo. Genéricamente la relación es 10UE por ng. La determinación cromogénica es la más sensible, aunque otros métodos (colorimétricos, fluorimétricos, GEL-CLOT) son utilizados de forma habitual en estas determinaciones. Ver anexo 3. |
Unidades formadoras de colonias (UFC) |
- Unidad de medida de bacterias viables. Refiere el número de colonias bacterianas que se han desarrollado en un medio de cultivo sólido. Se expresan en UFC por mililitro de líquido. Ver anexo 3. |
Ultrafiltración, como método de diálisis |
- Transporte convectivo de solutos a través de una membrana, mediante un gradiente hidrostático de presiones (presión transmembrana). |
Ultrafiltración, como tratamiento del líquido de diálisis |
- Es un proceso similar a la ósmosis inversa. Rechaza contaminantes entre 1.000 D y 0,1 μm. La ultrafiltración requiere presiones bajas para operar. Retiene fundamentalmente sustancias orgánicas, bacterias y pirógenos. La efectividad de las membranas en ultrafiltración se determina como el menor peso molecular que rechaza más del 90% (en inglés, MWCO). Ver anexo 2. |
Ultrafiltro |
- Filtro de membrana (polisulfona, poliamida, polietersulfona, posidina) empleado para eliminar los componentes microbianos del agua de diálisis, en el postratamiento del agua de diálisis o más comúnmente en los líquidos de diálisis. Algunos ultrafiltros retienen ET por adsorción. También se usa como sinónimo de dializador. Ver anexo 2. |
Ultravioleta |
- Radiación ultravioleta bactericida utilizada para eliminar microorganismos. UVC, longitud de onda-energía-fotón: 200-290 nm y 6,2-4,3 eV. Se recomienda 254 nm y 16 miliwat-s/cm2 y la utilización de un filtro de endotoxinas a continuación. ISO 13958:2009. Ver anexo 2. |
USP |
- United States Pharmacopoeia. Ver anexo 6. |
Velocidad de fluidificación |
- Es la velocidad de contralavado de un filtro de lecho a la que este se ve sometido a una fuerza ascendente igual a su peso. Su volumen aparente no varía, su esponjamiento es cero. Ver anexo 2. |
Venteo |
- Entrada y salida de aire que se produce cuando varía el volumen de un líquido almacenado en un bidón rígido. Puede estar dotado de un filtro de 0,2 μm para que ese aire entre en las debidas condiciones. Ver anexo 2. |
Volumen aparente de un lecho |
- Es el volumen que ocupa un lecho cuando se esponja con un lavado contracorriente. Ver anexo 2. |
Volumen real de un lecho |
- Es el volumen que ocupa un lecho en un recipiente. Se entiende que el espacio existente entre las partículas es un volumen ocupado por el propio lecho. Ver anexo 2. |
Abreviaturas
AAMI |
- Association for the Advancement of Medical Instrumentation: www.aami.org |
CSA |
- Asociación de Estándares Canadiense |
EBCT |
- tiempo de contacto con el lecho de carbón activado (TCL) |
HD |
- hemodiálisis |
ISO |
- International Organization for Standardization |
LAL |
- Limulus amebocito lisado |
LD |
- líquido de diálisis |
OI |
- ósmosis inversa |
ppm |
- partes por millón |
R2A |
- medio de cultivo R2A de Reasoner |
SDI |
- Silt Density Index |
SP |
- sustancias pirogénicas |
Test LAL |
- análisis de lisado de amebocito de Limulus |
TCL |
- tiempo de contacto con el lecho; en inglés, Empty Bed Contact Time (EBCT) |
TDS |
- sólidos totales disueltos |
TGEA |
- agar triptona glucosa extracto de levadura |
TSA |
- Bacto Tryptic Soy Agar: agar tripsonizado de caseína y soja |
UE |
- unidades de endotoxinas |
UI |
- unidades internacionales de endotoxinas |
UFC |
- unidades formadoras de colonias |
UV |
- ultravioleta |
3. Objetivo, ámbito y metodología utilizada
3.1. Objetivo
El objetivo de esta Guía es proporcionar recomendaciones sobre la calidad del agua, de los concentrados y del líquido de diálisis (LD) para la adecuada realización de las hemodiálisis (HD). La HD adecuada trata de promover el tratamiento óptimo de los pacientes en HD. Por otro lado, esta Guía trata de aportar criterios unificados de la calidad necesaria del agua, de los concentrados y del LD y, al tiempo, los métodos para alcanzar ese nivel de calidad y cómo mantenerlo.
3.2. Ámbito
El campo de aplicación comprende todo tipo de HD o hemodiafiltración o cualquier técnica depurativa extrarrenal que utilice LD. Su ámbito geográfico es el Sistema Nacional de Salud español, por estar la Guía adecuada a la realidad de la HD española actual. La Guía pretende ser un objetivo de calidad a mantener o alcanzar en las unidades de HD españolas, siendo sus recomendaciones asumibles por todo el personal sanitario, técnicos de diálisis y empresas dedicadas al campo de la diálisis.
3.3. Metodología
Constitución del grupo de expertos: la Sociedad Española de Nefrología nombró a un nefrólogo con gran experiencia en HD y coordinador de la primera edición de esta Guía (2004), como coordinador de esta segunda edición; a continuación se configuró el grupo de trabajo, que es multidisciplinar e incluye 4 nefrólogos y otros especialistas, expertos en distintos aspectos técnicos y científicos relacionados con el tratamiento del agua: un microbiólogo, 4 técnicos de HD, un responsable de producto y un investigador consagrado en temas de biocompatibilidad en diálisis. Este abordaje multidisciplinar es fundamental para poder tener una visión integral del tema, no solo desde el aspecto teórico de la revisión bibliográfica, sino desde un punto de vista de la experiencia en la práctica diaria.
Dinámica de reuniones: en la primera reunión se decidieron los aspectos a estudiar y su distribución entre los distintos expertos. En las siguientes reuniones se han discutido en conjunto las propuestas de cada experto, buscando conclusiones de consenso. Finalmente se realizó una reunión presencial de consenso final.
Se ha realizado una búsqueda de información, abarcando: literatura (Medline-PubMed, Cochrane); otras guías (ver anexo 6); informes de agencias de control de calidad y evaluación de tecnologías (ISO, Eu. Pharmacopoeia, AAMI, etc.; ver anexo 6).
Análisis de calidad de la evidencia: se ha utilizado la clasificación GRADE (Uhlig et al., Grading evidence and recommendations for clinical practice guidelines in nephrology. A position statement from kidney disease: improving global outcomes (KDIGO). Kidney Inter 2006;70:2058-65). El nivel de la calidad de la evidencia (A-D) y el grado de fuerza de la recomendación (1-3) se realizaron por consenso a propuesta de los autores de cada capítulo. El tema de la calidad del agua, de los concentrados y del LD, en algunos de sus aspectos, es peculiar en cuanto a la graduación de nivel de evidencia. Este tema se ha tratado en las ISO-AAMI. En esta Guía en ocasiones nos hemos ceñido a lo establecido por las ISO, en sus últimas ediciones, para cumplir uno de los objetivos de esta Guía, que es unificar criterios con otras recomendaciones/guías internacionales.
Las formas gramaticales empleadas se atienen a los siguientes significados, en relación al grado de evidencia o a lo mencionado en las ISO:
- Las formas verbales que utilizan futuros simples o simplemente el verbo «deber» significan que lo descrito es mandatario (exigible = recomendación fuerte).
- Las formas gramaticales que emplean verbos en su forma condicional o la palabra «recomendable» significan que lo descrito es recomendable, condicionado a lo que se explica (recomendable = recomendación baja).
- Las formas gramaticales que utilizan «podría» describen situaciones en las que para alcanzar un objetivo es necesario cumplir algunas condiciones (permisible o no graduada).
4. Pureza y calidad del agua para hemodiálisis
Como norma básica, cualquier tratamiento de agua para HD tiene que estar diseñado para satisfacer como mínimo las especificaciones de los niveles químicos y bacteriológicos recomendados en esta guía, así como su mantenimiento en el tiempo.
Dentro del concepto de agua utilizada para HD tienen que distinguirse 2 tipos diferentes. Estos son, el agua purificada o estándar (4.1) y el agua ultrapura (4.2). Los criterios de calidad microbiológica y de endotoxinas son diferentes para cada una de ellas. Estas guías entienden que en el momento actual se debe recomendar el uso de agua ultrapura en las unidades de HD, como principal componente del LD ultrapuro.
4.1. Agua purificada para hemodiálisis
4.1.1. Microbiología
Nivel máximo admisible de pureza microbiológica. El agua purificada que se emplea para diluir el concentrado de diálisis, desde el punto de vista de los requisitos bacteriológicos, debe contener menos de 100UFC/ml. ISO13959. 3.ª edición 2014.
Especificaciones. Estos números de UFC corresponden a la media del número total de bacterias aerobias viables, capaces de generar una colonia visible, de cada muestra sembrada, empleando el medio R2A, incubadas durante 7días a una temperatura entre 17 y 23 °C. ISO13959. 3.ª edición 2014.
Aunque hay poca base bibliográfica que lo apoye, sería deseable que los hongos no supusieran un porcentaje superior al 10% del total de las colonias de organismos aerobios (evidencia nivel C, 2).
Para más especificaciones y recomendaciones sobre este apartado, consultar el anexo 3.
Niveles de pureza microbiológica de actuación. Recomendamos que se tomen medidas correctoras, desinfecciones, cuando los recuentos bacterianos alcancen una cantidad del 50% de los exigibles: presencia de más de 50 UFC/ml de bacterias aerobias viables. ISO 13959. 3.ª edición 2014. Con niveles menores de contaminación en más de una muestra también es recomendable realizar una desinfección con el fin de prevenir la formación de biofilm bacteriano.
Niveles máximos admisibles de endotoxinas. El contenido de endotoxinas en el agua purificada para HD no debe exceder las 0,25UE/ml, medido mediante una prueba LAL con suficiente sensibilidad. ISO13959. 3.ª edición 2014.
La calidad bacteriológica del agua y del LD debe incluir la determinación de microorganismos y endotoxinas.
4.1.2. Niveles máximos de contaminantes químicos
El agua purificada para HD no debe contener una concentración de contaminantes mayor que las siguientes (ISO13959:2014 (ver anexo 5):
| Aluminio. Espectrometría de absorción atómica | 0,01 mg/l (10 μg/l) |
| Antimonio. Espectrometría de absorción atómica | 0,006 mg/l |
| Arsénico. Espectrometría de absorción atómica | 0,005 mg/l |
| Bario. Espectrometría de absorción atómica | 0,100 mg/l |
| Berilio. Espectrometría de absorción atómica | 0,0004 mg/l |
| Cadmio. Espectrometría de absorción atómica | 0,001 mg/l |
| Calcio. Espectrometría de absorción atómica | 2 mg/l |
| Cloro total. Colorimétrico | 0,100 mg/l |
| Cromo. Espectrometría de absorción atómica | 0,0140 mg/l |
| Cobre. Espectrometría de absorción atómica | 0.100 mg/l |
| Fluor. Cromatografía iónica | 0,200 mg/l |
| Magnesio. Espectrometría de absorción atómica | 4 mg/l |
| Mercurio. Espectrometría de absorción atómica | 0,0002 mg/l |
| Nitrato, como N. Colorimétrico | 2,0000 mg/l |
| Plata. Espectrometría de absorción atómica | 0,005 mg/l |
| Plomo. Espectrometría de absorción atómica | 0,005 mg/l |
| Potasio. Fotómetro de llama | 8 mg/l |
| Selenio. Espectrometría de absorción atómica | 0,0900 mg/l |
| Sodio. Fotómetro de llama | 70 mg/l |
| Sulfato. Método turbidimétrico | 100 mg/l |
| Talio. Espectrometría de absorción atómica | 0,0020 mg/l |
| Zinc. Espectrometría de absorción atómica | 0,100 mg/l |
Todos estos elementos se controlarán al menos una vez al año. En el caso del aluminio, el control será semestral.
Para más detalles en cuanto a la técnica analítica, se remite a la tabla 3 de la ISO13959:2014.
El agua purificada deberá tener una conductividad máxima de 5 μS·cm−1 a 25 °C (anexo 5). En situaciones de excepción se podrá aceptar menos de 20 μS·cm −1 a 25 °C mientras se identifica la causa del aumento de la conductividad (evidencia nivel C, 2).
Si a pesar de contar con un tratamiento del agua con doble ósmosis en serie o una ósmosis más un electrodesionizador en serie no se alcanza 5 μS·cm−1 de conductividad y todos los contaminantes químicos medidos, especificados en el apartado 4.1.2, están en niveles correctos, se fijará el nivel de conductividad existente como de referencia, siempre inferior a 20 μS·cm−1. En esos casos se identificara la causa del aumento de la conductividad, como puede ser dióxido de carbono, pH, Na, etc.
Una vez fijado el nivel de referencia, tanto si permanece en valores inferiores a 5 μS·cm−1 como en la excepción mencionada, aumentos significativos de la conductividad, en más de un 30% de la de referencia, implicarán la determinación de todos los contaminantes químicos, el control de la calidad del agua de aporte y se identificará la causa del aumento de la conductividad.
La conductividad del agua tratada se vigilará diariamente, anotándose su valor y las causas de sus cambios significativos.
Se debe calibrar el conductivímetro una vez al año como mínimo, y se recuerda la utilidad de compararlo con los TDS.
Se recomienda que la concentración máxima de aluminio en el agua tratada sea de 0,005 ppm (5 μg/l) (evidencia nivel C, 2).
4.2. Agua ultrapura para hemodiálisis
El uso de agua ultrapura es recomendable para fabricar un LD ultrapuro para todas las modalidades de HD (evidencia nivel C, 1).
4.2.1. Microbiología
Nivel máximo admisible de pureza microbiológica. El agua ultrapura que se emplea para diluir el concentrado de diálisis, desde el punto de vista de los requisitos bacteriológicos, debe contener menos de 10 UFC/100 ml (0,1 UFC/ml). ISO13959. 3.ª edición 2014.
Especificaciones (veranexo 3). Para poder medir con precisión estas cantidades es necesario analizar el contenido de una muestra mayor de 100 ml de agua ultrapura mediante filtración.
Niveles de pureza microbiológica de actuación. Recomendamos que se actúe cuando aparezca crecimiento bacteriano en los cultivos, con presencia de más de 5 UFC/100 ml de bacterias aerobias viables. Para aumentar la precisión del recuento de colonias haría falta procesar volúmenes mayores de 100 ml. Se repetirán los cultivos con un volumen mayor de muestra y con muestras por duplicado; si se confirma la contaminación, es recomendable realizar una desinfección con el fin de prevenir la formación de biofilm bacteriano.
Niveles máximos admisibles de endotoxinas.El contenido de endotoxinas en el agua ultrapura para HD no debe exceder las 0,03 UE/ml, medido mediante una prueba LAL con suficiente sensibilidad. ISO13959. 3.ª edición 2014.
4.2.2. Niveles máximos de contaminantes químicos en el agua ultrapura
El agua ultrapura para HD no debe contener una concentración de contaminantes químicos mayor que la especificada para el agua purificada para HD (apartado 4.1.2 y anexo 5).
El agua ultrapura deberá tener una conductividad máxima de 5 μS·cm −1 a 25 °C(anexo 5). En situaciones de excepción se podrá aceptar menos de 20 μS·cm−1 a 25 °C mientras se identifica la causa del aumento de la conductividad (evidencia nivel C, 2).
Si a pesar de contar con un tratamiento del agua con doble ósmosis en serie o una ósmosis más un electrodesionizador en serie no se alcanza 5 μS·cm−1 de conductividad y todos los contaminantes químicos medidos, especificados en el apartado 4.1.2, están en niveles correctos, se fijara el nivel de conductividad existente como de referencia, siempre inferior a 20 μS·cm−1. En esos casos se identificará la causa del aumento de la conductividad, como puede ser dióxido de carbono, pH, Na, etc.
Una vez fijado el nivel de referencia, tanto si permanece en valores inferiores a 5 μS·cm−1 como en la excepción mencionada, aumentos significativos de la conductividad, en más de un 30% de la de referencia, implicarán la determinación de todos los contaminantes químicos, el control de la calidad del agua de aporte y se identificará la causa del aumento de la conductividad.
La conductividad del agua tratada se vigilará diariamente, anotándose su valor y las causas de sus cambios significativos.
Se debe calibrar el conductivímetro una vez al año como mínimo, y se recuerda la utilidad de compararlo con los TDS.
Se recomienda que la concentración máxima de aluminio en el agua tratada sea de 0,005 ppm (5 μg/l) (evidencia nivel C, 2).
4.3. Diseño de un sistema de tratamiento de agua
No existe un tratamiento de agua igual para todas las unidades de diálisis, pues dependerá de la calidad química y bacteriológica del agua de aporte a tratar, su procedencia y posibles variaciones de los elementos disueltos en ella a lo largo del tiempo, limitaciones arquitectónicas, necesidades cuantitativas, necesidades cualitativas, presupuesto económico, perspectivas de evolución tanto de los propios tratamientos de agua como de las nuevas técnicas de diálisis.
La composición básica de un sistema de tratamiento de agua para HD debe consistir en un pretratamiento, donde se eliminarán la mayoría de los elementos indeseables, y un tratamiento con ósmosis inversa (OI) y algún otro elemento que permita alcanzar el nivel de agua purificada en su funcionamiento normal, generalmente una segunda etapa de ósmosis (evidencia nivel C, 1).
El pretratamiento deberá contar al menos con un filtro de retención de partículas en suspensión o sedimentos, descalcificador y filtro de carbón (anexo 2) diseñados para las características del agua de aporte, con aparatos duplicados si los niveles del elemento a eliminar se consideran altos y susceptibles de provocar graves problemas en caso de fallo (evidencia nivel C, 1).
Es básico tener presente los problemas que el mal diseño del pretratamiento puede tener en etapas posteriores: el cloro puede dañar las membranas de ósmosis, la presencia de calcio puede saturarlas, o pasar estos elementos a la red de distribución y, por tanto, llegar hasta el paciente.
El filtro de carbón debe ir siempre instalado inmediatamente antes de la OI y lo más próximo a esta, pues una vez que el agua está declorada puede correr serios riesgos de contaminación, sobre todo al paso de otros filtros donde se ralentiza su velocidad (evidencia nivel C, 1).
Cuando el agua de aporte tenga niveles elevados de cloraminas u otros contaminantes orgánicos, contaminación municipal, industrial o agrícola del agua, se recomienda la utilización de 2 filtros de carbón activado en serie.
Después del pretratamiento deben instalarse las membranas de ósmosis, interponiendo un filtro de al menos 5 μm, que evite la posibilidad de que pequeñas partículas de carbón pasen a la misma, entendiéndose esta como el elemento básico de tratamiento para obtener agua de calidad de acuerdo a las normas reflejadas.
La instalación de otros elementos posteriores a la ósmosis garantiza una mayor calidad del agua. Estos elementos pueden ser una segunda etapa de ósmosis, alimentada por el permeado de la primera y con bombas independientes entre ambas etapas de manera que, en caso de fallo de una, la otra pueda seguir suministrando agua, o un electrodesionizador. No se recomienda utilizar los desionizadores de resinas por su alto riesgo de contaminación (ver anexo 2).
Tanto el electrodesionizador como la lámpara ultravioleta deberían acompañarse siempre con la instalación de ultrafiltros capaces de retener hasta el nivel de endotoxinas, pues en el caso del primero no tiene capacidad de filtro, y la segunda puede aportar al agua endotoxinas derivadas de su acción bactericida.
El depósito de trabajo previo a la OI debe ser lo más pequeño posible. Los elementos posteriores a la primera etapa de ósmosis deben estar dispuestos de forma que permitan distintas configuraciones, pudiendo sumarse o complementarse; la más recomendable es una segunda etapa de ósmosis en serie.
Los elementos que puedan ser sometidos a desinfección y/o desincrustración deben poder contar con accesorios que permitan realizar esta función de la manera más rápida y fiable posible: bombas de adición de desinfectante incorporadas, sistemas programados de lavado, programas de los propios equipos y puntos de toma de muestras.
4.4. Almacenamiento y distribución del agua
Una vez tratada, el agua se debe distribuir directamente a los puestos de consumo sin tanques o bidones de almacenamiento, retornando la sobrante a la entrada del tratamiento. El sistema de tuberías y fontanería debe diseñarse para prevenir la contaminación bacteriana y ser fácilmente desinfectado (evidencia nivel C, 1).
Almacenamiento
El agua tratada almacenada es susceptible de contaminaciones, por lo que se debe evitar. El almacenamiento de agua genera dificultades de desinfección.
Al prescindir de depósitos de agua tratada debe garantizarse el suministro de agua de aporte. Los sistemas pueden ser:
- Doble acometida de agua.
- Depósito de agua de aporte, que deberá tener las características descritas a continuación y en el anexo 2.
- Depósito de agua pretratada, con las mismas características que el punto anterior. En este último caso, se precisa algún tratamiento conservante o desinfectante que garanticen la no contaminación del agua.
Cuando existan depósitos de agua, cualquiera que sea el volumen, deben estar herméticamente cerrados, opacos, preferiblemente de acero inoxidable, base cónica, con la salida de agua por la parte inferior y con filtro de venteo antibacteriano de 0,2 μm. La entrada de agua debe ser en forma de ducha.
Debe estar garantizado el volumen de agua necesario para completar un día de funcionamiento de la unidad de HD.
Red de distribución
El agua tratada se muestra ávida de adquirir sustancias de los elementos que estén en contacto con ella, por lo que la red de distribución debe estar realizada con materiales que no aporten nada al agua o se sospeche puedan hacerlo; no se puede utilizar cañerías de cobre, hierro o aluminio; sin fondos de saco, en tubo continuo que evite empalmes e intersecciones, con la menor longitud posible. Si se utiliza acero inoxidable, debe ser de calidad farmacéutica. El tubo que alimenta al monitor desde la red de distribución deberá considerarse como un elemento más de la propia red de distribución. Tiene que circular a velocidad que minimice los riesgos de contaminación y formación de biofilm, >1 m/s, por lo que se debe calcular especialmente su sección. El agua no consumida debe retornar al tratamiento de agua y pasar de nuevo por él.
Las uniones en los materiales plásticos implican recovecos y alteraciones bruscas en la linealidad del tubo que implican reservorios y ruptura del flujo laminar; ya existen en el mercado materiales plásticos que no presentan estos inconvenientes. Estas uniones se encuentran tanto en los codos cuando estos se colocan para cambiar la dirección del tubo, como en las derivaciones a los monitores y llaves. Cuando se opte por algún tipo de material, hay que tener presente cómo realiza las uniones, pegamentos o termosoldados, por la posibilidad de que los pegamentos sean capaces de aportar, con el paso del tiempo y por su degradación, elementos indeseables al agua. Actualmente existen tuberías de polímeros que obvian estos inconvenientes y resisten el calor sin deformarse. Este tipo de materiales son los recomendables para la red de distribución (ver anexo 2). Si la opción es acero inoxidable, presenta la ventaja de que se pueden utilizar sistemas de desinfección térmica o química, y su resistencia a los golpes o tracciones que se puedan hacer sobre él accidentalmente. Es fundamental la forma de realizar las soldaduras en este tipo de tubo, para que no sufran oxidación posterior.
Es necesario garantizar la total ausencia de fondos de saco; las tomas de los monitores deben ser consideradas como tales y, por tanto, también deben ser eliminadas, enfatizando en aquellas donde los tubos son traslúcidos. Para ello la red de distribución debe llegar hasta el monitor; la forma de realizarlo puede ser mediante instalación denominada en U, donde la red de distribución va hacia el monitor y retorna, yendo posteriormente al siguiente monitor; presenta la desventaja de que el tubo que va hasta el monitor es de la misma sección que el resto de la red.
La otra forma de realizarlo es mediante anillos secundarios: un anillo primario es el encargado de distribuir el agua por toda la unidad; un segundo anillo secundario lleva el agua hasta el monitor. Lógicamente, la dimensión de este anillo secundario es más pequeña que la del primario; en caso de rotura o estrangulamiento, solo afectaría al monitor conectado a él.
La figura 1 muestra las diferentes configuraciones para garantizar la circulación constante del agua, hasta el monitor. A la izquierda, instalación en U, y a la derecha, con anillos secundarios.
Filtro de endotoxinas
En el anillo de distribución del agua para HD debe existir un filtro de endotoxinas, cuando se cumpla cualquiera de estas 3 condiciones: que exista almacenamiento de agua tratada, no se disponga de doble etapa de ósmosis, después de lámpara UV, si se quiere alcanzar el nivel de calidad de agua ultrapura. Este filtro se colocara preferentemente en el inicio del anillo.
Sistema de desinfección por calor
Los sistemas de desinfección por calor, al menos del anillo de distribución del agua tratada, son muy recomendables. Junto a los anillos secundarios y los métodos de desinfección combinada con la de los monitores de HD, constituyen la forma más eficaz de prevenir la aparición de biofilm en el anillo de distribución del agua para HD. Por otro lado, evitan el riesgo de contaminación del LD por los desinfectantes químicos.
El diagrama adjunto muestra una posibilidad de configuración de un tratamiento de agua.
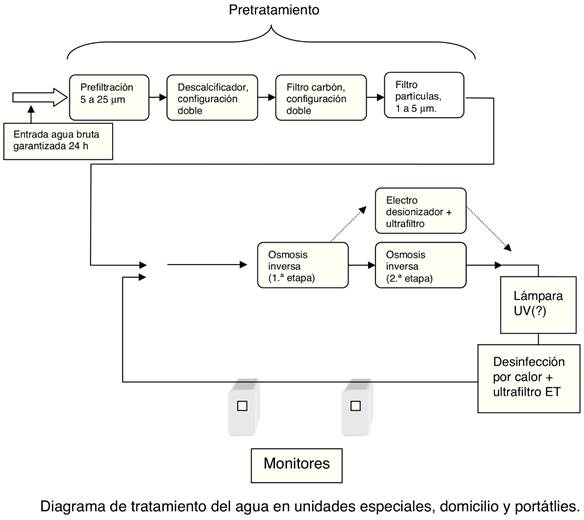
4.5. Tratamientos del agua en unidades especiales, domicilio y portátiles
Los tratamientos de agua para HD en unidades especiales (agudos, UCI, reanimación, etc.) deben tener las mismas características que los descritos antes y ser capaces de producir agua purificada para diálisis, según se especifica en esta guía, estando sometidos a los mismos controles y medidas preventivas que el resto de tratamientos de agua para HD.
Los tratamientos de agua para diálisis en domicilio y portátiles contarán como mínimo con un filtro de carbón activado, OI y un filtro de bacterias de 0,2 μ. La calidad del agua se controlará, como se especifica en el apartado 7 de esta guía, mensualmente, y se someterá a medidas preventivas, como se menciona en el apartado 8. Una vez comprobado, en un primer análisis bioquímico, que las sustancias mencionadas en el apartado 4.1.2 están en concentraciones admisibles, se anotará la conductividad del agua de permeado de la ósmosis y se tomará como referencia. Los cambios bruscos y significativos de la misma se investigarán. Esta metodología se debe mantener después de periodos de inactividad, si de nuevo se quiere utilizar el tratamiento del agua.
Los monitores de HD domiciliarios irán provistos de su correspondiente ultrafiltro de endotoxinas, que se recambiarán según las especificaciones del fabricante.
5. Concentrados para diálisis
Los sistemas de aporte de solutos para la producción de los LD pueden ser individuales, para un solo monitor de HD, o centralizados, para un grupo de monitores.
El agua utilizada para la fabricación del concentrado de diálisis debe cumplir al menos las normas exigidas para el agua purificada, especificadas en los apartados 4.1.1 y 4.1.2 (evidencia nivel C, 1).
Idealmente deberían tener el grado de calidad exigido para soluciones para infusión por vía parenteral.
En la actualidad debe utilizarse únicamente como concentrado básico el de bicarbonato.
Su composición se debería adecuar a la situación clínica de cada paciente, al igual que se hace con los demás factores que influyen en la eficacia y seguridad de la HD.
La concentración de los solutos identificados en la etiqueta estará presente dentro de ±5% o 0,1 mEq/l de margen de concentración, con excepción del sodio y cloro, cuyo margen de variabilidad será de ±2,5%. Estos márgenes se expresan respecto a la concentración en el LD, después de la dilución de los concentrados. ISO13958: 2009.
Todos los ingredientes deben constar en la etiqueta, así como sus cantidades y el nivel de pureza. La dilución que se debe emplear se mencionara como partes de concentrado por partes solución final (LD). En la etiqueta figurará la fecha de caducidad, que garantiza su estabilidad.
Si los concentrados contienen ingredientes no tradicionales, su margen de tolerancia será ±5% respecto a su concentración nominal.
Es recomendable el aporte, por los fabricantes, de certificados de calidad química y microbiológica de los lotes de concentrados suministrados.
Los contenedores, incluidos los tapones, deben ser de materiales que no interactúen con el concentrado, contaminándolo, y deben estar herméticos.
5.1. Concentrados individuales
Concentrado ácido
Es una solución ácida de sales concentradas, que puede contener dextrosa. Cuando se diluye con agua purificada y con el concentrado con bicarbonato produce el LD. En términos generales, la mayoría de los pacientes pueden dializarse con unas concentraciones iónicas estandarizadas del concentrado ácido, aunque es recomendable individualizar el tipo de concentrado para cada paciente (evidencia nivel B, 1)
Concentrado de bicarbonato
Es una solución concentrada de bicarbonato sódico que, cuando se diluye con agua purificada y con el concentrado ácido, se obtiene el LD. Algunos concentrados con bicarbonato también contienen cloruro sódico(evidencia nivel C, 1).
La forma de bicarbonato en polvo es actualmente el sistema recomendado para la fabricación del LD (evidencia nivel C, 1).
El bicarbonato sobrante de una diálisis debe desecharse (ver anexo 2) (evidencia nivel C, 2).
Concentrados con bicarbonato y citrato
El concentrado acido suele contener ácido acético como estabilizante de la mezcla con el bicarbonato. Se usa a concentraciones entre 3 y 10 mmol/l. Estas concentraciones provocan que se transfiera acetato al paciente durante la HD, elevando su concentración en sangre. Esta exposición al acetato aumenta en técnicas de hemodiafiltración en línea. El aumento de la acetatemia se ha asociado a varios efectos no deseados en el paciente. Por ello, desde hace años se han buscado otros ácidos como estabilizantes del LD. El uso de un LD con citrato surge como una alternativa para acidificar sin usar acetato. El citrato es un quelante del calcio que se usa también por su efecto anticoagulante al disminuir el calcio iónico. Se han descrito varios efectos beneficiosos a largo plazo en relación al citrato, como una menor trombogenicidad, la mejoría de los aclaramientos, de la inflamación, de la nutrición, de la tolerancia y del control ácido-base con menor acidosis prediálisis. Son necesarias más evidencias científicas que justifiquen el cambio del acetato por citrato en todas las HD.
Actualmente hay en el mercado concentrados con citrato sin acetato y con una mezcla de los 2 estabilizantes, aptos para diferentes monitores.
Formas de presentación
Podemos encontrar el concentrado ácido en
Garrafa.
Bolsa.
Cartucho seco de cloruro sódico + bolsa de iones.
Contenedor para distribuir centralizadamente (ver apartado 5.2).
Bajo esta clasificación podemos tener presentaciones que facilitan la individualización del tratamiento y otras que no la facilitan, o que la eliminan totalmente. Los sistemas de contenedores eliminan o dificultan la individualización del tratamiento respecto a la concentración de solutos en el LD.
Los sistemas de cartuchos secos de cloruro sódico más bolsa de iones lo facilitan plenamente, sin necesidad de aumentar el espacio de almacenamiento requerido; además son muy seguros, al ser de un solo uso.
Las garrafas de concentrado permiten la individualización, pero al aumentar el número de fórmulas a almacenar, también aumenta el espacio requerido y pueden ser menos seguras.
Las bolsas permiten la individualización con menor espacio que las garrafas y son preferibles, por la seguridad que ofrecen al ser de un solo uso y no poder rellenarse.
Podemos encontrar el concentrado de bicarbonato en cartuchos secos o garrafas.
Se desaconsejan las garrafas de bicarbonato, que se deben ir sustituyendo por cartuchos de bicarbonato en polvo (evidencia nivel C, 2).
5.2. Formas de presentación centralizadas
Los sistemas individuales de concentrados son preferibles, en cuanto a seguridad y posibilidad de individualización, a los centralizados, aunque los primeros sean más costosos y creen mayores problemas de almacenamiento y desechos. Los sistemas centralizados de fabricación de concentrado con bicarbonato son los más susceptibles a la contaminación microbiológica y, por lo tanto, se desaconsejan (evidencia nivel C, 1).
Los sistemas centralizados de fabricación in situ de los concentrados tienen que estar diseñados de manera que dispongan de una fuente de agua purificada, drenaje fácil y toma de tierra para descarga electrostática. Se realizarán con materiales que no causen contaminación al agua, que no sean corrosivos y que eviten la formación de hongos y algas.
Estos tanques de almacenamiento de la mezcla deberán ser vaciados y limpiados de restos antes de utilizar otros baños de concentrados, para prevenir la contaminación cruzada entre las diferentes fórmulas de concentrados. En el de ácido está prohibido usar aditivos, los cuales pueden distorsionar la composición del LD; únicamente se permite añadir potasio o calcio, indicando siempre la concentración final y mencionándolo en el etiquetado.
El tanque de bicarbonato sódico, no recomendado, debe reunir las características descritas, pero además las paredes y el fondo deben ser limpiados y desinfectados. El bicarbonato sódico puede emplearse líquido o en polvo. En ambos casos, y sobre todo cuando se utilice en polvo, deberá controlarse su concentración, habitualmente entre 34 y 40,8 mEq/l, previamente a su distribución.
La otra modalidad consiste en contenedores con concentrado prefabricado. Se distribuyen en contenedores o depósitos grandes, para luego distribuirlos directamente al mezclador del monitor de diálisis. La instalación debe permitir un espacio suficiente y acceso adecuado a tal fin.
La red de distribución de los concentrados deberá estar señalizada, de manera que las cañerías que distribuyan la mezcla ácida irán pintadas en su exterior de un color rojo y las del bicarbonato sódico, de color azul. Así mismo, es recomendable que los tanques sean translúcidos para conocer en todo momento sus niveles; no es recomendable utilizar tubos que indiquen el nivel, sobre todo en el de bicarbonato, para evitar el crecimiento de bacterias.
En todo caso, los sistemas de distribución del concentrado ácido, y en su caso el tanque para su fabricación, deben disponer de programas de desinfección, desincrustación y limpieza de la instalación, y esta debe realizarse a intervalos regulares, al menos anualmente, para garantizar una óptima calidad microbiológica del sistema (ver apartado 8.2).
5.3. Nivel de contaminación microbiológica
El grado de contaminación microbiológica máxima admitida estará de acuerdo con el nivel de pureza del agua purificada al final del periodo válido de conservación. Los niveles de contaminación microbiológica para los concentrados son los mismos que para el agua purificada (apartado 4.1) (evidencia nivel C, 2)
El concentrado de bicarbonato individual, una vez abierto el envase, debe manejarse con cuidado para prevenir una mayor contaminación bacteriana. El uso de envases previamente abiertos debe rechazarse, y debe desecharse la fracción sobrante de una diálisis (evidencia nivel C, 2).
Serán preferibles los concentrados esterilizados o desinfectados por algún procedimiento.
5.4. Niveles máximos de contaminantes químicos
El grado de pureza de los elementos utilizados en la fabricación de los concentrados debe ser alto y seguir las normas al respecto. En su producción se debe usar agua purificada (evidencia nivel C, 1).
Es muy recomendable que el fabricante especifique los niveles de los contaminantes químicos exigibles para el agua purificada. En Estados Unidos el Grade Chemical está regulado por la USP/National Formulary. Las sales usadas en la preparación de los concentrados puede ser fuente de contaminación e intoxicación por metales para el paciente. Ver también ISO13958: 2009.
6. Calidad del líquido de diálisis
Líquido de diálisis ultrapuro
Para todas las modalidades de HD, hemodiafiltración y hemofiltración se recomienda la utilización de LD ultrapuro.
6.1. Niveles máximos de contaminación microbiológica del líquido de diálisis
La contaminación bacteriana máxima admisible en el LD ultrapuro es de 0,1 UFC/ml, y la de endotoxinas, de 0,03 UE/ml. ISO1163: 2009.
La metodología para la determinación coincide con la del agua ultrapura para HD.
Para minimizar la inflamación del paciente en HD, todas las unidades de diálisis deben contar con LD ultrapuro para todas las modalidades de diálisis. El uso rutinario de LD ultrapuro exige la incorporación de ultrafiltros específicos en el circuito del LD (evidencia nivel B, 1). Estos ultrafiltros deben ser utilizados y recambiados según las especificaciones del fabricante.
Existirá un protocolo de actuación ante la evidencia de contaminación del LD de un monitor de HD. Esta actuación incluirá la retirada del monitor, recambio del ultrafiltro de ET y revisión general del funcionamiento del monitor. Se procederá a una desinfección y desincrustación completa, incluyendo el punto de conexión al anillo, la manguera, el circuito hidráulico interno y los Hansen.
6.2. Niveles máximos de contaminantes químicos
Las especificaciones son las mismas que las del agua purificada y ultrapura, apartados 4.1.2 y 4.2, respectivamente, excepto para los solutos que aportan los concentrados y la conductividad resultante(evidencia nivel B, 1).
6.3. Preparación del líquido de diálisis
El monitor de HD es el elemento encargado de mezclar las soluciones concentradas de electrólitos o en polvo con el agua tratada a una concentración electrolítica, pH y temperatura determinados por prescripción médica. El agua del LD debe ser debidamente desgasificada. La cantidad de electrólitos diluidos en el agua se controla con sistemas dobles, por medio de la conductividad eléctrica y/o el pH de la solución final (pHmetro). La temperatura se controla mediante un termómetro. Antes de ser enviado al dializador, el LD debe haber pasado por al menos un ultrafiltro. Los circuitos hidráulicos de los monitores, sin espacios muertos, son preferibles. Es necesario que todo el circuito hidráulico del monitor se desinfecte de forma automatizada y programable.
La conductividad del LD y su composición deberán coincidir con la prescrita por el médico.
El uso regular de un LD ultrapuro es, a largo plazo, la forma de prevenir o retrasar ciertas complicaciones relacionadas con la HD (evidencia nivel A, 1).
7. Control de calidad
La pureza química y microbiológica del agua y del líquido de HD debe monitorizarse regularmente y los resultados deben ser registrados. Han de existir protocolos con pautas de actuación en caso de que los límites de actuación o permitidos sean sobrepasados. Estos protocolos deben tener en cuenta incluso el cierre temporal de la unidad de diálisis cuando los límites de seguridad exigidos alcancen niveles inadmisibles (evidencia nivel C, 1).
7.1. Control técnico de los componentes del proceso
El control diario de elementos o parámetros fundamentales, de fácil y rápida supervisión, permite garantizar el correcto funcionamiento de los diferentes componentes del sistema de tratamiento del agua; además, puede evitar que incipientes problemas en algunos de ellos puedan convertirse en repercusiones graves para algún otro componente del sistema y afectar con ello la calidad del agua tratada. Por ello se controlarán a diario en el agua de aporte y en la tratada: niveles de cloro libre y total (cloraminas), dureza y conductividad. Al tiempo se controlarán las presiones y flujos de los diferentes componentes del equipo de tratamiento de agua y distribución (evidencia nivel C, 1).
Las actuales características demandadas en la calidad del agua para HD hacen necesario un mayor control de todos los elementos implicados en su producción. Es imprescindible llevar un correcto registro sobre todos los controles y actuaciones realizadas sobre el tratamiento de agua, así como observar los protocolos de mantenimiento indicados para cada elemento del tratamiento. Es necesario haber realizado con antelación un protocolo de actuación en caso de detectarse anomalías, dependiendo este del propio tratamiento de agua, del personal implicado, de las características de la propia unidad, etc., por lo que debe ser realizado de forma individualizada por cada unidad de HD.
Es necesario disponer de los manuales técnicos y de usuario de los diferentes equipos. El personal encargado del control debe recibir la suficiente formación e información de todos los elementos que componen el tratamiento de agua, así como contar con la acreditación adecuada.
Los controles periódicos pueden variar en función de los equipos y la calidad del agua a tratar; en algunos casos puede ser necesario realizarlos con mayor frecuencia, especialmente en la fase de validación o puesta en marcha. En esta fase está indicado realizar los controles diarios al menos al inicio de las sesiones de diálisis y al finalizar la última del día, para comprobar la eficacia de los elementos filtrantes, tanto para verificar el correcto volumen de los mismos como la programación de regeneraciones y/o contra lavados.
La frecuencia del control del sistema de tratamiento de agua se basa en 2 niveles, tanto para el control técnico como analítico: el primer nivel, durante la validación de una nueva planta de tratamiento, la reparación de una antigua o después de una contaminación que ha precisado una acción correctora; el segundo nivel, durante el mantenimiento, la supervisión del sistema de tratamiento en el día a día, una vez pasado el tiempo de validación. Los controles a realizar se pueden clasificar en técnicos, químicos y microbiológicos
La siguiente tabla pretende ser una herramienta para ayudar a la organización de los controles. Debería utilizarse de forma complementaría a las indicaciones dictadas por los fabricantes de los equipos, aunque en algunas ocasiones estas son un tanto relajadas en la periodicidad, dado el contexto donde son utilizados.
7.2. Controles analíticos de la calidad del agua y líquido de diálisis
La monitorización del sistema de agua debe ser realizada en diferentes puntos del proceso de producción del LD y con distinta frecuencia según las circunstancias:
-
Periodo de validación de un sistema nuevo de tratamiento de agua después de su instalación, después de una reparación importante o después de haberse detectado niveles elevados de contaminación que han obligado a una acción correctora. Es complicado definir de una forma concreta qué es una reparación importante o acción correctora; algunas sugerencias para interpretarlos como tales serían:
- Cualquier modificación que afecte a su denominación como «producto sanitario» de algunos de los equipos, conforme al Real Decreto 1591/2009.
- Cambios en la calidad de agua de aporte que motiven la instalación o la modificación de alguna parte del pretratamiento y/o del equipo de ósmosis.
- Contaminaciones repetitivas que obliguen, además de a la desinfección pertinente, a la modificación de alguna parte de la instalación por constatarse como posible foco del problema.
El periodo de validación de una reparación del tratamiento del agua puede ser compatible con el funcionamiento de la unidad de HD. Después de la reparación se realizará una desinfección completa, se comprobará el correcto funcionamiento de todos los elementos del tratamiento del agua y que la conductividad del agua tratada es <5 μS·cm−1. Al tiempo se realizarán los controles analíticos especificados en este apartado.
Periodo de mantenimiento: mantenimiento de un sistema en su funcionamiento rutinario.
7.2.1. Microbiológico
Los controles microbiológicos del agua purificada y ultrapura deberán hacerse semanalmente durante el primer mes de puesta en marcha de la unidad (fase de validación). Si alguno de los cultivos o ET fueran positivos, se realizarán las medidas correctoras necesarias y se alargará el periodo de validación otro mes más. Posteriormente, y en la fase de mantenimiento, se realizarán al menos una vez al mes (evidencia nivel C, 2).
Los controles del nivel de endotoxinas se realizarán mensualmente tanto en el periodo de validación como en el de mantenimiento (evidencia nivel C, 2).
Cada centro debe establecer un protocolo por escrito fijando la periodicidad del método y las responsabilidades de estos controles. Las unidades en funcionamiento deberán realizar como mínimo un control mensual de la calidad del agua de diálisis empleando la metodología de cultivo y los puntos de muestreo fijados en esta Guía. Para más detalles, ver anexo 3 (control microbiológico).
Puntos de toma de muestras para cultivos microbiológicos: en el periodo de validación se tomarán muestras del agua de aporte, del agua descalcificada, del agua inmediatamente antes del equipo de OI, del agua tratada a la salida de la ósmosis, del agua del final del anillo de distribución y al menos en el 10% de las tomas de agua para los monitores (puestos de HD) y del LD a la entrada al dializador con un mínimo del 10% de los monitores.
Los controles microbiológicos del agua no se realizarán antes de las 24h después de una desinfección.
En el periodo de mantenimiento se tomarán muestras para cultivos y ET del agua tratada a la entrada y retorno del anillo, después de la ósmosis y en un 10% de las tomas de agua de los monitores. Es necesario que al cabo de un año se hayan tomado muestras de todas las tomas de agua de los monitores, incluidas las no utilizadas. Respecto al LD, se tomarán muestras para cultivos y ET predializador en el 10% de los monitores. Al cabo de 12 meses todos los monitores, incluidos los de reserva, deben contar con un control (evidencia nivel C, 2).
En el periodo de mantenimiento no es necesario tomar muestras del agua de aporte o puntos intermedios del pretratamiento, a menos que se detecte contaminación o sospechas de alteraciones en la calidad del agua tratada.
Es aconsejable realizar muestreos entre la salida del filtro de carbón y la entrada al equipo de OI, especialmente si no se tiene un protocolo específico de desinfección periódica de este tramo.
Para los monitores se seguirá el mismo criterio que en el periodo de validación, con el fin de que no estén más de 12 meses sin control microbiológico.
En las instalaciones donde existan depósitos de almacenamiento de agua tratada, se tomarán también muestras a la entrada y salida de los mismos; generalmente coincidirán con la salida del equipo de ósmosis y el principio del anillo de distribución, respectivamente.
En caso de contaminación microbiológica ambiental de la unidad de HD, se puede realizar un control adicional en el drenaje de los monitores, pero es fundamental tener en cuenta que este tramo de tubería está expuesto a contaminaciones externas, por su proximidad o contacto directo con el desagüe.
En la HD domiciliaria con fabricación de LD se recomienda realizar un control microbiológico mensual, pudiendo alternarse una muestra de agua con una de LD.
Existen normas y guías locales más exigentes en cuanto al número de muestras y la frecuencia de su control.
7.2.2. Químico
La conductividad, corregida para 25°C, se medirá continuamente en el permeado de la ósmosis. Su lectura estará visible y conectada a algún sistema de alarma que alertará sobre sus cambios.
Se controlará diariamente: dureza, cloro libre y total (cloraminas). Sus puntos de muestreo se especifican en el apartado 7.1. Se realizarán preferentemente antes del inicio de la primera HD del día.
El control de todos los contaminantes químicos especificados en el apartado 5.2 (niveles máximos de contaminantes químicos) se realizará 2 veces en el periodo de validación y anualmente en el de mantenimiento. El aluminio se controlará semestralmente.
La muestra para la determinación de contaminantes químicos se obtendrá de una de las tomas de agua de los monitores.
Diariamente se medirá la dureza mediante un método de titulación o de manera permanente con un equipo de alarma. La regeneración debe ser adaptada al ciclo del volumen, a la actividad de la sal, a la capacidad de las resinas y a la dureza del agua, comprobándose el estado del programador diariamente.
Donde el sistema de desinfección del agua potable se realice mediante cloraminas, se debe detectar de forma indirecta su nivel en el agua, midiendo el de cloro libre y el total y calculando la diferencia.
Existen normas y guías locales más exigentes en cuanto al número de muestras y la frecuencia de su control.
8. Métodos de prevención y corrección
8.1. Métodos para el agua
Los procedimientos de desinfección, desincrustación y acción detergente son parte integral del sistema de mantenimiento de la planta del agua y de la red de distribución. La frecuencia, el tipo de desinfección y desincrustación (calor, químico, mixto) y los cambios periódicos de sus componentes (filtros, resinas, membranas, lámparas UV) deberían hacerse de acuerdo a las instrucciones del fabricante y adaptándose a los resultados del control microbiológico (evidencia nivel C, 1).
El objetivo del mantenimiento de un tratamiento del agua para diálisis y de los monitores de diálisis es prevenir que se contaminen, no es tratar las contaminaciones. No es admisible una metodología basada en tratar las contaminaciones. La prevención está basada en desinfecciones programadas; su frecuencia y tipo estarán en función del diseño del tratamiento del agua y de los monitores de diálisis. Los controles analíticos sirven para comprobar el buen funcionamiento, no para indicar desinfecciones (evidencia nivel C, 1).
Los sistemas de desinfección automatizada, tanto por calor, químicos o mixtos, del circuito de distribución del agua tratada asociados a un filtro de endotoxinas son muy recomendables. Permiten un mantenimiento más fácil y seguro de los estándares microbiológicos. Su programación automática frecuente permite la prevención de la contaminación. La desinfección térmica del anillo programable se recomienda para el mantenimiento de la producción de agua ultrapura (evidencia nivel C, 1).
Deberá tenerse en cuenta que los materiales de fabricación de los circuitos no contribuyan a la contaminación química del agua (aluminio, zinc, cobre, etc.) y sean compatibles con los diferentes desinfectantes a utilizar en su mantenimiento. Los materiales más adecuados para el circuito de distribución del agua son: acero inoxidable (mínimo INOX316); acrilonitrilo butadine estireno; polietileno reticulado (PEX-A); polipropileno; polifloruro de vinilo y policloruro de vinilo, y nuevos elementos como el PVDF (polifluoruro de vinilideno). En todo caso deberán estar etiquetados para uso sanitario y con marcado CE. Los resistentes a altas temperaturas son siempre preferibles.
Los de acero inoxidable permiten la desinfección térmica y química, pero lo importante en este caso es que se trate de un acero homologado y que las soldaduras no provoquen oxidación posterior.
Las desinfecciones preventivas pueden afectar a depósitos, pretratamiento, tratamiento, anillo y monitores.
La limpieza de la sala de HD y la de los desagües son otros aspectos a tener en cuenta.
Por todo lo anterior podemos definir lo que serían desinfecciones preventivas y desinfecciones correctoras. Las desinfecciones preventivas mínimas serían:
Una desinfección que comprenda el anillo debe hacerse al menos cada 4 meses. En el caso de aparecer contaminación microbiológica se realizará una desinfección correctora y se aumentará la frecuencia de las preventivas.
Si se cuenta con un sistema de desinfección por calor automático, recomendado para producir agua ultrapura, este se debería programar al menos una o 2 veces a la semana.
La desinfección completa, que incluya el pretratamiento, se debería hacer al menos anualmente coincidiendo con el cambio del carbón activado.
Idealmente, las desinfecciones del anillo deberían ir acopladas con desinfecciones de los monitores.
Cuando haya depósitos de agua tratada, la desinfección del anillo debe afectar al depósito.
Según las directrices de la norma ISO (ISO_DIS23500), el circuito de la unidad de OI debe desinfectarse de forma periódica. Esto incluye:
8.2. Métodos para los concentrados
Los concentrados individuales deben cumplir las especificaciones del etiquetado. Si se demuestra que están contaminados se rechazarán, se notificará y se cambiarán por un lote correcto.
En los sistemas centralizados se realizarán las desincrustaciones y desinfecciones y otras formas de prevención y tratamiento según especifique la empresa proveedora. Se recomienda la desinfección al menos cada 12 meses y realizar determinaciones analíticas bacteriológicas 3 días antes de su desinfección.
Ante la presencia de contaminación bacteriana del LD, con niveles adecuados en el agua, se debe sospechar como fuente de contaminación el concentrado, realizando los cultivos pertinentes.
8.3. Métodos para el líquido de diálisis
El mantenimiento y la desinfección periódica de los monitores de HD son obligatorios para prevenir la proliferación bacteriana y la formación de un biofilm en el circuito hidráulico. Para evitar la contaminación bacteriana y la transmisión de enfermedades vírales se recomienda la desinfección después de cada sesión de HD (evidencia nivel B, 1).
La realización de cualquier sesión de HD requiere que la composición del LD sea la correcta y que cualquier desinfectante sea completamente aclarado antes del comienzo.
La pauta y el tipo de desinfección se deben realizar según recomendación del fabricante del monitor, lo cual tiene que estar visado por el responsable de la clínica e informado a todo el personal que intervenga en dicho proceso. La realización de desinfecciones y aclarados debe quedar registrada, así como el nombre del responsable.
Las mangueras de los monitores y todos los elementos del circuito hidráulico que no entran en la desinfección automática del monitor se deberán desinfectar al menos anualmente.
Una vez realizada una desinfección de cualquier elemento de la producción del LD, tratamiento del agua, concentrados centralizados y monitores de diálisis, se debe realizar el aclarado pertinente y la comprobación del nivel residual del desinfectante (ver anexo 4).
9. Gestión de calidad del líquido de diálisis
9.1. Personal
El éxito del procedimiento de la gestión de calidad del agua y del LD incluye la colaboración de todo el personal que trabaja en la unidad de diálisis y se relaciona con los procedimientos a seguir: nefrólogos, enfermeras, técnicos, analistas, microbiólogos y preventivistas; todos deberán seguir de manera estricta los protocolos establecidos.
Debe haber, al menos, una persona encargada de realizar la gestión de calidad del tratamiento del agua.
Puede ser el encargado del mantenimiento y reparación de la unidad de tratamiento de agua. En el caso de que se trate de un contrato externo, lo realizará conjuntamente con un responsable de la unidad de HD. El personal encargado de realizar la gestión de calidad debe estar preparado específicamente para usar el equipo de tratamiento de agua, la metodología adecuada para los controles y acciones correctoras.
El personal encargado será sometido a auditorias periódicas, para confirmar su aptitud.
Los procedimientos incluirán la posibilidad del cierre temporal de la unidad de diálisis si se exceden los límites de seguridad por contaminantes.
9.2. Medios necesarios
El protocolo de control de calidad del LD tiene que ser debidamente especificado y seguido por las personas responsables. Los medios para su correcto funcionamiento serán los especificados en esta guía, en cada uno de los apartados. Estos medios personales y materiales deben ser facilitados por la empresa encargada o la entidad administrativa responsable de la asistencia de los pacientes en tratamiento en HD. La empresa o institución propietaria de la unidad de HD será la responsable de proveer los medios necesarios para su correcto funcionamiento.
No se debe dializar sin agua filtrada por carbón activado y osmotizada.
9.3. Documentación
Debe existir un libro de registro paginado, o soporte informático seguro y controlado, donde se anotarán todas las actuaciones realizadas respecto al tratamiento del agua, según especifica esta guía. La persona responsable del tratamiento del agua será el encargado de cumplimentarlo.
Los resultados sobre la pureza química y bacteriológica del agua de diálisis deben ser monitorizados de forma periódica y regular, y esos resultados serán debidamente registrados. Se deben tener procedimientos bien documentados, en los cuales se informe sobre los pasos a seguir en el caso de que los límites sean excedidos. También deben quedar registradas las acciones correctoras.
9.4. Responsabilidades
Cada persona que interviene en la gestión de la producción del LD es responsable de su cometido.
El responsable final de que el LD sea correcto, tanto en su composición química como respecto a la contaminación bacteriana, y de que cumplan los estándares descritos, es el médico encargado o responsable de la unidad de diálisis.
La entidad pública, empresa concertada o privada responsable de la asistencia sanitaria a los pacientes en HD deberá garantizar todos los medios necesarios para llevar a cabo este estándar de calidad.
Los procedimientos incluirán la posibilidad del cierre temporal de la unidad de diálisis si se exceden los límites de seguridad por contaminantes.
10. Justificación bibliográfica de la Guía
10.1. Pureza y calidad del agua para hemodiálisis
El agua de HD supone más del 96% del LD que se pone en contacto con el paciente a través del dializador, en una cantidad entre 90 y 240 l por sesión aproximadamente. Algunos contaminantes del agua se pueden transferir al paciente y acumularse en grandes cantidades. A esto habría que sumar el hecho de que la insuficiencia renal le impide eliminar los contaminantes acumulados, pudiéndole ocasionar una verdadera intoxicación. Existen numerosas publicaciones en la literatura médica que mencionan intoxicaciones agudas y crónicas en pacientes en HD producidas por contaminación del agua y que han condicionado una importante morbimortalidad1-17. Al ser el agua el principal componente del LD y el menos estandarizable, es uno de los que precisa un mayor control en su producción.
Al principio de la HD como técnica de tratamiento de la insuficiencia renal crónica, el tratamiento del agua intentaba prevenir el síndrome de agua dura y las contaminaciones bacterianas5. Posteriormente hubo que enfrentarse a contaminantes difíciles de eliminar, como es el caso de algunos metales como el aluminio, cuya intoxicación produce encefalopatía y osteomalacia1,2, o el caso de las cloraminas, que pueden provocar epidemias de anemización por hemólisis en las unidades de HD3,8. Al tiempo se han ido publicando casos de intoxicación por diversos contaminantes10-16.
En esta década, la mayor preocupación ha pasado a un campo limítrofe entre la repercusión clínica y subclínica, como es el caso de los pirógenos-endotoxinas. Sabemos actualmente que aunque no siempre aparecen reacciones a pirógenos, muchos de nuestros pacientes están expuestos a endotoxinas que condicionan una situación inflamatoria crónica que a la larga repercute en diversos aspectos clínicos de los pacientes17-28. Nuestro objetivo actual debe ser conseguir un líquido de HD ultrapuro, que solo contendrá agua y los componentes necesarios. Una parte fundamental de la biocompatibilidad de la HD la constituye el LD, y de ahí la importancia de su nivel de calidad18,21,26,27,29.
Es difícil precisar dónde se debe establecer el punto de corte en los niveles de sustancias potencialmente tóxicas en el LD. La AAMI fijó sus niveles límite en función de la toxicidad de las sustancias30. En una primera categoría incluyó los solutos que son añadidos en el LD, como Na, Ca, Mg y K, y estos fueron fijados en niveles que no influyesen en la concentración final en el LD; en la segunda categoría incluyó las sustancias reguladas por las normas del agua potable, como arsénico, cadmio, plomo, etc. (ver anexo 5), fijando su límite en un 10% de aquel; en la tercera incluyó las sustancias con especial importancia en la intoxicación de los pacientes en diálisis, como las cloraminas o el aluminio, limitando su nivel en función de los valores referidos como tóxicos en la literatura30. Desde 1981 se han ido conociendo nuevos tóxicos potenciales provenientes del agua, componentes del sistema de tratamiento del agua, concentrados y monitores, lo que ha obligado a añadir nuevos elementos en la lista de elementos a eliminar y controlar31. También ha aumentado la atención prestada a la contaminación bacteriana y su consecuencia, la endotoxinemia. En esta Guía se han tomado como límites máximos los marcados por la ISO de 2014 y complementados en ocasiones por las normas de la Farmacopea Europea. Está claro que se trata de un proceso en constante revisión, dependiendo de la aparición de nuevos tóxicos o nuevos niveles de toxicidad. En este sentido, se deben destacar 3 posibles cambios para el futuro.
El primero lo constituyen los niveles de aluminio. El aluminio en el agua se presenta como ion, asociado a sales y en forma coloidal, unido a materia orgánica. Dependiendo del pH, la forma iónica puede variar entre un catión trivalente a un anión complejo. Los descalcificadores solo eliminarían sus formas catiónicas. El aluminio coloidal no se podría eliminar con los desionizadores, y solo la OI sería capaz de eliminarlo. El aluminio se añade en ocasiones al agua como floculante de la materia orgánica, por lo que sus niveles pueden ser muy elevados. En estas situaciones la única forma de conseguir niveles óptimos en el LD es el trabajar en serie con 2 OI1.
Por otro lado, sabemos que el balance de aluminio durante la diálisis se establece entre el aluminio libre o ultrafiltrable del plasma (5-10% del total) y el aluminio del LD, y si queremos hacer un balance claramente negativo, manteniendo niveles de aluminio en sangre inferiores a 30-50 μg/l, debemos mantener una concentración en el LD inferior a 5 μg/l32. En la actualidad queremos que los pacientes en HD mantengan niveles de aluminio inferiores a 20 μg/l.
La medición de sustancias como el aluminio precisa una metodología exacta, utilizando agujas no metálicas, tubos especiales y evitando todo tipo de contaminaciones. La determinación se realizará por espectrofotometría de absorción atómica, en cámara de grafito para evitar contaminaciones. Dadas las características especiales del aluminio, si la determinación de aluminio en el agua está en buenos niveles (<5 μg/l) y la conductividad del agua es menor de 5 μS·cm, podemos presumir que las características del agua respecto a iones son correctas y que el resto de aniones y cationes tendrán niveles correctos. Tal vez la excepción a esta regla la constituyen las aguas con contenidos muy elevados de mercurio o hierro, que requiere para su eliminación sistemas de floculación y quelación.
El segundo tema de discusión lo constituye el nivel admisible de cloraminas. El cloro se añade al agua potable como bactericida a través de su gran capacidad oxidante. Esta función la realiza el cloro libre, que difunde rápidamente. La forma de mantener niveles estables de cloro libre es la formación de cloraminas, compuestos mono, bi o triclorados de nitrógeno, que liberan lentamente el cloro. Las cloraminas son capaces de atravesar la mayoría de los sistemas de tratamiento de agua, incluida la OI33,34. Existen fundamentalmente 2 sistemas para su eliminación del agua: su reacción con el carbón activado o con el bisulfito de sodio. La elección de un sistema u otro depende de las características del agua a tratar y del pH al que dan lugar estas reacciones, pues van a influir en el funcionamiento de la OI, según el tipo de membrana. Para la producción de agua purificada para HD se recomienda el carbón activado31,34,35, por tener un mantenimiento más fácil, ser más seguro y tener un espectro de retención más amplio.
El mantenimiento adecuado del carbón y su renovación periódica es fundamental. El paso a la sangre de pequeñas cantidades de cloraminas va a condicionar efectos oxidantes, siendo el más llamativo la hemólisis. Las cloraminas son difíciles de medir, por lo que se suele recurrir a estimarlas como la diferencia entre cloro total y cloro libre, método poco sensible. Realizando la medición así, los niveles admisibles de cloro total deberían ser inferiores a 0,06 mg/l, o los de cloraminas inferiores a 0,05 mg/l, no 0,1 ml/l, como se limita actualmente31,35,36. Se han publicado datos35,37 que demuestran mayor anemización asociada a niveles de cloraminas de alrededor de 0,1 ppm. Una solución alternativa que se utiliza en Estados Unidos es la colocación de 2 filtros de carbón activado en serie y hacer las determinaciones entre los 2.
El tercer tema de discusión es cómo se deben determinar las sustancias pirogénicas, las capaces de desencadenar inflamación en los pacientes en HD. El método de referencia es la prueba LAL. ¿Debemos utilizar métodos de determinación más sensibles de detectar endotoxinas (ET) o debemos buscar pruebas, sencillas y estandarizadas, que sean capaces de detectar ET y otras sustancias pirogénicas? Este tema se aborda más adelante.
Por tanto, de acuerdo con el grado de pureza deseada en el agua, la complejidad y el coste del sistema de tratamiento difieren significativamente. Pueden usarse 2 grados distintos de pureza para el agua en HD: agua purificada y agua ultrapura. El agua purificada es la forma básica de agua tratada, válida para las modalidades de HD convencional. La contaminación microbiológica del agua purificada debería cumplir las recomendaciones de la Farmacopea Europea, recuento bacteriano menor de 100 UFC/ml y menos de 0,25 UE/ml de endotoxinas. El agua ultrapura debe contener menos de 10 UFC/100 ml y 0,03 UE/ml, así como otros requerimientos especificados en estas guías.
El agua ultrapura se recomienda para producir un LD ultrapuro. El LD tendrá el grado de pureza del peor de sus componentes. El LD ultrapuro se recomienda para cualquier modalidad de HD. En España, en el año 2015, entre el 80 y el 90% de las HD se realizan con dializadores desechables de alta permeabilidad. Además es necesario para la HD de alto flujo y en las modalidades de hemodiafiltración y hemofiltración que usan la producción en línea del líquido de sustitución.
La dificultad económica para lograr un LD sin contaminación bacteriana ni ET es lo que sigue propiciando que se admitan 2 niveles de calidad en muchas guías. Lo óptimo sería un LD de calidad farmacéutica semejante a la de las soluciones parenterales. Sabemos que se puede observar estimulación de los monocitos con niveles plasmáticos de ET tan bajos como 0,05 ng/ml38. Hay que tener en cuenta que el estímulo se produce con la exposición acumulada durante la sesión de HD, y además se potencia por otros estímulos coadyuvantes, como pueden ser el complemento, activado por la membrana del dializador o el acetato del LD. Por eso se ha escogido un nivel de ET para el LD ultrapuro semejante al de los líquidos estériles, que son los que aseguran que no hay niveles suficientes de ET para estimular a los monocitos. La contaminación bacteriana es el origen de las ET y de otras sustancias con capacidad pirogénica, por lo que debe ser la menor posible. El límite para el agua purificada de 100 UFC/ml, como señalan la mayoría de las normas al uso, incluida la Farmacopea Europea, puede que no sea suficiente. Conseguir un LD con una contaminación bacteriana baja implica que sea así la de sus 3 componentes. También hay que tener en cuenta que el LD es un medio mejor que el agua para el crecimiento bacteriano, por lo que el crecimiento exponencial bacteriano es mayor en el LD que en el agua purificada. A pesar de estas dificultades, el nivel microbiológico recomendable del agua para fabricar LD ultrapuro debe ser el del agua ultrapura39,40.
Bibliografía
10.2. Diseño de un sistema de tratamiento de agua
Actualmente el componente fundamental del tratamiento de agua para HD es la OI.
El diseño técnico consiste en la unión óptima de los distintos componentes del tratamiento del agua en lo que se refiere a tamaño, posición y pureza que garantice la calidad del agua tratada. La combinación de un sistema de pretratamiento de agua (descalcificador, carbón activado y microfiltros), módulos de OI y un sistema de tuberías directo, sin depósito si es posible, representa la configuración mínima exigida para producir agua purificada y prevenir la contaminación microbiológica.
Para producir agua ultrapura se utiliza un sistema basado en la existencia de un segundo módulo de OI y/o un desionizador electroquímico colocado en serie. Un sistema como este permite la producción de agua ultrapura de acuerdo a unos criterios de pureza muy exigentes.
Para prevenir la contaminación bacteriana y la formación de un biofilm, el sistema de distribución del agua debe estar diseñado a conciencia. Los materiales válidos para la red de tuberías están hechos de acero inoxidable o polietileno. El mayor esfuerzo debe dirigirse para conseguir una configuración adecuada del anillo de distribución, siendo las tuberías lineales, favoreciendo el flujo continuo y a alta velocidad y previniendo el estancamiento de agua evitando así los espacios muertos1,2. La inclusión en el tratamiento del agua de un sistema de desinfección por calor, con programación automática, preferiblemente sincronizada con la de los monitores, anillos secundarios y un ultrafiltro para endotoxinas son una necesidad si se quiere obtener agua ultrapura3.
La destilación es un sistema de purificación del agua que se basa en su cambio de estado, pasando de un estado líquido a gas mediante calor, para posteriormente condensarse a través de su enfriamiento y volver a su estado líquido inicial. Es efectivo eliminando todo tipo de contaminantes, salvo los volátiles. A pesar de su gran efectividad, no se emplea habitualmente en HD por resultar caro y aparatoso1,2.
Para más detalles, ver anexo 2.
Bibliografía
10.3. Concentrados para diálisis
El concentrado puede ser el punto de partida de la contaminación bacteriana del LD, sobre todo si se usa bicarbonato en forma líquida, que constituye un excelente medio de cultivo para el crecimiento bacteriano. Además, las sales usadas en la preparación del concentrado pueden dar lugar a intoxicación por metales pesados1.
La Real Farmacopea Española y la Farmacopea Europea2 mencionan las características que deben cumplir los concentrados o disoluciones para HD. Admite una variabilidad de ±2,5% en las concentraciones finales de Na, variabilidad difícilmente admisible en clínica. Esta variación representa ±3,5 mmol/l, que para una concentración de 140 mmol/l representaría unos márgenes entre 136,5 y 143,5 mmol/l de Na. La HD, con esas 2 concentraciones extremas, es totalmente distinta3. Aunque los monitores, a través del control de la conductividad, pueden corregir parcialmente estos errores, también tienen su variabilidad. Los márgenes de variabilidad para K, Cl, Mg y Ca son ±5%, teniendo en este caso menos importancia clínica. Esa norma establece la concentración de endotoxinas admisible como menor de 0,5UE/ml en la solución ya diluida, aunque no menciona el método de determinación. Propone como método de detección de pirógenos la inoculación a conejos. En esta Guía se ha establecido un nivel de exigencia microbiológico, igual que el del agua purificada. El margen de variabilidad de Na se ha establecido en ±2,5% de acuerdo con la ISO13958:2009 y la forma de determinar las ET mediante la prueba LAL, por estar mejor estandarizada.
La calidad de los concentrados se basa en el grado de pureza de los ingredientes, tanto el agua como los solutos. Keshaviah et al.4 sugieren que los niveles de contaminación, fundamentalmente por metales traza, deben ser como máximo de una magnitud, que una vez diluidos para fabricar el LD no sobrepasen los niveles fijados para el agua purificada (apartado 4.1.2). La Farmacopea Europea 3.ª edición determina que el contenido de aluminio del cloruro sódico utilizado para los concentrados para HD debe ser inferior a 0,2 ppm.
El uso de un LD con citrato surge como una alternativa para acidificar sin usar acetato. El citrato es un quelante del calcio que se usa también por su efecto anticoagulante al disminuir el calcio iónico5. Se han descrito varios efectos beneficiosos a largo plazo en relación al citrato, como una menor trombogenicidad, mejoría de los aclaramientos, de la inflamación, nutrición, tolerancia y del control ácido-base, con menor acidosis prediálisis5-13. Son necesarias más evidencias científicas que justifiquen el cambio del acetato por citrato en todas las HD.
Bibliografía
10.4. Líquido de diálisis
Los monitores de HD han mejorado en muchos aspectos técnicos, aunque todavía no se ha logrado que garanticen la esterilidad de su circuito hidráulico mientras trabajan. Las cubas del baño de diálisis de los primeros monitores eran un punto de contaminación bacteriana, al igual que los sistemas de recirculación, los Canister. Los sistemas de control de la ultrafiltración en circuito cerrado también presentaban problemas para su desinfección. Las máquinas actuales representan una clara ventaja respecto a las anteriores en cuanto a la garantía de su nivel de desinfección. La utilización del bicarbonato como alcalinizante ha supuesto un verdadero problema respecto al riesgo de contaminación bacteriana. Cualquiera de los sistemas proporcionadores de bicarbonato no son estériles y su riesgo de contaminación es muy alto. El riesgo de contaminación bacteriana de los concentrados ácidos es mínimo en comparación con los de bicarbonato.
El uso rutinario de agua ultrapura para abastecer los monitores de HD no es suficiente para garantizar la pureza microbiológica del LD. El bicarbonato de los LD es un excelente medio de cultivo para el crecimiento bacteriano, pudiendo ser el origen de bacteriemias y reacciones a pirógenos. El monitor facilita la contaminación del LD por la complejidad de su circuito hidráulico. Varios factores, como el diseño del circuito hidráulico o una desinfección inadecuada, favorecen el crecimiento bacteriano y la formación de un biofilm en el circuito. La contaminación microbiológica del LD o la presencia en este de productos derivados de las bacterias crean potencial patología en el paciente en HD, que debe prevenirse mediante el uso de líquido ultrapuro. Por lo anterior se deben realizar controles periódicos de la calidad del LD, según se especifican en el apartado 7, comprobándose que se cumplen las especificaciones de calidad del apartado 6.
Microbiología
Existen microorganismos perfectamente aclimatados a un medio tan hostil como es el de los circuitos de agua tratada, en los que, por poner un ejemplo, apenas hay nutrientes. Son microorganismos especiales y que como tales deben valorarse. La calidad bacteriológica del LD depende en gran medida del diseño de la planta de tratamiento del agua, de su sistema de distribución, de la calidad de los concentrados para diálisis y del método de desinfección del circuito y monitores y, cómo no, del método de control que utilicemos. En concreto nos referimos a la metodología para cultivar las muestras de agua y LD.
Endotoxinas
Los microorganismos, si el sistema está estanco, no van a pasar del LD a la sangre, pero sí van a poder pasar las ET y otras sustancias pirogénicas (SP). Las SP son productos bacterianos que se liberan con la lisis bacteriana o son excretadas. Algunas de estas sustancias tienen pesos moleculares inferiores a 10 kD y, por tanto, pueden pasar las membranas de diálisis por difusión. Las endotoxinas más conocidas corresponden a lipopolisacáridos de la membrana de los microorganismos gramnegativos, la mayoría de ellos detectables por la prueba del LAL. Existen otras toxinas bacterianas (SP), como exotoxinas, peptidoglucanos y muramilpéptidos. La característica compartida por estas sustancias es su capacidad para actuar como pirógenos. Entre estos contaminantes, las ET son las que poseen una mayor potencia pirogénica.
La determinación de ET bacterianas se realiza mediante el test del limulus (LAL), y puede realizarse mediante: a)gelificación, quizás el más habitual; se basa en la capacidad de estas sustancias para formar geles, o b)turbidimetría, basado en la capacidad que tienen las endotoxinas para reaccionar con sustratos endógenos que se escinden generando turbidez y colorimétricos, que suponen una modificación del anterior y cuya base es la capacidad de las endotoxinas para reaccionar con sustancias que desarrollen color. Además de estos métodos cuantitativos, existen otros métodos de detección de contaminación por ET basados en su actividad inmunógena, como son: la producción de citoquinas por monocitos o neutrófilos o el marcaje isotópico y la determinación de anticuerpos anti-ET. Como hemos comentado con anterioridad, el método más utilizado es el LAL. Cuando se quiera controlar el agua purificada bastará con utilizar una técnica sencilla como el Gel-Clot. Sin embargo, si se quiere que sea suficientemente sensible (0,01 UE/ml), habrá que recurrir a pruebas cromogénicas cinéticas1.
La determinación de ET puede interferirse por factores como la composición o el grado de turbidez del vehículo de la muestra, por lo que es aconsejable remitir diferentes muestra patrón al laboratorio, las cuales sirvan de referencia. Así mismo, las ET se adhieren con facilidad a ciertos plásticos, por lo que es aconsejable utilizar tubos de vidrio o plásticos de baja afinidad para proteínas (mini sorp tubes).
Las ET LAL detectables son solo una parte de las SP, y además las de mayor peso molecular. El método más útil de determinación de SP en HD es medir su repercusión en los pacientes a través de la producción de citoquinas por los monocitos, pero es un método laborioso y caro. Se ha propuesto un método más sencillo2. Las SP pasan a la sangre en el dializador fundamentalmente por retrofiltración, pero las de pequeño peso molecular también pueden pasar por retrodifusión. El paso a sangre se ha demostrado con todas las membranas de diálisis y no solo depende de la cantidad de SP, sino también de su calidad. Con las membranas de alta permeabilidad las reacciones a pirógenos serían más frecuentes que con las de baja permeabilidad3. Las SP atravesarían con mayor facilidad las primeras y la retrofiltración es más común con ellas. En la determinación de ET no solo sería importante el método utilizado, sino que también lo sería el momento de su toma y la conservación de las muestras. Una vez las SP están en la sangre, la inducción de los monocitos no es lineal, sino que entran en juego otros factores que pueden aumentar o disminuir la producción de citoquinas4. Este proceso es multifactorial, y en él influyen: la cantidad y el tipo de toxina, el tipo de membrana, los factores plasmáticos y la actuación concomitante de otros sistemas de activación e inactivación monocitaria5. Se sabe que la presencia de proteínas, o sangre entera, es un factor potenciador. Se conocen al menos 2 proteínas: una transportadora (LBP) y otra con capacidad de permeabilidad necesarias en este proceso (BPI)6. También entran en juego algunas citoquinas contrarreguladoras, como la IL-107. El estado de nutrición y el sistema inmune jugarían un papel a este nivel. En la producción de citoquinas por los monocitos es muy importante la presencia de otros estímulos o señales al mismo tiempo, como puede ser la activación del complemento por la membrana del dializador o el acetato del LD.
Todo lo anterior explica por qué las correlaciones entre las unidades formadoras de colonias en los cultivos (UFC/ml), niveles de ET, LAL detectables y producción de citoquinas son generalmente malas. La destrucción de bacterias disminuye su concentración en el líquido, pero posiblemente dará lugar a un aumento de la concentración de ET, y estas serán capaces de inducir la producción de citoquinas si atraviesan la membrana de diálisis y se unen a otros factores concomitantes activando a los monolitos. Algunas ET en niveles plasmáticos tan bajos como 0,05 ng/ml son capaces de inducir la formación de IL-18.
La activación crónica de citoquinas da lugar a una serie de alteraciones de la respuesta inmune produciendo una situación de inflamación crónica9-15. Las reacciones a pirógenos aparecerían en el 1-5% de las HD. Serían más frecuentes con membranas de alta permeabilidad y disminuyen si el LD es filtrado con una membrana con capacidad adsorbente, como la polisulfona o poliamida16-18. La utilización de ultrafiltros de polisulfona, poliamida o posidina para filtrar el LD es efectiva, consiguiendo un líquido con un nivel ínfimo de endotoxinas y bacterias. Lo anterior implica una menor producción de citoquinas16,19,20. Estos filtros logran su efecto por adsorción y no solo por su punto de corte, que es de 60 kD, y por tanto superior al PM de numerosas SP. Por esto es importante su recambio periódico.
La exposición a las endotoxinas y otras sustancias pirogénicas en el LD se relacionan con parte de la endotoxinemia de los pacientes en HD y algunas de sus complicaciones inflamatorias, vasculares y nutricionales20.
El LD se produce en el monitor. La antigüedad del mismo, independiente de un mantenimiento adecuado, se relaciona con la seguridad y la eficiencia en su fabricación. Se recomienda que los monitores de HD tengan una vida útil que no supere los 7 años o las 30.000 h de funcionamiento21,22.
Bibliografía
10.5. Control de calidad
La frecuencia del control del sistema de tratamiento de agua se basa en 2 niveles, tanto para el control técnico como para el analítico: el primer nivel, durante la validación de una nueva planta de tratamiento, la reparación de una antigua o después de una contaminación que ha precisado una acción correctora; el segundo nivel, durante el mantenimiento o la supervisión del sistema de tratamiento en el día a día, una vez pasado el tiempo de validación. Los controles a realizar se pueden clasificar en técnicos, químicos y microbiológicos1-4.
Los controles técnicos de la producción del agua purificada comprenden verificar que el agua de aporte, a tratar, cumple con los criterios de calidad requeridos para agua de consumo humano5-7. Es fundamental tener información sobre los contaminantes del agua de aporte y sus cambios; de estos es necesario realizar su detección precoz, para evitar colapsos del tratamiento de agua e intoxicaciones masivas. Una parte importante de los incidentes relacionados con el agua para HD, o con el funcionamiento del propio tratamiento, vienen derivados de la calidad del agua de aporte8-12.
La correcta eficacia del descalcificador y del declorador, así como el estado de los programadores que gestionan el sistema de trabajo-regeneración y/o contralavado, deben comprobarse diariamente; se recomienda que sea antes de comenzar con las sesiones diarias, y también es útil al finalizar el ciclo de funcionamiento, antes de la regeneración, e incluso combinando ambas alternativas, principalmente en la fase de validación. Se medirá la dureza del agua que sale del descalcificador. Pueden usarse kits de titulación desechables, sensibilidad <1 mg/dl, o bien un sistema de medición permanente por medio de una sonda automática, equipados con un sistema de alarma o métodos colorimétricos. El sistema de regeneración del descalcificador depende de la cantidad de resinas, de salmuera y de la programación del elemento de control. Para la decloración deben hacerse controles de cloro total, combinado y libre, mediante kits desechables, reactivos o bien colocando un clorómetro en el circuito, con el fin de controlar el nivel de cloraminas y su eliminación después del filtro/s de carbón activado13-15.
El correcto funcionamiento de la OI y/o del electrodesionizador debe comprobarse diariamente midiendo la conductividad del permeado, así como el porcentaje de agua de rechazo y las presiones de trabajo16-19.
El control regular del SDI (fundamentalmente en el agua antes del equipo de OI, pero también en el agua de aporte o a lo largo del pretratamiento) determina una evaluación de la calidad del agua con que se hace trabajar al equipo de OI, especialmente cuando la duración de las membranas es notablemente menor a la prevista y/o cuando no se alcanza la calidad de agua esperada. Las condiciones del agua a tratar pueden variar sustancialmente a lo largo del tiempo; el aumento o los cambios de los solventes (especialmente de tipo coloidal) en ella pueden ser tales que no lleguen a ser retenidos en la proporción adecuada por el pretratamiento. Conocer este valor ayuda a determinar las posibles acciones a acometer para optimizar las condiciones de trabajo de las membranas de OI: modificaciones o acciones correctoras en el pretratamiento de agua, solicitud de las condiciones de calidad del agua de aporte y de las instalaciones hidráulicas anteriores al tratamiento de agua, etc. El SDI antes del equipo de OI debe ser al menos <5, y cuanto menor sea, mejores serán el rendimiento y la duración de las membranas de OI20-22. En las páginas técnicas de los diferentes fabricantes de membranas de OI y en cualquiera de los manuales de tratamiento de agua de las unidades de HD encontraremos la referencia del valor de SDI requerido.
La regularidad con que se mida este índice vendrá determinada por las propias condiciones y variables explicadas. Inclusive habrá unidades donde no sea necesario determinarlo regularmente por la buena calidad del agua sin tratar.
Los detalles de la monitorización química se mencionan en el anexo de control de contaminantes químicos. Siempre se deben hacer pensando en evitar intoxicaciones crónicas.
En cuanto a la contaminación microbiológica, lo primero es evitar que el LD sea una fuente de bacteriemia y de reacciones a pirógenos23-25. En un segundo nivel, más exigente, se trata de evitar el paso de ET y otras sustancias pirogénicas a los pacientes, lo que justifica su control periódico. Cuando se observen cultivos positivos reiterados, mayores de 50 UFC/ml y que son resistentes a las desinfecciones, se debe sospechar la existencia de biofilm y espacios muertos en las conducciones26,27. Es obligatoria la monitorización semanal durante la fase de validación, el primer mes. Durante la fase de mantenimiento el control debe ser al menos mensual. La monitorización microbiológica es parte integral de este proceso de garantía. Es fundamental la existencia de protocolos para registrar el grado de contaminación del agua a lo largo de la cadena. Deberían existir dispositivos de recogida de muestras, colocados en puntos clave, de cara a conseguir una correcta supervisión. Las muestras de agua deben cultivarse regularmente según el apartado de control microbiológico, buscando la mayor sensibilidad28,29. En estas guías se recomienda como medio de cultivo el R2A y, en ocasiones, TGEA30.
La frecuencia y los métodos usados para el análisis microbiológico deben adaptarse al grado de contaminación de la planta en concreto y a la frecuencia de desinfección del sistema. Los métodos usados para el control microbiológico se describen en el anexo 3, de control microbiológico. Se debe usar el método más sensible, aunque ajustado al grado de contaminación. El control microbiológico debe hacerse con especial énfasis en las zonas críticas de la cadena, entre las que destaca el final del anillo de distribución del agua tratada.
El nivel de ET debe controlarse al menos mensualmente. Se recomienda realizar la prueba LAL, con un método con suficiente sensibilidad para la determinación a efectuar31,32.
El registro gráfico y el almacenamiento de todos los controles físicos, microbiológicos y químicos son fundamentales en todo este proceso de control, para utilizarlos como herramienta de evaluación a lo largo del tiempo y como acreditación de consecución y mantenimiento de la calidad, tanto de los componentes del proceso como de los productos obtenidos.
Por último, conviene recordar que tanto los monitores de HD como los tratamientos de agua están afectados por las normas referentes a productos sanitarios33.
Bibliografía
10.6. Métodos de prevención y corrección
Aunque no pueden establecerse normas generales, se puede afirmar que la desinfección frecuente del sistema de tratamiento de agua es fundamental para prevenir la contaminación. Cuando se abre un nuevo sistema de tratamiento, hay que desinfectar semanalmente para limpiar de forma adecuada las resinas y el sistema de tuberías. Después, la frecuencia de desinfección debe adaptarse a la configuración del sistema en cuestión y a los resultados de los controles microbiológicos. El intervalo óptimo entre desinfecciones debería establecerse en base a la cinética de recontaminación tras cada proceso de desinfección. La única forma de prevenir la formación de un biofilm es el uso precoz del método de desinfección adecuado. La frecuencia, el tipo de desinfección, la concentración y el tiempo de exposición al agente dependen del tipo de material usado en el circuito, y deben adaptarse a las recomendaciones del fabricante. Es muy aconsejable una desinfección completa de todo el sistema al menos una vez al año.
Se deben establecer normas para la desinfección regular del sistema de tratamiento de agua que impidan la formación de un biofilm. El mantenimiento de la planta de tratamiento de agua incluye una serie de medidas que implican ciclos de desinfección frecuentes, ya sean químicos, por calor o mixtos, de la cadena completa, filtro y resinas de intercambio, que dependen del grado de contaminación, así como la destrucción del biofilm del circuito. Los cambios periódicos de los distintos componentes del sistema, como son las resinas, el descalcificador y el electrodesionizador, el carbón activado y los filtros, deben hacerse de acuerdo con los resultados microbiológicos y según la fecha de caducidad. Se consigue así evitar la diseminación a partir de resinas muy contaminadas1.
Un problema de gran importancia es la formación de un biofilm bacteriano en los circuitos. Generalmente se relaciona con recuentos repetidos de más de 50 UFC/ml en el agua o en el LD. En su destrucción es fundamental usar tanto desinfectantes como detergentes en concentraciones y tiempo suficientes2,3. En ocasiones obligan a revisar la instalación e incluso a cambiar componentes.
La desinfección de los monitores de HD, ya sea por calor o mediante uso de agentes químicos, debe llevarse a cabo tras finalizar cada sesión. El correcto mantenimiento de los monitores implica una limpieza regular del circuito hidráulico con un detergente que elimine residuos orgánicos, una descalcificación con una solución ácida para remover los precipitados de calcio y fosfatos, así como la desinfección con un agente químico y/o calor. En cualquier caso, la limpieza, la descalcificación y la desinfección han de adaptarse a las recomendaciones del fabricante. El recambio del circuito es aconsejable en casos de alta contaminación o presencia de un biofilm en él.
La limpieza del sistema de tratamiento de agua, de su distribución y de las máquinas de HD en general se realizará según las especificaciones de cada fabricante, que estarán de acuerdo con la resistencia a la corrosión de los materiales empleados. En ocasiones, a pesar de seguir estas especificaciones, podemos encontrar contaminaciones bacterianas resistentes al tratamiento. En estos casos deberemos cambiar de producto, previo conocimiento de sus propiedades y forma de acción. Tres son los fines que debe alcanzar la limpieza: 1) desinfección bacteriana, incluidas las esporas, fúngica y viral; 2) desincrustación o descalcificación, y 3) limpieza o eliminación de los depósitos de proteínas, lípidos y otros productos orgánicos, mediante acción detergente. Las 3 acciones están imbricadas. Sirva de ejemplo el tratamiento de la existencia de un biofilm bacteriano, en el que más importante que la acción bactericida es la limpieza y la desincrustación. Cada uno de los productos químicos más usados en la limpieza tiene una acción predominante: el hipoclorito es, en concentraciones suficientes, buen bactericida y limpiador de depósitos orgánicos; el ácido peracético es fundamentalmente bactericida y algo desincrustante; el ácido acético es desincrustante y discretamente bactericida, y el ácido cítrico es el mejor desincrustante. Lo anterior significa que lograr los 3 requisitos precisa de la utilización de más de un producto, como son la clásica asociación de hipoclorito y ácido acético. Cuando existe evidencia de importantes depósitos de carbonato cálcico y magnésico en los circuitos de las máquinas, hay que recurrir al ácido cítrico.
En los métodos de desinfección hay que tener en cuenta el tiempo de contacto o de exposición necesario para la acción bactericida, que es muy variable según el desinfectante y el microorganismo a tratar y dependiente de la concentración lograda y la temperatura. El formaldehído al 4% a 20 °C necesita 24 h para lograr una buena desinfección, mientras que el ácido peracético al 1% a 20 °C necesita 11 h, y el glutaraldehído al 0,75% necesita solo 1 h. Otro aspecto es la capacidad de estas sustancias para provocar corrosión: así, el hipoclorito de sodio (lejía), que mediante su capacidad oxidante es un buen detergente, es capaz de modificar las propiedades de ciertas membranas como la polisulfona, aumentando 10 veces su eliminación de proteínas4. Entre las distintas sustancias desinfectantes existen incompatibilidades, por lo que no se pueden usar juntas; en todo caso, secuencialmente después de los convenientes aclarados. Los ácidos acético, peracético y cítrico no se deben mezclar con el hipoclorito ni con el peróxido de hidrógeno; en general, con todas las bases. Los aldehídos no se mezclarán con los ácidos, amoniaco ni fenol. En general, todas estas sustancias son tóxicas y deben manejarse con las debidas precauciones. La mayoría de ellas son capaces de desencadenar reacciones alérgicas. En el mercado existen mezclas de desinfectantes especialmente diseñadas para la HD, como son: Instrunet HD® (clorito sódico al 1,15% y ácido peroxiacético al 0,06%); Dialox® (peróxido de hidrógeno, ácido acético y ácido peroxiacético); Actril® (peróxido de hidrógeno al 0,8% y ácido peroxiacético al 0,06%)5; Puristeril 340® (peróxido de hidrógeno y ácido peroxiacético), y Cold Sterilant® (peróxido de hidrógeno al 20-24%, ácido peracético al 4-6% y ácido acético al 8-10%).
La metodología para la desinfección del sistema de tratamiento del agua implicaría los siguientes aspectos: Se debe hacer periódicamente, antes de detectar un nivel de contaminación elevado. Se utilizará el producto o productos elegidos según las recomendaciones mencionadas y las especificadas por el fabricante. El esquema que se menciona a continuación está diseñado para el Dialox®, pero puede servir para otros desinfectantes cambiando la concentración y tiempo de contacto. En este caso la concentración a utilizar es del 5%, 5l de Dialox® diluidos en 95l de agua. Es necesario que esta disolución alcance todos los puntos del sistema durante al menos 30 min. Es preferible que el contacto se realice en una situación dinámica, con el desinfectante circulando. Posteriormente se realizará un lavado riguroso y se comprobará en diversos puntos y fundamentalmente en las tomas de los monitores que el desinfectante se ha aclarado, para lo que se utilizarán los detectores adecuados. En el caso en cuestión, papel almidonado a base de yoduro de potasio, que detecta hasta 40 ppm, o tiritas enzimáticas, que detectan hasta 7 ppm. Antes de la desinfección se debe estar seguro de que todos los componentes del sistema son compatibles con el desinfectante.
Un control microbiológico regular es fundamental para optimizar la desinfección y comprobar su eficacia.
Respecto al LD y los monitores de HD, y para cumplir las normas básicas de seguridad, se deben definir de acuerdo con el tipo de monitor y su especificación técnica, instrucciones que han de seguirse paso a paso antes del inicio de cada sesión. El usuario debe asegurarse de que:
La ultrafiltración del LD, mediante un ultrafiltro apropiado a baja presión, es el método que se está utilizando para obtener un LD ultrapuro. La mayoría de estos filtros son de membranas sintéticas con un punto de corte o exclusión molecular de alrededor de 40 kD y con gran capacidad adsortiva. Las membranas más usadas en estos filtros son la polisulfona y la poliamida. Actualmente se están usando para filtrar el LD justo antes del dializador8-10. Con ellos se eliminan todo tipo de partículas, bacterias y endotoxinas, muchas de ellas provenientes de los circuitos de la máquina de HD. De esta forma se previene el paso al paciente a través del dializador. Tanto la hemofiltración como la hemodiafiltración en línea requieren monitores específicos que incluyan «esterilización fría» del LD por medio de 2 o más ultrafiltros. Hoy por hoy, la ultrafiltración del LD es el único método que se ha demostrado efectivo en la práctica clínica diaria. Las características de estos ultrafiltros son:
Principalmente son filtros de fibra hueca compuestos por membranas sintéticas (polisulfona, poliamida, posidina).
Tienen que estar colocados en serie en la línea del LD.
Purifica el LD mediante filtración (basándose en exclusión de tamaño y estructura de las paredes) y los mecanismos de adsorción (debido a las interacciones hidrofóbicas).
Debe producir un LD de gran calidad «ultrapuro».
Debe garantizar una calidad microbiológica equivalente a la exigida para las soluciones parenterales (solución de infusión o hemofiltración).
Se debe controlar su estanqueidad y desinfectar periódicamente.
-
Ultrafiltro esterilizado con una capacidad de retención de:11
Respecto a los sistemas centralizados de concentrados, los de bicarbonato se desaconsejan en esta guía, y los de ácido se contaminan con poca frecuencia. Se recomiendan desincrustaciones, lavados y revisiones periódicas de los mismos12.
Bibliografía
10.7. Justificación de la necesidad de utilizar un líquido de diálisis ultrapuro en la hemodiálisis actual
Las guías ANSI/AAMI1 recomendaban que las características del líquido puro para HD no debe exceder de 200 unidades formadoras de colonias (UFC)/ml y 2 EU/ml de endotoxinas, y para líquido ultrapuro no debe exceder de 0,1 UFC/ml y 0,03 EU/ml de endotoxinas. La European Renal Best Practice (EBPG)2 publicada en 2002 recomendaba para el líquido puro <100 CFU/ml y <0.250 EU/ml, mientras que para líquido ultrapuro recomendaba <0,1 CFU/ml y 0,03 EU/ml. Esta diferencia fue unificada por la International Organization for Standardization con ISO11663 en 2009 y 23500 en 20113, que recomendó un líquido puro con <100 CFU/ml y <0,5 EU/ml, y un líquido ultrapuro de <0,1 CFU/ml y <0,03 EU/ml. El líquido de sustitución, según todas estas guías, usado para HD debe tener <10−6 CFU/ml y <0,03 EU/ml.
La Sociedad Japonesa de Nefrología4 establece como estándares microbiológicos en el líquido puro <100 CFU/ml, y de endotoxinas de <0,05 EU/ml, medidas un mínimo de una vez al mes, y en todas las máquinas una vez al año. Los estándares de líquido ultrapuro son de <0,1 CFU/ml y <0,001 EU/ml. El nivel de alerta debe ser un 50% del máximo tolerable en cualquiera de los casos, excepto el valor de endotoxinas en el líquido ultrapuro. Esta sociedad recomienda en el líquido de sustitución <10−6 CFU/ml y <0,001 EU/ml.
El LD ultrapuro es absolutamente necesario cuando se usa como líquido de sustitución para técnicas de hemofiltración o hemodiafiltración en línea. Para minimizar la inflamación del paciente en HD, todas las unidades de diálisis deberían trabajar para conseguir LD ultrapuro para todas las modalidades de diálisis. El uso rutinario de LD ultrapuro exige la incorporación de ultrafiltros específicos en el circuito del LD (evidencia nivel B, 1).
Los estándares son variables, y algunas recomendaciones sugieren reducir a 0,1 UFC/ml, usando métodos microbiológicos sensibles, y ET < 0,03 UE/ml para definir un LD ultrapuro5. El líquido ultrapuro se consigue usando 3 principios básicos: agua ultrapura, ultrafiltros estériles interpuestos en la ruta del líquido en máquinas de HD bien diseñadas y un estricto cumplimiento de los procedimientos de desinfección y monitorización microbiológica.
La utilización en la actualidad de dializadores con membranas de alta permeabilidad especialmente diseñados para permitir el trasporte convectivo obligan, según todas las recomendaciones, a la generalización del LD ultrapuro6,7.
El uso de LD ultrapuro se acompaña de una reducción del estado inflamatorio del paciente8. La mejoría de ese estado reduce las necesidades de factores eritropoyéticos9, reduce los niveles de B2 microglobulina10, y mejora el perfil lipídico y de mieloperoxidasa11,12. La activación de los monocitos y la apoptosis mejoran al usar LD ultrapuro13. De la misma manera su uso mejora la conservación de la función renal residual14 y el estatus nutricional15. El LD ultrapuro se asocia a un descenso de las endotoxinas vasculares, con lo que mejora la elasticidad vascular y la inflamación sistémica16.
Un metaanálisis reciente muestra que el uso de LD ultrapuro en los pacientes en HD hace descender los marcadores de inflamación y estrés oxidativo, aumenta la albúmina sérica, la hemoglobina y disminuye los requerimientos de eritropoyetina17. También concluye que aunque esos resultados son marcadores subrogados, se puede imaginar que debe de tener un beneficio cardiovascular. En otro estudio han encontrado una mayor supervivencia en los pacientes tratados con diálisis de alta permeabilidad cuando se usa un LD ultrapuro, comparado con un líquido convencional o puro18.
El uso de LD ultrapuro debe ser obligado en los pacientes que están siendo dializados con membranas de alto flujo y en aquellos con mayor trasporte convectivo, como la hemodiafiltración online. El motivo es la evidencia de que su uso en estos pacientes mejora la supervivencia y los episodios cardiovasculares19-21. En España, donde el 80-90% de los pacientes se dializan con membranas de alta permeabilidad, es obligado que todos los monitores cuenten con ultrafiltros y los pacientes se beneficien de un LD ultrapuro.
Bibliografía
10.8. Agua ultrapura, conductividad y sólidos totales disueltos1
En otras actividades, ajenas a la diálisis, se entiende como agua ultrapura aquella cuya conductividad no supera 0,5 μS·cm−1, dado de que es muy importante que el agua no pueda comportarse como un conductor eléctrico, sin especificar el uso para el que está destinado (laboratorios de fotografía, fabricación de componentes electrónicos, etc.). Al utilizar este mismo término para el agua de HD y fijar el límite de conductividad en 5 μS·cm−1, hay que tener en cuenta algunas consideraciones.
El límite de conductividad exigido en diálisis tiene como objetivo que la concentración de contaminantes químicos del líquido de diálisis, valorados en conjunto, no supere los niveles considerados como tóxicos para los pacientes1. No se trata, por tanto, de un problema del agua como conductor eléctrico. Los solutos, sólidos o sales totales disueltos (TDS), en miligramos/litro, y la conductividad se relacionan de la siguiente manera: los TDS son equivalentes a la conductividad del agua, en microsiemens, multiplicado por un factor que varía de 0,54 a 0,96 dependiendo del soluto, aunque generalmente se suele escoger un valor entre ambos. Según esta conversión, 2 mg/l de cualquier sustancia o de la suma de varias de ellas disueltas en el agua implicaría una conductividad de entre 2,08 y 3,7 μS. Si en vez de 2 mg/l fueran 4 mg/l, el valor de TDS, estando las concentraciones de los solutos dentro del margen establecido, la conductividad podría estar fuera del margen considerado idóneo del agua purificada y ultrapura para HD2,3.
Si comparamos esto con los valores máximos de los componentes químicos que pueden estar presentes en el agua para HD, ultrapura o no, veremos que choca que determinados elementos puedan estar en cantidades de hasta 50 mg/l (sodio) y por tanto incompatibles con la conductividad indicada. De esta forma, si tuviéramos agua con los niveles microbiológicos, endotoxinas y químicos dentro de los niveles requeridos para agua ultrapura indicados en la guía, pero con la conductividad fuera de los rangos indicados, ¿sería correcto decir que esa agua no cumple con los requisitos recomendados para utilizarla en HD como agua ultrapura?
El agua pretratada puede contener una concentración elevada de cloruro sódico procedente de los descalcificadores, en función de la dureza del agua de aporte3. Cuanto mayor sea la dureza del agua, mayor intercambio en el descalcificador entre iones de calcio y magnesio con los de cloruro sódico, y por tanto mayor cantidad de este llegará a la ósmosis. Esto se puede contrarrestar utilizando en serie una OI y un electrodesionizador, con lo que tendríamos unos niveles de conductividades por debajo de 0,5 μS. Este aparataje no se está utilizando habitualmente en los tratamientos de agua para HD, aunque podría ser recomendable en aquellos sitios con agua de aporte de elevada dureza y/o donde se quiera rebajar la conductividad.
A la vez hay que tener en cuenta que los gases disueltos en el agua interfieren en la medida de la conductividad; uno de ellos, el CO2, puede provenir de forma natural de la propia agua o puede que se añada, en ocasiones, para obtener un pH óptimo. También se pueden añadir otros elementos para corregir el pH y que pueden influir en la conductividad final4.
Teniendo en cuenta los datos y razonamientos anteriores, se puede admitir que tanto el agua purificada como la ultrapura tengan una conductividad mayor a la recomendada, siempre que los niveles de elementos químicos, microbiológicos y endotoxinas se encuentren dentro de los niveles indicados5.
A partir de esta argumentación, es fundamental insistir en que la conductividad que se logre en condiciones óptimas de funcionamiento, cumpliendo todos los parámetros fisicoquímicos, se mantenga en el tiempo y que los cambios, si superan un margen preestablecido, impliquen diagnóstico y corrección en caso necesario, de tal manera que la conductividad será el elemento de vigilancia y control inmediato del funcionamiento del equipo de OI5.
El Silt Density Index (SDI) debe ser menor de 5 en el agua de aporte al equipo de OI; hay manuales técnicos de membranas o equipos de ósmosis que recomiendan que sea menor de 3. Cuando se produce saturación prematura de las membranas de ósmosis (pérdidas de caudal de producción y/o variaciones de presiones) es conveniente conocer este índice y su variabilidad en el tiempo para saber la adecuación del agua. La ASTM International (anteriormente American Society for Testing and Materials) regula la forma de medir este índice6.
Esta Guía requiere un nivel de conductividad y su seguimiento porque es el método disponible en todos los tratamientos de agua y el que mejor nos puede avisar de una malfunción del tratamiento del agua.
Bibliografía





















