INTRODUCCIÓN
La generación de tejido funcional mediante ingeniería tisular tiene un alto impacto en diversas áreas de la medicina regenerativa, entre las que se encuentra el tejido esquelético. Los primeros implantes fueron utilizados en el ámbito de la medicina, en concreto en 1909, cuando se desarrollaron las agujas de Kirschner y los clavos de Steinman para la fijación de fracturas óseas, donde el material utilizado fue el acero inoxidable. A lo largo de los años, se procedió a la mejora del acero, buscando que este fuese más resistente a la corrosión y que no provocase efectos nocivos en el cuerpo humano. En 1940 se comenzó el estudio del titanio (Ti) como biomaterial para implante óseo1.
El cambio de fase determina el cambio de estructura cristalina del material cuando es sometido a cambios de temperatura. El titanio es un metal cuya transformación alotrópica ocurre a 882ºC y pasa de una fase a, que presenta una estructura hexagonal y compacta (HCP), poco deformable y resistente a temperatura ambiente, a una fase ß caracterizada por estructura cúbica y centrada en el cuerpo (BCC), la cual es fácilmente deformable, lo que permite la realización de tratamientos térmicos que tienen como finalidad optimizar las propiedades del material2.
Entre las características que hacen del titanio uno de los mejores materiales para implantes óseos podemos destacar su mayor resistencia especifica (resistencia/densidad), su alta ductilidad y su inferior módulo de Young3 frente a otros elementos como, por ejemplo, el acero inoxidable. A su vez, se trata de un material no ferromagnético, lo que no presenta inconvenientes a la hora de realizar una prueba al paciente con implante de Ti por resonancia magnética. El anclaje al tejido óseo es posible gracias a la capa de óxido formada en el material al ser pasivado4.
Actualmente se utiliza el Ti comercial puro (c.p.) y otras aleaciones como Ti-6Al-4V principalmente para los implantes óseos5. Sin embargo, ambos elementos presentan un alto módulo elástico (E: 100-112 GPa) en comparación con el módulo elástico del hueso cortical (18,6-20,7 GPa) y trabecular (10,4-14,8 GPa) (Tabla 1) lo que produce el efecto de apantallamiento de tensiones o stress-shielding6. Este fenómeno se debe a que la rigidez del material del implante óseo es superior a la rigidez del hueso, lo que hace que toda la carga recaiga sobre el implante óseo. El remodelado óseo se ve en gran medida regulado por las cargas mecánicas a las que se ve sometido, de manera que la presencia de cargas estimula su formación ósea, y la ausencia de las mismas aumenta la reabsorción. Como consecuencia de la disminución de carga soportada por el hueso, este disminuye su densidad en la zona próxima al implante y, por tanto, puede producirse tanto la fractura prematura del mismo como el aflojamiento del implante5.
En la actualidad, para eliminar el fenómeno del apantallamiento de tensiones, se busca disminuir el módulo elástico, para lo cual se dispone de varias soluciones. Una de ellas, disminuir la densidad del material empleado, mediante la porosidad. Sin embargo, al aumentar la porosidad, se produce la disminución de la resistencia mecánica. Otro enfoque sería la búsqueda de aleaciones de Ti de estructura cúbica centrada en las caras (BCC) o aleaciones β-Ti, las cuales son de bajo módulo elástico y no presentan disminución de resistencia mecánica. Para la estabilización de la fase ß se requiere de elementos β-estabilizadores: el Mo, V, Ta, Nb y Zr como elementos β-isomorfos y Cr, Co, Cu, Fe y Ni como elementos β-eutectoides. La ventaja de los elementos β-isomorfos es su alta cantidad de solución sólida sustitutiva y su incapacidad de formar compuestos intermetálicos de Ti, que poseen E elevado. Por tanto, se ha demostrado que elementos como el Nb y el Ta poseen un elevado nivel de biocompatibilidad y habilidad para prevenir el incremento de partículas, lo cual evitaría una mala interfaz de cohesión7.
El niobio (Nb) y el tantalio (Ta) son dos metales de transición muy utilizados en aleaciones; en especial, el Nb se utiliza en la formación del acero. Hasta 1866, se pensó que ambos elementos eran el mismo, ya que presentan características físico-químicas muy similares. La aleación de TiNbTa destaca por su alta estabilización de comportamiento, por la ausencia de fase a, lo que permite una disminución del módulo elástico (49 + 3 GPa), su excelente resistencia elástica (sy>1860 MPa) y su alta biocompatibilidad7,8. Por lo tanto, un material como el TiNbTa, con una buena combinación de alta resistencia y bajo módulo de Young cercano al del hueso, podría utilizarse para evitar el aflojamiento de los implantes para así evitar la cirugía de revisión (Tabla 1).
Tabla 1. Características físicas del titanio puro, las distintas fases y el hueso: módulo elástico y resistencia elástica
En los últimos años, se han desarrollado toda una serie de técnicas con el objetivo de obtener materiales porosos que presenten un módulo de Young más cercano al del hueso cortical. En concreto, Chicardi et al. han conseguido fabricar una aleación de TiNbTa con propiedades fisicoquímicas más semejantes a las que presenta el hueso9. No obstante, la mejora en el diseño de materiales, destinados a ser utilizados como injertos óseos, debe considerar la capacidad de osteointegración de los mismos, y en este sentido es necesario evaluar la citotoxicidad y la capacidad de adhesión, proliferación y diferenciación de células osteoblásticas influida por el material. Nuestro objetivo principal fue evaluar las características osteointegradoras de la aleación TiNbTa, con un módulo de Young similar al del hueso trabecular, y compararlas con el Ti puro.
MATERIAL Y MÉTODOS
1. Cultivo celular
La línea celular MC3T3 (subclon 4) de ATTC (Manassas, Virginia, EE.UU.) se cultivó en medio α-MEM (Gibco, Thermo Fischer Scientific, España) suplementado con 1% de L-glutamina (200 mM) y 10% de suero bovino fetal. Para inducir la diferenciación, las células fueron tratadas con un medio de cultivo osteogénico suplementado con ácido ascórbico 50 g/ml (Merck, Alemania) y β-glicerofosfato 10 nM (StemCell Technologies, Canadá). Las células fueron sembradas en discos, de 3 mm de espesor y 7 mm, de titanio c.p. y de TiNbTa a una densidad de 5x103, en condiciones de 5% de CO2 a 37ºC. Se realizaron cambios de medios cada 48 h. Los cultivos se realizaron por triplicado y las lecturas de la viabilidad celular y la actividad fosfatasa alcalina se realizaron después de 4 y 7 días.
2. Viabilidad celular
El ensayo Alamar Blue (AlamarBlue Cell Viability Reagent. Invitrogen, España) se llevó a cabo de acuerdo con las instrucciones del fabricante. AlamarBlue es un compuesto no tóxico, permeable a las células, que es de color azul y no fluorescente. Las células viables mantienen un ambiente reductor dentro de su citoplasma. El reactivo AlamarBlue es una forma oxidada de redox y de color azul. Cuando se incuba con células viables cambia de color azul a rojo y se vuelve fluorescente. Este cambio se puede detectar utilizando métodos de absorbancia.
A los 4 y 7 días se transfieren los discos con crecimiento celular a un nuevo pocillo y se añaden 80 µL de AlamarBlue sobre el disco y posteriormente se añaden 720 µL de medio de cultivo; este medio se incuba durante 2 horas a 37ºC y se mide la absorbancia a la longitud de onda de excitación y emisión respectiva de 570 y 600 nm (TECAN, Infinity 200 Pro). Los resultados se presentan como el porcentaje de reducción. Los experimentos se realizaron por triplicado en cada cultivo.
3. Fosfatasa alcalina
Analizamos la actividad de la fosfatasa alcalina (ALP) de acuerdo con el protocolo del fabricante (kit de ensayo de fosfatasa alcalina Colorimétrica, Abcam ab83369, Reino Unido) en el sobrenadante de cultivo. El ensayo se realizó a los 4 y 7 días, a través de la conversión de un fosfato de p-nitrofenilo incoloro en un p-nitrofenol de color. Se mide la absorbancia a 405 nm de 4-nitrofenol (TECAN, Infinity 200 Pro), y la actividad de ALP se calculó a partir de una curva estándar. Los experimentos se realizaron por triplicado en cada cultivo.
4. Fijación para SEM
Para visualizar las células en la microscopía electrónica de barrido (SEM), las células MC3T3 se cultivaron en discos de titanio c.p. y Ti NbTa durante 4 y 7 días por triplicado. Las muestras fueron fijadas con formol 10%, seguido de un paso de deshidratación con soluciones etanólicas y recubiertos por recubrimiento de oro utilizando un revestimiento de esputo (Pelco 91000, Ted Pella, Redding, California, EE.UU.). Todas las micrografías se obtuvieron utilizando un microscopio electrónico de barrido Jeol JSM-6330F y el voltaje de aceleración fue de 10 kV para imágenes SEM.
5. Análisis estadístico
Todos los experimentos in vitro se realizaron por triplicado para cada condición estudiada. Las variables fueron analizadas para la distribución de la normalidad mediante la prueba de Kolmogorov-Smirnov. Se realizó la prueba t de Student para determinar diferencias estadísticamente significativas entre los dos grupos.
Para el manejo estadístico de resultados se ha utilizado el paquete SPSS versión 22.0 para Windows (IBM Corp., Armonk, Nueva York, EE.UU.). En todos los casos se consideró como nivel de significación p<0,05.
Los datos son expresados como media ± desviación estándar (DS).
RESULTADOS
Los cultivos celulares en los discos de Ti c.p. y en la aleación tuvieron un crecimiento celular similar. A los 7 días de crecimiento las células presentaron al microscopio óptico (M.O.) una morfología columnar y basófila compatible con el inicio de la diferenciación (Figura 1). La superficie del disco no deja pasar la luz, por lo que resulta complejo apreciar las células con claridad. Sin embargo, en las partes destacadas se pudo observar que se había producido cierta adhesión celular en el material, lo cual indicaría que la aleación presenta buenas cualidades para ser utilizada en implantes.
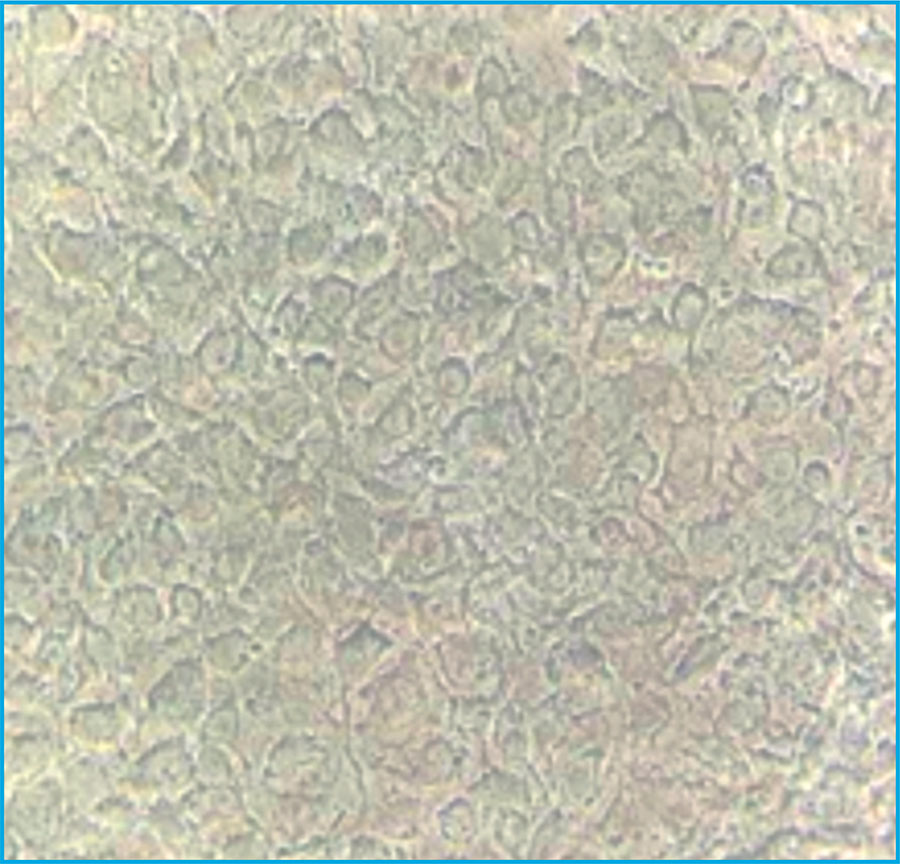
Figura 1. Fotografía de microscopio óptico invertido (Olympus CKX53) con objetivo de medio aumento 40X, de las células crecidas a los 7 días en los discos de TiNbTa
Viabilidad celular
La figura 2 representa la viabilidad de la línea celular en función del tiempo de crecimiento celular (4 y 7 días) sobre los discos de Ti c.p. y TiNbTa. A los 4 días de cultivo, la viabilidad celular en los discos de TiNbTa fue similar a la de los discos de Ti c.p. Mientras que a los 7, observamos un ligero ascenso de la viabilidad en las muestras de TiNbTa y un descenso en las muestras de Ti c.p., aunque sin diferencias significativas. En todos los casos el porcentaje de viabilidad siempre fue superior al 150%. Se considera efecto tóxico cuando la viabilidad es inferior al 75%, por lo que, con los resultados obtenidos, se puede deducir que el cultivo celular es viable a lo largo de toda la duración del cultivo en todas las condiciones.
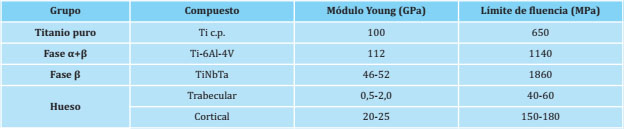
Actividad fosfatasa alcalina
Cuantificamos los valores de la actividad de la fosfatasa alcalina (ALP) en los cultivos de células MC3T3 a los 4 y 7 días. La figura 3 representa la media y la desviación estándar de los resultados obtenidos en ambas condiciones de cultivos. En los discos de Ti c.p., los resultados obtenidos mostraron una disminución de la actividad enzimática, siendo estadísticamente significativa la diferencia encontrada entre los días 4 y 7 (p=0,001). En los discos de TiNbTa, también se observó una disminución de la actividad con el tiempo de cultivo y existió una diferencia significativa entre los días 4 y 7 de cultivo (p=0,006). En ambas condiciones a los 4 días se obtuvo la máxima actividad enzimática, dado que hay una mayor proliferación y crecimiento celular, como los valores de viabilidad corroboraron, y a partir del día 7, las células presentaron un fenotipo más diferenciado, como observamos en las imágenes de SEM, y la actividad de la ALP disminuyó.
Morfología celular por microscopía electrónica de barrido
Se realizó un estudio preliminar para estudiar la morfología y adhesión celular sobre el material de estudio TiNbTa comparado con el crecimiento en Ti c.p. Para ello, visualizamos las muestras de ambos tipos de disco a los 4 y 7 días de cultivo. A los 4 días, se observaron pequeñas agrupaciones celulares en ambos tipos de superficie y de densidad similar. A los 7 días, las imágenes demostraron un crecimiento en monocapa en toda la superficie del disco, siendo similar en ambos materiales. También se observaron uniones entre célula-células y célula-biomaterial. Las células se adhirieron a través de filopodios (finas proyecciones celulares, flecha amarilla) y lamelopodios (extensiones más amplias, asterisco amarillo), demostrando de esta forma la conexión de las células con el biomaterial. Empezamos a observar la presencia de pequeñas vesículas de estructura hexagonal, sugiriendo una posible nucleación de hidroxiapatita, sobre la superficie celular, sugiriendo el inicio del desarrollo del proceso de mineralización (Figura 4).

Figura 4. Microfotografías de microscopio electrónico de barrido a 4 y 7 días de cultivos de osteoblastos sobre la superficie de Ti cp. o TiNbTa. La morfología celular y proliferación es mostrada en las dos superficies testadas. Interacciones célulacélula a través de filopodios (flechas amarillas) e interacciones célula-superficie mediante lamelopodios (asterisco amarillo)
DISCUSIÓN
Los problemas inflamatorios y degenerativos de los huesos y articulaciones afectan a millones de personas en todo el mundo. De hecho, representan la mitad de las enfermedades crónicas en personas mayores de 50 años en países desarrollados10. Estas enfermedades a menudo requieren cirugía, incluida el reemplazo de toda la articulación en casos de deterioro. Este hecho, acompañado del aumento de la esperanza de vida y el envejecimiento de la población, ha traído consigo una gran demanda de derivados sanitarios, entre los que destacan el desarrollo de implantes quirúrgicos y materiales con mayor periodo de vida útil.
Los biomateriales constituyen uno de los avances más importantes en la medicina actual: estos mejoran la calidad de vida de los pacientes y reducen el tiempo de curación y la convalecencia de enfermedades. En 2009, Bjursten resaltó la importancia de incrementar la unión del implante al hueso, dado que la vida media de un implante está comprendida entre 10 y 15 años7,8, lo que implica un aumento en el número de intervenciones quirúrgicas de revisión.
En nuestro estudio hemos realizado pruebas para valorar un material nuevo, la aleación TiNbTa, con un módulo de Young similar al del hueso trabecular. Numerosos estudios han demostrado la disminución del módulo elástico en aleaciones con Nb y Ta, como por ejemplo el Ti35Nb5Ta7Zr, que muestra un módulo elástico de 55GPa11. La ventaja en comparación con el Ti c.p. o la aleación Ti-6Al-4V sería el inferior módulo de Young de la aleación estudiada, lo cual reduciría considerablemente el apantallamiento de tensiones.
El porcentaje de viabilidad se relaciona ampliamente con las propiedades biocompatibles y citotóxicas del material; diversos autores12,13 han demostrado cómo porcentajes elevados de viabilidad son óptimos para considerar un material candidato a ser utilizado como implante óseo en humanos. Nuestros cultivos, a los diferentes tiempos de estudio, presentaron un alto grado de biocompatibilidad, así como una ausencia de toxicidad. Se obtuvieron resultados positivos entre la línea celular y el material. Se podría sugerir que si este material fuese implantado tendería a sintetizar la matriz ósea, se adheriría bien al hueso y resultaría biocompatible14-15.
Los valores de viabilidad nos demuestran que no existen diferencias en el crecimiento celular entre la aleación TiNbTa y Ti c.p, y en todas las condiciones los valores se encuentran por encima del 75%. Por tanto, ambos materiales resultarían no citotóxicos y por tanto viables. Por otro lado, la adecuada actividad del metabolismo celular confirma que la aleación no libera residuos tóxicos para nuestras células15-18. Estudios previos de implantación animal de materiales como el Nb y el Ta en tejidos blandos y duros de ratas han demostrado la elevada biocompatibilidad de los metales y la osteogénesis19,20.
También cuantificamos la actividad celular midiendo la actividad de ALP. Una actividad aumentada de ALP se relaciona directamente con la proliferación celular y es un marcador de diferenciación del fenotipo osteoblástico. En tejidos como huesos y cartílagos, la ALP se expresa en las fases iniciales del proceso de calcificación y más adelante, en el desarrollo, la expresión de la ALP disminuye. Se ha demostrado que cuando la actividad ALP disminuye, aumenta la diferenciación celular14.
Nuestros valores confirman que el cultivo en los discos con el nuevo material presenta actividad ALP que varía según el tiempo de estudio. Al inicio del cultivo, a los 4 días, las células MC3T3 presentaron una mayor proliferación celular en Ti c.p. que las cultivadas sobre el material de aleación, indicando un crecimiento más lento en los discos de TiNbTa durante los primeros días de cultivo. A los 7 días, los valores de ALP fueron similares en ambas muestras e inferiores a los iniciales, lo que demuestra que el cultivo se está comportando con características similares en cuanto a proliferación y diferenciación. En las imágenes obtenidas por SEM, observamos que a los 7 días las células tapizaron en su totalidad la superficie de los discos, el crecimiento celular se dio por igual en ambas muestras y llegaron a la confluencia celular, y la menor actividad concordó con las imágenes de células que están iniciando el proceso de mineralización. Además, empezamos a observar la secreción de material que formará la matriz extracelular por parte de los osteoblastos, y se observó en la superficie de las células un aumento de moléculas con apariencia de hidroxiapatita21. Por otro lado, los osteoblastos presentaron filopodios y lamelopodios, estructuras celulares esenciales durante el proceso de adhesión celular, lo que nos indica que la unión a otras células y al material es directa; otros autores describen estas uniones en células MC3T3 y discos de Ti c.p.22,23.
En conclusión, nuestro estudio in vitro nos permite concluir que la aleación novedosa que combina elementos como el Nb y el Ta con el Ti, además de mejorar las propiedades mecánicas del material, resulta, a corto plazo, biocompatible con las células osteoblásticas, comportándose con características de viabilidad, proliferación, diferenciación y capacidad de adhesión de líneas celulares osteoblásticas, de forma muy semejante a como lo hace el Ti puro.











 text in
text in