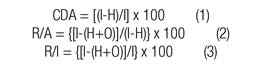INTRODUCCIÓN
La nutrición enteral (NE) se define como el uso de "alimentos con propósitos médicos" independientemente de la ruta de suministro, la cual puede ser oral, a través de sondas, vía nasogástrica, nasoenteral o percutánea 1. La NE puede considerarse como una técnica relativamente moderna y en continuo desarrollo, que en su concepto literal puede dar cabida a un amplio abanico de posibilidades que abarca desde infusiones de líquidos no calóricos, pasando por dietas de tipo culinario hasta las modernas dietas órgano-específicas administradas mediante sofisticadas técnicas.
La NE es el mejor recurso para alimentar o complementar la alimentación de personas con deficiencias o con alguna patología cuando se conserva total o parcialmente la funcionalidad del tracto gastrointestinal 2. En la NE total los productos utilizados constituyen la fuente exclusiva de nutrientes para el paciente, por lo que es fundamental asegurar que su utilización metabólica y sus efectos biológicos sean máximos.
Aunque las primitivas dietas enterales químicamente definidas iban dirigidas a patologías específicas, fundamentalmente digestivas (las llamadas "dietas elementales" o "elementales de 1.ª generación"), la industria, en su constante esfuerzo de innovación, ha ido desarrollando formulaciones aplicables a situaciones clínicas que cursan con funcionalismo intestinal normal o poco alterado, y que pueden presentarse en el marco de patologías muy variadas. Nacieron así los preparados que actualmente se conocen con el nombre de "dietas poliméricas estándar" ajustadas a las necesidades diarias de nutrientes, que constituyen un soporte nutritivo exclusivo en multitud de situaciones clínicas.
Actualmente, aunque estas dietas de tipo estándar representan una parte muy importante del tratamiento nutricional por vía enteral por su aplicabilidad a la mayoría de los pacientes, siguen desarrollándose dietas específicas, utilizables en patologías concretas, en las que su uso puede tener ventajas sobre las dietas convencionales. En estos casos, la utilización de ingredientes específicos que suministren tanto macronutrientes como micronutrientes con elevada disponibilidad y que se ajusten a las necesidades de los pacientes de acuerdo con su patología es un aspecto crítico en los procesos de innovación de nuevas fórmulas para NE.
Dentro de este contexto, este trabajo revisa algunos de los ingredientes funcionales más importantes utilizados actualmente para la innovación de productos de utilidad en NE, así como sus efectos fisiológicos y bioquímicos en el tratamiento de diversas patologías.
COMPUESTOS NITROGENADOS
PROTEÍNAS
Calidad nutricional
Las proteínas son el principal componente estructural y funcional de todas las células del organismo y sus constituyentes, los aminoácidos (AA), son los sillares de las proteínas, que actúan, además, como precursores de ácidos nucleicos, neurotransmisores y otras moléculas esenciales para la vida 3,4. Por lo tanto, un aporte dietético adecuado de proteína en cantidad y calidad es esencial para mantener la integridad y la función celular y para lograr un buen estado de salud 4.
Los requerimientos de AA se expresan en términos de proteína dietética y no como cantidades separadas de cada uno de ellos. En la dieta, las proteínas forman parte de numerosos alimentos y su composición de aminoácidos es diferente según la fuente alimentaria. Por lo tanto, dependiendo de la cantidad y del tipo de alimento que se consuma, puede llegarse o no a alcanzar las recomendaciones de ingesta 5.
La calidad nutritiva de una proteína se define como su capacidad (o de una mezcla de ellas) para cubrir los requerimientos de un individuo 6, y depende fundamentalmente de la composición de AA y de su biodisponibilidad. Para medir la calidad proteica de un alimento, existen métodos químicos, biológicos y microbiológicos. Dentro de los biológicos se han usado, y se siguen usando, el coeficiente de eficacia proteica (PER), el valor biológico (VB) y la utilización neta proteica (NPU) 6,7.
La evaluación de la calidad proteica se realiza a través de un bioensayo basado en el método diseñado por Thomas-Mitchell 6,8 modificado. Esta clase de ensayo utiliza ratas en crecimiento y evalúa la ganancia de peso por gramo de proteína ingerido (PER). Asimismo, se determina el coeficiente de digestibilidad aparente de la proteína (CDA), la utilización metabólica de la proteína, calculada a través de la relación nitrógeno retenido/absorbido (R/A) y la incorporación de la proteína al metabolismo, calculada a través de la relación nitrógeno retenido/ingerido (R/I).
Para la estimación de estos índices, se utilizan las siguientes ecuaciones:
Donde: I = nitrógeno ingerido; H = nitrógeno fecal; O = nitrógeno urinario.
Es necesario indicar que un valor de 2,5 para el PER es el mínimo necesario considerado para las fórmulas lácteas para nutrición infantil por la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica y, por similitud, para las dietas para nutrición enteral 9. Por otra parte, la digestibilidad de huevo, leche, carne y proteína aislada de soja supera el 95%, y la de cereales, guisantes y arroz se encuentra entre 80% y 90% 10. En una publicación de la FAO de 1981, que incluye una gran cantidad de ensayos, se menciona un VB medio para la caseína del 79,7% y una NPU media de 72,1% 11.
Nuestro grupo de investigación demostró hace algunos años que una mezcla proteica constituida por un 50% de caseinato potásico, un 25% de suero lácteo y un 25% de guisante presenta valores de PER, CDA, R/A y R/I similares a los de la proteína patrón de crecimiento, por lo que puede ser utilizada en productos de nutrición enteral 12.
En 1989, la Comisión Conjunta de Expertos FAO/OMS sobre la "Evaluación de la calidad de la proteína" recomendó el uso de la puntuación corregida de los aminoácidos de acuerdo con su digestibilidad (PDCAAS) para la evaluación de la calidad de la proteína en humanos. Al calcular los PDCAAS, la puntuación del aminoácido limitante (es decir, la relación entre el primer aminoácido limitante en un gramo de la proteína objeto del estudio y el de la proteína de referencia o valor requerido) es multiplicado por la digestibilidad de la proteína con la intención de valorar hasta qué punto la fuente de proteína puede satisfacer la demanda de aminoácidos y permitir la predicción de la utilización de la proteína de la dieta.
En este sentido, los hallazgos y conclusiones del informe n.º 92 de la FAO (2011) sobre "Evaluación de la calidad de la proteína de la dieta en nutrición humana", traducido al español por la Fundación Iberoamericana de Nutrición (FINUT) conjuntamente con varios documentos adicionales 13, han sido los siguientes:
En la evaluación de la calidad de la proteína, los aminoácidos de la dieta deben ser considerados como nutrientes individuales y, siempre que sea posible, en las tablas de alimentos deben proporcionarse los datos para los aminoácidos digestibles o biodisponibles sobre la base de la individualidad de los aminoácidos.
Se recomienda una medida nueva de la calidad de la proteína, la denominada "puntuación de los aminoácidos indispensables digestibles" (DIAAS), para reemplazar a la de PDCAAS. La DIAAS se define como: DIAAS % = 100 x (mg del aminoácido indispensable digerible en 1 g de la proteína de la dieta / [mg del mismo aminoácido en 1 g de la proteína de referencia]).
La utilización de la digestibilidad de los aminoácidos, tanto ileal como fecal, puede estar sujeta a limitaciones importantes, pero se concluye que, consideradas en su conjunto, la digestibilidad ileal de la proteína o del aminoácido (determinada en el íleon terminal al final del intestino delgado) refleja mejor las cantidades de los aminoácidos absorbidos y debe ser utilizada al calcular los DIAAS (Tabla I). La digestibilidad debe basarse en la digestibilidad ileal real de cada aminoácido determinada preferiblemente en humanos y, si no es posible, en cerdos o ratas en desarrollo, en este orden.
Cuando se trata de alimentos susceptibles de sufrir daños durante su procesamiento, debe utilizarse el contenido en lisina "reactiva" en vez de la lisina "total" para el cálculo de los DIAAS. Igualmente debe utilizarse la digestibilidad ileal real de la lisina reactiva (disponibilidad de lisina) en vez de la lisina total.
Los patrones de puntuación de los aminoácidos (es decir, los patrones de aminoácidos de la proteína de referencia) recomendados para calcular los DIAAS para lactantes desde el nacimiento hasta los 6 meses, para los niños desde los 6 meses a los 3 años y para los niños mayores, adolescentes y adultos se encuentran resumidos en diversas tablas del informe de la consulta de expertos 13. A efectos reguladores, se recomiendan dos patrones de puntuación: la composición en aminoácidos de la leche materna para las fórmulas de lactantes y el patrón para los niños de 6 meses a 3 años para los otros grupos.
Al elaborar los DIAAS, debe calcularse la relación para cada aminoácido indispensable de la dieta y designar como DIAAS al valor más bajo. Los valores de DIAAS pueden estar por debajo (o en algunas circunstancias, por encima) del 100%. Los valores por encima del 100% no deben ser truncados, excepto cuando los cálculos de DIAAS se realicen para ingesta de proteína o aminoácidos para dietas mixtas o alimentos como única fuente.
Aunque se dispone de una colección de la información actual disponible sobre la digestibilidad ileal real de los aminoácidos de los alimentos para los humanos, tras su valoración se ha llegado a la conclusión de que los datos disponibles son claramente insuficientes (Tabla II y Tabla III). Por tanto, se necesitan urgentemente más datos (determinados en humanos y modelos animales) sobre la digestibilidad ileal real de los aminoácidos de los alimentos para humanos. Se necesitan también comparaciones entre especies (humanos, cerdos y ratas) de la digestibilidad ileal real de los aminoácidos. En ese sentido, el informe hace recomendaciones para investigaciones futuras en esta área.
Tabla I. Promedio de los coeficientes de digestibilidad ileal y fecal aparentes de los aminoácidos en adultos ileostomizados y sanos (65 kg de peso) que recibieron una dieta basada en carne, verduras y cereales y una dieta basada en productos lácteos, respectivamente (de Rowan et al., 1994)1

Fuente: FAO-FINUT. Evaluación de la calidad de la proteína de la dieta en nutrición humana. Consulta de expertos. Granada, 2017. Disponible en: http://www.finut.org/category/publicaciones/
1Aminoácidos para los que se encontraron diferencias ileo-fecales significativas (p < 0.05)
*Significancia al nivel < 0.05
**Significancia al nivel 0.01
***Significancia al nivel de 0.001.
Tabla II. Digestibilidad ileal del nitrógeno determinada en humanos
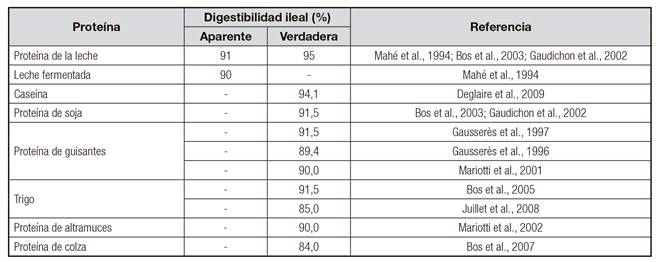
Fuente: FAO-FINUT. Evaluación de la calidad de la proteína de la dieta en nutrición humana. Consulta de expertos. Granada, 2017. Disponible en: http://www.finut.org/category/publicaciones/
Tabla III. Digestibilidad ileal verdadera (%) del nitrógeno y de los aminoácidos de la dieta para proteínas de leche o soja en voluntarios humanos sanos (de Gaudichon et al., 2002)
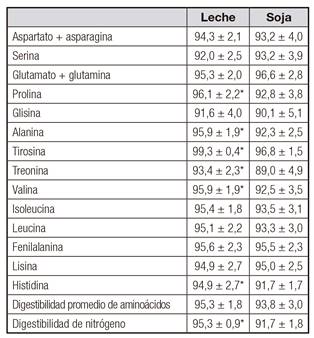
Fuente: FAO-FINUT. Evaluación de la calidad de la proteína de la dieta en nutrición humana. Consulta de expertos. Granada, 2017. Disponible en: http://www.finut.org/category/publicaciones/
Los valores son medias ± desviación estándar (n = 7 y n = 6 para leche y soja, respectivamente).
*Significativamente diferentes para el grupo de la soja (ANOVA, p < 0,05).
En particular, en el campo de la NE sería deseable investigar la disponibilidad de los aminoácidos en las diferentes formulaciones tanto de dietas estándar, normo e hiperproteicas como de dietas para el tratamiento de patologías específicas.
FACTORES QUE AFECTAN A LA CALIDAD PROTEICA
Existen numerosos factores que afectan a la calidad proteica, además de su composición en aminoácidos y sus propiedades digestivas características: factores intrínsecos, como la propia fuente proteica, su estructura secundaria, terciaria y cuaternaria o si la proteína misma tiene propiedades antinutricionales. También debe tenerse en cuenta el tipo de procesado al que ha sido sometida y la forma de almacenamiento 14,15.
Respecto al procesado de los alimentos, debe mencionarse que los tratamientos tecnológicos afectan a la funcionalidad de la proteína modificando su estado físico y los aminoácidos que la componen y, en ocasiones, hidrolizándola en pequeños péptidos 14. En este sentido, es importante señalar que algunos procesos tecnológicos, como la hidrólisis, pueden modificar sensiblemente la biodisponibilidad de los aminoácidos 13 (Tabla IV). En este campo aún queda bastante por investigar, ya que la mayoría de los estudios llevados a cabo se han realizado sobre las modificaciones de la lisina, pero no existe apenas información acerca de otros aminoácidos 16,17.
Tabla IV. Digestibilidad ileal aparente y verdadera de los aminoácidos para formulaciones mixtas basadas en caseína intacta o hidrolizada en humanos adultos. Valores medios y desviaciones estándar para datos globales (Deglaire et al., 2009)
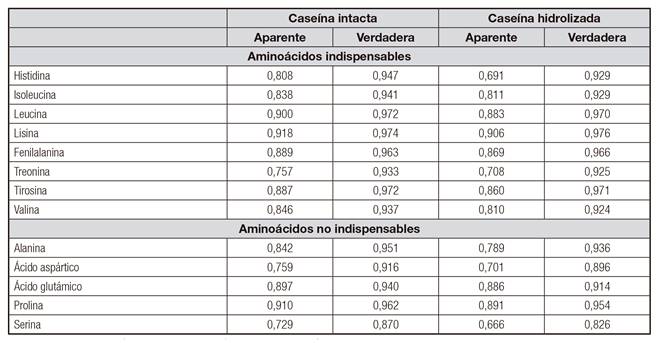
Fuente: FAO-FINUT. Evaluación de la calidad de la proteína de la dieta en nutrición humana. Consulta de expertos. Granada, 2017. Disponible en: http://www.finut.org/category/publicaciones/
Un tema reciente y de gran interés es la formación por el procesado de compuestos tóxicos, como la formación de acrilamida a partir de los residuos de asparragina tras la reacción de Maillard 14, aspecto con escasa información en el caso de los productos para NE.
La presencia de factores antinutricionales naturales (inhibidores de la tripsina, taninos, fitatos, glucosinolatos, etc.) o formados en el almacenamiento o procesado de los alimentos (lisinoalanina, D-aminoácidos) puede afectar la utilización digestiva y metabólica de la proteína y, por tanto, la biodisponibilidad de los aminoácidos, en algunos casos con reducciones de hasta el 50% 15,18.
PROTEÍNAS FUNCIONALES Y PÉPTIDOS BIOACTIVOS
Las proteínas funcionales y los péptidos bioactivos son proteínas y péptidos que, además de su valor nutricional por ser fuente de aminoácidos, son capaces de ejercer efectos biológicos específicos 19,20.
La mayoría de los péptidos bioactivos se generan espontáneamente durante la digestión in vivo a partir de las proteínas que los contienen. De hecho, la existencia de péptidos bioactivos como parte de la secuencia de aminoácidos en proteínas alimentarias se conoce desde hace más de 25 años. No obstante, también se han obtenido nuevos péptidos bioactivos a partir de proteínas alimentarias mediante digestión enzimática in vitro, empleando enzimas proteolíticas de origen microbiano o fúngico 21. Es más, se han obtenido péptidos modificados, diseñados a partir de péptidos naturales, con el fin de incrementar la actividad de estos últimos; es decir, por semisíntesis 22.
Por tanto, toda fuente de proteína alimentaria es en principio susceptible de aportar péptidos funcionales. Así, se han aislado péptidos a partir de hidrolizados enzimáticos de proteínas de muy diversa procedencia, como leche, sardina, maíz, soja, huevo, gelatina, etc. 20. La literatura científica evidencia que los péptidos bioactivos pueden ejercer su acción tanto a nivel local (tracto gastrointestinal) como sistémico 19,20,21,22,23, ya que pueden atravesar el epitelio intestinal y llegar a tejidos periféricos a través de la circulación sanguínea 22,23.
El concepto de funcionalidad de las propias proteínas alimentarias tampoco es nuevo. De hecho, la existencia de proteínas funcionales en la leche materna se conoce desde hace más de 50 años y hoy en día resulta evidente si se tiene en cuenta que los recién nacidos poseen un sistema digestivo inmaduro y, por tanto, dependen de distintas proteínas presentes en la leche materna (inmunoglobulinas, enzimas -lisozima y lactoperoxidasa- o proteínas de unión al hierro -lactoferrina y transferrina-) y de las células inmunocompetentes (macrófagos, granulocitos y linfocitos T y B) para combatir infecciones potenciales 24,25.
Por otra parte, la leche aporta una serie de proteínas, denominadas en conjunto factores de crecimiento (factores de crecimiento epidérmico [EGF], factor de crecimiento transformante [TGF-] o factores de crecimiento similares a la insulina [IGF]), que pueden tener un papel importante en la maduración y en la función del sistema intestinal y del sistema inmune del neonato, en función de sus efectos sobre el mantenimiento, la reparación y la proliferación celular 34,35,36.
Existen, por último, tanto en la leche materna como en el calostro, hormonas, como la del crecimiento (GH), que parecen ejercer un importante papel en el desarrollo y en la función intestinal, y neuropéptidos como la neurotensina, la sustancia P, la somatostatina y el péptido intestinal vasoactivo. Entre estos, tanto el péptido intestinal vasoactivo como la sustancia P poseen actividades inmunomoduladoras 24,25,26.
Por tanto, el concepto realmente novedoso desde el punto de vista de la nutrición es la utilización de las proteínas y los péptidos procedentes de alimentos con el fin de mejorar una función biológica o de tratar, de prevenir o de reducir el riesgo de enfermedad. Así, varios péptidos y proteínas han sido propuestos para el tratamiento de enfermedades dentales, de la mala absorción de minerales, de la diarrea, de la hipertensión, de la trombosis o de inmunodeficiencias 19,20,21,22,23. La leche, el huevo y la soja son las fuentes de proteínas funcionales y péptidos bioactivos más estudiadas hasta la fecha.
COMPUESTOS NITROGENADOS NO PROTEICOS
El término condicionalmente esencial (o semiesencial), aplicado inicialmente a los aminoácidos, se utiliza de forma generalizada para otros nutrientes. Un nutriente condicionalmente esencial es un compuesto producido usualmente en cantidades adecuadas por síntesis endógena, pero que se requiere de forma exógena bajo determinadas circunstancias. Así, la arginina, la glutamina, la cisteína, la glicina, la prolina y la tirosina son aminoácidos semiesenciales. Entre los derivados de aminoácidos, la carnitina, la colina y las poliaminas tienen también el carácter de compuestos condicionalmente esenciales. Asimismo, los nucleótidos de la dieta se consideran compuestos semiesenciales debido a que algunos tejidos de rápido crecimiento (como el intestino, la médula ósea y los linfocitos) utilizan preferentemente bases púricas y pirimidínicas preformadas para la síntesis de ácidos nucleicos 27.
La arginina está implicada en las funciones endotelial, inmunitaria, gastrointestinal y renal, así como en la reproducción, el desarrollo neonatal, la curación de heridas y la tumorogénesis. La glutamina es necesaria para el mantenimiento de la integridad intestinal y tiene efectos beneficiosos en estados catabólicos como la sepsis, la infección, el trauma y el cáncer, y los nucleótidos están involucrados en el crecimiento y la diferenciación celular, y tienen efectos sobre el metabolismo lipídico, la microbiota intestinal y el sistema inmunitario, tanto en los lactantes como en los adultos 28.
Aunque algunas fórmulas para NE incluyen algunos aminoácidos como arginina, glutamina y nucleótidos, son necesarios nuevos estudios que investiguen el papel funcional de estos compuestos en diversas patologías que cursan con alteraciones del sistema inmunitario y de los procesos inflamatorios.
LÍPIDOS
El interés de los lípidos a lo largo de estos últimos años ha ido incrementándose a medida que han ido conociéndose sus implicaciones en numerosos mecanismos biológicos; entre ellos, los procesos de regulación de la inflamación y de la respuesta inmunitaria 29.
Los lípidos de la dieta, además de servir como fuente de ácidos grasos esenciales, fuente calórica y como portadores de vitaminas liposolubles, son un componente estructural fundamental de las membranas celulares, donde regulan su fluidez e intervienen en la actividad de los receptores, por lo que juegan un importante papel en la respuesta inmunológica, tanto a nivel del mantenimiento de las estructuras celulares como a nivel de la comunicación intra e intercelular 29.
En las últimas décadas, el conocimiento acerca de las propiedades antiinflamatorias de los lípidos ha facilitado el desarrollo de productos adaptados a la NE que han sido utilizados como terapia en numerosas enfermedades de base inflamatoria.
Durante los procesos inflamatorios se producen mediadores químicos, como los eicosanoides y docosanoides, a partir de ácidos grasos poliinsaturados presentes en las membranas celulares 30. La actividad inflamatoria de estas moléculas depende del ácido graso precursor. Los derivados del ácido araquidónico (AA) (20:4 n-6), que a su vez deriva del ácido graso esencial linoleico (LA) (18:2 n-6), tienen una elevada actividad proinflamatoria, mientras que los derivados del eicosapentaenoico (EPA) (20:4 n-3) y del docosahexaenoico (DHA) (22:6 n-3), derivados a su vez del ácido -linolénico (18:3 n-3), son débilmente inflamatorios. Así, al ingerir aceites de pescado o de algas marinas, ricos en ácidos grasos n-3, aumenta el contenido de EPA y de DHA y disminuye el de AA en todas las células, incluidas las del sistema inmunitario, por lo que se reduce la estimulación inflamatoria debido a la presencia de mediadores menos activos. Este parece ser el mecanismo inmunomodulador fundamental de las dietas ricas en n-3, si bien en los últimos años se ha descubierto que existen una serie de mediadores de la resolución de la inflamación, tales como lipoxinas, resolvinas y protectinas, que derivan de los ácidos grasos poliinsaturados y que también parecen desempeñar un papel fundamental en estos procesos (Fig. 1). Asimismo, pero mediante mecanismos diferentes de acción, se ha demostrado que el ácido oleico disminuye la intensidad de algunos procesos inflamatorios, al disminuir la producción de mediadores quimiotácticos de inflamación.

Figura 1. Esquema general de la síntesis de eicosanoides y docosanoides y su papel en la inflamación (AT-LXA4: lipoxina A4 mediada por aspirina; COX-2: ciclooxigenasa 2; DHA: ácido docosahexaenoico; EPA: ácido eicosapentaenoico; 17S-HDHA: ácido hidroxidocosahexaenoico; 14S-HpDHA y 17S-HpDHA: ácidos hidroperoxidocosahexaenoicos; 5Hp-18R-HEPE: ácido hidroperoxi-hidroxieicosapentaenoico; 18R-HEPE: ácido hidroxieicosapentaenoico; 15S-HETE y 15R-HETE: ácidos hidroxieicosatetraenoicos; LOX: lipooxigenasas; LTA4, LTB4 y LTC4: leucotrienos; LXA4: lipoxina A4; MaR1: maresina 1; PD1: protectina D1; PGD2 y PGE2: prostaglandinas; PGH2: prostaglandina hidroperóxido; Rv: resolvinas). (Adaptado de Serhan y Petasis, 2011).
De forma general, puede concluirse que la suplementación de dietas para utilización en nutrición enteral con ácidos grasos poliinsaturados (AGPI) n-3 y oleico resulta beneficiosa para el tratamiento de ciertas patologías en las que los procesos inflamatorios participan activamente en su desarrollo, mejorando su evolución y disminuyendo las dosis de fármacos antiinflamatorios con importantes efectos secundarios. Asimismo, existen algunas atractivas vías de investigación destinadas a conseguir revertir la caquexia cancerosa con la adición de AGPI n-3 a las fórmulas de nutrición enteral. Dentro de este contexto, el desarrollo de mezclas de lípidos con triacilglicéridos de composición estructurada debe suponer un avance importante en la mejora de las formulaciones para NE.
HIDRATOS DE CARBONO
Las fórmulas para NE utilizan una gran variedad de hidratos de carbono como fuente de energía, aunque predomina el uso de maltodextrinas de peso molecular variable, ya que son una excelente fuente de glucosa y permiten mantener la osmolaridad dentro de un rango deseable para evitar procesos de diarrea indeseables.
En varias patologías, como la diabetes y el síndrome metabólico, usualmente asociado a la obesidad, así como en otras situaciones de resistencia insulínica, como los grandes traumas y pacientes en unidades de cuidados intensivos, se trata de utilizar hidratos de carbono con bajo índice glucémico (IG), como las maltodextrinas entrecruzadas por vía química o enzimática y, en ocasiones, monosacáridos como la fructosa.
El IG se define como el aumento del área bajo la curva (area under the curve, AUC) de la respuesta de la glucosa en sangre obtenida con una ración de 50 g de hidratos de carbono disponibles en un alimento, expresada como porcentaje de la respuesta, en el mismo sujeto, tras la ingesta de 50 g de glucosa 31. El IG es una propiedad de los hidratos de carbono individuales de los alimentos evaluados tal cual, sin añadirles nada, y se utiliza frecuentemente de forma incorrecta para indicar "respuesta glucémica" en diversas situaciones, que incluyen: mezclas de comidas, alimentos que contienen hidratos de carbono no disponibles y diferencias entre sujetos. Se sabe que la grasa y la proteína afectan a las respuestas glucémicas, pero estos efectos no tienen nada que ver con la respuesta glucémica de los hidratos de carbono. Además, los efectos de la grasa y de las proteínas añadidas sobre las respuestas glucémicas difieren en los sujetos normales y en los sujetos con diabetes mellitus de tipo 2 (DM2). Por tanto, los términos IG y "respuesta glucémica" no deberían confundirse.
El concepto de "carga glucémica" (CG) se define como la suma de todos los hidratos de carbono contenidos por ración de cada alimento ingeridos al día multiplicada por su IG (3297) 32. Cuando se aplica a alimentos de forma individual, la carga glucémica se define como el IG por los gramos de hidratos de carbono divididos por 100 33. Brand-Miller y cols. 34 concluyeron que la CG de la dieta era válida como medida de la respuesta glucémica global de un alimento o una dieta y de la demanda de insulina.
Los efectos sobre el metabolismo y la salud derivados de una menor ingesta de hidratos de carbono dependen de lo que se consuma en su lugar. Todos los estudios epidemiológicos y los ensayos a corto y largo plazo muestran que los efectos conseguidos tras la modificación del IG de la dieta no son iguales a los efectos conseguidos tras modificar la cantidad de hidratos de carbono. Por tanto, se necesitan más investigaciones para determinar si la CG predice respuestas glucémicas agudas y si son beneficiosos los métodos específicos de reducir la CG de la dieta, además de reducir el IG 31.
Poco después de surgir el concepto de IG, se sugirió también la necesidad de una medida de la secreción de insulina provocada tras la ingesta de los alimentos para ayudar a comprender el mecanismo por el cual se alteran las respuestas de glucosa, así como para aportar información que sea clínicamente útil para el diseño de dietas. La respuesta insulinémica (o índice insulinogénico [IinI]) no es necesariamente proporcional a la respuesta de glucosa, y otros nutrientes diferentes a los hidratos de carbono también influyen de forma global en la respuesta de insulina posprandial 35.
Existen numerosos factores insulinotrópicos que son conocidos como potenciadores del efecto de estimulación de la glucosa y que actúan mediando la secreción posprandial de insulina. Estos factores incluyen aminoácidos específicos, ácidos grasos y hormonas gastrointestinales como el péptido gastrointestinal insulinotrópico (GIP), el péptido 1 análogo del glucagón (GLP-1), el propio glucagón y la colecistoquinina (CCK) 36. La adición de grasas a comidas ricas en hidratos de carbono reduce la glucemia, pero no modifica la respuesta insulinémica 37.
Las maltodextrinas entrecruzadas, así como los almidones de tipo IV, no solo tienen un bajo IG, sino que también exhiben un reducido InI, por lo que son de utilidad en el desarrollo e innovación de numerosas dietas para NE. Además, al no ser hidrolizadas y absorbidas completamente a nivel intestinal, actúan como verdaderos prebióticos, contribuyendo al establecimiento de una microbiota intestinal en la que predominan las bacterias Gram positivas y, por otra parte, determinan una mayor saciedad.
La fructosa se ha utilizado con frecuencia en dietas para NE en las que se deseaba disponer de hidratos de carbono de bajo IG. Sin embargo, actualmente se sabe que la fructosa en dosis relativamente elevadas se absorbe en grandes cantidades, no solo a través del transportador GLUT 5, sino a través del transportador GLUT2, que migra desde la zona basal de los enterocitos a su parte apical 36,38. Una vez alcanza el hígado, la fructosa es metabolizada de inmediato, en su mayoría hasta triosas-fosfato, dando lugar a acetil-CoA y, por tanto, a la síntesis de triacilglicéridos y de colesterol. Este hecho hace que la fructosa, aunque tenga un IG bajo, no sea adecuada en el tratamiento de pacientes con DM2 o enfermos críticos en los que la propia resistencia tisular periférica a la insulina inhibe la utilización de los lípidos circulantes, lo que conduce a una hipertrigliceridemia, que en el caso de los pacientes con DM es un factor de riesgo para la enfermedad cardiovascular 39.
FIBRA DIETÉTICA
La fibra dietética comprende un conjunto muy heterogéneo de moléculas complejas que ha ido aumentando con los años, a medida que se han descubierto nuevos componentes. Basándose en los avances más recientes, la definición propuesta por diversos autores es: "Cualquier componente de la dieta que alcanza el colon sin ser absorbido en un intestino humano sano". Esta definición no restringe la fibra dietética a los hidratos de carbono clásicos, sino también a otras sustancias, como la lignina, inulina y ciertos oligosacáridos, como fructooligosacáridos, galactosiloligosacáridos y lactosiloligosacáridos 40.
Algunas fibras de carácter soluble sufren fermentación anaerobia por la microbiota bacteriana colónica con producción de ácidos orgánicos, como el lactato, y ácidos grasos de cadena corta (SCFA) (acetato, propionato butirato) y la consiguiente disminución del pH intraluminal. Estos ácidos grasos son rápidamente absorbidos por la mucosa intestinal y constituyen una fuente importante de sustratos para el metabolismo del colonocito (especialmente el butirato), estimulan el trofismo de la mucosa, la absorción de agua y sodio e inducen la producción de mucina y de enzimas que favorecen la regeneración de la mucosa 41. Por otra parte, los SCFA, en parte, pasan a la circulación sistémica y ejercen efectos beneficios en otros tejidos periféricos, como el músculo, el tejido adiposo y el hígado, estimulando los procesos oxidativos y la sensibilidad a la insulina, procesos mediados por receptores específicos de SCFA y la enzima tisular AMP-quinasa 42.
El ácido graso de cadena corta más estudiado ha sido el butirato, del que se ha demostrado que tiene un efecto antiinflamatorio directo debido a la inhibición de la transmigración del factor nuclear NF-kB al núcleo y su subsecuente unión al DNAD, lo que previene la transcripción de los mediadores proinflamatorios. Se ha visto también que inhibe la activación y la proliferación de linfocitos y la actividad de mieloperoxidasa en neutrófilos, responsable de lesiones tisulares específicas 42.