INTRODUCCIÓN
Cuando se intenta definir la calidad dentro de un contexto sanitario, desde un principio hay que ser reflexivos sobre el gran número de posibles y legítimas definiciones que se pueden plantear en función del enfoque considerado. Una aproximación a este concepto sería definirla como aquella propiedad o conjunto de propiedades inherentes a un servicio asistencial que permiten apreciarlo como igual, mejor o peor que los restantes servicios de su misma especie. De esta definición se derivan tres características importantes. En primer lugar, la necesidad de entender el concepto de calidad como un término relativo. En segundo lugar, que el concepto lleva implícito el de comparación ("igual, mejor o peor") y, por último, la necesidad de contar con un estándar, norma o modelo con el cual compararse 1.
Así pues, de acuerdo al enfoque que se tenga en consideración, la definición de la calidad asistencial puede ser diversa. Teniendo en cuenta esta heterogeneidad, Avedis Donabedian sistematizó la evaluación de la calidad de la asistencia sanitaria como una triada de estructura, proceso y resultados. Las medidas o indicadores estructurales son aquellos que evalúan las características de todo el entorno sanitario, los indicadores de proceso evalúan el desempeño durante la prestación del servicio y los de resultado evalúan los efectos de la atención que se proporcionó 2.
Como no podía ser de otra forma, y tomando en consideración la importancia que ha ido adquiriendo la medida de la calidad a todos los niveles dentro de los sistemas de salud, se han incorporado a esta evaluación sistemática y a través de herramientas como los indicadores sugeridos por Donabedian los procedimientos realizados en las unidades de endoscopia. Sin embargo, uno de los grandes retos a los que se enfrenta el médico especialista en aparato digestivo o endoscopista en el día a día es mantener una alta calidad en las colonoscopias que realiza a pesar del incremento progresivo de la demanda. Es, por tanto, fundamental implementar programas de mejora continua de la calidad, para los que se necesitan indicadores basados en la evidencia científica válidos y fiables. En consonancia con esta necesidad, la Sociedad Española de Patología Digestiva ha desarrollado el proyecto de indicadores en endoscopia digestiva. Dando continuidad a este planteamiento, el presente estudio contempla los procedimientos e indicadores de calidad recomendados en colonoscopia. Es relevante hacer referencia al primer estudio con el cual se inició este proyecto 3, puesto que en él se revisaron conceptos sobre los aspectos generales y fundamentales de la calidad tales como: dimensiones o valores y la importancia de desarrollar indicadores siguiendo la línea propuesta por Donabedian y desde el enfoque de la endoscopia 1,2,3,4. En consecuencia, este estudio pretende proponer los procedimientos e indicadores de estructura, proceso y resultado necesarios para aplicar y evaluar la calidad en la colonoscopia.
METODOLOGÍA
El estudio se desarrolló en dos fases. La primera, formando un grupo multidisciplinar de trabajo con base en el Hospital Clínico Universitario Virgen de la Arrixaca de Murcia que realizó una revisión bibliográfica y el diseño del procedimiento para colonoscopia diagnóstica. En una segunda fase, se revisaron y analizaron las propuestas del grupo por parte de un panel de profesionales seleccionados desde la SEPD hasta alcanzar una versión definitiva. Posteriormente, se diseñaron las fichas técnicas para cada uno de los indicadores propuestos para evaluar estos procedimientos.
Estrategias de búsqueda bibliográfica y selección de estudios
Se han utilizado dos estrategias de búsqueda bibliográfica: la primera, dirigida a guías de práctica clínica (GPC), y la segunda, orientada en artículos originales y revisiones. Las GPC de colonoscopia se han extraído de tres fuentes internacionales (Agency for Healthcare Research and Quality [AHRQ], National Institute for Health and Care Excellence [NICE], Scottish Intercollegiate Guidelines Network [SIGN]) y una española (GuíaSalud), así como de revisiones en páginas web de las principales sociedades de endoscopia y gastroenterología (American Society for Gastrointestinal Endoscopy [ASGE], American Gastroenterological Association [AGA], European Society of Gastrointestinal Endoscopy [ESGE], Sociedad Española de Endoscopia Digestiva [SEED], SEPD y Asociación Española de Gastroenterología [AEG]). Para la búsqueda de artículos originales, se han utilizado las bases de datos Web of Knowledge (WoK), PubMed y Cochrane, a través de una estrategia de búsqueda consistente en la selección de todos los documentos fechados entre el 1 de enero de 2006 y el 10 de agosto de 2016 que contuvieran cualquiera de los siguientes descriptores: [colonoscop*] con estos otros [informed consent, quality, safety, (security), assessment, assurance, indicators, criteria]. Filtros activados: clinical trial, controlled clinical trial, meta-analysis, randomized controlled trial, review, guideline, practice guideline, publication date from 2006/01/01 to 2016/08/10; humans; adults; language: English, Spanish. De forma complementaria, se llevó a cabo una revisión de la bibliografía de los estudios originales que fueron seleccionados e incluidos en el análisis y de las guías clínicas y metaanálisis publicados, seleccionando aquellas referencias no detectadas previamente y consideradas de interés. Tras haber completado el protocolo de búsqueda, los artículos incluidos fueron revisados y analizados por separado por dos revisores. Cada revisor cribó los estudios aplicando cualquiera de los siguientes criterios: a) el documento incluye recomendaciones sobre la correcta preparación, ejecución y seguimiento; b) el documento incluye o propone indicadores de calidad relacionados con estructura, proceso o resultado. Los estudios seleccionados por un solo revisor fueron cotejados por el resto para decidir su selección definitiva o no. Para examinar homogéneamente cada documento seleccionado se elaboró una tabla en la cual se registró información sobre indicadores de estructura, proceso o resultado, y si dicha información era explícita o no. Además, se incluyó en la tabla el tipo de estudio referenciado (ensayos clínicos, estudios observacionales, metaanálisis, etc.), que se identificó como referido a colonoscopia.
Diseño de los procedimientos de colonoscopia
Tomando como punto de partida la bibliografía seleccionada y la experiencia de los autores, se recopilaron y ordenaron las actividades necesarias para cada uno de los procedimientos. En el caso de los procedimientos comunes a toda exploración endoscópica, las diferencias estructurales, funcionales y organizativas lógicas entre las diferentes unidades clínicas de endoscopia digestiva restringen su desarrollo a mínimos. Igualmente, al no ser objeto del trabajo, se excluyó la descripción de técnicas específicas que pudieran aplicarse en algunas situaciones. El resultado se diagramó empleando flujogramas o diagramas de vías paralelas. Las propuestas del grupo fueron revisadas y analizadas por un panel de profesionales seleccionados desde la SEPD hasta alcanzar una versión definitiva.
Diseño de indicadores
Para obtener indicadores válidos se determinó la calidad del conocimiento disponible sobre las actividades incluidas en los procedimientos y los documentos seleccionados en la búsqueda. Esto se llevó a cabo utilizando el método de graduación de la calidad del conocimiento disponible del modelo GRADE. En el sistema GRADE, la calidad de la "evidencia" (se empleará en adelante este término, sin entrecomillar, en el sentido de "mejor conocimiento disponible basado en pruebas") se clasifica, inicialmente, en alta o baja según provenga de estudios experimentales u observacionales. Posteriormente, según una serie de consideraciones de elementos que pueden disminuir o aumentar la calidad de partida, la graduación queda en alta, moderada, baja y muy baja 4,5. Para asegurar la fiabilidad y facilitar el cálculo de los indicadores seleccionados en las unidades clínicas, cada uno de ellos se acompaña de una ficha que incluye: ámbito de aplicación (procedimiento[s] en los que se aplica); denominación; fórmula de cálculo; tipo de indicador según el modelo de Donabedian 3; relación temporal con la prueba (preprocedimiento, procedimiento, posprocedimiento); dimensión de la calidad con que se relaciona; justificación, exclusiones y aclaraciones; y nivel de evidencia que lo sustenta.
RESULTADOS Y DISCUSIÓN
Resultados de la búsqueda
Se inició el proceso de selección suprimiendo las duplicidades y, al analizar título y/o resumen, se excluyeron aquellos estudios que abordaban explícitamente la colonoscopia en cribado de cáncer, los que no estaban bien referenciados, los que se hallaban solo en formato de resumen, por no estar disponibles, por ser anteriores a 2006, por tratar sobre temas de pediatría, veterinarios o endoscopias no digestivas, o por estar publicados en idioma distinto al castellano o al inglés. Hemos hecho una excepción al realizar el análisis y la búsqueda con la definición de cáncer de intervalo, nacido muy específicamente de la colonoscopia de cribado, por tratarse de un indicador de resultado directo de la calidad de una colonoscopia, si bien se conoce que no es el único factor que puede influir en su desarrollo, tal y como se comentará después.
En total, se han incluido en el análisis por pares 260 estudios y han sido valorados en texto completo, tratándose de ensayos clínicos tanto aleatorizados como no aleatorizados, así como de series de casos de alta calidad, revisiones y metaanálisis, un total de 107.
Procedimiento de la colonoscopia
Se ha plasmado en un diagrama (Fig. 1) cuya descripción de pasos correlativos es la siguiente:
1. Situar al paciente en posición correcta:
- Decúbito lateral izquierdo, aunque en caso de que no se emplee el método es posible la colocación en supino.
- Cabeza en posición neutra con ayuda de almohada.
- Si precisa acceso venoso, usar preferentemente brazo derecho.
2. Comprobar correcto funcionamiento del endoscopio:
- Visión adecuada y de calidad.
- Angulación del extremo.
- Aire y agua.
- Succión.
3. Lubricar endoscopio.
4. Insertar endoscopio:
- Tacto rectal con lubricación generosa.
- Seleccionar técnica de inserción (podría ser híbrido o mixto, por tramos):
Método de una persona. El endoscopista es autónomo para la inserción. La ayuda del asistente es solo para compresión abdominal, cambios posturales o necesidad de soporte.
Método asistido. El asistente maneja la caña del endoscopio y el endoscopista, los controles.
- Atravesar esfínter anal. Tres alternativas:
Presionar oblicuamente con el índice hasta que se relaja el esfínter.
Introducir la punta del pulgar para sustituirla por el tubo.
Inserción directa.
5. Avanzar hacia fondo cecal:
- Maniobrar en todo el trayecto de forma adecuada:
Ejecutar movimientos de progresión del tubo de poco recorrido para evitar formación de bucles.
Mantener siempre el endoscopio en el centro de la luz colónica.
Coordinar adecuadamente los movimientos de rotación (torque) y de angulación con ambas manos.
Superar angulaciones con movimientos ligeros de pulsión, seguidos de pequeña retirada y rotación horaria del tubo, para mantener la rectificación.
Insuflar para mejorar visibilidad, evitando la sobredistensión.
Los cambios posicionales pueden ayudar a franquear zonas complicadas del colon.
- Mantener una actitud adecuada ante los hallazgos:
Extirpar o biopsiar las lesiones según tipo, tamaño y consistencia.
Referenciar las lesiones, incluyendo aspecto, forma, tamaño y diagnóstico de presunción.
Ubicar las lesiones mediante distancias desde ano/ciego o con referencias anatómicas cuando es posible (colon transverso, ciego, ángulos hepático y esplénico, anastomosis, cicatrices, etc.).
- Atravesar el recto empujando el endoscopio.
- Atravesar colon sigmoides empujando el tubo en sentido antihorario, habitualmente formando un bucle alfa, con ayuda del auxiliar.
- Deshacer el bucle en colon descendente, retirando el colonoscopio y aplicando torque en sentido horario.
- Progresar empujando el tubo hasta colon transverso.
- Superar la angulación de la porción media del colon transverso retirando el endoscopio con torque horario, al tiempo que se aspira suavemente.
- Para superar el ángulo hepático, aplicar aspiración y suave torque. Puede ser necesario aplicar compresión en epigastrio para prevenir bucles en colon transverso.
- Empujar y aspirar en colon ascendente hasta llegar a fondo cecal.
- Considerar registro de imagen.
6. Valorar la entrada en íleon:
- Sopesar según la indicación de la prueba, los hallazgos realizados y la facilidad anatómica.
7. Retirar el tubo:
- Maniobrar lentamente.
- Limpiar exhaustivamente, eliminando restos de moco.
- Mirar detrás de cada haustra.
- Observar con detalle para identificar irregularidades en haustras y alteraciones de la circulación submucosa.
- Mantener una actitud adecuada ante los hallazgos:
Pólipos:
- Describir morfología (clasificación de París), tamaño y ubicación.
- Valorar magnificación para mejorar el diagnóstico.
- Extirpar o biopsiar.
Lesiones sospechosas de cáncer:
- Localizar y biopsiar.
- Marcar con tinta china (excepto recto bajo y ciego).
- Progresar hacia ciego si la lesión es franqueable.
- Tomar biopsia.
- Describir extensión, afectación parcheada o continua.
- Intentar ver íleon.
Lesiones vasculares (angiodisplasias, etc.):
- Describir.
- Valorar electrocoagulación.
Divertículos:
- Describir.
- Evitar insuflación, en especial si hay componente inflamatorio.
- Aspirar la mayor cantidad de aire posible por tramos.
8. Visualizar recto:
- Apoyar tubo en la pared y girar para realizar retroversión en ampolla rectal.
- Inspeccionar mucosa.
9. Finalizar exploración:
- Retirar completamente el tubo.
- Pasar el endoscopio al personal auxiliar para su limpieza y nueva preparación.
Indicadores
En la tabla 1 se puede ver un esquema general de los indicadores específicos para el procedimiento de la colonoscopia (en negrita), junto a los generales de todos los procedimientos endoscópicos.
De las diferentes dimensiones de la calidad, una de las más olvidadas en las diferentes guías sobre calidad en colonoscopia es la eficiencia. En esta guía se ha planteado la eficiencia como una dimensión transversal que refleje el modo de evaluar los indicadores propuestos. Por ejemplo, se ha incluido un indicador poco habitual denominado "todos los pólipos extirpados", para insistir en la necesidad de resolver en un solo procedimiento las necesidades del paciente. También la eficiencia nos ha influido a la hora de definir los indicadores de extirpación de adenomas, basándonos exclusivamente en la colonoscopia índice (excluyendo las colonoscopias de repetición para completar un procedimiento anterior).
B.06. Intervalo adecuado entre colonoscopias
Se han publicado varias guías de práctica clínica respecto al seguimiento de estos pacientes 7,8,9. Estas guías están basadas fundamentalmente en estudios poblacionales y ensayos clínicos con diferentes tipos de seguimiento que tienen en cuenta el riesgo de desarrollo de nuevas lesiones después de la colonoscopia índice. En este estudio se recomienda que cada Unidad de Endoscopia digestiva se adhiera a una de estas guías para establecer su propia práctica y evalúe el indicador propuesto.
La extirpación de adenomas o de pólipos serrados durante una colonoscopia es un factor de riesgo para el desarrollo posterior de nuevos adenomas y cáncer colorrectal. La indicación de la colonoscopia como seguimiento de adenomas o pólipos serrados previamente extirpados es, hoy día, uno de los motivos más frecuentes de colonoscopia. Con frecuencia puede existir una sobreindicación por este motivo, lo que supone una sobrecarga de trabajo innecesaria. Por otro lado, un seguimiento inapropiado o laxo supone el riesgo de desarrollo de nuevas lesiones o incluso de cáncer colorrectal para el paciente. Un seguimiento apropiado previene la aparición de cáncer colorrectal, aunque no de una manera completa. El seguimiento tras la extirpación de un adenoma colónico va a depender de tres factores: la calidad de la colonoscopia índice, las características y el número de las lesiones extirpadas y la técnica o dificultad de extirpación del adenoma o pólipo serrado 10,11.
C.04. Preparación del colon
Conseguir una preparación o limpieza colónica adecuadas es uno de los problemas de calidad más frecuentes en colonoscopia 12. Una buena o, al menos, moderadamente buena limpieza colónica facilita una mejor detección de adenomas de colon, como se ha comprobado en varios ensayos clínicos y metaanálisis 13,14. Así, indirectamente, como se verá más adelante, evita el desarrollo de cáncer colorrectal. Las guías de práctica clínica publicadas, basadas en revisiones sistemáticas y metaanálisis, recomiendan el uso de dosis dividida o la totalidad de la dosis de limpieza colónica administrada pocas horas antes del procedimiento 15,16,17,18. La preparación del colon ha de ser individualizada para cada paciente en función de sus riesgos personales 19. El estándar recomendado de limpieza adecuada varía entre el 85% y el 90%, siendo este último valor el recomendado para las colonoscopias de cribado 20,21. En este trabajo se plantea como recomendación la utilización de la escala de Boston 22,23. Utilizando esta escala es recomendable que la valoración de cada segmento sea al menos dos o tres 13.
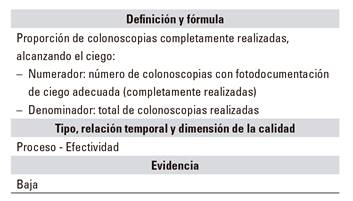
C.05. Colonoscopia completa
Uno de los objetivos técnicos de cualquier colonoscopia es la exploración completa del colon. Las exploraciones incompletas se asocian a un mayor riesgo de cáncer de intervalo 24. En la práctica clínica, el cumplimiento de este indicador ha podido ser muy variable hasta hace poco tiempo 25,26,25,26,27,28,12. Se considera una colonoscopia completa cuando la punta del endoscopio supera la válvula ileocecal, lo que permite valorar la cara medial del ciego (un punto frecuente de aparición de cáncer de intervalo) y la zona del orificio apendicular. En el informe debe constar que se identificaron las estructuras propias del ciego (válvula ileocecal y orificio apendicular). Además, se debe documentar el ciego mediante una imagen que incluya el orificio apendicular y el pliegue característico del ciego 20,21,29,30,31.
C.06. Extirpación de todos los pólipos menores de 20 mm
La colonoscopia, como cualquier otro procedimiento médico, ha de resultar coste-efectiva, a ser posible, al primer intento. Uno de los objetivos técnicos ha de ser la extirpación de todos los pólipos, que, en principio, estén al alcance de cualquier endoscopista medio 12,25. Aunque existen escalas para evaluar la dificultad de extirpación de un pólipo, aún no están suficientemente validadas 11. No hay mucha evidencia al respecto, pero se considera que un indicador basado en el tamaño de los pólipos (20 mm) puede dar una idea de la calidad técnica global de la extirpación de pólipos por parte del endoscopista. Algunos pacientes pueden presentar pólipos complejos o muy numerosos. Un endoscopista puede elegir entre extirpar inicialmente los más difíciles y posponer los más sencillos para una segunda colonoscopia, o bien, extirpar todos los pólipos de un segmento determinado 30. Al igual que otros indicadores que veremos más adelante, este indicador solo debe ser valorado en las colonoscopias índice. Se considera la colonoscopia índice como la primera llevada a cabo al paciente (por síntomas, cribado, seguimiento adecuado).
C.07. Todos los pólipos menores de 20 mm extirpados en un solo fragmento
Dentro de los indicadores de evaluación de la capacidad técnica de los endoscopistas en lo relativo a la extirpación de pólipos, se pueden considerar varios: como el porcentaje de pólipos extirpados en un fragmento o el índice de fragmentos por mucosectomías mayores de 2 cm. Técnicamente, se considera posible extirpar la mayoría de los pólipos menores de 20 mm en un solo fragmento por parte de la mayoría de los endoscopistas 32. No obstante, algunos pólipos menores de 20 mm pueden presentar problemas de accesibilidad que hagan aconsejable la extirpación en dos o más fragmentos.
C.08. Tiempo de retirada
El tiempo de retirada es considerado un indicador de calidad indirecto, relacionado con los índices de detección de adenomas y cáncer de intervalo 33,34. Es, por tanto, un indicador a considerar especialmente en aquellos médicos con índices de detección de adenomas bajos. Este indicador se evalúa sobre las colonoscopias en las que no se encuentran pólipos. El estándar considerado varía entre seis y ocho minutos, como promedio de las colonoscopias llevadas a cabo por un endoscopista 35,36. Es importante destacar que la longitud del colon es variable y que, para un colon corto con una limpieza colónica adecuada, el tiempo de retirada necesario podría ser inferior al estándar. No todos los estudios encuentran valor a este indicador 37,38.
C.09. Toma de biopsias en pacientes con diarrea crónica
En pacientes con diarrea acuosa intermitente o crónica se ha descrito la prevalencia de colitis microscópico en torno al 9,5-13,7% 39,40. El diagnóstico de estas enfermedades podría mejorar la calidad de vida mediante el tratamiento específico con medicamentos como la budesonida oral 41. Hasta el momento, la única forma de diagnosticar la colitis microscópica (colágena o linfocítica) es la toma de biopsias sistemática durante la colonoscopia en este tipo de pacientes. Se recomiendan varias pautas posibles, como la toma de biopsias a lo largo de todo el colon, que incluiría al menos cuatro biopsias de colon proximal a ángulo esplénico 42,43.
C.10. Número y distribución de biopsias en pacientes con enfermedad inflamatoria intestinal (EII)
En los pacientes con enfermedad inflamatoria intestinal con afectación colónica existe un riesgo incrementado de cáncer colorrectal 44. Dicho riesgo es mayor cuanto más extensa sea la afectación colónica y más largo el tiempo de evolución de la enfermedad. En estos pacientes, el cáncer de colon es precedido del desarrollo de displasia. Los programas de seguimiento de estos pacientes con múltiples biopsias pueden mejorar su esperanza de vida. Recientemente, varios ensayos clínicos han mostrado una mayor eficacia de la detección de displasia mediante endoscopia de alta resolución y cromoendoscopia 45, aunque en la práctica clínica los resultados pueden ser contradictorios 46,47. A través de este estudio se recomienda, en pacientes con enfermedad inflamatoria crónica intestinal en seguimiento para cribado de displasia y cáncer colorrectal, llevar a cabo el programa con cromoendoscopia y biopsias dirigidas o bien mediante la pauta clásica de toma de biopsias en cuatro cuadrantes cada diez centímetros.
D.04. Registro de preparación del colon
Para poder establecer el intervalo de seguimiento adecuado o, simplemente, para saber si la colonoscopia era de calidad, se hace necesario disponer de dicho dato en el informe. La calidad de limpieza colónica ha de quedar registrada en el informe mediante una escala validada y por segmentos 22,23,36,48. Sin embargo, con frecuencia, existe una importante variabilidad por la que este y otros aspectos importantes de la colonoscopia no aparecen en los informes 39.
D.05. Registro de tiempo de retirada
Con la finalidad de proporcionar a la persona que recibe el informe de la colonoscopia un dato que permita evaluar la calidad de la misma, se propone incluir este indicador. Sin embargo, como se comentó previamente, lo importante es el promedio de retirada por endoscopista en las colonoscopias. No obstante, es probable que la inclusión de este indicador inste a los endoscopistas a mantener un promedio de retirada alto 36.
E.01. Incidencia de efectos adversos
En la línea de mejora de los propios endoscopistas, los servicios de endoscopias digestivas han ido introduciendo en su gestión la medición de eventos adversos (EA). Aunque habitualmente se cree que los EA graves son poco frecuentes o raros, cuando se realiza una colonoscopia se puede causar un número considerable de hospitalizaciones inesperadas, costos considerables de atención médica y muertes en una población sana. La endoscopia digestiva baja, incluida la colonoscopia, se ha utilizado cada vez más, sobre todo como una herramienta de cribado del CRC en Europa y Estados Unidos en los últimos años, apoyada por un creciente número de evidencias de la efectividad en la reducción de la incidencia y la mortalidad. Por lo tanto, el conocimiento de los resultados adversos causados por la colonoscopia en la práctica rutinaria es crucial para quienes toman las decisiones en política sanitaria 49,50.
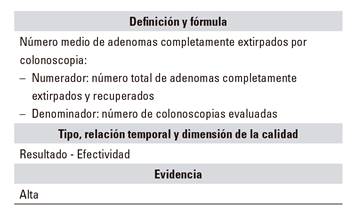
E.04. Media de adenomas por colonoscopia
Estos dos indicadores son complementarios entre sí. Aunque se han utilizado términos como índice de detección de adenomas o tasa de detección de adenomas, estas denominaciones son confusas y sería preferible referirnos a estos indicadores como porcentaje de colonoscopias con al menos un adenoma extirpado y número de adenomas extirpados por colonoscopia. La idea es utilizar un lenguaje natural que sea comprensible por todos los implicados en el proceso de la colonoscopia: desde el público general hasta los gestores, así como cualquier persona involucrada, independientemente de su nivel de formación.
Tradicionalmente se ha utilizado el porcentaje de colonoscopias con al menos un adenoma como el indicador fundamental. Este ha sido el más estudiado y el mejor relacionado con la prevención del cáncer colorrectal y cáncer de intervalo, tanto para colonoscopias de cribado como de no cribado 34,49,50. Incluimos aquí el indicador de media de adenomas extirpados por colonoscopia como un indicador más de calidad técnica del endoscopista 51,52. Actualmente no disponemos de estándares adecuados para la población general. Mientras aparecen nuevos datos, proponemos un estándar del 20% para el porcentaje de colonoscopias con al menos un adenoma para el conjunto de todas las colonoscopias índice, independientemente de edad e indicación.
Otros indicadores posibles serían: porcentaje de colonoscopias con adenoma avanzado, número medio de adenomas avanzados por colonoscopia, número de adenomas en pacientes con adenoma o número de adenomas menos el primer adenoma. Aunque permiten diferenciar entre la calidad de los endoscopistas, requieren un número muy alto de pacientes.
E.05. Incidencia de cáncer de intervalo poscolonoscopia
Este indicador es, potencialmente, el mejor indicador de resultado de la colonoscopia, especialmente en los programas de cribado de cáncer colorrectal 5,7. Es verdad que se sale de nuestros objetivos al analizar los indicadores para las colonoscopias en general, pero de forma teórica es el indicador más impactante pues uno de los objetivos fundamentales de llevar a cabo una colonoscopia es la prevención a largo plazo del desarrollo de cáncer colorrectal. Una inspección adecuada de la mucosa, acompañada de resección de las lesiones detectadas, evita la aparición de cáncer colorrectal. Sin embargo, se sabe que existe un importante número de lesiones no detectadas. Además, algunas lesiones, incluso planas o de pequeño tamaño, pueden ser muy agresivas, lo que da lugar a una prevalencia variable de cáncer colorrectal poscolonoscopia, entre los tres y cinco años de su realización, de entre el 0% y el 9% 37,38,49. Un tiempo de retirada alto, una mejor limpieza colónica, un intervalo de seguimiento adecuado en pacientes con adenoma y una mayor extirpación de adenomas previenen la aparición de cáncer colorrectal 39,40,48,50,51,52. Este indicador se enfrenta a problemas potenciales como la pérdida de seguimiento de los pacientes, el largo intervalo entre la última colonoscopia y la ocurrencia del evento o la baja incidencia de cáncer poscolonoscopia. El método de cálculo para cada unidad de endoscopia aún no está bien establecido, aunque idealmente debería incluir todas las colonoscopias realizadas, incluso las normales. Sin embargo, esta investigación recomienda que forme parte del programa de seguimiento de pacientes con adenomas o pólipos serrados de colon para facilitar la monitorización del indicador 41,42,43,44,45,46.
CONCLUSIONES
En este artículo se plantea la aplicación de una serie de indicadores para incluir en los programas de mejora de calidad en colonoscopia, junto a los indicadores generales propuestos en el primer artículo. El número total de indicadores resultantes para evaluar una única colonoscopia puede llegar hasta 30. Incluso si se cuenta con un sistema informatizado de datos, el manejo de estos, resultantes de una monitorización continúa de la calidad y basado en todos estos indicadores, puede dar lugar a un trabajo que puede ser difícil de acometer. Por ello, es importante centrar la evaluación en indicadores clave. Diferentes sociedades científicas coinciden en la importancia de medir de forma rutinaria indicadores relevantes en el desempeño de las unidades de endoscopia, que permitan ciclos de mejora continuos de acuerdo a sus resultados. Sin embargo, si una unidad de endoscopia desarrolla su trabajo por encima del estándar durante la monitorización continua de un determinado indicador, y mantiene esta capacidad a largo plazo, estaremos llevando a cabo una actividad de monitorización innecesaria, que no detecta oportunidades de mejora. Por este motivo, es mejor ser flexibles en cada unidad e ir adaptando las tareas de monitorización de indicadores a las necesidades de mejora de cada unidad. En otras tareas de calidad, como a la hora implantar un ciclo de mejora o rediseñar la actividad asistencial, es mejor evaluar la calidad con el mayor número posible de indicadores.











 texto en
texto en