Introducción
La detección precoz de complicaciones en la fístula arteriovenosa (FAV) es uno de los retos a los que se enfrentan las enfermeras en hemodiálisis (HD). En este sentido, se están desarrollando programas estruc turados de seguimiento y monitorización del acceso vascular (AV) del paciente, bajo el amparo de las reco mendaciones de las principales guías clínicas1,2con el objetivo de mantener una buena calidad dialítica.
La efectividad de estos programas debe encaminarse a la vigilancia periódica del AV, reducción en las tasas de trombosis y disminución en la utilización de catéteres venosos centrales derivados de una complicación en la FAV3,4.
Estos programas de seguimiento proponen la utiliza ción de la Ecografía Doppler (ED), así como de los mé todos dilucionales de screening para la determinación indirecta del flujo sanguíneo (QA) de la FAV. La ED se ha convertido en el nuevo gold standar para el diagnós tico de la estenosis en la FAV desplazando el uso de la fistulografía, debido a sus altos costes. Además, la ED permite la determinación directa del QA5. De esta forma, solo estaría recomendada la utilización de fistu lografía, en casos en la que la ED no sea concluyente y exista sospecha de una gran estenosis en la íntima del vaso sanguíneo.1 Sin embargo, la fácil aplicación y pre cisión de los métodos dilucionales, así como, la escasa variabilidad interobservador, hacen que sean las técni cas más utilizadas para la medición del QA4.
La primera determinación indirecta del QA a través del principio de dilución fue descrita en 1995 por Krivitski6, siendo el punto de partida del desarrollo de varias técnicas que permiten su cálculo durante la sesión de hemodiálisis. Hoy en día, dos de los méto dos más extendidos y con rendimiento equivalente son la ultrasonografía dilucional (UD) y la termodilución (TD)7,8,9,10,11. En ambos, el QA se calcula de manera indirecta través de la cuantificación de la recirculación existente con y sin inversión de las líneas sanguíneas de hemodiálisis.
Uno de los requerimientos de ambos métodos dilucionales es la punción retrograda de la aguja arterial, es decir, en dirección proximal a la anastomosis en contra del flujo sanguíneo. Las condiciones de mezcla entre el flujo sanguíneo de la FAV con el indicador utilizado (temperatura en TD o suero salino en UD) es el principal argumento de este requisito. En TD, si no se cumple esta premisa, en la descripción del método se refiere la posibilidad de generar un canal de flujo directo entre la cánula arterial y venosa resultando los valores de medida de recirculación incorrectos por falta de mezcla10,11,12. Igualmente en la validación de la medida por UD, se describe la existencia de una mayor turbulencia al estar las líneas invertidas que hace que la mezcla de sangre y bolo salino sea más adecuada6. Sin embargo, estas recomendaciones chocan con los recientes estudios que relacionan una menor supervivencia del AV con la punción retrograda de la aguja13, de manera que las últimas recomendaciones de las guías del AV es la punción de ambas agujas a favor de flujo(1). Son varios los autores que han validado los métodos estudiando la relación entre dos14,15,16o entre los tres17, pero no se especifica la colocación de la aguja arterial en el momento de la medición. Si bien, para UD algún autor ha referido que el sentido de la aguja arterial es un factor condicionante en la medición del flujo del acceso18, no conocemos referentes que midan la concordancia de resultado de medida según la punción de la aguja arterial en TD y, en ninguno de los casos, se ha analizado el impacto clínico de la metodología de punción en la medición del QA.
Por lo tanto, el objetivo principal de este estudio fue cuantificar el error de medición generado por la punción a favor de flujo en la aplicación práctica de los métodos dilucionales y analizar su repercusión clínica en contraste con ED. Los objetivos secundarios fueron evaluar el impacto del método de punción sobre las presiones dinámicas del AV, las incidencias en la manipulación del mismo y la adecuación de la diálisis durante la sesión en la que se realizan las medidas.
Material y Método
Estudio observacional trasversal, realizado en tres centros periféricos de hemodiálisis de Castilla y León pertenecientes a la FRIAT. Se seleccionó como población de estudio a los pacientes portadores de FAV en programa de hemodiálisis periódica que dieron su consentimiento (n=37). Se definió como criterio de inclusión un período de maduración de la FAV superior a un mes. Se excluyeron las FAV en las que la aguja venosa de retorno sanguíneo se puncionaba en una vena distinta a la arterializada ya que imposibilita la medición del QA con métodos dilucionales.
Como variable primaria, se midió el QA vascular mediante dos métodos dilucionales (termodilución y ultrasonografía dilucional) y ecografía Doppler en ambas técnicas de punción. Como variables secundarias se recopilaron; recirculación y presiones dinámicas con líneas de hemodiálisis en posición normal e invertida para TD, complicaciones con la punción, tiempo necesario para realizar la medición y KT de la sesión medido mediante dialisancia iónica. Todas ellas fueron recogidas utilizando la punción de la aguja arterial a contraflujo y a favor de flujo. Como datos complementarios, se recogieron las variables demográficas (edad y sexo), otras variables relacionadas con la FAV (tipo acceso vascular y tiempo del mismo).
Los parámetros de estudio se recogieron en la historia clínica informática mediante el programa Nefrosoft® V.6.5.6.
Medidas del flujo vascular
Todas las determinaciones con métodos dilucionales se realizaron en los primeros 90 minutos de tratamiento para evitar influencias en la medida del QA producidas por los cambios de volemia4. El flujo de bomba fue 250 ml/min, valor dentro de los rangos recomendados en ambos métodos (200 a 350 ml/min)12,19y que nos garantizaba la obtención de flujo necesario para realizar la medida en posición invertida. En TD, el ratio de ultafiltración durante la medición fue constante, al igual que en la UD, donde además se suspendieron las infusiones que pudieran alterar la dilución a medir19. En la medida de lo posible, se mantuvieron las mismas condiciones térmicas ambientales. Las medidas fueron tomadas por el mismo personal en cada centro y las punciones se realizaron por trabajadores experimentados.
Ultrasonografía dilucional: Para el cálculo de QA por UD, se precisó de un monitor externo, Nephoflow®, colocando un sensor Doppler en cada línea de diálisis y administrando un bolo de 10 mililitros suero fisiológico isotónico (indicador) durante 3-5 segundos en la cámara venosa, con las líneas en posición normal e invertida. El QA se calcula automáticamente través del software incorporado al monitor externo mediante la siguiente fórmula:
QA = Qb x (Sv/Sa - 1) = Qb x (1/R-1)
Donde Qb es el flujo efectivo de sangre, Sv/Sa es la ratio entre las áreas registradas por los 2 sensores Doppler en las líneas venosa y arterial, respectivamente, después de la inyección del bolo del indicador y R es la recirculación existente con las líneas sanguíneas invertidas.
Termodilución: Para obtención las medidas de TD se utilizó el módulo de temperatura sanguínea BTM® (Blood Temperature Monitor) incorporado en los monitores de hemodiálisis 4008 y 5008 de Fresenius Medical Care.
Ecografía doppler: Para la obtención de datos mediante ecografía doppler se utilizó un ecógrafo marca Mindray modelo Z6 con sonda lineal L14-6P. Las medidas se realizaron, para fístulas nativas, en la zona medio-braquial a nivel de la arterial humeral, salvo un paciente que se evidencia la ausencia de arterial humeral y se realiza el sumatorio de la arterial radial y ulnar a ese nivel. Para fístulas protésicas la medición se realiza en la zona previa a la punción arterial.
Se realizaron tres mediciones consecutivas (calculándose la media) en modo longitudinal, con una angulación = 60º y con un volumen de muestra de 2/3 del vaso. Se realizaron los ajustes de PRF, línea de base y ganancia necesarios para optimizar la imagen. La media de las velocidades medias se obtuvo indicando al ecógrafo la curva de al menos dos complejos cardiacos. El diámetro se midió en la zona volumen de muestra evitando sobreestimar el mismo. El cálculo del QA vascular se basó en la siguiente fórmula:
Qa = TAMEAN (cm/s) x p(d2/4) (cm2) x 60 (s)
Donde QA es el flujo de sangre (ml/min), TAMEAN es la media de las velocidades medias medidas por el doppler pulsado (cm/s); esta medida se calcula automáticamente por el equipo indicándole el inicio y final del complejo o ciclo cardiaco; d es el diámetro del vaso en modo longitudinal; la formula presupone forma circular del vaso para calcular el área del mismo (cm2).
Análisis estadístico
El abordaje estadístico se llevó a cabo con el programa IBM SPSS Statistics v20. Las variables se presentaron con su media y desviación estándar o cifras absolutas y porcentajes. La comparación de variables se realizó como datos pareados de cada paciente. Se concretó el análisis de significación estadística para p = 0,05 utilizando la prueba t-Student o Wilcoxon tras determinar la normalidad con la prueba de Kolmogorov-Smirnov. Atendiendo a este criterio de normalidad, se utilizó el test paramétrico de Pearson o el no paramétrico de Rho de Spearman para el análisis correlacional. Para el estudio de la concordancia se ha utilizado el coeficiente de correlación intraclase (ICC)20, el método Bland-Altman21y el índice de Kappa de Cohen (K)22.
Resultados
Se analizaron a 37 pacientes, la edad media de los pacientes fue 72,88± 14,53 años. Respecto a las características de la FAV, 35 fueron FAV nativas (95%) y dos protésicas (5%). De las cuales, 18 correspondían a FAV radio-cefálicas (49%), seis humero-basílicas (16%), ocho humero-cefálicas (22%), dos humero-axilar (5%) y tres humero-medianacubital (8%).
La media de tiempo de permanencia del acceso vascular fue de 35,73± 31,04 meses. En el 100% de las fístulas (37) se pudo medir el QA con TD (utilizando los dos modos de punción) y con ED. En cuanto a la UD, el 13% (5 de 37) de las FAV mostraron una lectura errónea por causa desconocidas en alguno de los modos de punción por lo que fueron excluidas del análisis con este método.
La media de QA con aguja arterial a contraflujo y a favor de flujo fue 724,86+335,45 ml/min y 789,02+378,11 ml/min con TD (p=0,131) y 769,68+390,96 ml/min y 781,87+369,68 ml/min con UD (p=0,809), respectivamente.
En los dispersogramas que se muestran en la Figura 1, se observa la correlación existente entre los valores de QA medidos con la técnica retrograda y anterógrada en la punción arterial. Sin embargo, la presencia de esta alta correlación y la no significancia mostrada en el análisis de comparación de medias, no garantiza la concordancia de los resultados obtenidos. Más informativo es la estimación del sesgo generado por la punción anterógrada (diferencial medido entre el QA con aguja arterial en punción anterógrada y retrograda). Para la TD, el sesgo fue 64,16±279,83ml/min y 12,18±283,02ml/min para la UD.
En la Figura 2, se muestra el procedimiento de Bland-Altman a través del cual se representa el comportamiento del sesgo de la punción arterial a favor de flujo frente al valor de QA obtenido utilizando el modo de punción de referencia (punción a contraflujo), estableciendo unos límites de acuerdo al 95%. La amplitud de los límites de acuerdo observados va a tener un mayor impacto para las medidas de flujo menores de 500ml/min, resultando más útil, expresar el sesgo de la punción arterial a favor de flujo como porcentaje. Para el uso de la TD el sesgo fue 11,04±30,88% (de -49,48% a 71,56%) y 11,23±40,27% (de -79,45% a 101,91%) para la UD.
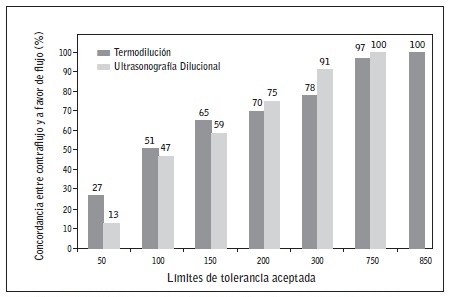
El ICC fue 0,831 (95% IC: 0,698-0,909) para la TD y 0,724 (95% IC: 0,509-0,854) para UD. La Figura 3, nos permite observar el grado de acuerdo en función de la tolerancia de las diferencias que se pretendan aceptar, para ello, se representó en el eje horizontal la diferencia absoluta entre las dos mediciones para cada sujeto y en el eje vertical la proporción de casos en los que las discrepancias igualan al menos cada una de las diferencias observadas.
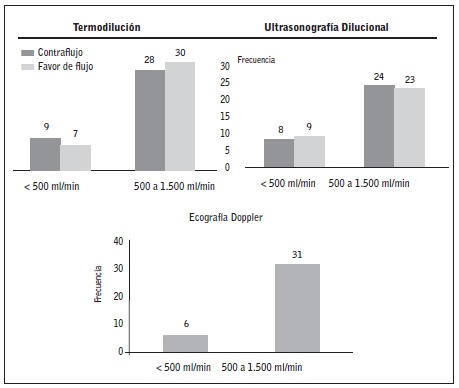
En la Tabla 1 se muestra el análisis cuantitativo de QA, correlación y concordancia de los dos métodos dilucionales analizados con respecto a la ED. En cuanto al análisis cualitativo de concordancia, en la Figura 4, se muestra la clasificación de las FAV según los valores obtenidos de QA en función de los puntos de ml/min, para TD fue del 91% (K=0,841) y 82% para UD (K=0,760). Utilizando la ED como referencia, el grado de acuerdo fue del 86% (K=0,586) con respecto a la utilización de la TD con punción a contraflujo, del 92% (K=0,720) con la TD a favor de flujo, del 78% (K=0,349) en relación a la UD con punción a contraflujo y del 81% (k=0,400) a favor de flujo.
Se valoró el impacto sobre el AV del modo de punción utilizado en las mediciones. De las 296 punciones de FAV realizadas para el análisis, 148 para la rama arterial (74 a favor de flujo y 74 a contraflujo) y 148 para la línea venosa, no se reflejaron complicaciones puncionando la aguja arterial a favor de flujo. Sin embargo, con la utilización del modo de punción a contraflujo, en un 11% (8 de 74) de las canalizaciones se registraron incidencias con la manipulación de AV.
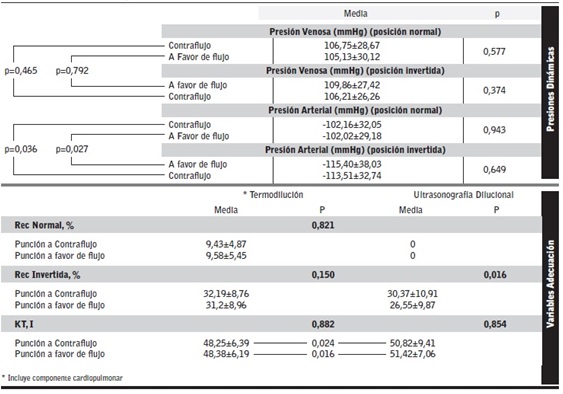
La media de tiempo empleado para el procedimiento de cuantificación del QA con TD fue de 66,25±8,49 minutos utilizando la punción a contraflujo y de 65,76±7,96 minutos con la punción a favor de flujo (p=0,596). Respecto al uso de la UD, el tiempo empleado fue de 9,18±1,11 minutos utilizando la punción a contraflujo y de 9,12±1,3 minutos con la punción a favor de flujo (p=0,730). Dado la clara diferencia de tiempo intermétodo (p<0,05), se procedió a la monitorización de las presiones dinámicas del AV durante el uso de la TD (Tabla 2), encontrándose únicamente diferencia significativa en la variable Presión Arterial en posición normal frente a posición invertida en ambos modos de punción.
Por último, en la Tabla 2 también se muestran los datos de recirculación y KT medido a través de dialisancia iónica en las sesiones en las que se efectuaron las cuantificaciones de QA. Se evidenciaron diferencias significativas en la UD entre punción a favor y a contraflujo en los valores de recirculación invertida, así como, en los valores de KT intermétodo.
Discusión
Uno de los factores clave para el mantenimiento de la supervivencia de la FAV son las prácticas relativas a la canulación23. Sobre este aspecto se han desarrollado multitud de estudios y controversias24, siendo la orientación de la punción arterial, uno de los temas más tratados. Recientemente, a raíz de los resultados expuestos por Parisotto et al. donde evidenció el impacto negativo que tiene la dirección a contraflujo de la aguja arterial en la supervivencia del AV13. En muchas de las unidades la opción anterógrada, se ha convertido en la estrategia de punción de referencia. Sin embargo, la punción retrograda es un factor condicionante en la medición del QA con métodos dilucionales, poniendo en jaque a los protocolos para su monitorización, ya que su diseño orientado a satisfacer las mejores condiciones para su aplicación, choca con las nuevas recomendaciones sobre la punción. Esta circunstancia ha generado la necesidad de conocimiento sobre el sesgo que genera la punción anterógrada, su comportamiento y su repercusión clínica, con el fin de adaptar los programas de seguimiento y monitorización del AV a la realidad de las unidades de hemodiálisis para garantizar su éxito.
En nuestro estudio, el sesgo generado por la punción anterógrada nos invita a afirmar que ambas estrategias de punción no son equivalentes para la medición del QA utilizando la TD y la UD. Las cuantificaciones realizadas con la punción anterógradas generaron medidas que sobrestimaban a las realizadas con la estrategia de punción de referencia en un 65% de los casos en TD y en un 59% en la UD. Sin embargo, según se muestra en la representación gráfica de Bland-Altman para ambos métodos de medición, existe una mayor concordancia de resultados para valores de QA inferiores a 700 ml/min, que empeora a medida que la magnitud de flujo aumenta. Dicho fenómeno fue descrito previamente por Merino et al25 y la causa suponemos que se deba a las condiciones de mezcla del indicador utilizado. En este aspecto, Krivitski describe que las peores condiciones de mezcla posible se relacionan con el perfil de flujo laminar y que tanto la velocidad de bomba, como la magnitud del flujo de la FAV, el diámetro del acceso vascular y la posición de las agujas son fundamentales para crear unas condiciones ideales de mezcla6. Creemos que las turbulencias generadas a flujos bajos consiguen compensar el perfil de flujo laminar que no es capaz de quebrar la punción anterógrada. En esta, los valores de recirculación invertida, parámetro fundamental para el cálculo matemático del QA, tienden a ser más bajos ya que parte del indicador se escapa por la falta de turbulencia sin producirse la mezcla. Esto provoca que la punción anterógrada pueda sobrestimar en flujos bajos. Sin embargo, a flujos mayores de 800 ml/min el contexto de flujo laminar se intensifica siendo las condiciones de mezcla impredecibles, por lo que la posición de las agujas, distancia y orientación, como los otros factores descritos previamente, serán los principales protagonistas de la mezcla.
Por otra parte, en los distintos estudios que comparan los diversos métodos de medición y que son la base bibliográfica de las principales Guías Clínicas para recomendar su uso indiferenciado, se describen diferencias entre métodos dilucionales de hasta 300 ml/min7,8 y hasta 600 ml/ml14entre métodos de cálculo directo e indirecto del QA. Tomando estas referencias como niveles de tolerancia aceptables y comparándolo con los datos expuestos en nuestro estudio, observamos que las discrepancias no son desmesuradas. Así, el grado de acuerdo entre estrategias de punción es del 78% para TD y 81% en UD para tolerancias de 300 ml/min y mayor del 95% en ambos métodos para tolerancias de 600 ml/min.
Sin embargo, ¿Cuánto es razonable que difieran las estrategias de punción para dar validez a los resultados? La estadística por sí sola no puede responder a esta pregunta, puesto que la decisión sobre lo que es un acuerdo aceptable es exclusivamente clínica. Por tanto, resulta interesante conocer si el sesgo generado por la punción anterógrada tiene impacto en la identificación de las FAV susceptibles de intervención. El valor umbral de QA considerado para indicar una prueba de imagen varía según las curvas ROC de sensibilidad-especificidad obtenida en diversos estudios.26,27Sin embargo, el criterio más extendido, considera un flujo menor a 500 ml/min, indicativo de valoración1,2. Atendiendo a esto, observamos que el 100% y el 88% de las FAV medidas con punción anterógrada utilizando TD y UD respectivamente y que fueron identificadas con flujo menor de 500 ml/min, también lo fueron con la medición en la punción retrograda. Del mismo modo, de las fístulas que fueron etiquetadas con flujos mayores a 500 ml/min utilizando la punción anterógrada, el 93% también lo ha sido con la punción de referencia, tanto utilizando la TD como en UD. Atendiendo a esto, consideramos que la buena concordancia entre estrategias de punción descrita en estos flujos, nos permite asumir el sesgo generado ya que no influirá en las decisiones sobre la intervención.
Caso contrario sospechamos que ocurra con las FAV con flujo mayor de 2000 ml/min. A pesar de que nuestro estudio no identifica a ninguna FAV en ese estrato de flujo, la variabilidad del sesgo observada a esas magnitudes, nos hace pensar que la estrategia de punción anterógrada es inadecuada para el screening del síndrome de hiperflujo. Sin embargo, creemos que la precisión a estos volúmenes de flujo no es tan significativa, ya que no toda insuficiencia cardíaca en un paciente de diálisis es causada por un marcado desarrollo fistular, y es más, un abordaje inadecuado a causa de un diagnóstico diferencial deficiente, puede agravar el problema de base, así como privar al paciente de un acceso vascular de forma injustificada28. Esto nos lleva a considerar que la utilización de la medición del QA por sí sola no es suficiente para el diagnóstico diferencial del síndrome de hiperflujo.
Si comparamos los resultados de los métodos dilucionales con los obtenidos con el uso de la ED observamos que la concordancia clínica empeora. Esta situación no es de extrañar, pues, a pesar de que existen multitud de estudios que demuestran la equivalencia para la cuantificación del QA entre ED y los métodos dilucionales14,16, también otros muchos no han encontrado tasas de correlación adecuadas entre ellos5,29. La causa fundamental es la gran variabilidad inter e intraobservador que tiene este instrumento de medición provocando que cualquier mínima variación en la medida, por ejemplo en la sección del vaso, genere grandes cambios en el cálculo de QA. Aun así, en TD, el grado de acuerdo clínico en la clasificación de las fístulas utilizando la punción anterógrada es bueno.
Por otra parte, la no valoración del comportamiento del sesgo en el análisis prospectivo del QA, es una limitación de este estudio. Las principales Guías Clínicas reflejan que una disminución temporal del QA mayor del 20-25% es una potente variable predictiva de trombosis30. Sin embargo, la baja sensibilidad de estos métodos31,32 nos lleva a pensar que la punción retrograda no ha de ser referente para contrastar el impacto clínico del sesgo generado por la punción anterógrada en la valoración prospectiva del QA. Así que, a falta de estudios que aborden este tema, consideramos que en la valoración prospectiva del QA, las mediciones han de ser realizadas con el mismo método y con la misma estrategia de punción con el fin de que cada paciente sea referente de sí mismo.
Otro aspecto importante a la hora de decidir la utilización de una u otra estrategia de punción para la medición del QA, es el impacto que esta tenga sobre el propio AV, así como, en la eficacia de la sesión objeto de medición. Atendiendo a esto, en nuestro estudio, solo se detectaron incidencias con las canalizaciones retrogradas. Hay que tener en cuenta que en las unidades en las que se han recogido los datos, siguiendo las últimas recomendaciones del cuidado del acceso vascular, hacía tiempo que se estaba puncionando de manera anterógrada. Esto hace que la FAV esté desarrollada para ese tipo de técnica y los propios profesionales, hayan adquirido habilidades para el desarrollo de la misma. Por tanto, la punción en zonas nuevas y el cambio de posición en cuanto a la destreza de los profesionales, puede haber sido la causa de las incidencias en la punción retrograda. Esto nos lleva a pensar si es conveniente, en las unidades en las que está protocolizada la punción anterógrada, asumir el riesgo de la canulación retrograda para medir el QA o el sesgo generado por la punción a favor de flujo.
Por otra parte, tenemos que tener en cuenta que los métodos dilucionales requieren una inversión de líneas de hemodiálisis. Una de las preocupaciones de los profesionales al aplicar los mismos, es si la FAV puede verse afectada por los cambios de presiones dinámicas con los que se trabaja en posición invertida durante la medición. Debido a que el tiempo de inversión de líneas en UD es muy corto, no consideramos necesario la monitorización de los registros de presiones dinámicas. Lo contrario ocurre con la utilización de la TD donde el tiempo de inversión está alrededor de los 25 minutos, generando así, la necesidad de monitorización de este parámetro. En nuestro estudio, sólo hemos detectado variaciones significativas en la presión arterial entre las medidas realizadas en posición normal e invertida en ambas técnicas de punción. Esto se explica porque en la posición invertida de las líneas de hemodiálisis, la sangre se extrae de la zona distal a la anastomosis y la distancia a la misma hace que el flujo sea menor a pesar de la recirculación forzada. Sin embargo, aun con las diferencias detectadas entre modos de punción, los valores no exceden los límites descritos en los que la succión forzada del flujo del acceso puede dañar la capa intima del vaso33.
Respecto al análisis de la eficacia de la sesión de diálisis objeto de medición, las variables tiempo del procedimiento y KT, son fundamentales. No hemos evidenciado diferencias significativas entre ambos modos de punción, sin embargo, sí entre métodos de medición. La medida utilizando la TD tiene la ventaja de que se realiza mediante un biosensor integrado en el monitor de diálisis, lo que hace que resulte más cómodo para los profesionales de enfermería ya que no requiere de un aparataje externo como ocurre con la UD. Por otro lado, la medida de QA por UD es significativamente más rápida que la realizada con TD, con lo que el impacto sobre el KT será menor, de modo que cada método ofrece una serie de ventajas sobre el anterior.
Conclusiones
La estrategia de punción basada en la orientación de la aguja arterial a favor y en contra flujo no son intercambiables a la hora de la cuantificación del QA con TD y UD. En ambos métodos de medición, el comportamiento del sesgo generado por la punción a favor de flujo es similar, siendo más considerable e imprevisible a altas magnitudes de flujo.
Sin embargo, en contraste con Eco-doppler ambos métodos y modos de punción son fiables para el descarte de FAV susceptibles de valoración, ya que el sesgo a flujos bajos es mínimo, asumible desde un punto de vista clínico, con el fin de descartar la presencia de estenosis con flujos menores de 500 ml/m.
En flujos altos las condiciones de la mezcla son imprevisibles y el sesgo aumenta, por lo que en estas magnitudes de flujo, el valor de QA por sí solo, no nos afectará a las decisiones sobre la intervención.
Las posibles complicaciones en la manipulación del acceso a la hora de cambiar la forma de punción para la medición del QA, convierten al modo de punción arterial a favor de flujo en la opción ideal en las unidades donde esta protocolizada esta estrategia de punción.
La elección de uno u otro método de medición ha de responder a las necesidades de cada unidad. El método TD es más cómodo que el UD al no depender de un dispositivo externo. Sin embargo, el tiempo empleado durante la medición es mayor afectando negativamente a la dosis de diálisis durante la sesión.