INTRODUCCIÓN
La incidencia de aneurismas de arteria carótida interna extracraneal no se conoce a ciencia cierta, se estima que está alrededor del 0,1-2 % (1), puede ser espontáneo u ocurrir accidentalmente después de una lesión penetrante o iatrogénica. Los pacientes permanecen asintomáticos hasta que aparecen complicaciones como: eventos cerebrovasculares (ECV) definitivos o transitorios (AIT) (43,9 %) (2), como retinopatía isquémica, hemorragia con síntomas de compresión en cuello, afectación de pares craneales o incluso ser una emergencia potencialmente mortal. La localización más frecuente es a nivel del bulbo carotídeo y en la carótida interna proximal. La forma, crecimiento y ubicación dependen de factores independientes y el tratarlos de una manera oportuna es una actitud acertada (1,3). Se han descrito procedimientos de reconstrucción extraanatómica de la arteria carótida que han sido difíciles de realizar por la dificultad en la exposición y el riesgo de ECV. El avance de los procedimientos endovasculares ha obtenido resultados satisfactorios a corto plazo (3). Los stents de celdas abiertas (Acculink®, Precise® y Protégé™) se reservan para anatomías tortuosas, mientras que los stents de celdas cerradas (Xact®, Cristallo®, Adapt™, Wallstent™) y los micromallados (GORE®, Casper™, CGuard™, Roadsaver®) se han presentado como opción dentro de terapia endovascular para aneurismas de carótida por una mejor capacidad de andamiaje y en especial los últimos como efecto diversor de flujo, aunque hay pocos informes sobre pacientes con lesiones aneurismáticas espontáneas tratados por este método.
CASO CLÍNICO
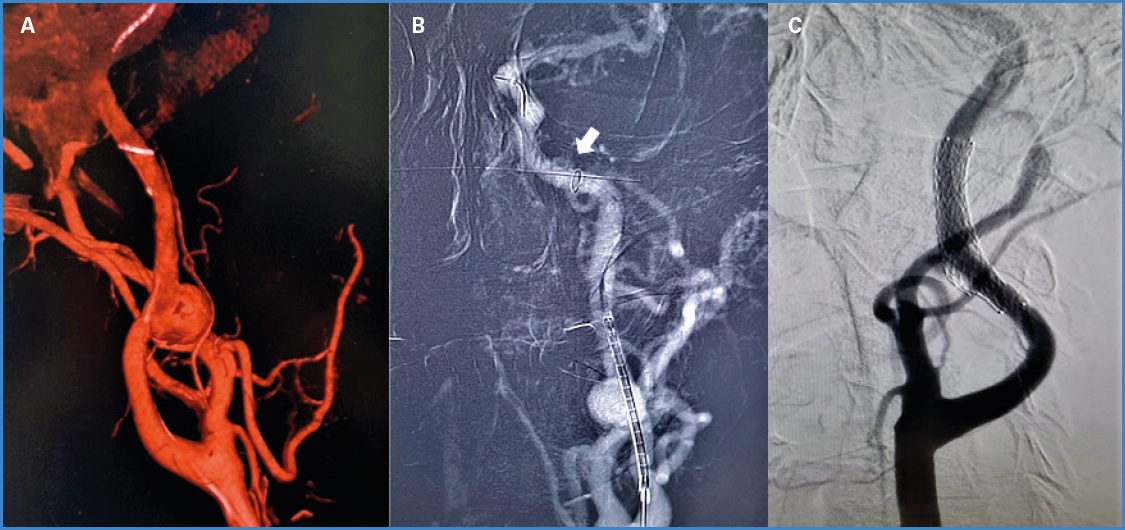
Paciente de 61 años con antecedente de hipertensión arterial en tratamiento y eventos cerebrovasculares transitorios en seis ocasiones, SARS-CoV-2 PCR positivo en julio de 2020, padre y hermanos presentaron eventos cardiacos y cerebrovasculares isquémicos, su último episodio de ECV se presentó en octubre del año 2020. Acude a consulta externa refiriendo clínica de desorientación en tiempo y espacio acompañado de amnesia transitoria, la exploración evidencia masa pulsátil a nivel carotídeo no móvil depresible, trill a la palpación y soplo sistodiastólico a la auscultación, la tomografía craneocervical muestra dilatación aneurismática de arteria carótida interna izquierda (ACII) en su porción C1, con infartos lacunares en parénquima cerebral, manejado inicialmente con ácido acetilsalicílico 81 mg (ASA) como parte de prevención secundaria. Se realizó angiografía digital de vasos del cuello lo que confirmó la presencia de un aneurisma de 14,33 × 10,79 mm con un cuello de 11,67 mm en pared posterior de la ACII segmento C1, localizado aproximadamente a 4 cm de la bifurcación carotídea, siendo los diámetros de la arteria carótida interna proximal y distal 0,78 y 0,74, respectivamente. Se realizó tratamiento endovascular por acceso femoral derecho y colocación de stent micromallado (CGuard™) de 8 × 40 mm utilizando sistema de protección FilterWire EZ™ 3,5 × 5,5 mm × 190 cm en el segmento C2 para mayor seguridad (Figs. 1A y 1B). La evolución posoperatoria fue favorable, no se presentaron complicaciones posteriores y el paciente fue dado de alta administrando antiagregación doble con clopidogrel y ácido acetilsalicílico (DAPT).
DISCUSIÓN
Los aneurismas de carótida son una patología rara y representa solo el 0,4 a 4 % de todos los aneurismas de las arterias periféricas (2). La clínica es variada e importante, y se puede presentar como ECV, masa cervical pulsátil, dolor o como un hallazgo incidental en estudios de imagen. Su probable etiología está relacionada a la displasia fibromuscular, síndrome de Marfan, Ehlers-Danlos, osteogénesis imperfecta, pseudoxantoma elástico, enfermedad renal poliquística y la neurofibromatosis, y en algunos casos se atribuyeron causas idiopáticas influenciadas por la hipertensión arterial, dislipidemia o genética (4). Aunque el diagnóstico se puede realizar con ecografía o tomografía computarizada (sensibilidad del 97,7 % y una especificidad del 100 %), el estándar de oro para el diagnóstico sigue siendo la angiografía digital por sustracción (DSA) (sensibilidad superior al 99 % y especificidad del 100 %) (5).
Desde que Cooper documentó el primer procedimiento exitoso en 1805, el tratamiento según la literatura puede realizarse mediante cirugía abierta convencional o métodos endovasculares, utilizando stents, stents recubiertos o coils, pero tanto las intervenciones como la toma de decisiones sobre el manejo deben evaluarse de forma individual y de preferencia por un grupo multidisciplinario en la elección del mejor método terapéutico (6,7). La poca frecuencia en los reportes de aneurismas y pseudoanuerismas carotídeos espontáneos hace que su manejo sea todavía controversial; una de las series más detalladas y representativas fue publicada en el 2015 por el grupo de la Clínica Mayo y consta de 141 casos reportados en 15 años; hubieron 116 pseudoanuerismas (82 %) y 25 aneurismas verdaderos (18 %), el manejo se realizó mediante cirugía abierta, endovascular (stent cubierto, descubierto, sacrificio carótida o embolización) y clínico con antiagregante y anticoagulantes (4,5). Li y cols. en 2011 reportaron la colocación de stents endovasculares a un total de 224 pacientes en 113 estudios con aneurismas de arteria carótida extracraneal con un éxito del 92,8 % (2).
El sistema de stent protector embólico carotídeo CGuard™ es un dispositivo de nitinol delgado, cubierto de una malla de polietileno tereftalato MicroNet con un tamaño de poro de 150 a 180 micras, diseñado para prevenir eventos embólicos durante y después del tratamiento (8), y posee una alta flexibilidad y fuerza radial, así como adaptabilidad a la luz del vaso permitiendo el tratamiento de esta patología (9). La medición se realizó mediante reconstrucción 3D en angiografía con sobredimensión de 1 mm para un adecuado posicionamiento del stent y principalmente rectificar la arteria, corrigiendo el inflow hacia el aneurisma (Fig. 1C). Adicionalmente se usó el sistema de protección embólica FilterWire EZ™ para reducir el riesgo de ECV en un 38 %, RR 0,62 (IC del 95 % 0,54 a 0,72) (10) lo que permitió cubrir la solución de continuidad, prevenir la embolización de trombos formados por el flujo turbulento en el saco aneurismático y excluir satisfactoriamente el aneurisma carotídeo sin complicaciones. La antiagregación fue inicialmente manejada con ASA 81 mg cada día como parte de prevención secundaria de AIT; después se adicionó clopidogrel 75 mg una vez al día durante la semana del preoperatorio y se mantuvo durante el procedimiento. Se recomendó seguir esta terapia al menos 6 meses después del alta para posteriormente continuar solo con un antiagregante en terapia extendida por un año. El control clínico al mes fue satisfactorio y las reconstrucciones multiplanares en angio-TAC corroboraron el cierre aneurismático con permeabilidad en el injerto, circulación carotídea y cerebral (Fig. 2). La sintomatología clínica del paciente descrita inicialmente cedió y hasta el momento no ha presentado molestias o nuevo episodio AIT o ECV establecido.