INTRODUCCIÓN
El tratamiento endovascular (EVAR) del aneurisma de aorta abdominal (AAA) ha demostrado en numerosos ensayos clínicos aleatorizados que ofrece ventajas frente a la reparación abierta, como: menor tiempo de estancia hospitalaria, menor tasa de complicaciones cardiológicas y respiratorias y menor necesidad de transfusiones. Sin embargo, una de las principales complicaciones de la terapia endovascular es la presencia de endofugas intraoperatorias o en el seguimiento (1-3).
Se denomina endofuga a la presencia de flujo en el interior del saco aneurismático tras el EVAR (4). La más frecuente es la endofuga de tipo II (EFT2), que aparece en un 20-40 % de los casos, y que se debe al flujo retrógrado hacia el saco aneurismático por arterias lumbares (AL) o por la arteria mesentérica inferior (AMI). En algunos estudios concluyen que la EFT2 por AMI tiene peor pronóstico (4,5).
El crecimiento del saco aneurismático puede conllevar un aumento en el número de reintervenciones e incluso un aumento en su tasa de ruptura (4).
La embolización preventiva de la AMI se ha postulado como una opción válida para la prevención de EFT2 durante el seguimiento y la reducción del diámetro del saco aneurismático (6-8).
Nuestro objetivo es evaluar los resultados en nuestra serie de casos tratados con embolización de la AMI previa al implante de la endoprótesis, como método útil para disminuir las EFT2 durante el seguimiento.
MATERIAL Y MÉTODOS
Población
Se realizó un análisis retrospectivo de los pacientes tratados en nuestro centro con embolización de la AMI previa al EVAR entre los años 2019-2021. Los datos demográficos de los pacientes se muestran en la tabla I.
Los criterios utilizados para la embolización de la AMI fueron un diámetro > 3 mm con presencia de al menos dos AL con diámetro > 2 mm enfrentadas a la salida de AMI o la coexistencia de aneurismas aortoilíacos. Estos criterios están apoyados en el ensayo clínico aleatorizado recientemente publicado por Samura et al. (9).
En dos de los casos se llevó a cabo la embolización de la AMI en un primer tiempo y posteriormente el EVAR, mientras que en los otros cinco pacientes se realizó en el mismo procedimiento. Estos dos pacientes presentaban de manera concomitante aneurismas ilíacos bilaterales. En primer lugar, se realizó la embolización de la AMI y de una de las arterias hipogástricas y, en un segundo tiempo (2 semanas después), se completó el procedimiento endovascular mediante EVAR con extensión a la arteria ilíaca externa (AIE) en el eje con embolización de la hipogástrica previa + branch ilíaco en el eje ilíaco contralateral.
Procedimiento
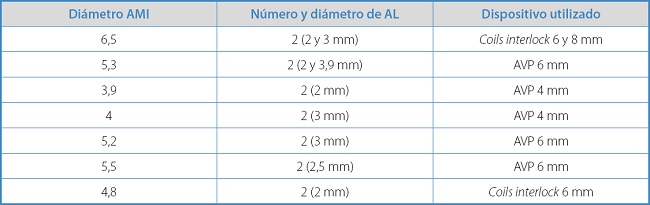
La embolización se realizó bajo anestesia regional y por acceso femoral ecoguiado. Se colocó un introductor 6F y guía de 0,035” apoyada en catéter 4F. Una vez cateterizado el ostium de la AMI, se realizó embolización con coils interlock de 6 y 8 mm (Boston Scientific, Marlborough, Massachusetts, EE. UU.) o dispositivos AVP II de 6 y de 4 mm (St. Jude Medical, St. Paul, Minnesota, EE. UU.) según se detallan en la tabla II.
El éxito técnico se definió como la oclusión del ostium de la AMI con permeabilidad de sus ramas distales en la arteriografía final.
Al finalizar el procedimiento, los pacientes pasan las primeras 12 horas en la sala de reanimación y, si no existen complicaciones, posteriormente van a la planta de hospitalización para completar el posoperatorio.
Objetivos
El objetivo principal fue evaluar el resultado de la embolización de la AMI en la prevención de EFT2. Los objetivos secundarios son la regresión del saco aneurismático y la tasa de reintervención debido a EFT2.
Imágenes preoperatorias
Se realizaron angio TC preoperatorios con cortes de 0,75 mm en todos los pacientes. Las mediciones de la aorta se realizaron con el software de imágenes médicas Philips IntelliSpace 9.0. Se incluyeron: diámetro de la AMI, diámetro máximo del saco aneurismático, diámetro y longitud del cuello proximal, diámetro y longitud de las arterias ilíacas comunes y número y diámetro de las arterias lumbares.
El diámetro aórtico medio previo al procedimiento endovascular fue de 58 mm (rango 40-90 mm). El 42 % presentaba aneurismas aortoilíacos. El diámetro medio de la AMI en el TC previo a la intervención fue 5,02 ± 0,9 mm. En cuanto al dispositivo de embolización, en cinco de los casos se utilizó un amplatzer vascular plug (AVP), mientras que en dos restantes se emplearon coils.
Todos los pacientes presentaban, al menos, dos AL enfrentadas al origen de la AMI con diámetro > 2 mm.
Imágenes de seguimiento
En cuanto al seguimiento, se realizaron angio TC de control al mes y a los 12 meses, mientras que a los 6 meses el control se realizó ecográficamente. En caso de ausencia de EFT2, la revisión anual se lleva a cabo con ecografía y radiografía de abdomen. Por patologías de otra índole, algunos de los pacientes tenían TC abdominales, que se utilizaron para toma de mediciones durante el seguimiento.
RESULTADOS
Entre 2019 y 2021 se llevó a cabo la embolización preventiva de AMI en 7 pacientes varones, a los que posteriormente se realizó EVAR. La edad de media fue 72,1 años.
El éxito técnico fue del 100 %, con una mediana de seguimiento de 20,7 meses (12,9-26,3 meses).
Se objetivó una mediana regresión del saco aneurismático de 5,08 mm (rango 2-14 mm), que fue significativamente mayor en aquellos pacientes que no presentaban aneurismas ilíacos asociados (p < 0,01).
La mediana de estancia hospitalaria para aquellos pacientes a los que se realizó la embolización y el EVAR en el mismo acto quirúrgico fue de 36 horas (34-37 horas). Sin embargo, en aquellos pacientes a los que se les realizó embolización sin inmediato EVAR, el ingreso fue de 24 horas (22-28 horas).
En los angio TC realizados al mes y a los 12 meses posoperatorios se objetivó una correcta embolización de la AMI con permeabilidad de sus ramas distales. No aparecieron fugas de tipo II durante el seguimiento.
Durante el seguimiento no aparecieron complicaciones derivadas del punto de punción ni datos de isquemia mesentérica. No hubo reintervenciones posteriores relacionadas con la patología aórtica.
DISCUSIÓN
Muchos son los estudios que han demostrado que la presencia de EFT2 después del EVAR está directamente relacionada con la permeabilidad de las arterias AMI y lumbares (8-10). En el estudio prospectivo aleatorizado de Samura et al. (9) concluyen que la embolización preventiva de la AMI en pacientes de alto riesgo, con similares características preoperatorias a las formuladas en nuestro estudio, disminuye la presencia de EFT2 durante el seguimiento (24,5 % frente a 49,1 %, p = 0,009).
Burbelko et al. (10) demostraron que el flujo de sangre generado por la presencia de EFT2 puede ir transmitiendo presión al saco aneurismático, y con ello, un aumento en el riesgo de ruptura. Otros autores, por el contrario, opinan que las fugas de tipo II pueden tratarse de forma conservadora sin crecimiento del saco, ya que hasta un 58 % se resuelve de forma espontánea (10-13).
En nuestro centro, del total de EVAR realizados durante los últimos años, se objetivaron EFT2 en un 20 % en el seguimiento. Entre las complicaciones, la más habitual es el aumento progresivo del diámetro del saco aneurismático, seguida por la necesidad de reintervenciones; el porcentaje de rotura de este es muy bajo. En la mayoría de los casos esta EFT2 dependía de la AMI, que presentaba un diámetro mayor de 3 mm, por lo que se planteó la embolización de la AMI como método preventivo de la presencia de EFT2. En la actualidad, y con base en los resultados obtenidos, en todos aquellos pacientes en los que se cumplen los criterios de embolización previamente descritos, estamos realizando embolización exclusiva de la AMI seguida del EVAR con resultados aún a corto plazo similares a los aquí descritos.
Varios estudios (14-16) comentaron que la embolización tanto de la AMI como de las AL reduce aún más la EFT2 que la embolización de la AMI sola, logrando una disminución de la presencia de endofugas, que se redujo del 3,6 % al 47,8 % en el grupo control. Sin embargo, el grupo de Alerci (14,16) informó de que la embolización de las AL fue técnicamente difícil debido a su diámetro pequeño, así como a la tortuosidad que presentan, lo que requirió un tiempo de procedimiento más prolongado y una tasa de éxito menor (alrededor del 60 %). En aquellos casos en los que se realizó embolización de la AMI, pero no fue posible la embolización de todas las AL, no se objetivó un crecimiento del saco aneurismático.
Otro estudio publicado recientemente recomienda la embolización de las AL previa al EVAR cuando presenten un diámetro interno ≥ 2,0 mm y un diámetro máximo de la luz aórtica sin trombo ≤ 36,1 mm, ya que es más factible la canulación de las AL cuanto menor sea el diámetro aórtico. A pesar de lo anterior, la tasa de éxito que obtuvieron fue del 73 % frente al 96 % que se logró solo embolizando la AMI (15).
Entre los resultados hallados en la literatura sobre la embolización exclusiva de la AMI previa al procedimiento endovascular destacan: una tasa de éxito muy alta (entre el 93,8 y el 100 %) con una tasa de complicaciones baja (cerca del 0 %) (6-8,18), además de una disminución significativa en la presencia de EFT2 y en el diámetro del saco aneurismático. Sólo el estudio de Ward et al. (8) reportó la muerte de un paciente tras isquemia; sin embargo, este había sido intervenido previamente de hemicolectomía.
En la mayoría de las publicaciones se reflejan los resultados de la embolización preventiva, pero son menos frecuentes los artículos en los que aparecen los resultados de la embolización de la AMI en un segundo tiempo en caso de observarse fuga durante el seguimiento. En el metaanálisis publicado por Karh et al. (19) obtuvieron una tasa de éxito técnico del 71,5 % de los tratamientos de endofugas de tipo II posteriores al EVAR, por lo que abogan así por la embolización de la AMI antes del EVAR.
La principal limitación de nuestro estudio es el pequeño número de pacientes incluidos y el corto tiempo de seguimiento (12 meses). Se trata de un estudio retrospectivo y unicéntrico, por lo que en un futuro podría plantearse la realización de un estudio prospectivo y aleatorizado para confirmar los resultados tan prometedores obtenidos en cuanto a la disminución de las EFT2.
CONCLUSIÓN
La embolización de la AMI previa al EVAR en pacientes con un diámetro de > 3 mm y presencia de al menos dos AL con diámetro > 2 mm o aneurismas aortoilíacos parece proteger frente al desarrollo de EFT2 a los 12 meses, a la espera de poder confirmar los resultados a medio y largo plazo, con un alto éxito técnico y una aceptable regresión del saco aneurismático.











 texto en
texto en