Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos Españoles de Urología (Ed. impresa)
versión impresa ISSN 0004-0614
Arch. Esp. Urol. vol.62 no.5 jun. 2009
Antígeno prostático-específico, citoquinas pro-inflamatorias y patología prostática (Hiperplasia benigna y Cáncer). Relación con la malignidad
Prostatic specific antigen (PSA), pro-inflammatory cytokines, and prostatic pathology (Benign prostatic hyperplasia and cancer). Relationship with malignancy
José Ramón Cansino Alcaide1, Raúl Vera San Martín2, Fermín Rodríguez de Bethencourt Codes1, Yosra Bouraoui2,3, Gonzalo Rodríguez Berriguete2, Ridha Oueslati3, Manuel Pérez-Utrilla1, Javier De la Peña Barthel1, Ricardo Paniagua Gómez-Álvarez2 y Mar Royuela García2.
1Departamento de Urología del Hospital La Paz. Madrid. España.
2Departamento Biología Celular y Genética. Universidad de Alcalá. Alcalá de Henares. Madrid. España.
3Unité d'Immunologie Microbiologie Environnementale et Cancérogenèse à la Faculté des Science de Bizerte. Túnez.
Este Trabajo ha sido subvencionado por el Ministerio de Educación y Ciencia (SAF2007-61928) y el Programa de Cooperación Interuniversitaria e Investigación Científica (PCI-Mediterráneo) (A/011430/07) (España).
Dirección para correspondencia
RESUMEN
Objetivo: El cáncer es un proceso complejo en el cual las citoquinas juegan un importante papel. Las citoquinas son proteínas solubles de bajo peso molecular, que participan en la transmisión celular y en diferentes patologías. Las citoquinas pro-inflamatorias (IL-1, TNF-a e IL-6) están muy relacionadas con el desarrollo del cáncer de próstata. El objetivo de nuestro trabajo consistió en relacionar la expresión (mediante inmunocitoquímica y Western blot) de diferentes citoquinas pro-inflamatorias (IL-1, TNF-a e IL-6) con los niveles de antígeno prostático específico (PSA) en suero, tanto en pacientes normales (sin patología prostática) como en condiciones patológicas (hiperplasia y cáncer), así como su posible papel en la progresión tumoral. Se discutirá el posible uso de estas citoquinas como diana terapéutica.
Métodos: Este estudio se ha realizado en 5 pacientes normales, 25 pacientes diagnosticados de hiperplasia benigna de próstata (HBP) y 17 pacientes de cáncer (CP). Se han realizado análisis de Western blot e inmunocitoquímica. Los niveles séricos de PSA se midieron mediante un "PSA DPC immulite assays" (Diagnostics Products Corporation, Los Angeles, CA).
Resultados: En HBP, IL-1a, IL-6 y TNF-a, solo se expresan en pacientes con niveles séricos de PSA de 0-4 ng/ml ó 4-20 ng/ml, pero no en el grupo >20 ng/ml. En cáncer, estas citoquinas se expresan en pacientes con niveles séricos de PSA >4 ng/ml, aunque la expresión de estas citoquinas se eleva considerablemente cuando los niveles de PSA son >20 ng/ml.
Conclusiones: En cáncer, podría existir una asociación entre elevada expresión de citoquinas pro-inflamatorias (IL-1, TNF-a e IL-6), elevados niveles séricos de PSA y progresión del cáncer. Un mejor conocimiento de los mecanismos biológicos de esta asociación, podrían ayudarnos a encontrar una posible diana terapéutica para los pacientes con patología prostática.
Palabras clave: TNFa. IL-1. IL-6. PSA. Cáncer de próstata.
SUMMARY
Objectives: Cancer is a complex process in which cytokines play an important role. Cytokines are low-molecular weight soluble proteins involved in cellular transmission signals and several disorders. Pro-inflammatory cytokines (IL-1, TNF-a and IL-6) are involved in prostate cancer development. The aim of this study was to relate the expression (analyzed by Western blot and immuno-histochemistry) of several pro-inflammatory cytokines (IL-1, TNF-a and IL-6) with serum levels of prostate-specific antigen (PSA) in normal (no pathological samples) as pathological samples (hyperplasia and cancer), in order to elucidate their possible role in tumor progression. We are also discussing the possible use of these cytokines as a potential therapeutic target.
Methods: This study was carried out in 5 normal, 25 benign prostatic hyperplastic (BPH) and 17 prostate cancer (PC) human prostates. Immunohistochemical and Western blot analysis were performed. Serum levels of PSA were assayed by a PSA DPC immulite assays (Diagnostics Products Corporation, Los Angeles, CA)
Results: In BPH, IL-1a, IL-6 and TNF-a were only expressed in patients with PSA serum levels of 0-4 ng/ml or 4-20 ng/ml, but not in the group >20 ng/ml. In PC these cytokines were only expressed in patients with PSA serum levels >4 ng/ml, although the expression of these cytokines was elevated when PSA levels were >20 ng/ml.
Conclusions: In PC there might be an association between high expression of pro-inflammatory cytokines (IL-1, TNFa and IL-6), elevated serum levels of PSA and cancer progression. A better understanding of the biologic mechanism of this association may improve the finding of new targets for therapy in these patients.
Key words: TNFa. IL-1. IL-6. PSA. Prostate cancer.
Introducción
La familia de la IL-1 está compuesta por dos factores (IL-1a e IL-1b)(1), dos receptores de transmembrana (IL-1RI e IL-1RII) (2) y el receptor antagonista IL-1Ra. La afinidad de IL-1a, IL-1b e IL-1Ra por los receptores IL-1RI e IL-1RII difiere dependiendo del ligando. IL-1a e IL-1Ra presentan mayor afinidad por IL-1RI que IL-1b, mientras que IL-1b tiene la mayor afinidad por IL-1RII (3). La expresión de la familia de IL-1 ha sido estudiada en diferentes tumores, entre ellos el cáncer de próstata, en el que Ricote y cols. (4) proponen que la familia de la IL-1 podría estar relacionada con la proliferación celular, pues la immunoexpresión de IL-1a e IL-1Ra es característica en CP comparado con próstata normal y HBP.
TNF-a se ha propuesto como promotor tumoral (5). Diferentes estudios relacionan la producción de TNF-a endógeno con invasión tumoral y desarrollo de metástasis (6, 7). En cáncer de próstata se han relacionado los niveles séricos de TNF-a con el desarrollo de la enfermedad, asociando los niveles séricos de TNF-a, el estado de desarrollo de la enfermedad y la presencia de metástasis (8). La dualidad funcional de TNF-a en tejidos tumorales viene determinada por las señales intracelulares que desencadena su llegada a la superficie celular al interaccionar con sus receptores de membrana (TNFRI y TNFRII) y activar diferentes rutas de transducción. La expresión y la funcionalidad de TNF-a y sus receptores se ha estudiado en diferentes tumores como de esófago (9), próstata (1 0), folículo tiroideo (11), piel (1 2), ovario (13) y mama (14).
Interleukina-6 (IL-6) es una citoquina multifunctional producida por diferentes tipos celulares como linfocitos T, fibroblastos o monocitos. Esta citoquina actúa mediante un complejo receptor de membrana formado por el receptor a de la IL-6 (IL-6Ra) y una glicoproteína 130 (gp130). Primero IL-6 se une a IL-6Ra, aunque esta unión no es suficiente para iniciar la señal de transducción, aunque atrae a gp 130, el cual dimeriza y se inicia la señal intracelular (15). Junto con su papel inmunológico, IL-6 participa en la proliferación celular de diferentes tejidos como hueso (16), testículo (espermatogénesis) (17), piel (18) y sistema nervioso (19). Se ha visto que IL-6 también estimula el desarrollo de diferentes tumores como el melanoma, carcinoma de células renales, carcinoma ovárico, linfomas, carcinoma de mama (20) o de próstata (21, 22).
PSA es un marcador órgano-específico, con alta sensibilidad pero baja especificidad para la detección del cáncer de próstata, existiendo situaciones que provocan una elevación temporal de sus niveles no relacionados con procesos tumorales como pueden ser manipulaciones de la glándula prostática (tacto rectal, sondaje, biopsias...) (23) y enfermedades benignas (hiperplasia, infección...) (24). Además, se han observado niveles normales en pacientes con patología tumoral. Así, PSA no es siempre indicativo del grado de evolución de la enfermedad (25).
Actualmente, diferentes grupos de investigación centran sus esfuerzos en la búsqueda de nuevos marcadores bioquímicos capaces de predecir la presencia y el pronóstico del cáncer de próstata. En este sentido, las citoquinas pro-inflamatorias se han relacionado con la producción de PSA y la progresión del cáncer de próstata (26-28).
Presentación
El objetivo de nuestro trabajo consistió en relacionar la expresión de estas citoquinas pro-inflamatorias (IL-1, TNF-a e IL-6) analizadas mediante Western blot e immunohistoquímica con los niveles séricos de PSA en muestras normales y patológicas (HBP y CP) de próstata. Pretendemos estudiar el papel que desempeñan estas citoquinas en la progresión tumoral. También se discuten los diferentes usos de estas citoquinas como factores potencialmente terapéuticos.
Materiales y métodos
Para realizar los estudios se utilizaron: 25 muestras procedentes de resección transuretral de varones (edad entre 55 y 85 años) diagnosticados clínica e histopatológicamente de Hiperplasia Benigna de Próstata (HBP); 17 muestras procedentes de varones (edad entre 57 y 88 años) procedentes de prostatectomías radicales y diagnosticados de cáncer de próstata (CP) con un gradiente Gleason de 3-5; y 5 muestras procedentes de varones (entre 20 y 38 años) obtenidas mediante autopsia (8-10 horas tras su muerte) sin historia conocida de enfermedad reproductiva, endocrina o relacionada. Cada muestra se dividió en tres porciones: una procesada inmediatamente para inmunohistoquímica y otras dos porciones congeladas en nitrógeno líquido y mantenidas a -80oC para Western blot. Todos los datos patológicos, clínicos o personales fueron usados de forma anónima y para ello, separados de la identificación personal. Este estudio ha sido aprobado por el comité Ético del "Military Hospital of Tunis (HMPIT) and Hospital of Fatouma Bourguiba of Monastir" (Túnez) (de donde procedían las muestras) y realizado con el consentimiento de los respectivos pacientes o sus familiares (en caso de muestras procedentes de autopsia).
Las determinaciones de los niveles de PSA sérico se realizaron antes de la prostatectomía radical mediante el ensayo "PSA DPC immulite" (donado por "Diagnostics Products Corporation, Los Ángeles, CA, USA"). Estos ensayos se realizaron siguiendo las instrucciones de la casa comercial. Se trata de un inmunoensayo tipo "sándwich", en fase sólida y con doble lugar de unión para anticuerpos monoclonales y policlonales anti-PSA. La reacción se desarrollo con un compuesto quimioluminiscente. Este ensayo considera como normales los niveles de PSA inferiores a 4 ng/ml.
Los anticuerpos primarios usados fueron: TNF-a (cabra anti-humano), IL-1a (conejo anti-humano) e IL-6 (conejo anti-humano). Todos ellos proceden de Santa Cruz Biotechnology, Ca, USA.
Los tejidos fueron homogeneizados en un tampón de extracción (Tris-HCl 0.05 M y pH: 8) con una mezcla adicional de inhibidores de proteasas (10 mM iodoacetamida, 100 mM phenil-metil sulfónico fluorado, 0.01 mg/ml inhibidores de la tripsina de soja y 1 ml/ml de leupeptina) junto con Tritón X-100 al 0.5%. Los homogeneizados se centrifugaron 10 minutos a 10000 rpm, desechando los precipitados. Con el fin de poder comparar los resultados obtenidos en las diferentes muestras, se calculó la concentración de proteína en los distintos sobrenadantes mediante la técnica Bradford. Posteriormente, los sobrenadantes se mezclaron con tampón de muestra (SDS al 10% en Tris-HCl pH 8 con glicerol al 50%, 2-b-mercaptoetanol 0.1 mM y azul de bromofenol al 0.1%), se calentaron a 100oC durante 5 minutos y se cargaron alícuotas de 10 ml en minigeles de SDS-poliacrilamida con un gradiente de concentración del 15%. Las proteínas se trasfirieron a membranas de nitrocelulosa. Posteriormente, estas membranas se sumergieron en Blotto (SIGMA) al 5% en PBS durante 1 hora a temperatura ambiente en agitación. Se incubaron (toda la noche a temperatura ambiente y agitación) con anticuerpo primario diluido en solución de bloqueo (diluida 1+9 en TBS). Las diluciones usadas para los anticuerpos primarios fueron de 1:100 (IL-1a y TNF-a) y 1:200 (IL-6). Se lavaron tres veces con solución de lavado (5 minutos cada lavado) y se incubaron con el anticuerpo secundario unido a peroxidasa a una dilución 1:4000 en solución de bloqueo (diluida 1+9 en TBS) durante 1 hora a temperatura ambiente con agitación. Tras tres lavados (de 10 minutos cada uno) se reveló la actividad peroxidasa usando el kit ECL de Amershan.
Los tejidos se fijaron en formaldehido al 10% en tampón fosfato 0.1M durante 24 horas, deshidratados y embebidos en parafina. Las secciones se procesaron siguiendo el método del ABC. Tras desparafinar, las secciones se hidrataron e incubaron durante 30 minutos en H2O2 al 0.3% en metanol para inhibir la actividad de la peroxidasa endógena. Posteriormente se incubaron durante toda la noche a 4oC con los anticuerpos primarios a una dilución de 1:50 en TBS con BSA al 1%. Posteriormente las secciones se lavaron y se incubaron con inmunoglobulinas biotiniladas anti-anticuerpo primario (Dako, Barcelona, España) diluidos 1:500 en TBS. Tras un nuevo lavado en TBS se incubaron durante una hora con el complejo estreptavidina-biotina (Vector Laboratories, Burlingame, CA, USA) diluido 1:500 en TBS y se revelaron con DAB (3,3'-diaminobenzidine) (Sigma, Barcelona, España) usando el método de intensificación de niquel-glucosa oxidasa (29). Finalmente las secciones se deshidrataron y se montaron en DePex (Probus, Barcelona, España).
La especificidad de la técnica se chequeó realizando una serie de controles negativos y positivos. Como negativo, secciones de cada grupo (normal, HBP y cáncer) se incubaron con suero preinmune a la misma concentración de inmunoglobulinas usadas para cada anticuerpo primario o usando péptidos bloqueantes (Santa Cruz Biotechnology). Como positivo, se incubaron secciones de timo (TNF-a e IL-6) y amígdala (IL-1a) con los mismos anticuerpos usados en este estudio.
Para cada anticuerpo, se cuantificó histológicamente la intensidad de marcaje obtenido. En cada próstata se seleccionaron al azar seis secciones histológicas. Con el objetivo de 40X se midió la intensidad de marcaje (densidad óptica) por unidad de superficie del epitelio mediante un analizador de imagen automático (Motic Images Advanced version 3.2, Motic China Group Co., China). Para cada sección positiva se utilizó un control negativo, de tal forma que la densidad óptica del control se restó de la sección marcada. Posteriormente se calculó la media, así como la desviación Standard de la media. Los mismos estudios cuantitativos se desarrollaron en PN y CP. La significación estadística se estudió mediante el test exacto de Fisher y el test de ANOVA para p<0.05 (usando el programa informático GraphPad PRISMA 3).
Resultados
Western blot
En los grupos de HBP y PC, se observó una única banda (en su correspondiente peso molecular) para IL-1a (17 kDa), TNF-a (17 kDa) e IL-6 (21 kDa) (Fig. 1). En próstata normal, sólo se observo señal para TNF-a e IL-6 (también en su correspondiente peso molecular) (Figura 1).
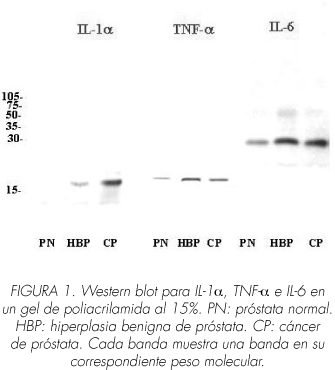
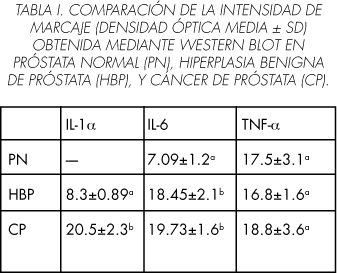
El análisis densitométrico de las bandas en IL-1a e IL-6 mostró un incremento en CP frente a BPH, y a su vez, en este grupo frente a PN. Para TNF-a, no se observaron diferencias estadísticamente significativas entre los tres grupos de pacientes (Tabla I).
Immunohistoquímica
No se observó immunomarcaje en los controles negativos incubados con suero pre-immune o usando anticuerpos preabsorbidos con un exceso de antígeno purificado. Las secciones de timo (IL-6 y TNF-a) y amigdala (IL-1a), usadas como controles positivos, siempre fueron positivas.
Para cada anticuerpo, el porcentaje de pacientes positivos se muestra en la Tabla II.
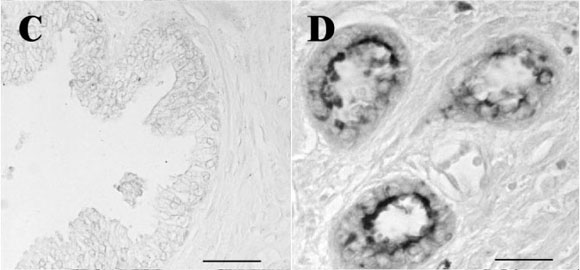
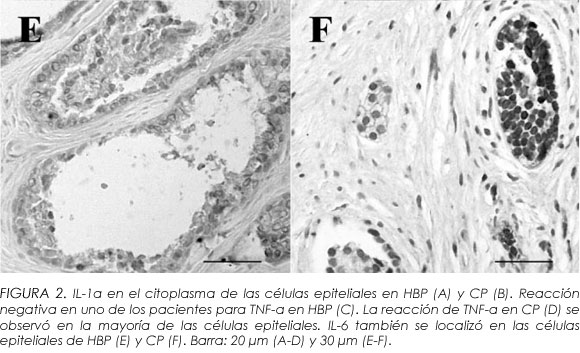
No se detectó IL-1a en ninguna muestra de próstata normal. Entre los pacientes con HBP (Figura 2A), se observó marcaje en el 50% de las muestras de aquellos que tenían niveles de PSA entre 0-4 ng/ml y un 60% de muestras de aquellos que tenían niveles de PSA entre 4-20 ng/ml (Tabla II). En los pacientes con CP (Figura 2B), IL-1a se expreso en los grupos con niveles de PSA entre 4-20 ng/ml (75%) y PSA >20ng/ml (70% de los pacientes).
Se observo marcaje para TNF-a en próstata normal (40%), HBP (40%) y CP (35.2%) (Tabla II). En HBP (Figura 2C) el porcentaje de pacientes positivos desciende cuando aumentan los niveles de PSA. En CP (Figura 2D) la señal sólo se detectó en dos grupos de pacientes: con niveles de PSA entre 4-20 ng/ml y >20 ng/ml.
En Próstata normal, todas las muestras fueron positivas para IL-6. En HBP (Figura 2E), sólo se observaron muestras positivas en dos grupos de PSA: 0-4 ng/ml (68% de los pacientes) y 4-20 ng/ml de PSA (76.5% de los pacientes). El 76.5 % de los pacientes con cáncer fueron positivos para IL-6 (Figura 2F, Tabla II).
Discusión
Catolona y cols. (30) establecieron como referencia los rangos de 0-4 ng/ml para definir niveles de PSA normales, rangos de 4-10 ng/ml para establecer un incremento de probabilidad de aparición de cáncer de próstata y superiores a 10 ng/ml como elevada probabilidad de aparición de cáncer de próstata. Sin embargo, estudios posteriores sugieren que niveles de 10 ng/ml tienen poca correlación con cáncer de próstata (31). Por ello, nosotros establecemos en 20 ng/ml el grupo de elevada probabilidad de cáncer de próstata.
En este estudio, IL-1a (no se expresa en próstata normal) se detecto en el 56% de los pacientes con HBP y el 70% de los pacientes con CP. Resultados similares se observaron en nuestro grupo en trabajos previos (4), sugiriendo que IL-1a en células epiteliales podría estar involucrada en el incremento de la proliferación celular asociada con HBP y cáncer. A su vez, los pacientes con elevada expresión de IL-1a, también presentan elevados niveles de PSA (>20ng/ml). Estos resultados sugieren que los grupos de pacientes con alta expresión de IL-1a en células epiteliales, presentarían mayor proliferación celular y altos niveles de PSA.
En una línea celular de melanoma (A375), Lázár-Molnár y cols. (32) observaron que la producción endógena de IL-1a se asociaba con resistencia exógena a estímulos anti proliferativos, unidos a un incremento en la producción de IL-6 de forma autocrina. Resultados previos observados en nuestro laboratorio, mostraban un aumento de la expresión de IL-6 en células epiteliales de cáncer de próstata (22). Como el incremento en la expresión de IL-6 se ha asociado con mal pronóstico en cáncer de próstata (33-34), evaluar los inductores de la expresión de IL-1a e IL-6 podría ser un paso importante en la valoración de la malignidad. Resultados similares se han descrito en cáncer de mama, donde la expresión de IL-6 se asocia con un aumento de los marcadores de proliferación celular (20).
Los efectos descritos para IL-6 en cáncer de próstata son contradictorios. En algunos trabajos se describe que podría promover el crecimiento (35-36), mientras que en otros estudios se describe como un represor del crecimiento celular (26). En nuestro estudio, además de la expression de IL-6 en HPB y CP; se describe una asociación entre elevada expresión de IL-6, elevada expresión de IL-1a (64.7% de las muestras) y altos niveles de PSA (>20 ng/ml).
En el caso de TNF-a también se han descrito efectos contradictorios. Lejeune y cols. (37) observaron que la administración local de altas dosis de TNF-a destruía selectivamente los vasos sanguíneos del tumor y por lo tanto su gran poder anticancerígeno en melanoma. Sin embargo, diferentes estudios sugieren que TNF-a endógeno está implicado en el crecimiento de las células tumorales y en las interacciones con el estroma facilitando la invasión tumoral y el desarrollo de metástasis (7, 8). En nuestro estudio, nosotros hemos observado que alta expresión de IL-6 se asocia con elevada expresión de TNF-a (35.2% de las muestras) y con altos niveles de PSA (>20 ng/ml).
De acuerdo con nuestros resultados, sugerimos que en HBP, la alta expresión de citoquinas pro-inflamatorias podría estar asociada con elevada producción de PSA. En CP, la alta expresión de estas citoquinas y los elevados niveles de PSA podrían estar involucrados en el cambio de polaridad de las células epiteliales así como en la cantidad de células basales. Al mismo tiempo, estas citoquinas podrían estar involucradas indirectamente en el incremento de los niveles de PSA circulatorio.
Conclusiones
En CP podría existir una asociación entre altos niveles de citoquinas pro-inflamatorias (IL-1, TNF-a e IL-6,), inflamación, elevados niveles séricos de PSA y progresión tumoral. La inhibición de estas citoquinas podría ser una posible diana terapéutica en el tratamiento de CP. Un mejor conocimiento de los mecanismos biológicos y del papel que desempeña la elevación del PSA circulante relacionado con la expresión tisular de estas citoquinas, podría mejorar el manejo clínico y encontrar nuevos objetivos terapéuticos en estos pacientes.
Bibliografía y lecturas recomendadas (*lectura de interés y **lectura fundamental)
*1. Dinarello C A. The interleukin-1 family: 10 years of discovery. FASEB J, 1994; 8: 1314. [ Links ]
2. Sims J E, Dower S K. Interleukin-1 receptors. Eur. Cytokine Netw, 1994; 5: 539. [ Links ]
3. Boraschi D, Bossu P, Macchia G, et al. A. Structure-function relationship in the IL-1 family. Front. Biosci., 1: d270, 1996. [ Links ]
**4. Ricote M, Garcia-Tuñon I, Bethencourt F R, et al. Interleukin-1 (IL-1alpha and IL-1beta) and its receptors (IL-1RI, IL-1RII, and IL-1Ra) in prostate carcinoma". Cancer, 2004; 100: 1388. [ Links ]
5. Balkwill F. Tumor necrosis factor or tumor promoting factor? Cytokine Growth. Factor Rev, 2002; 13: 135. [ Links ]
6. Beutler B A. The role of tumor necrosis factor in health and disease. J. Rheumatol. Suppl, 1999; 57: 16. [ Links ]
7. Kollias G, Douni E, Kassiotis G, et al. On the role of tumor necrosis factor and receptors in models of multiorgan failure, rheumatoid arthritis, multiple sclerosis and inflammatory bowel disease. Immunol. Rev, 1999; 169: 175. [ Links ]
**8. Michalaki V, Syrigos K, Charles P, et al. Serum levels of IL-6 and TNF-alpha correlate with clinicopathological features and patient survival in patients with prostate cancer. Br. J. Cancer, 2004; 90: 2312. [ Links ]
9. Hubel K, Mansmann G, Schafer H et al. Increase of anti-inflammatory cytokines in patients with esophageal cancer after perioperative treatment with G-CSF. Cytokine, 2000; 12: 1797. [ Links ]
**10. De Miguel M P, Royuela M, Bethencourt F R, et al. Immunoexpression of tumour necrosis factor-alpha and its receptors 1 and 2 correlates with proliferation/apoptosis equilibrium in normal, hyperplasic and carcinomatous human prostate. Cytokine, 2000; 12: 535. [ Links ]
11. Zubelewicz B, Muc-Wierzgon M, Wierzgon J. Genetic disregulation of gene coding tumor necrosis factor alpha receptors (TNF alpha Rs) in follicular thyroid cancer preliminary report. J. Biol. Regul. Homeost. Agents, 2002; 16: 98. [ Links ]
12. Scott K A, Arnott C H, Robinson S C, et al. TNF-alpha regulates epithelial expression of MMP-9 and integrin alphavbeta6 during tumour promotion. A role for TNF-alpha in keratinocyte migration? Oncogene, 2004; 23: 6954. [ Links ]
13. Rzymski P, Opala T, Wilczak M, et al. Serum tumor necrosis factor alpha receptors p55/p75 ratio and ovarian cancer detection. Int. J. Gynaecol. Obstet, 2005; 88: 292. [ Links ]
**14. García-Tuñon I, Ricote M, Ruiz A, et al. Role of tumor necrosis factor-alpha and its receptors in human benign breast lesions and tumors (in situ and infiltrative). Cancer Sci, 2006; 97: 1044. [ Links ]
**15. Heinrich P C, Behrmann I, Mueller-Newen G, et al. Interleukin 6-type cytokine signaling throught the gp130/jak/stat pathways. Biochem. J, 1998; 334: 297. [ Links ]
16. Kurihara N, Bertolini D, Suda T, et al. IL-6 stimulates osteoclast-like multinucleated cell formation in long term human marrow cultures by inducing IL-1 release. J. Immunol, 1990: 144: 4226. [ Links ]
17. Hacovirta H, Syed B, Jegou B, et al. Function of Interleukin-6 as an inhibitor of meiotic DNA synthesis in the rat seminiferous epithelium". Mol. Cell. Endocrynol, 1995; 108: 193. [ Links ]
18. Krueguer J, Krane J, Carter D, et al. Role of growth factors, cytokines, and their receptors in the pathogenesis of psoriasis. J. Invest. Dermatol, 1990; 94: 135s. [ Links ]
19. Hama T, Miyamoto M, Tsuki H, et al. Interleukin-6 is a neurotrophic factor for promoting the survival of cultured basal forebrain cholinergic neurons fron postnatal rats. Neurosci. Lett, 1989; 104: 340. [ Links ]
**20. García-Tuñon I, Ricote M, Ruiz A, et al. IL-6, its receptors and its relationship with bcl-2 and bax proteins in infiltrating and in situ human breast carcinoma. Histopathology, 2005; 47: 82. [ Links ]
**21. Keller E T, Wanagat J, Ershler W B. Molecular and cellular biology of interleuklin-6 and its receptor. Front. Biosci, 1996; 1: 340. [ Links ]
**22. Royuela M, Ricote M, Parsons M S, et al. Immunohistochemical analysis of IL-6 family of cytokines and their receptors in benign, hyperplastic and malignant human prostate. J. Pathol, 2004; 202: 41. [ Links ]
23. Polascik T J, Oesterling J E, Partin A W. Prostate specific antigen: a decade of discovery - what we have learned and where we are going. J. Urol, 1999; 162: 293. [ Links ]
*24. Bozeman C B, Carver B S, Eastham J A, et al. Treatment of chronic prostatitis lowers serum prostate specific antigen. J. Urol, 2002; 167: 1723. [ Links ]
**25. Roddam A W, Duffy M J, Hamdy F C, et al. NHS Prostate Cancer Risk Management Programme. Use of prostate-specific antigen (PSA) isoforms for the detection of prostate cancer in men with a PSA level of 2-10 ng/ml: systematic review and meta-analysis. Eur. Urol, 2005; 48: 386. [ Links ]
26. Spitto M T, Chang T D. STAT3 mediates IL-6-induced growth inhibition in the human prostate cancer line LNCaP. Prostate, 2000; 42: 88. [ Links ]
**27. Schalken J A. Molecular and cellular prostate biology: origin of prostate-specific antigen expression and implications for benign prostatic hyper-plasia. B.J.U. Int, 2004; 93: 5. [ Links ]
*28. Lin D L, Whitney M C, Yao Z, et al. Interleukin-6 induced androgen responsiveness in prostate cancer cells through upregulation of androgen receptor expression. Clin. Cancer Res, 2001; 7: 1773. [ Links ]
29. Hsu S M, Soban E. Colour modification of diaminobenzidine (DAB) precipitation by metallic ions and its application to double immunohistochemistry. J. Histochem. Cytochem, 1982; 30: 1079. [ Links ]
**30. Catalona W J, Smith D S, Ratliff T L, et al. Measurement of prostate-specific antigen in serum as a screening test for prostate cancer. N. Engl. J. Med, 1991; 324: 1156. [ Links ]
**31. Stamey T A. Preoperative serum prostate-specific antigen (PSA) below 10 microg/l predicts neither the presence of prostate cancer nor the rate of postoperative PSA failure. Clin. Chem, 2001; 47: 631. [ Links ]
32. Lazar-Molnar E, Hegyesi H, Toth S, et al. Autocrine and pararine regulation by cytokines and growth factors in melanoma. Cytokine, 2000; 12: 547. [ Links ]
*33. Twillie D A, Eisenberger M A, Carducci M A, et al. Interleukin-6: a candidate mediator of human prostate cancer morbidity. Urology, 1995; 45: 542. [ Links ]
*34. Shariat S F, Andrews B, Kattan M.W, et al. Plasma levels of interleukin-6 and its soluble receptor are associated with prostate cancer progression and metastasis. Urology, 2001; 58: 1008. [ Links ]
35. Mora L B, Buettner R, Seigne J, et al. Constitutive activation of Stat3 in human prostate tumors and cell lines: direct inhibition of Stat3 signaling induces apoptosis of prostate cancer cells. Cancer Res, 2002; 62: 6659. [ Links ]
36. Liu X H, Kirschenbaum A, Lu M, et al. Prostaglandin E(2) stimulates prostatic intraepithelial neoplasia cell growth through activation of the interleukin-6/ GP130/ STAT-3 signaling pathways. Biochim. Biophys. Res. Commun, 2002; 290: 249. [ Links ]
*37. Lejeune F J, Liénard D, Matter M, et al. Efficiency of recombinant human TNF in human cancer therapy. Cancer Immun, 2006; 6: 6. [ Links ]
 Dirección para correspondencia:
Dirección para correspondencia:
J. R. Cansino Alcalde
General Varela, 32 -4o B
28020 Madrid. (España)
urocansino@yahoo.es
Recibido: 12 de octubre 2008











 texto en
texto en