Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Actas Urológicas Españolas
versión impresa ISSN 0210-4806
Actas Urol Esp vol.33 no.9 oct. 2009
Malacoplaquia testicular: aportación de un nuevo caso y revisión de la literatura científica
Malacoplakia of the testis: a new case report and a literature review
Silvia Álvarez Bandrésa, Rosa M. Guarch Troyasb, José L. Cebrián Lostala, Luis Ripa Saldíasa, Álvaro de Pablo Cárdenasa y José D. Jiménez Parraa
aServicio de Urología, Hospital Virgen del Camino, Pamplona, Navarra, España
bServicio Anatomía Patológica, Hospital Virgen del Camino, Pamplona, Navarra, España
Dirección para correspondencia
RESUMEN
La malacoplaquia es un proceso granulomatoso crónico de naturaleza benigna, poco frecuente, que afecta de forma preferente al tracto genitourinario. El compromiso testicular representa el 12%; se ha descrito el primer caso de malacoplaquia a este nivel en 1958. Desde entonces, 40 casos se han publicado en todo el mundo. Presentamos un nuevo caso de malacoplaquia testicular y epididimaria en un varón de 68 años diagnosticado de orquiepididimitis complicada, al que se le practicó orquiectomía con el fin de descartar proceso neoformativo maligno. El estudio histológico objetivó la presencia de un infiltrado inflamatorio crónico con histiocitos de citoplasma eosinófilo, en el interior de los cuales se visualizaron los característicos cuerpos de Michaelis-Gutmann, que dieron el diagnóstico de malacoplaquia.
A propósito de este nuevo caso, y por lo inusual de su presentación, realizamos una revisión de la literatura científica de la entidad que nos ocupa.
Palabras clave: Malacoplaquia testicular, Malacoplaquia epididimaria, Cuerpos de Michaelis-Gutmann.
ABSTRACT
Malakoplakia is a uncommon chronic granulomatous condition of a benign nature preferentially occurring in the genitourinary tract. Testes are affected in 12% of cases, and the first case of testicular malakoplakia was reported in 1958. Forty cases have been reported worldwide since that date. We report a new case of testicular and epididymal malakoplakia in a 68-year-old male patient diagnosed of complicated orchiepididymitis who underwent orchidectomy to rule out a malignant tumor. The histopathological study demonstrated a chronic inflammatory infiltrate with histiocytes with an eosinophilic cytoplasm containing the characteristic Michaelis-Gutmann bodies diagnostic of malakoplakia.
In connection with this new case and because of its unusual presentation, the literature on testicular malakoplakia is reviewed.
Key words: Testicular malakoplakia, Epididymal malakoplakia, Michaelis-Gutmann bodies.
Introducción
La malacoplaquia (MLP) es una enfermedad inflamatoria crónica inusual, de etiología incierta, aunque frecuentemente asociada a infección por bacterias gramnegativas, en especial Escherichia coli1.
Descrita inicialmente por Michaelis y Gutmann2 en 1902, fue Von Hansemann quien, en 1903, empleó el término malacoplaquia (del griego malakós, blando, y plakos, placa)3 para definir este proceso en alusión a su aspecto macroscópico.
El tracto genitourinario es, con diferencia, el más afectado y representa, según Stanton y Maxted1, el 58% de los casos, pudiendo comprometer a cualquier sistema o aparato del organismo.
En 1958, Haukohl y Chinchinian4 publicaron el primer caso de MLP testicular, y se han recogido en la literatura científica 40 casos en los que el proceso involucra al testículo de forma aislada, 14 con afectación testicular y epididimaria5, y es siendo mucho menos frecuente la afectación exclusiva del epidídimo, con un total de 11 casos publicados hasta la fecha.
A continuación, presentamos un nuevo caso de MLP testicular con afectación epididimaria, revisando los aspectos clínicos, diagnósticos, anatomopatológicos, etiopatogénicos y terapéuticos.
Caso clínico
Paciente de 68 años de edad, con antecedentes de retraso mental grave y sordomudez secundaria a meningitis en la infancia. Consultó en nuestro servicio de urgencias por cuadro de dolor e inflamación en el hemiescroto izquierdo de más de 3 semanas de evolución, que no cedía a pesar de tratamiento antibiótico y antiinflamatorio. A la exploración, se objetivó un aumento generalizado del contenido escrotal, más marcado en lado izquierdo, con testículo doloroso a la palpación, de consistencia firme, superficie lisa y epidídimo engrosado.
El testículo derecho fue normal. El sedimento de orina reveló la presencia de piuria.
Por ecografía se objetivó un teste izquierdo aumentado de tamaño, heterogéneo, con una zona en situación medial con múltiples cavidades quísticas, algunas de ellas hipoecogénicas (fig. 1).
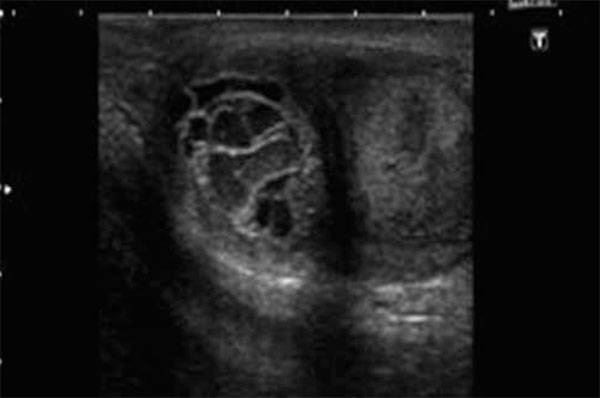
Figura 1 - Aspecto ecográfico heterogéneo de la lesión testicular.
Diagnosticado de orquitis evolucionada, se dio de alta al paciente con tratamiento analgésico-antiinflamatorio.
A los 8 días acudió a revisión en la consulta de urología, donde a la palpación se delimitaba claramente un nódulo, que planteaba diagnóstico diferencial con neoplasia testicular.
Se realizó una orquiectomía radical izquierda, previa determinación de marcadores tumorales (b-HCG, alfa-fetoproteína y LDH), que fueron normales.
Macroscópicamente, la superficie de sección de la pieza de orquiectomía mostró un engrosamiento de la túnica albugínea, con zonas hemorrágicas. El parénquima testicular estaba aumentado de consistencia, con presencia al corte de tractos fibrosos blanquecinos y placas amarillentas (fig. 2). El examen microscópico reveló la existencia de una hipoespermatogénesis marcada con hialinización de los túbulos seminíferos (fig. 3), así como un proceso inflamatorio crónico, constituido por histiocitos, abundantes células plasmáticas y células gigantes. En el interior de algunas de estas células, se reconocieron los característicos cuerpos de Michaelis-Gutmann (fig. 4) con aspecto en "ojo de búho", que dieron positivo para la tinción de Von Kossa, demostrando su composición de calcio y sugiriendo así el diagnóstico de MLP.
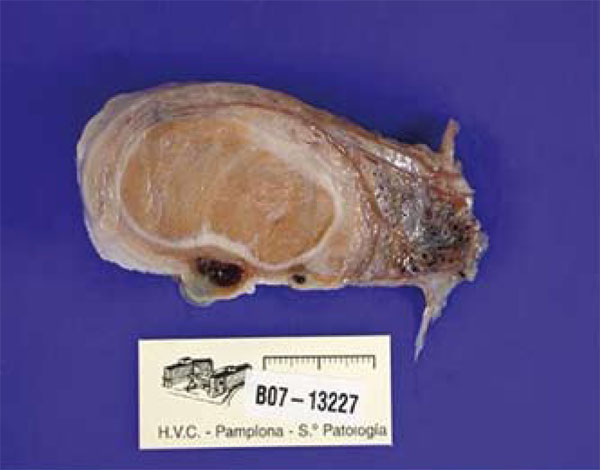
Figura 2 - Aspecto macroscópico del testículo al corte.
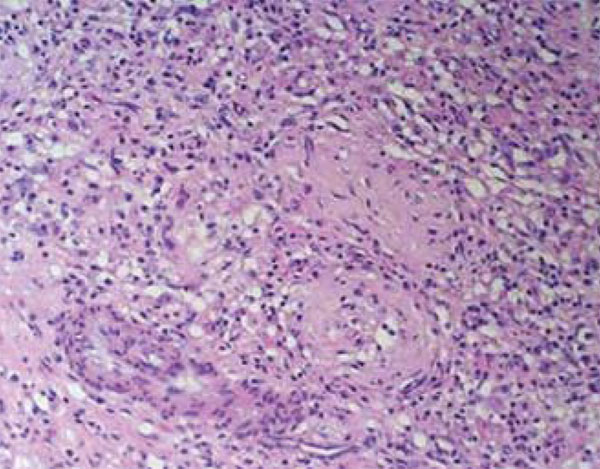
Figura 3 - Examen microscópico del parénquima testicular que muestra la presencia de
un infiltrado inflamatorio crónico, con marcada hipoespermatogénesis y hialinización
de los túbulos seminíferos.
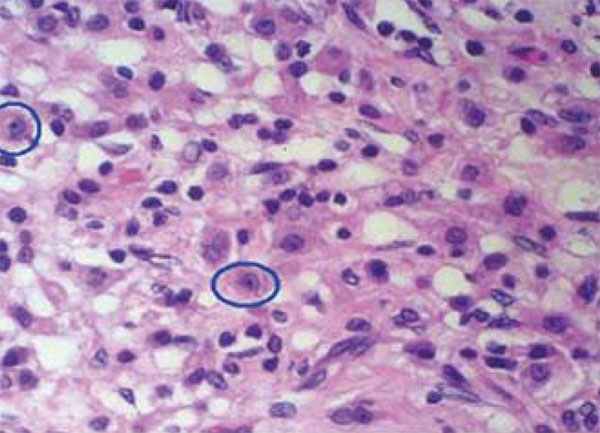
Figura 4 - Células plasmáticas y células gigantes con cuerpos de
Michaelis-Gutmann en su interior.
Estas alteraciones inflamatorias también afectaban al epidídimo de forma parcial.
Con el diagnóstico de MLP testicular y epididimaria, se completó el tratamiento con una pauta de fluoroquinolonas durante 3 meses, tras lo cual la evolución es satisfactoria y el paciente se encuentra asintomático.
Discusión
Las descripciones de Michaelis-Gutmann2 y Von Hansemann1,3 dieron a conocer hace ya más de un siglo esta enfermedad granulomatosa crónica, que puede presentarse en cualquier lugar del cuerpo; el aparato genitourinario es el más comúnmente afectado1.
Durante prácticamente 50 años, se pensó que la MLP afectaba exclusivamente a éste, hasta que en 1958 Haukohl y Chinchinian4 describen el primer caso fuera del mismo, en un paciente con afectación testicular.
La MLP testicular representa el 12% de los hallazgos de esta extraña enfermedad, y son únicamente 11 los casos de MLP epididimaria publicados hasta la fecha, sumando así uno más a la literatura científica mundial.
Se han propuesto múltiples teorías que explican la etiopatogenia de esta entidad y aún sigue sin estar aclarada, si bien se acepta un origen multifactorial en el que se reconocen 3 factores principales implicados: una alteración de la función fagocítica de los macrófagos6, una infección por gérmenes gramnegativos1 y una respuesta inmunológica alterada7.
Se ha demostrado una fagocitosis ineficaz como resultado de un defecto en la respuesta lisosómica de los macrófagos ante una infección bacteriana, generalmente por bacilos coliformes (E. coli en el 76% de los casos)1. La razón es un desequilibrio entre el adenosinmonofosfato cíclico y el guanosinmonofosfato cíclico (CMPc), a favor del primero, lo que provoca una deficiente degranulación lisosómica de los monocitos y, en consecuencia, una pobre actividad bactericida8.
Pacientes inmunodeprimidos7, debilitados o con procesos crónicos (neoplasias9, diabetes, hepatopatías alcohólicas10, tuberculosis y sida) son los más afectados. Asimismo, se ha confirmado su asociación con hipogammaglobulinemia11 y deficiencias selectivas de inmunoglobulina A12. En nuestro caso, no obstante, no se demostró causa alguna que justificara el desarrollo de la enfermedad, si bien es cierto que tampoco se realizaron cultivos que pusieran de manifiesto una infección subyacente.
La presentación clínica, así como la sintomatología, dependerán de la localización de la lesión. A nivel testicular habitualmente se presenta en forma de orquiepididimitis aguda o crónica, de evolución tórpida, que en el caso de nuestro paciente motivó el inicio del estudio; no es infrecuente la formación de abscesos con fistulización, condición que se describe hasta en un 70% en algunas series13.
En otras ocasiones, se presenta como una masa intraescrotal indolora, remedando un tumor de testículo1,8.5 Así pues, a pesar de su carácter inflamatorio y por consiguiente benigno, la MLP testicular suele acabar en orquiectomía, como ocurrió en nuestro paciente, y como única medida para diferenciarlo de otros procesos de naturaleza maligna o infecciones.
El diagnóstico diferencial, por tanto, deberá hacerse con tumores testiculares y otros procesos inflamatorios, como tuberculosis, histoplasmosis y criptococosis. La orquitis granulomatosa idiopática también debe excluirse, habiéndose descrito su asociación con MLP14.
El diagnóstico definitivo viene dado durante el examen anatomopatológico1,3, bien mediante estudio de la pieza de orquiectomía como en nuestro caso, o bien tras punción aspiración con aguja fina15, como método diagnóstico preliminar a procedimientos más invasivos.
Macroscópicamente, las lesiones producidas por la MLP dan una imagen de placas o nódulos blandos y de color amarillento, que histológicamente están constituidos por un infiltrado inflamatorio inespecífico con fibrosis y una proliferación de histiocitos voluminosos de citoplasma acidófilo, denominados células de Von Hansemann16. En su interior, se diferencian unas estructuras calcificadas, basófilas e intensamente PAS positivas, que corresponden a los cuerpos de Michaelis-Gutmann17 en diferentes estadios de maduración1, descritos por primera vez en 1902 y patognomónicos de la enfermedad6. Ultraestructuralmente, contienen fragmentos de bacterias digeridas de forma incompleta17, sobre los que se depositan sales de calcio y hierro en capas concéntricas, dando positividad para las tinciones de Von Kossa, como en nuestro caso, y Pearls, respectivamente1, lo que les confiere ese aspecto característico en diana u ojo de búho, como muestra la figura 4.
Se han propuesto distintas modalidades terapéuticas además de la resección quirúrgica; el tratamiento médico de la enfermedad basado en antibioterapia es un buen ejemplo; están indicadas pautas largas de aquellos antimicrobianos con mayor penetración a través de la membrana celular. Las fluoroquinolonas, y más concretamente el ciprofloxacino, por el que finalmente optamos en nuestro paciente como tratamiento complementario a la cirugía, se consideran de elección por su alta efectividad (80-90%)18, aunque también se han publicado buenos resultados con rifampicina, cotrimoxazol y gentamicina16. Además, cabe destacar el empleo de sustancias que mejoran la función lisosomal y potencian la fagocitosis. Así, se ha visto que la vitamina C o el betanecol (agonista colinérgico)1,3,11 son capaces de aumentar los niveles de GMPc en el interior de los macrófagos.
En general, el pronóstico es bueno, y es muy rara la recurrencia tras la orquiectomía, debiendo someter a todo paciente con diagnóstico de MLP a revisiones periódicas por la posibilidad de recidiva.
Bibliografía
1. Stanton MJ, Maxted W. Malakoplakia: a study of the literature and current concepts of pathogenesis, diagnosis and treatment. J Urol. 1981;125:139. [ Links ]
2. Michaelis L, Gutmann C. Ubre Einschlüsse in Blasentumore. Klin Med. 1902;47:208. [ Links ]
3. McClure J. Malakoplakia. J Pathol. 1983;140:275-330. [ Links ]
4. Haukohl RS, Chinchinian H. Malakoplakia of testicle - report of a case. Am J Clin Pathol. 1958;29:473-8. [ Links ]
5. Carvajal A, Vélez A, Escobar AM, Restrapo JM, Aristizábal JM, Robledo M. Malakoplakia de testículo. Rev CAU. 2003;15:52-53. [ Links ]
6. Lou TY, Teplitz C. Malakoplakia: pathogenesis and ultraestructural morphogenesis. A problem of altered macrophage (phagolysosomal) response. Hum Pathol. 1974;5:191. [ Links ]
7. Biggar WD, Keating A, Brear RA. Malakoplakia: evidence for an acquired disease secondary to immunosuppression. Transplantation. 1981;31:109-12. [ Links ]
8. El Ouakdi M, Zermani R, Bojnah H, Ayed M, Ben Jilani S, Zmerli S, et al. Malacoplasie genito-urinaire. A propos de cing cas. Revue de la literatura. Ann Urol Num. 1989;3:197-200. [ Links ]
9. Lew S, et al. Renal cell carcinoma with malakoplakia. Eur Urol. 1988;14:426. [ Links ]
10. Ling BN, Delaney VB, Campbell WG Jr. Acute renal failure due to bilateral renal parenchymal malakoplakia. Am J Kidney Dis. 1989;13:430. [ Links ]
11. Webb M, Pincott JR, Marshall WC, Spitz L, Harvey BA, Soothill JF. Hypogamamaglobulinemia and malakoplakia: response to bethanecol. Eur J Pediatr. 1986;145:297. [ Links ]
12. Witherington R, Branan WJ Jr, Wray BB, Best GK. Malakoplakia associated with vesicoureteral reflux and selective Immunoglobulin A deficiency. J Urol. 1984;132:975. [ Links ]
13. Brown RC, Smith BH. Malakoplakia of the testis. Am J Clin Pathol. 1967;47:135. [ Links ]
14. Mc Clure J. Malakoplakia of the testis and its relationship to granulomatous orchitis. J Clin Pathol. 1980;33:670-8. [ Links ]
15. Kapasi H, Robertson S, Futter N. Diagnosis of renal malakoplakia by fine needle aspiration citology. A case report. Acta Cytol. 1998;42:1419-23. [ Links ]
16. Dasgupta P, Womack C, Turner AG, Blackford HN: Malakoplakia. Von Hansemann´s disease. BJU Int. 1999;84:464-9. [ Links ]
17. Stevens S, Mc Clure J. The histochemical features of the Michaelis-Gutman body and a consideration of the pathophysiological mechanisms of it´s formation. J Pathol. 1982;137:119-23. [ Links ]
18. Dohle G, Zwartendijk J, Van Krierken JH. Urogenital malakoplakia traeated with Fluorquinolones. J Urol. 1993;150: 1518-20. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: Silvia81mdc@hotmail.com
(S. Álvarez Bandrés).
Recibido: 15 de enero de 2008
Aceptado: 20 de abril de 2008














