Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.25 no.4 Madrid jul./ago. 2010
Influencia de la grasa de la dieta en el metabolismo glucídico de mujeres obesas con el genotipo Pro12Pro en el gen PPARgama2
Influence of fat diet in glicidic metabolism in obese women with PRO12PRO genotype in PPARgamma2 gene
V. Chaia Kaippert1, E. Lopes Rosado1, G. Rosa1, E. M.a Morais Oliveira2, S. Kimi Uehara1, C. Lima D'Andrea1, J. Nogueira1 y M. Fofano do Lago1
1 Instituto de Nutrição Josué de Castro (INJC) da Universidade Federal do Rio de Janeiro (UFRJ). Brasil.
2Embrapa (Empresa Brasileira de Pesquisa Agropecuária) Agroindústria de Alimentos. Rio de Janeiro, Brasil.
Dirección para correspondencia
RESUMEN
Introducción: El receptor activado por proliferadores de peroxisomas (PPARγ2) es un factor de transcripción adipogénico que influye en la resistencia a la insulina (RI) en la presencia de agonistas como los ácidos grasos poliinsaturados (AGPI).
Objetivo: Evaluar la influencia de la grasa de la dieta en el metabolismo glucídico de mujeres con obesidad mórbida y con el genotipo Pro12Pro en el gen PPARγ2.
Métodos: Fueron seleccionadas 25 mujeres con genotipo Pro12Pro. La ingesta habitual de lípidos fue estimada por registros alimentarios, siendo utilizada para la división de los grupos, GA (hasta un 30% del valor energético total (VET)) y GB (por encima de un 30% del VET). Fueron realizadas evaluaciones bioquímicas y antropométricas en ayuno, siguiendo la comida test rica en AGPI n-6 y los análisis bioquímicos postprandiales en GA y GB. La RI y la sensibilidad a la insulina (SI) fueron evaluadas por HOMA-IR (Homeostasis Model Assessment) y QUICKI (Quantitative Insulin Sensitivity Check Index), respectivamente.
Resultados y discusión: GA presentó HOMA-IR y QUICKI normales. GB presentó el índice de masa corporal (IMC), HOMA-IR, ingesta de ácidos grasos saturados (AGS) y monoinsaturados (AGMI) superiores a GA (p < 0,05). En GB, los AGMI se correlacionaron negativamente con HOMA-IR, glucosa e insulina en ayuno, y positivamente con QUICKI. Los lípidios totales y AGS contribuyeron al aumento de la masa corporal y RI. Sin embargo, los AGMI parecen reducir el impacto de la dieta hiperlipídica en el metabolismo glucídico. Se propone que mujeres obesas con el genotipo Pro12Pro en el gen PPARγ2 eviten dietas ricas en lípidos y AGS, priorizando AGMI para el control de la obesidad y mejora de la SI.
Palabras clave: Obesidad mórbida. Resistencia a la insulina. PPARγ2. Lípidos dietéticos.
ABSTRACT
Introduction: The peroxisome proliferator-activated receptor gamma 2 (PPARγ2) is an adipogenic transcription factor that influences in insulin resistance (IR) in the presence of agonists such as polyunsaturated fatty acids (PUFA).
Objective: Evaluate the influence of dietary fat in glicidic metabolism in morbidly obese women with Pro12Pro genotype in the gene PPARγ2.
Methods: Were selected 25 women with genotype Pro12Pro. The fat intake was estimated by food records, being used for the division of groups, GA (until 30% of the total energy expenditure (TEE)) and GB (greater than 30% of the TEE). Biochemical and anthropometric evaluations were conducted in fasting, following the test meal high in n-6 PUFA and postprandial biochemical evaluations. IR and insulin sensitivity (IS) were assessed by HOMA-IR (Homeostasis Model Assessment) and QUICKI (Quantitative Insulin Sensitivity Check Index), respectively.
Results and discussion: GA presented normal HOMAIR and QUICKI. GB presented higher body mass index (BMI), HOMA-IR, saturated fatty acids (SFA) and monounsaturated (MUFA) intake higher, compared with GA (p < 0.05). In GA, the MUFA intake was negatively correlated with HOMA-IR, fasting glucose and insulin, and positively with QUICKI. The fat and SFA intake contributed to the increase in body mass and IR. However, MUFA intake may have reduced the impact of high fat diet in glicidic metabolism. It is suggested that obese women with Pro12Pro genotype in the PPARγ2 gene avoid high fat and SFA diets, prioritizing MUFA for controlling obesity and improving the IS.
Key words: Morbidly obesity. Insulin resistance. PPARγ2. Dietary fats.
Introducción
La obesidad es un enfermedad considerada epidemia mundial, que satura los servicios de salud con el aumento de la demanda de recursos para el tratamiento de otras enfermedades crónicas no transmisibles, como la diabetes mellitus tipo 2, hipertensión arterial sistémica, enfermedades coronarias, entre otras, asociadas a la obesidad1.
Factores relacionados al estilo de vida, tales como la dieta y el ejercicio físico, los cambios neuroendocrinos, además del componente hereditario, están involucrados en el génesis de la obesidad2.
Las formas mas comunes de obesidad son de origen poligénica, además, implican interacciones complejas entre diferentes genes y entre genes y los factores ambientales, llevando a fenotipos de obesidad multifactoriales3.
La obesidad, especialmente a nivel visceral, está directamente relacionada con la resistencia a la insulina (RI), que se caracteriza por la disminución de la eficiencia de esta hormona en estimular la captación de la glucosa en el músculo esquelético y tejido adiposo, lo que puede predisponer el individuo obeso a una serie de enfermedades crónicas no transmisibles1. En este contexto, estudios han puesto de manifiesto el papel importante de los receptores activados por la proliferación de peroxisomas de la isoforma γ y serie2 (PPARγ2)3 como factores de transcripción adipogénicos3,4 que pueden actuar en la mejoría de la sensibilidad a la insulina (SI)5.
Para que el PPARγ2 tenga su función en los genes diana, debe ser activado por ligantes naturales, como los ácidos grasos poliinsaturados (AGPI) de cadena larga, derivados de eicosanoides y lípidos oxidados, o agonistas sintéticos como los hipolipemiantes y antidiabéticos4.
La activación del PPARγ2 se asocia con la expresión de enzimas involucradas con la captura y el transporte de ácidos grasos, conllevando a un aumento de la adipogénesis y reducción de las concentraciones plasmáticas de ácidos grasos libres. Por lo tanto, hay reducción del deposito de grasa en el hígado y tejido muscular, aumentando la SI en estos tejidos6.
En los últimos años, se han identificado variantes genéticas del PPARγ2, entre los cuales destaca el polimorfismo Pro12Ala, el cual es frecuente en poblaciones caucasianas (entre el 12 y el 14%)7. Todavía, los estudios no son conclusivos en cuanto el efecto del polimorfismo del PPARγ2 en la obesidad3,5,7,8. Se sugiere que el alelo Ala se asocia con menor índice de masa corporal (IMC) y aumento de la SI, lo que refleja menor actividad transcripcional del receptor5. Como lo demuestra Robitaille y cols.8, los individuos homocigotos Pro12Pro parecen ser más sensibles a diferentes estímulos ambientales, especialmente a la ingesta de lípidos.
Aunque los factores genéticos presenten fuerte influencia sobre el desarrollo de la RI, la dieta y el estilo de vida tienen un importante papel en su etiología9. En este contexto, los factores nutricionales, especialmente la alta ingesta de grasa, afectan la SI, independiente de sus efectos sobre el peso corporal10.
Los ácidos grasos saturados (AGS) contribuyen al exceso de peso corporal debido a la baja capacidad oxidativa y al aumento de la expresión de genes implicados en la proliferación de los adipocitos, estando además directamente relacionados con el desarrollo de la RI.
Por el contrario, los ácidos grasos insaturados promueven la SI11. Sin embargo, considerando el genotipo del sujeto en relación al PPARγ2, hay que considerar el tipo de ácido graso insaturado a ser prescrito12.
El presente estudio tuvo como objetivo evaluar la influencia de los lípidos dietéticos en la RI, insulinemia y glucemia de mujeres con obesidad mórbida con el genotipo Pro12Pro en el gen PPARγ2.
Métodos
Población
Se ha realizado un ensayo clínico, no randomizado y no controlado en 25 mujeres adultas (22 a 48 años) con obesidad mórbida.
El protocolo (no 116/05) del estudio fue aprobado por el Comité de Ética en Investigación (CEP) del Hospital Universitário Clementino Fraga Filho (HUCFF) de la Universidad Federal de Rio de Janeiro (UFRJ).
Los criterios de inclusión fueron mujeres adultas con historia familiar de obesidad, no menopáusicas, con IMC igual o superior a 40 kg/m2,13. Fueron excluidas del estudio las mujeres fumadoras, con diagnóstico previo de enfermedad renal crónica, enfermedades infecciosas, diabetes mellitus y/o otras enfermedades crónicas no transmisibles, embarazo, lactancia, con uso de medicamentos para pérdida de peso y/o hipolipemiantes, dieta especial, o que presentaron pérdida de peso por encima de 3 kg en el último mes.
Diseño del estudio
La evaluación de la ingesta habitual de grasa fue hecha para la división de los grupos, siendo: GA, con ingesta de grasa hasta un 30% del valor energético total (VET) (n = 5), y GB, con ingesta de lípidos por encima de un 30% del VET (n = 20).
Para la evaluación del efecto agudo de la comida test rica en AGPI n-6, se hizo un ensayo clínico. Las mujeres se presentaron al Laboratorio de Análisis Clínicas de la Facultad de Farmacía (LACFAR) de la UFRJ a las 7 h, tras ayuno de 12 horas, para recoger la sangre destinada a las evaluaciones bioquímicas (colesterol total y sus fracciones, triglicéridos, glucosa e insulina) y moleculares (genotipaje del gen PPARγ2), siguiendo la evaluación antropométrica.
La comida test fue administrada vía oral. A los 60 y 120 minutos tras la ingesta de la comida fueron recogidas muestras de sangre para la evaluación de las concentraciones de glucosa plasmática e insulina sérica postprandiales.
Evaluación de la ingesta habitual de grasa
La ingesta habitual de grasa fue estimada por medio de registros alimentarios de tres días alternos, siendo dos días típicos y un atípico, antes del ensayo clínico. El análisis de la composición de la dieta fue hecha por el programa computacional Food Processor versión 12 (Esha Research, Salem, EUA, 1984), después del ajuste de los alimentos consumidos por la población brasileña.
Análisis bioquímicos
Todos los parámetros bioquímicos fueron evaluados en el LACFAR, excepto la insulina sérica, que fue evaluada en el laboratório de APAE (Associação dos Pais e Amigos dos Excepcionais).
Para el colesterol total, HDL-colesterol y triglicéridos séricos se utilizaron kits comerciales COLESTEROL Liquiform (Labtest Diagnóstica S.A., Brasil), COLESTEROL HDL (Labtest Diagnóstica S.A., Brasil) y TRIGLICÉRIDES Liquiform (Labtest Diagnóstica S.A., Brasil), respectivamente.
Las concentraciones séricas de LDL-colesterol y de VLDL-colesterol fueron determinadas por la fórmula de Friedwald y cols.14.
Los valores de normalidad utilizados para los triglicéridos, colesterol total, HDL-colesterol y LDL-colesterol fueron < 150 mg/dL, < 200 mg/dL, > 60 mg/dL y < 130 mg/dL, respectivamente15.
La glucosa plasmática fue evaluada utilizándose el kit comercial GLICOSE PAP Liquiform (Labtest Diagnóstica S.A., Brasil). Valores de glucosa por abajo de un 100 mg/dL fueron considerados normales, según la Asociación Americana de Diabetes16.
La determinación de la insulina sérica fue hecha por la técnica de radioimunoensaio (RIA), utilizándose la insulina COAT-A-COUNT® (Diagnostic Products Corporation®, USA).
Las mujeres fueron classificadas como normoinsulinémicas, cuando la insulina en ayuno estuvo por debajo de 9 mU/mL, o hiperinsulinémicas, cuando la insulina en ayuno estuvo por encima de 9 mU/mL17.
La RI fue estimada utilizándose el cálculo de HOMA-IR (Homeostasis Model Assessment) según Matthews y cols.18. Se consideró RI valores de HOMAIR ≥ 2,7119.
Fue utilizado el cálculo de QUICKI (Quantitative Insulin Sensitivity Check Index) para evaluar la SI, según Katz y cols.20. Fueron adecuados los valores de QUICKI por encima de 0,3321.
Evaluación antropométrica
Se consideraron las variables de peso corporal y altura para seleccionar las mujeres con IMC igual o superior a 40 kg/m2 y calcular el VET de la comida test. La circunferencia de la cintura (CC) también fue determinada.
El peso y la altura corporal fueron medidos utilizándose balanza antropométrica digital mecánica (Filizola®) con precisión de 100 g y capacidad máxima de 150 kg y antropómetro con escala de 0,1 cm, respectivamente. Las mujeres fueron evaluadas con mínimo de ropas posible y sin zapatos. El IMC fue calculado utilizándose el peso e la estatura al cuadrado22.
La CC fue obtenida con cinta inextensible e inelástica, siendo medida en el punto medio entre la última costilla y la cresta ilíaca23.
Evaluación del genotipo del PPARγ2
Los análisis moleculares fueron hechos en el Laboratorio de Bioquímica y Biología Molecular del Schistosoma mansoni de la UFRJ.
Las muestras de DNA genómico fueron aisladas a partir de muestras de sangre integral utilizándose kit comercial (MasterPureTM Genomic DNA Purification Kit, EPICENTRE® Biotechnologies) y almazenadas a -20 oC hasta la amplificación del DNA, la cual fue hecha por medio de la técnica de PCR (reacción en cadena de la DNA polimerasa), siendo utilizado un par de iniciadores: sense (5'- GCC AAT TCA AGC CCA GTC - 3') e antisense (5'- GCC ATG TTT GCA GAC AGT GTA TCA GTG AAG GAA TCG CTT TCC G - 3')24.
Las condiciones de amplificação del PPAR?2 y detección del alelo Pro12Pro fueron realizadas de acuerdo con Rosado y cols.12.
Elaboración de la comida test
El gasto energético total de las mujeres fue estimado según la FAO/OMS25. El valor calórico de la comida test fue equivalente a un desayuno (15 a 20% del VET), siendo normoglicídica, normoproteica y normolipídica, conteniendo aproximadamente un 15% de AGPI (media de un 88,6% y 11,4% de AGPI n-6 y n-3, respectivamente), alrededor de un 10% de ácidos grasos monoinsaturados (AGMI) y menos de un 10% de AGS. La cantidad de macronutrientes de la comida test fue basada en las recomendaciones para sujetos eutróficos (abajo de un 10% del VET de AGS y AGPI, y entre un 10 y 15 % del VET de AGMI)15.
La comida test fue compuesta por tarta de zanahoria sin crema, tostadas de pan franceé, queso blanco con aceite de soja y leche sin grasa. La composición nutricional de la comida test fue de 511,2 ± 50,4 kcal, siendo un 50,0 ± 0,6% de hidratos de carbono, un 19,0 ± 1,7% de proteínas, un 35,1 ± 0,5% de lípidos, un 14,6 ± 0,5% de AGPI, un 9,3 ± 0,2% de AGMI, un 9,2 ± 0,4% de AGS y un 5.485,9 ± 871,4 UI de vitamina A. El análisis de la composición química de las comidas test fue hecha en el programa computacional Food Processor versión 12 (Esha Research, Salem, EUA, 1984).
Análisis estadístico
El análisis estadístico fue utilizado el programa computacional SPSS versión 11.0, siendo considerados significativos los valores de p < 0,05.
Para la verificación de la distribución de las variables continuas de interés (clínicas1, antropométricas2 y bioquímicas3) fue realizado el test de adherencia de Kolmogorov-Smirnov (1: edad; 2: peso corporal, IMC y CC; 3: insulina sérica y glucosa plasmática, triglicéridos, colesterol total y fracciones (HDL-colesterol, LDL-colesterol y VLDL-colesterol) y valores de HOMA-IR y QUICKI).
Para la comparación entre las medias de los grupos fueron calculadas las estadísticas básicas de posición (media) y dispersión (desviación estándar).
Como las variables continuas presentaron distribución normal, se utilizó la prueba paramétrica t-Student para las comparaciones entre grupos y la correlación de pearson para los análisis entre las variables dietéticas y bioquímicas.
Resultados
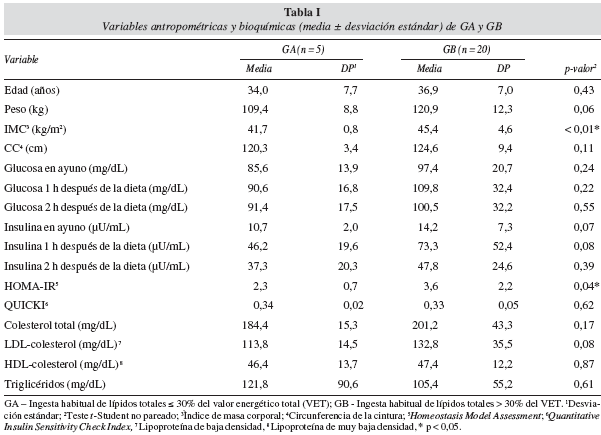
En la tabla I son presentadas las características antropométricas y bioquímicas de GA y GB. Las mujeres con alta ingesta de lípidos en la dieta habitual (GB) presentaron mayor IMC y HOMA-IR (p < 0,05), comparadas con GA. Solamente GB presentó RI, según HOMA-IR (HOMA-IR > 2,71)19. Los dos grupos presentaron SI adecuada, según QUICKI. Ambos grupos presentaron acumulación excesiva de grasa abdominal, verificada por la CC26. Con relación al perfil lipídico en sangre, ambos grupos presentaron valores normales de triglicéridos y bajas concentraciones de HDL-colesterol15. GB presentó el colesterol total y LDL-colesterol séricos próximos a los límites de normalidad (201,2 ± 43,3 mg/dL y 132,8 ± 35,5 mg/dL, respectivamente).
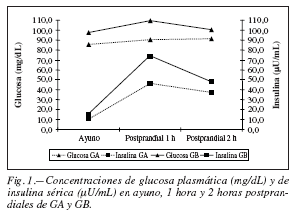
Las variaciones en las concentraciones de glucosa e insulina antes y después de la comida test en GA y GB pueden ser observadas en la figura 1. GA y GB presentaron la glucosa en ayuno normal16, y la insulina en ayuno por encima de la recomendación17. Sin embargo, GB presentó glucosa plasmática e insulina sérica superior en todos los tiempos evaluados después de la comida test.
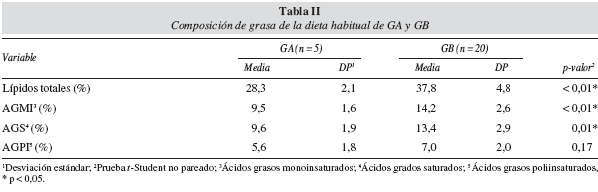
En relación a la cantidad de grasa ingerida, GB presentó mayor ingesta de AGS (p < 0,05) y monoinsaturados (AGMI) (p < 0,05), comparado con GA. No hubo diferencia (p > 0,05) de la ingesta de AGPI entre los grupos (tabla II).
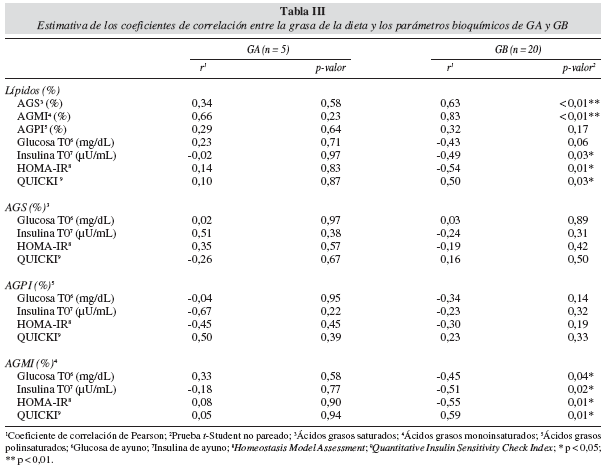
En GB, la ingesta habitual de lípidos (%) se correlacionó positivamente con la ingesta habitual de AGS y AGMI (r = 0,63 y 0,83, respectivamente, p < 0,05) y con QUICKI (r = 0,50, p < 0,05) y, negativamente con la insulina de ayuno (r = - 0,49, p < 0,05) y el HOMA-IR (r = -0,54, p < 0,05). La ingesta de AGS no se correlacionó con estos parámetros. La ingesta de AGMI se correlacionó negativamente con las concentraciones de glucosa plasmática (r = -0,45, p < 0,05), de insulina sérica de ayuno (r = -0,51, p < 0,05) y HOMA-IR (r = -0,55, p < 0,05), y positivamente con QUICKI (r = 0,59, p < 0,05) (tabla III). En GA, no fueron observadas correlaciones (p > 0,05) entre el perfil lipídico de la dieta y los parámetros bioquímicos.
Discusión
La obesidad es considerada uno de los problemas más graves de salud pública en la actualidad y su prevalencia aumenta acentuadamente en todo el mundo1. Es una enfermedad compleja y de etiología multifactorial. En este sentido se hace importante destacar las interaciones entre los genes y el ambiente2.
A pesar del avance en los estudios que buscan evaluar nuevas alternativas para la prevención y el tratamiento de la obesidad, estudios con obesidad mórbida todavía son raros debido a las dificultades, principalmente en lo que se refiere a las limitaciones físicas de estos individuos, lo que limita estudios con grandes muestras.
Los factores de trascripción que regulan el adipogénesis, como el receptor nuclear PPARγ son destacados3,4. Además, ligantes del PPARγ tienen demostrado excelente actividad antidiabética, aunque gran parte de este factor de transcripción sea expreso en el tejido graso y no en el tejido muscular27.
Las informaciones a cerca del tipo de AGPI más potente para la ativación del PPARγ son escasas, ya que en la mayoría de los estudios no se hace la distinción cuanto al tipo de AGPI utilizado por los sujetos. Pocos estudios evaluaron los efectos de diferentes tipos de AGPI en la expresión del gen28.
En estudio realizado por Spurlock y cols.28, los animales que recibieron dieta suplementada con aceite de azafrán (alrededor de un 80% de ácido linoleico - 18:2 n-6) presentaron niveles de mRNA del PPARγ2 cuatro veces mayor en relación al grupo control.
Además de la adiposidad y de la predisposición genética, los factores dietéticos, especialmente la alta ingesta de lípidos, están asociados con la patogénesis de la RI10.
La SI también es afectada por la calidad de los lípidos de la dieta, independiente de sus efectos en el peso corporal. Los AGS están asociados con intolerancia a la glucosa, pero los lípidos insaturadas mejoran la respuesta a la insulina11.
Las ventajas de los AGPI en la SI resultan en modificaciones en la composición de las membranas celulares29, alteraciones en la producción de adipocinas como el factor de necrose tumoral-α (TNF-α) y adiponectina30, además del control de la transcripción de genes específicos, incluyendo aquellos involucrados en el metabolismo lipídico y de la glucosa, como el PPARγ228,29.
Los resultados observados en el presente estudio demuestran claramente el efecto del exceso de la grasa dietética en el peso corporal y en la RI, ya que GB, con ingesta de lípidos por encima de un 30% del VET, presentó mayor IMC y RI, al contrario de GA, que tuvo menor IMC y no presentó RI (HOMA-IR = 2,3)19. Sin embargo, la estimativa de la SI no demonstró diferencia entre los grupos (p > 0,05). El factor ambiental tuvo fuerte influencia en los parámetros evaluados, principalmente el IMC y la RI.
GA y GB presentaron insulina de ayuno por encima de 9 mU/mL, indicando estado de hiperinsulinemia, según Sánchez-Margalet y cols.17. A pesar de no ser significativo (p > 0,05), se resalta que GB presentó insulina de ayuno superior, comparado con GA (14,2 ± 7,3 mU/mL vs. 10,7 ± 2,0 mU/mL, en GB y GA, respectivamente).
Se hace hincapié que el tipo de ácido graso consumido, independiente de la cantidad del mismo, presenta influencia en el peso corporal, perfil lipídico y RI. En GB, además de la ingesta excesiva de lípidos, se sugiere que el alto consumo de AGS (13,4% en GB, versus 9,6% en GA, p < 0,05) influyó en la RI y aumento de la masa corporal.
Como se destaca por algunos autores, los AGS tienen menos efecto sobre la saciedad31, son poco oxidados para generar energía y se almacenan, son difícilmente movilizados por estímulo lipolítico y aumentan la expresión de los genes asociados con la proliferación de los adipocitos, siendo fortemente relacionados con el desarrollo de la obesidad y de la RI9, 11.
Con el fin de analizar los efectos de la ingesta de AGPI n-6, ligante natural del PPARγ2, en las concentraciones de glucosa e insulina posprandiales, se ofreció un desayuno con aproximadamente un 15% del VET de este tipo de lípido. A pesar de no significativo (p > 0,05), GB presentó glucosa plasmática e insulina sérica de ayuno y postprandial superiores a GA. Además, se observó mayor HOMA-IR (p < 0,05) en este grupo, lo que demuestra que las mujeres que consumian habitualmente mayor percentual de lípidos presentaban menor SI, independiente de la comida test, ya que la misma fue igual para los dos grupos.
Considerando el genotipo Pro12Pro en el gen PPAR?2, la literatura científica demuestra que la ativación del gen por ligantes se asocia al aumento del almacenamiento de grasa por los adipocitos y, consecuentemente, menores concentraciones de ácidos grasos libres plasmáticos. De esta manera, ocurre menor deposición de grasa y menor efecto tóxico de las mismas en el hígado y tejido muscular, proporcionando aumento en la SI en estos tejidos8.
Teniendo en cuenta que todas las mujeres presentaban el genotipo Pro12Pro y que no hubo diferencia en la ingesta de AGPI (ligante del PPARγ2) entre los grupos, se puede sugerir que las concentraciones elevadas de glucosa e insulina, además de la RI y mayor IMC en GB, pueden resultar de la elevada ingesta habitual de lípidos y de AGS (factores ambientales).
Según Rosado y cols.12, sujetos con el genotipo Pro12Pro deben controlar la ingesta de grasas totales y AGS, probablemente debido a la baja capacidad de oxidación de los mismos, en contraste, sujetos con el alelo Ala en el gen PPARγ2 demuestran aumento en la oxidación de grasas, evaluada por calorimetría indirecta. Además, la presencia del alelo variante en el gen sugiere beneficios en el control de la ingesta de alimentos y facilidad en la pérdida de peso por medio de una dieta rica en lípidos32.
Robitaille y cols.8 resaltaron que aunque los AGPI sean considerados los ligantes naturales preferenciales del PPARγ2, los AGS también son capaces de promover la activación del gen, pero en menor extensión. Por lo tanto, el aumento en la ingesta de lípidos totales y AGS puede favorecer la ligación del PPARγ al elemento responsivo (PPRE) de genes diana involucrados en el adipogénesis.
En sujetos con el alelo Ala12, el aumento de la ingesta de ácidos grasos tendría poco o ningún efecto en el lipogénesis debido a la baja afinidad de ligación del complejo ácido graso-PPARγ con el elemento responsivo a proliferadores de peroxisomas (PPRE) de los genes diana. De acuerdo con Deeb y cols.5, la isoforma Ala puede resultar en estímulo menos eficaz de los genes diana del PPARγ y predisponer al menor acúmulo de tejido graso, lo que puede resultar en aumento de la SI.
Considerándose que el genotipo del PPARγ2 influye en su actividad y, consecuentemente, en el peso corporal y la RI, el presente estudio tuvo como objetivo garantizar que todas las mujeres seleccionadas presentaban el genotipo Pro12Pro.
El análisis de correlación demostró que las mujeres que consumian lípidos totales por encima de las recomendaciones (GB), priorizaban los AGS y AGMI. Teniéndose en cuenta la fuerte correlación positiva y significativa entre la ingesta de lípidos y de AGMI (r = 0,83, p < 0,05) y entre los AGMI y QUICKI (r = 0,59, p < 0,05) en GB, es probable que este tipo de lípido tendría reducido el impacto de la dieta hiperlipídica en la RI.
Posiblemente, estos efectos no se han detectado en GA, debido a la reducida ingesta habitual de AGMI, comparado con GB (9,5% vs. 14,2%, p < 0,05) (tabla II). Cabe señalar que, de acuerdo con las recomendaciones nutricionales del Consenso Latinoamericano sobre Obesidad33, la ingesta de AGMI debe ser igual a un 13% del VET para obesos.
Confirmando los datos anteriores, en GB, la ingesta habitual de AGMI se correlacionó negativamente con las concentraciones de glucosa e insulina de ayuno y con HOMA-IR, lo que refuerza el papel de este tipo de lípido en la mejora de la SI.
Se observó que después de la ingesta de la comida test rica en AGPI n-6, los grupos presentaron glucosa postprandial normal (< 140 mg/dL)16, pero GB presentó mayor secreción de insulina (1 hora y 2 horas postprandiales) para mantener el control glucémico.
GA y GB presentaron ingestas de 5,6 ± 1,8% y 7,0 ± 2,0% de AGPI en relación al VET (p > 0,05), respectivamente, estando en conformidad con las recomendaciones para sujetos obesos (abajo de un 10% del VET)33.
En este estudio, la ingesta habitual de AGPI no se correlacionó con el metabolismo glucídico y RI (glucosa, insulina y HOMA-IR). Quizás, si la ingesta de este tipo de lípido fuera mayor, entre el 10 y 15% del VET, tal como se propone en la comida test, podríamos verificar efectos positivos del mismo en la SI.
Cabe señalar que el tipo de AGPI más ingerido por la población brasileña es el AGPI n-6, ya que las principales fuentes de este ácido graso son las grasas vegetales (margarina, aceite de soja, maíz y girasol). Sin embargo, hay baja ingesta de AGPI n-3, los cuales están presentes en peces de agua fría34.
Estudios citados anteriormente señalan que los resultados controversos observados en algunos trabajos se pueden atribuir a diversos aspectos como la heterogeneidad de las poblaciones estudiadas, tales como los fenotipos clínicos de delgadez y obesidad; el tipo de estudio; la composición lipídica de la dieta; interacciones entre genes o entre gen y ambiente, entre otros. En nuestro estudio, hemos controlado algunos de los factores mencionados anteriormente, ya que la población es homogénea, pues solamente estudiamos mujeres con obesidad mórbida sin el variante Ala en el gen, con características físicas, bioquímicas y clínicas semejantes. Además, fue evaluada la ingesta habitual de lípidos y la interacción entre gen y ambiente.
Es esencial llevar a cabo estudios que evaluen los efectos de los AGPI, con distinción entre n-3 y n-6, además del análisis de otros genes candidatos a la obesidad. También es importante la asociación de los genes con factores ambientales, particularmente dietéticos. Hacemos hincapié que el gen evaluado en el presente estudio, asi como otros relacionados con la obesidad, pueden ser regulados nutricionalmente, lo que refuerza la necesidad de investigaciones que consideren los análisis de expresión génica, lo que permitirán otras conclusiones en relación a las interacciones entre genes y nutrientes.
En conclusión, la ingesta excesiva de lípidos y de AGS contribuye para la adiposidad y RI. Sin embargo, la ingesta de AGMI puede reducir el impacto de la comida test rica en lípidos en el metabolismo glucídico. En este sentido, se sugiere que mujeres con el genotipo salvaje en el gen PPARγ2 eviten la ingesta excesiva de lípidos (por encima de un 30% del VET), en particular de AGS, priorizando la ingesta de grasas no saturadas, especialmente AGMI, con el fin de evitar la ganancia de peso corporal y mejorar la SI.
Agradecimientos
A las mujeres que participaron del estudio. A los profesores Franklin D. Rumjanek y Marcelo R. Fantappié, Nívea Amoedo y otros colaboradores del Laboratório de Bioquímica e Biologia Molecular do Schistosoma mansoni de la UFRJ; a Dra. Maria de Fátima Santos de Oliveira y otros profesionales de la APAE - Tijuca/RJ; al profesor Marcos Fleury del Laboratório de Análises Clínicas (LACFAR) de la Facultad de Farmacía/UFRJ; a Dra Iva Marques Lopes, por la revisión del español.
Apoyo: CNPq (Conselho Nacional de Desenvolvimento Científico e Tecnológico) y FAPERJ (Fundação Carlos Chagas Filho de Amparo à Pesquisa do Estado do Rio de Janeiro).
Referencias
1. Diretrizes Brasileiras de Obesidade, Associação Brasileira para o Estudo da Obesidade e da Síndrome Metabólica, 2007. [ Links ]
2. Marques-Lopes I, Marti A, Moreno-Aliaga MJ, Martinez A. Aspectos genéticos da obesidade. Rev Nutr 2004;17 (3): 327-38. [ Links ]
3. Cecil JE, Watt P, Palmer CN, Hetherington M. Energy balance and food intake: The role of PPARg gene polymorphisms. Physiol Behav 2006; 88: 227-33. [ Links ]
4. Kersten S, Desvergne B, Wahli W. Roles of PPARs in health and diseases. Nature 2000; 405 (25): 421-4. [ Links ]
5. Deeb SS, Fajas L, Nemoto M, Pihlajamäki J, Mykkänen L, Kuusisto J y cols. Pro12Ala substitution in PPARy2 associated with decrease receptor activity, lower body mass index and improved insulin sensitivity. Nat Genet 1998; 20: 284-7. [ Links ]
6. Anaya COM, Ariza IDS. Avances en obesidad. Rev Fac Med Univ Nac Colomb 2004; 52 (4): 270-86. [ Links ]
7. Buzzetti R, Petrone A, Ribaudo MC, Alemanno I, Zavarella S, Mein CA y cols. The common PPAR-g2 Pro12Ala variant is associated with greater insulin sensitivity. Eur J Hum Genet 2004; 12: 1050-4. [ Links ]
8. Robitaille J, Després J-P, Pérusse L, Vohl M-C. The PPARgamma P12A polymorphism modulates the relationship between dietary fat intake and components of the metabolic syndrome: results from the Québec Family Study. Clin Genet 2003; 63: 109-16. [ Links ]
9. Saravanan N, Haseeb A, Ehtesham NZ, Ghafoorunissa. Diferencial efetua de dietético saturou e ácidos trans-gordurosos em expressão de genes associada com sensibilidade de insulina em rato tecido gorduroso. Eur J Endocrinol 2005; 153: 159-65. [ Links ]
10. Bisschop PH, Metz J, Ackermans MT, Endert E, Pijl H, Kuipers F y cols. A. Dietary fat content alters insulin-mediated glucose metabolism in healthy men. Am J Clin Nutr 2001; 73: 554-9. [ Links ]
11. Storlien LH, Higgins JA, Thomas TC, Brown MA, Wang HQ, Huang XF y cols. Diet composition and insulin action in animal models. Br J Nutr 2000; 83 (Supl. 1): S85-90. [ Links ]
12. Rosado EL, Bressan J, Hernández JAM, Martins MF, Cecon PR. Efecto de la dieta y de los genes PPARg2 y b2-adrenérgico en el metabolismo energético y en la composición corporal de mujeres obesas. Nutr Hosp 2006; 21 (3): 317-31. [ Links ]
13. World Health Organization (WHO). Obesity: prevention and managing the global epidemic. Geneva, 1998. [ Links ]
14. Friedwald WT, Levy RI, Fredrickson DS. Estimation of the concentration of low-density lipoprotein cholesterol in plasma, without use of the preparative ultracentrifuge. Clin Chem 1972; 18: 499-502. [ Links ]
15. III Diretrizes Brasileiras sobre Dislipidemias e Diretriz de Prevenção da Aterosclerose do Departamento de Aterosclerose da Sociedade Brasileira de Cardiologia. Arq Bras Cardiol 2001; 77 (Supl. III): 1-48. [ Links ]
16. American Diabetes Association (ADA). Diagnosis and classification of Diabetes Mellitus. Diabetes Care 2007; 30 (Supl. I): S42-S47. [ Links ]
17. Sánchez-Margalet V, Valle M, Ruz FJ, Gascón F, Mateo J, Goberna R. Elevated plasma total homocysteine levels in hyperinsulinemic obese subjects. J Nutr Biochem 2002; 13: 75-9. [ Links ]
18. Matthews DR, Hosker JP, Rudenski BA, Naylor DF, Treacher DF, Turner RC. Homeostasis model assessment: insulin resistance and ?-cell function from fasting plasma glucose and insulin concentrations in man. Diabetologia 1985; 28: 412-9. [ Links ]
19. Geloneze B, Geloneze SR, Ermetice MN, Repetto EM, Tambascia MA. The threshold value for insulin resistance (HOMAIR) in an admixtured population. IR in the Brazilian Metabolic Syndrome Study. Diabetes Res Clin Pract 2006; 72 (2): 219-20. [ Links ]
20. Katz A, Nambi SS, Mather K, Baron AD, Follmann DA, Sullivan G y cols. Quantitative insulin sensitivity check index: a simple, accurate method for assessing insulin sensitivity in humans. J Clin Endocrinol Metab 2000; 85 (7): 2402-10. [ Links ]
21. Bonneau GA, Rascon CMS, Pedrozo WR, Ceballos B, Leiva R, Blanco N y cols. Presencia de insulinorresistencia en Síndrome metabólico. Rev Argent Endocrinol Metab 2006; 43: 215-23. [ Links ]
22. World Health Organization (WHO). Physical Status: the use and interpretation of anthropometry. Technical report series 854, pp. 1-452, Geneva, 1995. [ Links ]
23. World Health Organization (WHO). Measuring obesity-classification and description of anthropometric data. Report of a WHO Regional Office Consultation on the Epidemiology of Obesity. Copenhagen, Denmark: WHO Regional Office for Europe, Nutrition Unit. (Document EUR/ICP/NUT 125), 1988. [ Links ]
24. Gen Bank DNA. AB005520. Homo sapiens ppar [gi:2605488]. www.ncbi.nlm.nih.gov/genbank. Acesso em 24/01/2003. [ Links ]
25. Organización Mundial De La Salud (OMS). Necesidades de energía y de proteínas. Informe de una Reunión Consultiva Conjunta FAO/OMS/UNU de Expertos. Ginebra, 1985. [ Links ]
26. The International Federation of Diabetes (IDF) consensus worldwide definition of the metabolic syndrome. International Diabetes Federation, 2005. [ Links ]
27. Rosen ED, Macdougald OA. Adipocyte differentiation from the inside out. Nat Rev 2006; 7: 885-96. [ Links ]
28. Spurlock ME, Houseknecht KL, Portocarrero CP, Cornelius SG, Willis GM, Bidwell CA. Regulation of PPARg but not obese gene expression by dietary fat supplementation. J Nutr Biochem 2000; 11: 260-6. [ Links ]
29. Lombardo YB, Chicco AG. Effects of dietary polynsaturated n-3 fatty acids on dyslipidemia and insulin resistance in rodents and humans. A review. J Nutr Biochem 2006; 17: 1-13. [ Links ]
30. Flachs P, Mohamed-Ali V, Horakova O, Rossmeisl M, Hosseinzadeh-Attar MJ, Hensler M y cols. Polyunsaturated fatty acids of marine origin induce adiponectin in mice fed a high-fat diet. Diabetologia 2006; 49 (2): 394-7. [ Links ]
31. Lawton CL, Delargy HJ, Brockman J, Smith FC, Blundell JE. The degree of saturation of fatty acids influences post-ingestive satiety. Br J Nutr 2000; 83: 473-82. [ Links ]
32. Rosado EL, Bressan J, Martins MF, Cecon PR, Martínez JA. Polymorphism in the PPARgamma2 and beta2-adrenergic genes and diet lipid effects on body composition, energy expenditure and eating behavior of obese women. Appetite 2007; 49 (3): 635-43. [ Links ]
33. Documento do Consenso Latino-Americano sobre Obesidade, Ministério da Saúde, 1999. [ Links ]
34. Tabela Brasileira de Composição de Alimentos (TACO) / NEPA (Núcleo de Estudos e Pesquisa em Alimentação) - UNICAMP (Universidade Estadual de Campinas). Versão II. 2.ed. Campinas: SP: NEPA-UNICAMP, 2006. 113 p. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Eliane Lopes Rosado.
Universidade Federal do Rio de Janeiro.
Centro de Ciências da Saúde. Instituto de Nutrição Josué de Castro.
Departamento de Nutrição e Dietética.
Avda. Brigadeiro Trompovisky, s/n, Bloco J, 2o andar, sala 24.
CEP: 21949-900 Brasil.
E-mail: elianerosado@nutricao.ufrj.br / vanessachaia@uol.com.br
Recibido: 30-IV-2009.
Revisado: 29-VII-2009.
Aceptado: 18-VIII-2009.