Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.28 no.3 Madrid may./jun. 2013
https://dx.doi.org/10.3305/nh.2013.28.3.6355
Estrés oxidativo; estudio comparativo entre un grupo de población normal y un grupo de población obesa mórbida
Oxidative stress; a comparative study between normal and morbid obesity group population
Leonardo De Tursi Ríspoli1, Antonio Vázquez Tarragón2, Antonio Vázquez Prado1, Guillermo Sáez Tormo (CIBEROBN)3, Ali Mahmoud Ismail1 y Verónica Gumbau Puchol1
1Servicio de Cirugía General y Aparato Digestivo. Hospital General Universitario. Valencia.
2Servicio de Cirugía General y Aparato Digestivo. Hospital Universitario Dr. Peset. Valencia.
3Departamento de Bioquímica y Biología Molecular. Servicio de Análisis Clínicos-CDB. Hospital General Universitario. Valencia. España.
El presente trabajo se ha llevado a cabo con fondos del Instituto de Investigación Carlos III, RD06/0045 y FIS PI10/OO82 concedidos al prof. Guillermo Saez Tormo.
Dirección para correspondencia
RESUMEN
Objetivo: Determinar el grado de Estrés Oxidativo en pacientes obesos mórbidos comparando los resultados con los de una población normal.
Material y método: Hemos estudiado los metabolitos más representativos del EO, tanto en sangre (MDA, 8-oxo-dG, GSSG y la relación GSSG/GSH) como en orina (8-oxo-dG), así como el antioxidante GSH.
Realizamos un análisis descriptivo de la muestra. Se realizó la prueba de Kolmogorv-Smirnov para evaluar si la distribución de los distintos metabolitos seguía un modelo de normalidad. En los casos de distribución normal, se empleó la T de Student para comparar medias, utilizando la U de Mann-Whitney para los datos no paramétricos, utilizando en los contrastes de hipótesis el nivel de significación p < 0,05.
Resultados: Los pacientes fueron 28 en cada grupo, sin diferencias estadísticamente significativas en cuanto a edad y sexo. El grupo de pacientes con obesidad mórbida presentó un IMC medio de 50,1 ± 4 y de 23,9 ± 6 el grupo normopeso. Un 67,8% de los pacientes obesos mórbidos presentaron comorbilidades. No había patología asociada en el grupo control. Todos los valores de los distintos metabolitos de EO fueron más elevados en el grupo de obesos mórbidos que en el grupo control mientras que la actividad de los sistemas antioxidantes (GSH) fue menor en el grupo de obesos mórbidos.
Conclusión: Los valores de los metabolitos de EO obtenidos en el grupo de obesos mórbidos confirma la presencia de EO en la obesidad, de un modo que se puede considerar patológico dadas las diferencias obtenidas en el grupo de población normal.
Palabras clave: Obesidad. Obesidad mórbida. Estrés oxidativo. Radicales libres. Antioxidantes.
ABSTRACT
Objective: To determine the level of oxidative stress in morbid obese patients by comparing their results to those of a normal population.
Material and methods: We have studied the metabolites most representative of OS, both in the blood (MDA, 8-oxo-dG, GSSG and the ratio GSSG/GSH) and in the urine (8-oxo-dG), as well as the GSH antioxidant. A descriptive analysis of the sample was performed. The Kolmogorv-Smirnov test was used to assess whether the distribution of the different metabolites was normal. In the case of normal distribution, the Student's t test was used to compare the means, the Mann-Whitney U test was used for non-parametric data, with a significance level of p < 0.05 for hypothesis contrast.
Results: There were 28 patients in each group, without statistically significant differences regarding age and gender. The group of patients with morbid obesity presented an average BMI of 50.1 ± 4 and 23.9 ± 6 in the group with normal weight. 67.8% of the patients with morbid obesity had other comorbidities. There were no associated pathologies in the control group. All the values for the different OS metabolites were higher in the group of patients with morbid obesity than in the control group, whereas the activity of the antioxidant systems (GSH) was lower in the group with morbid obesity.
Conclusion: The figures of OS metabolites obtained in the group of patients with morbid obesity confirm the presence of OS in obesity at a pathological level given the differences obtained in the group of normal population.
Key words: Obesity. Morbid obesity. Oxidative stress. Free radicals. Antioxidants.
Abreviaturas
MDA: Malondialdehido.
8-oxo-dG: 8-oxo-deoxiguanosina.
GSSG: Glutatión oxidado.
GSH: Glutatión reducido.
IMC: Índice de masa corporal.
EO: Estrés oxidativo.
RL: Radicales libres.
ROS: Especies reactivas de oxígeno.
OM: Obesidad mórbida.
CHGUV: Consorcio Hospital General Universitario de Valencia.
ADN: Ácido desoxirribonucleíco.
SAHS: Síndrome de apnea-hipopnea del sueño.
HTA: Hipertensión arterial.
Introducción
El estrés oxidativo (EO) es un tipo de estrés químico que ocurre en el organismo, secundario a una excesiva producción de moléculas sumamente reactivas conocidas como Radicales Libres (RL), responsables de alteraciones en la estructura y función de diversas moléculas vitales y por tanto del deterioro progresivo de los distintos órganos y sistemas.
Los agentes oxidantes pueden ser exógenos o endógenos. De estos, entre los más dañinos están las especies reactivas del oxígeno (ROS) y los peróxidos lipídicos, cuya peculiaridad de tener uno o más electrones desapareados en su orbital más externo, hace que sean moléculas muy reactivas, de vida media muy corta y con capacidad de producir daño en todas las biomoléculas.
Para contrarrestar los efectos deletéreos de estas especies reactivas, el organismo dispone de agentes antioxidantes responsables de su control homeostático1, siendo el equilibrio entre la formación de los agentes oxidantes y las defensas antioxidantes lo que determina la adecuada funcionalidad del organismo2.
En condiciones de metabolismo aeróbico normal, las especies derivadas del oxígeno se producen en baja cantidad y el daño que causan a las células es mínimo al ser reparado constantemente.
El EO se ha relacionado con múltiples enfermedades de carácter inflamatorio y/o degenerativo3,4, y a pesar de que se constata su presencia en el desarrollo de las mismas, no se dispone aún de suficiente información que esclarezca si el EO se debe considerar como una nueva entidad o condición patológica. Ello también implica que no dispongamos de unos valores de EO que nos permitan decir a partir de cuales se puede considerar patológico, si bien existen distintos grupos que a nivel multicéntrico trabajan en esta línea de investigación biomédica5 y, como resultado, algunos de los productos de EO ya forman parte del grupo de marcadores emergentes o potencialmente emergentes para el estudio evolutivo de enfermedades cardiovasculares6,7.
La obesidad y con mayor fundamento la obesidad mórbida (OM), es una de las patologías que despierta en la actualidad el interés de buen número de investigaciones puesto que en ella la formación de RL ha ido asumiendo gran trascendencia. Presentamos un estudio del EO en pacientes obesos mórbidos y su comparación con los valores de una población con normopeso a fin de comprobar si, al tratarse la obesidad de un proceso inflamatorio crónico, existe una alteración del mismo que indicaría un daño crónico.
Material y método
Hemos estudiado la presencia del EO mediante la valoración de los metabolitos más representativos del mismo en sangre y/o orina, en un grupo de pacientes obesos mórbidos (grupo obeso) cuyos valores han sido comparados con los obtenidos en un grupo control (grupo normopeso) formado por personas de edad y género similar, pero sin sobrepeso ni comorbilidad asociada.
El grupo normopeso (n = 28) lo forman voluntarios sanos y el grupo obeso (n = 28) son pacientes de la consulta hospitalaria, candidatos a cirugía bariátrica, remitidos al Servicio de Cirugía.
Todos han sido detalladamente informados del estudio, que fue aprobado por el Comité Ético y de Investigación del CHGUV. Mediante explicación, lectura y entendimiento del proyecto, todos los pacientes de la serie aceptaron participar en el mismo, para lo que firmaron un consentimiento informado. El estudio se realizó sobre muestras biológicas, sangre y orina, que han sido procesadas en la Unidad de Toxicología Metabólica del Departamento de Bioquímica de la Facultad de Medicina de Valencia, así como por el Servicio de Análisis Clínicos del CHGUV.
Del grupo obeso hemos realizado dos subgrupos, uno con los pacientes que no presentaron ninguna comorbilidad asociada y otro en el que una o varias de ellas estaban presentes, tratando de valorar si el EO está implicado de manera independiente en la obesidad o si lo está por sus patologías asociadas, comparando entre si los resultados obtenidos en los dos subgrupos y los de cada uno de ellos con los del grupo normopeso.
Para la valoración del EO se han determinado tanto los productos de oxidación molecular como del antioxidante glutatión reducido (GSH) y oxidado (GSSG), para calcular el porcentaje de la relación GSSG/GSH como índice de estado redox y EO8.
Entre los productos de oxidación molecular, se han seleccionado como marcadores más representativos de EO in vivo el malondialdehido (MDA) purificado y cuantificado siguiendo el método descrito por Wong9, la base nucleotídica modificada 8-oxo-deoxiguanosina (8-oxo-dG) tanto en el ADN genómico10 como su eliminación por la orina11, así como la relación GSSG/ GSH. Como antioxidante se ha cuantificado la concentración de GSH.
El estudio estadístico se ha realizado mediante los programas informáticos de Excel XP y SPSS para Windows versión 15.0, utilizando en los contrastes de hipótesis el nivel de significación p < 0,05. Hemos realizado un análisis descriptivo de la muestra empleando los valores medios ± desviación estándar para los datos cuantitativos y las proporciones para las variables cualitativas.
Antes de realizar las oportunas comparaciones entre los niveles de EO oxidativo entre los grupos casos y controles, se realizó la prueba de Kolmogorv-Smirnov para evaluar si la distribución de los distintos metabolitos de estrés seguía modelo de normalidad o no. En los casos de distribución normal, se empleó la prueba de la T de Student para comparar medias, utilizando la prueba de la U de Mann-Whitney para los datos no paramétricos. Hemos utilizando el nivel de significación p < 0,05 en los contrastes de hipótesis.
Resultados
Los pacientes del grupo obeso, tenían una media de edad de 43,2 ± 1 años y 42 ± 1 el grupo normopeso. No existen diferencias estadísticamente significativas en cuanto a edad y sexo entre ambos grupos.
El grupo obeso presentó un IMC medio de 50,1 ± 4, mientras que el del normopeso fue de 23,9 ± 6 (p < 0,01). En el grupo obeso, un 67,8% presentaron SAHS, un 53,5% HTA, un 46,4% dislipidemia y un 39,2% diabetes. No había patología asociada en el grupo normopeso. El subgrupo obeso con comorbilidades lo forman 22 mujeres y un hombre, con media de edad de 43,3 ± 9 años y un IMC medio de 50,8 ± 6 k/m2. El subgrupo obeso sin comorbilidades lo forman 5 mujeres con una edad media de 42,8 ± 5 años y un IMC medio de 46,8 ± 7 k/m2.
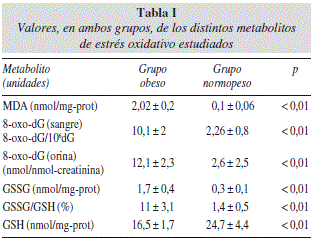
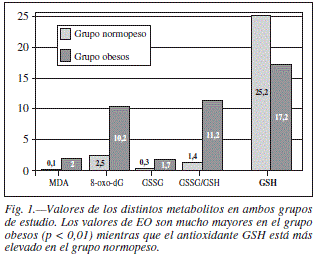
Todos los valores de los distintos metabolitos de EO fueron más elevados en el grupo obeso que en el normopeso con diferencias estadísticamente significativas (p < 0,01), mientras que la concentración de antioxidante (GSH) fue menor en el grupo obesos (p < 0,01). Los resultados se muestran en la tabla I y la figura 1.
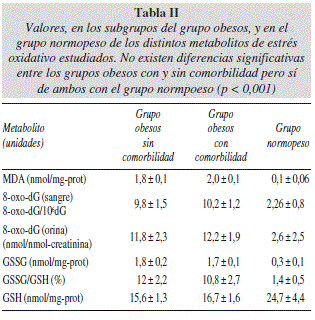
No hubo diferencias estadísticamente significativas entre los pacientes del grupo obesos con comorbilidad y los sin comorbilidad, pero si de ambos subgrupos con los valores del grupo normopeso (p < 0,01). Los resultados se muestran en la tabla II.
Discusión
El EO se ha relacionado con numerosas enfermedades crónicas3,4,12-15 disponiendo en la actualidad de datos suficientes que confirman su participación en la fisiopatología de diferentes afecciones cardiovasculares13.
Dado que la obesidad constituye un importante factor de riesgo para el desarrollo de enfermedades cardiovasculares13, se considera que está muy relacionada con el EO16,17. De igual manera se da gran importancia a los RL en la patogenia de enfermedades que se encuentran asociadas frecuentemente a la OM, tal como la diabetes18,19, SAHS20, HTA21,22, dislipidemia23-25, o el síndrome metabólico19,26, presentes en gran número de pacientes (82,1%) que conforman el grupo obesidad de nuestro estudio.
A pesar de los numerosos estudios publicados sobre la obesidad, es poco lo que se conoce acerca de su asociación con marcadores de daño oxidativo27. Un posible mecanismo de esta relación sea quizás el origen intrínseco al propio tejido adiposo, siendo la hipoxia el factor desencadenante, ya que el excesivo crecimiento del tejido adiposo durante el desarrollo de la obesidad produciría un proceso inflamatorio crónico28, inducido por agrupaciones de adipocitos modificados que se convertirían en una fuente inagotable de citoquinas inflamatorias con importantes efectos bioquímicos.
Otro mecanismo implicaría un efecto de los triglicéridos elevados sobre el funcionamiento de la cadena respiratoria mitocondrial, inhibiendo la translocación de adenin-nucleótidos y fomentando la creación de oxígeno29.
En nuestro estudio hemos comprobado como tanto el subgrupo de pacientes obesos sin comorbilidades asociadas, como el que sí las tenían, presentaron niveles de metabolitos de EO más elevados que los del grupo normopeso. Esto hace pensar que la obesidad por si sola, sin patología asociada, se comporta como una entidad capaz de inducir EO, quizás por el hacho de ser un proceso inflamatorio crónico28.
Si bien no existe una teoría generalmente aceptada por la comunidad científica sobre si está justificado considerar al EO como fisiológico y cuáles son los valores de su umbral a partir del cual podemos definirlo como patológico, es interesante señalar que la atenuación de su intensidad se ha convertido hoy día en una atractiva diana terapéutica30,31, por ello, asumiendo que por cada una de las estructuras susceptibles de modificación por el EO existe un marcador representativo que lo identifica, es posible llegar a una medición aproximada y aceptable del EO utilizando diferentes indicadores del daño oxidativo.
Cabe decir que en la actualidad no existe un método único que permita la objetividad en la determinación y caracterización del EO, y que muchas de las técnicas de medición disponibles no están todavía estandarizadas. Para obviar estos inconvenientes se recurre generalmente a la valoración de sus metabolitos, sin estar del todo claro si para su cuantificación es suficiente la determinación de uno solo de los biomarcadores hasta ahora identificados o es necesaria la de varios en conjunto.
Nosotros hemos valorado distintos metabolitos a fin de evitar que el uso de uno solo de ellos pudiera dar un resultado que, aunque correcto, no fuera capaz de determinar realmente la presencia de EO. El hecho de utilizar varios y que su comportamiento sea similar en todos, es lo que nos hace pensar que efectivamente lo que observamos es la realidad. A tal propósito, en este estudio hemos utilizado los que están considerados como los índices más representativos, reproducibles y fiables para evaluar el estado de EO tisular1,3. Es el caso del MDA, considerado como el representante más sensible del daño fosfolipídico de la membrana celular32. La peroxidación lipídica es un indicador básico de la oxidación de las lipoproteínas de membranas y la cuantificación de sus productos primarios, como los dienos conjugados, puede determinarse a través de la concentración de MDA, lo cual lo convierte en un indicador de EO muy importante.
La misma importancia tiene la 8-oxo-dG como expresión del daño nuclear33. Puesto que el ADN sufre procesos de reparación y los productos de su oxidación representan el daño oxidativo global en el organismo, siendo la 8-oxo-dG producto de la acción de los ROS sobre el carbono 8 de la guanina en el ADN tanto genómico como mitocondrial, el aislamiento de esta base nucleotídica del ADN modificada por el estrés resulta fundamental a la hora de valorar el EO. Por otra parte, el interés bioquímico y clínico de este metabolito reside en su reconocido potencial mutagénico. Es sabido que la presencia de 8-oxo-dG en la estructura del ADN se traduce en la inestabilidad genética propensa al acumulo de mutaciones34, un mecanismo que podría explicar la mayor incidencia carcinogénica de los pacientes obesos35.
Por último, estudiamos el glutatión tanto en su forma reducida (GSH) como en su forma oxidada (GSSG) y su cociente (GSSG/GSH) como expresión de sufrimiento metabólico intracelular36. En condiciones fisiológicas la glutatión reductasa (GR) cataliza la reducción del GSSG a GSH. En situaciones de aumento de especies reactivas (ROS) donde la actividad de la GR está mermada, la capacidad de la célula de reducir GSSG resulta comprometida y ello lleva a un incremento de su concentración. Al ser el GSSG un metabolito capaz de atravesar fácilmente las membranas biológicas y acceder al torrente circulatorio, ocasiona un aumento del cociente GSSG/GSH lo que explica el aspecto más interesante del glutatión como índice de EO, puesto que su nivel sanguíneo refleja el daño que se ha producido en otros tejidos36.
A pesar de los problemas metodológicos encontrados, en nuestro estudio, hemos comprobado como todos los pacientes obesos mórbidos que componían la serie presentaron, en condiciones basales, valores de EO superiores a los encontrados en el grupo normopeso. En concreto, al comparar el valor medio de cada metabolito entre ambos grupos, observamos como en todos ellos los valores eran claramente superiores en el grupo obesos y en alguno con diferencias de hasta 20 veces mayor, como es el caso del MDA.
Por otro lado, la situación opuesta se ha observado al valorar el estado antioxidante en ambos grupos. En efecto, al comparar el antioxidante natural estudiado (GSH) y su cociente GSSG/GSH, hemos observado que los valores medios en el grupo normopeso fueron de 24,7 ± 4,4 nmol/mg y 1,44 ± 0,5% respectivamente, mientras que en el grupo obesos fue de 16,5 ± 1,7 nmol/mg y 8,2 ± 2,4% respectivamente, es decir que el grupo obesos presentó valores menores de antioxidantes, con diferencia significativa estadísticamente, que los del grupo normopeso, con lo que se confirma la presencia de EO en el grupo obesos, con elevada formación de RL y escasa de antioxidantes que los compensen.
El haber comprobado la existencia de EO en una población sana, ya que el estudio de los metabolitos del mismo muestra su presencia en dicha población, puede inducir a afirmar que estos niveles pueden considerarse "normales", es decir, fisiológicos e inherentes a la propia vida. Por el contrario, los niveles obtenidos en condiciones normales en la población obesa estudiada, podría permitir afirmar que en la obesidad mórbida existe un EO con valores "patológicos", todo esto dentro del contexto de no poder definir ni asegurar cuales son los valores "normales" y cuando estos valores pueden ser considerados "patológicos".
Conclusión
Si bien nos crea cierta incertidumbre considerar fisiológico la existencia del EO en sujetos sanos no obesos aunque presenten valores bajos, encontrarlo con valores elevados en pacientes obesos mórbidos nos permite definirlo, con alto grado de fiabilidad, como claramente patológico.
Referencias
1. Flora SJ. Role of free radicals and antioxidants in health and disease. Cell Mol Biol 2007; 53: 1-2. [ Links ]
2. Sies H. Biological redox systems and oxidative stress. Cell Mol Life Sci 2007; 64: 2181-8. [ Links ]
3. Cerdá C, Salvador A, Ocete MD, Torregrosa R, Fandos-Sánchez M, Sáez G. Estrés oxidativo, envejecimiento y cáncer. En: Biogerontología Médica. Autores: José Ramón Ramón, Reinald Pamplona, Juan Sastre. Editorial Ergon. Madrid 2009; pp: 71-85. [ Links ]
4. Zafrilla P, Morillas J, Mulero J, Xandri JM, Santo E, Caravaca G. Estrés oxidativo en enfermos de Alzheimer en diferentes estadios de la enfermedad. Nutr Hosp 2004; 19: 63. [ Links ]
5. European Standards Committee on Urinary (DNA) Lesion Analysis, Evans MD, Olinski R, Loft S, Cooke MS. Toward consensus in the analysis of urinary 8-oxo-7,8-dihydro-2'-deoxyguanosine as a noninvasive biomarker of oxidative stress. FASEB J 2010; 24: 1249-60. [ Links ]
6. Blankenberg S, Rupprecht HJ, Bickel C, Torzewski M, Hafner G, Tiret L, et al. AtheroGene Investigators. Glutathione peroxidase 1 activity and cardiovascular events in patients with coronary artery disease. N Engl J Med 2003; 349: 1605-13. [ Links ]
7. Steinberg D, Witztum JL. Oxidized low-density lipoprotein and atherosclerosis. Arterioscler Thromb Vasc Biol 2010; 30: 2311-6. [ Links ]
8. Navarro J, Obrador E, Pellicer JA, Asensi M, Viña J, Estrela JM. Blood glutathione as an index of radiation-induced oxidative stress in mice and humans. Free Radic Biol Med 1997; 22: 1203-9. [ Links ]
9. Wong SHY, Knight JA, Hopfer SM, Zaharia O, Leach CN Jr, Sunderman FW Jr. Lipoperoxides in plasma as measured by liquid-chromatographic separation of malondialdehyde thiobarbituric acid adduct. Clin Chem 1987; 33: 214-20. [ Links ]
10. Muñiz P, Valls V, Perez-Broseta C, Iradi A, Climent JV, Oliva MR, et al. The role of 8-hydroxy-2'-deoxyguanosine in rifamycin-induced DNA damage. Free Radic Biol Med 1995; 18: 747-55. [ Links ]
11. Espinosa O, Jiménez-Almazán J, Chaves FJ, Tormos MC, Clapes S, Iradi A, et al. Urinary 8-oxo-7,8-dihydro-2'-deoxyguanosine (8-oxo-dG), a reliable oxidative stress marker in hypertension. Free Radic Res 2007; 41: 546-54. [ Links ]
12. Kontush K, Schekatolina S. Vitamin E en neurodegenerative disorders: Alzheimer's disease. Ann NY Acad Sci 2004; 1031: 249-62. [ Links ]
13. Heistad DD. Oxidative stress and vascular diseases: 2005 Duff lecture. Arterioscler Thromb Vasc Biol 2006; 26: 689-95. [ Links ]
14. Valko M, Rhodes CJ, Moncol J, Izakovic M, Mazur M. Free radicals, metals and antioxidants in oxidative stress-induced cancer. Chem Biol Interact 2006; 160: 1-40. [ Links ]
15. Abilés J, de la Cruz AP, Castaño J, Rodríguez-Elvira M, Aguayo E, Moreno-Torres R, et al. Oxidative stress is increased in critically ill patients according to antioxidant vitamins intake, independent of severity: a cohort study. Crit Care 2006; 10: R146. [ Links ]
16. Fenster C, Weinsier R, Darley-Usmar VM, Patel RP. Obesity, aerobic exercise and vascular disease: the role of oxidant stress. Obes Res 2002; 10: 964-8. [ Links ]
17. Keaney JF Jr, Larson MG, Vasan RS, Wilson PW, Lipinska I, Corey D, et al. Obesity and systemic oxidative stress. Arterioscler Thrombosis Vasc Biol 2003; 23: 434-9. [ Links ]
18. Heistad DD. Oxidative stress and vascular diseases: 2005 Duff lecture. Arterioescler Thromb Vasc Biol 2006; 26: 689-95. [ Links ]
19. Kadowaki T, Yamauchi T, Kubota N, Hara K, Ueki K, Tobe K. Adiponectin and adiponectin receptors in insulin resistance, diabetes, and the metabolic syndrome. J Clin Invest 2006; 116: 1784-92. [ Links ]
20. Yamauchi M, Kimura H. Oxidative stress in obstructive sleep apnea: putative pathways to the cardiovascular complications. Antioxid Redox Signal 2008; 10: 755-68. [ Links ]
21. Redón J, Oliva MR, Tormos C, Giner V, Chaves J, Iradi A, et al. Antioxidant activities and oxidative stress byproducts in human hypertension. Hypertension 2003; 41: 1096-101. [ Links ]
22. Giner V, Tormos C, Chaves FJ, Sáez G, Redón J. Microalbuminuria and oxidative stress in essential hypertension. J Intern Med 2004; 255: 588-94. [ Links ]
23. Hopps E, Noto D, Caimi G, Averna MR. A novel component of the metabolic syndrome: The oxidative stress. Nutr Metab Cardiovasc Dis 2010; 20: 72-7. [ Links ]
24. Ferri J, Martínez-Hervás S, Espinosa O, Fandos M, Pedro T, Real JT, et al. 8-oxo-7,8-dihydro-2'-deoxyguanosine as a marker of DNA oxidative stress in individuals with combined familiar hyperlipidemia. Med Clin (Barc) 2008; 131: 1-4. [ Links ]
25. Martínez-Hervas S, Fandos M, Real JT, Espinosa O, Chaves FJ, Saez GT, et al. Insulin resistance and oxidative stress in familial combined hyperlipidemia. Atherosclerosis 2008; 199: 349-84. [ Links ]
26. López-Uriarte P, Nogués R, Saez G, Bulló M, Romeu M, Masana L et al. Effect of nut consumption on oxidative stress and the endothelial function in metabolic syndrome. Clin Nutr 2010; 29: 373-80. [ Links ]
27. Yang R. Effect of antioxidant capacity on blood lipid metabolism and lipoprotein lipase activity of rats fed a high-fat diet. Nutrition 2006; 22: 1185-91. [ Links ]
28. Vincent HK, Innes KE, Vincent KR. Oxidative stress and potential interventions to reduce oxidative stress in overweight and obesity. Diabetes ObesMetab 2007; 9: 813-39. [ Links ]
29. Fenster CP, Weinsier RL, Darley-Usmar VM, Patel RP. Obesity, aerobic exercise, and vascular disease: the role of oxidant stress. Obes Res 2002; 10: 964-8. [ Links ]
30. Grune T. Markers of oxidative stress in ICU clinical settings: present and future. Curr Opin Clin Nutr Metab Care 2007; 10: 712-7. [ Links ]
31. Trayhurn P, Woods IS. Adipokines: inflammation and the pleitropic role of white adipose tissue. Br J Nutr 2004; 92: 347-55. [ Links ]
32. Arab K, Steghens JP, Plasma lipd hydroperoxides measurement by an automated xylenol orange method. Anal Biochem 2004; 325: 158-63. [ Links ]
33. Evans MD, Cooke MS. Oxidative DNA damage and disease: induction, repair and significance. Mutat Res Rev 2004; 567: 1-61. [ Links ]
34. Oliva MR, Ripoll F, Muñiz P, Iradi A, Trullenque R, Valls V, et al. Genetic alterations and oxidative metabolism in sporadic colorectal tumors from a Spanish community. Mol Carcinog 1997; 18: 232-43. [ Links ]
35. Li Q, Zhang J, Zhou YN, Qiao L. Obesity and gastric cancer. Front Biosci 2012; 17: 2383-90. [ Links ]
36. Jones DP. Redox potential of GSH/GSSG couple: assay and biological significance. Methods Enzymol 2002; 348: 93-112. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Antonio Vázquez Prado.
Hospital General Universitario.
C/ Alcacer, 7 bis, 2o-3a.
46014 Valencia.
E-mail: vprado.a@gmail.com
Recibido: 4-XII-2012.
Aceptado: 8-I-2013.