Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.33 supl.4 Madrid 2016
https://dx.doi.org/10.20960/nh.348
Nutrición en enfermedad inflamatoria intestinal
Nutrition in inflammatory bowel disease
María Josefa Martínez Gómez, Cristóbal Melián Fernández y María Romeo Donlo
Sección de Gastroenterología y Nutrición. Hospital Infantil Universitario Niño Jesús. Madrid
Dirección para correspondencia
RESUMEN
La enfermedad inflamatoria intestinal (EII) es una patología crónica que cursa en brotes. En los últimos años se ha visto un aumento de la incidencia, sobre todo en edades más tempranas. La malnutrición se encuentra frecuentemente asociada a esta patología, por tanto, es de vital importancia una intervención nutricional adecuada, especialmente en pacientes pediátricos, que intente asegurar no solo un óptimo crecimiento, sino también una mejoría de la clínica. Nuestro objetivo será actualizar, según la evidencia publicada, el conocimiento del papel de la nutrición en la enfermedad y en el tratamiento de la misma.
La desnutrición en estos pacientes es frecuente y se ve influida por varios factores, como son la disminución de la ingesta alimentaria, el aumento de las necesidades de nutrientes, el aumento de las pérdidas proteicas y la malabsorción de los nutrientes. Por esto se debería realizar un seguimiento nutricional a todos ellos en el que se hicieran mediciones antropométricas, determinaciones analíticas y densitometría, para establecer las necesidades y el aporte calórico suficiente adaptado a cada paciente.
El uso de la nutrición enteral como tratamiento en la enfermedad de Crohn con brote leve-moderado en población infantil está ampliamente demostrado; incluso ha demostrado ser superior al uso de corticoides. Por todo ello podemos concluir recalcando que la intervención nutricional es un pilar fundamental en el manejo de los pacientes con EII, cuya finalidad es evitar y/o controlar la desnutrición relacionada con la enfermedad para disminuir su morbimortalidad y mejorar su calidad de vida.
Palabras clave: Nutrición. Enfermedad inflamatoria intestinal. Colitis ulcerosa. Enfermedad de Crohn. Pediatría.
ABSTRACT
Inflammatory bowel disease (IBD) is a chronic pathology that has an outbreaks course that in recent years have seen an increase in incidence, especially at younger ages. Malnutrition is frequently associated with this condition, therefore, it is very important to ensure a right nutritional intervention, especially in pediatric patients, to ensure an optimal growth and also an improvement in the clinic. Our goal will be updated the role of nutrition in this disease and in its treatment based on the published evidence.
Malnutrition in these patients is frequent and is influenced by various factors such as, decreased food intake, increased nutrient requirements, increased protein loss and malabsorption of nutrients. Therefore there should be a nutritional monitoring of all of them, in which anthropometric measurements, laboratory tests and densitometry were made to establish the needs and sufficient caloric intake tailored to each patient.
The use of enteral nutrition as a treatment in Crohn's disease with mild to moderate outbreak in child population, is amply demonstrated, has even shown to be superior to the use of corticosteroids. Therefore we can conclude by stressing that nutritional intervention is a mainstay in the management of patients with IBD, which aims to prevent and/or control disease-related malnutrition to decrease morbidity and mortality and improve quality of life.
Key words: Nutrition. Inflammatory bowel disease.a Ulcerative colitis. Crohn's disease. Pediatrics.
Introducción
El término enfermedad inflamatoria intestinal (EII) incluye dos entidades: la colitis ulcerosa (CU) y la enfermedad de Crohn (EC). Ambas cursan de forma crónica con brotes de actividad inflamatoria. Se definen de acuerdo a criterios clínicos, radiológicos, endoscópicos e histológicos. La EC consiste en una afectación transmural y parcheada de cualquier tramo del tracto digestivo, mientras que en la CU la afectación se limita a la mucosa y tiene carácter continuo. Existe una tercera entidad conocida como EII no clasificada que comparte características de ambas entidades y representa el 30% de las formas pediátricas (1).
La EII es una entidad de etiopatogenia desconocida en la que se produce una activación inapropiada y sostenida del sistema inmune de la mucosa intestinal en individuos genéticamente predispuestos. Se han estudiado distintos factores exógenos que pudieran estar implicados, como la apendicectomía, las infecciones ocurridas durante la infancia, las complicaciones perinatales y el papel de la dieta. Con respecto a esta última, se han implicado distintos aspectos nutricionales y dietéticos tanto a nivel etiológico como en el tratamiento, ya que la malnutrición es una característica común a esta enfermedad.
Además, hay que tener en cuenta que la EII en la edad pediátrica presenta ciertas peculiaridades clínicas y psicosociales que hacen que sea necesario realizar un diagnóstico y tratamiento precoces.
EPIDEMIOLOGÍA
A día de hoy la EC ha aumentado su incidencia (4,5/100.000), mientras que la de CU (2/100.000) se ha estabilizado, aunque estos datos varían en función de las distintas regiones. La mayoría de los casos se diagnostican entre la segunda y la tercera década de la vida y solo un 5% antes de los 5 años de edad, correspondiendo la mayoría de los casos a CU o formas no clasificadas. Mientras que la EC es más frecuente en varones (1,5:1), no existe predominio de sexo en la CU. La prevalencia global de la enfermedad es del 0,4% (2).
MALNUTRICIÓN Y EII
Existe una alta prevalencia de malnutrición en los pacientes con EII, ocurriendo en el 50-70% de los pacientes con EC y el 18-62% de la CU (3), lo cual es reseñable, ya que la desnutrición relacionada con la enfermedad empeora el pronóstico de la misma debido a que altera la función del sistema inmune, retrasa la curación de las mucosas y disminuye la funcionalidad del paciente. Todo ello contribuye a aumentar su morbimorbilidad, implicando el deterioro de la calidad de vida del paciente y su familia, así como un importante aumento de los gastos a nivel sanitario.
Se conocen distintos factores asociados a la actividad inflamatoria presente en la EII, como son el aumento de los niveles de TNF-alfa, IL-6 y IL-1 beta, que conducen a una alteración del eje GH/IGF1 y GNRH, lo que se traduce en un retraso puberal y del crecimiento (4).
Detrás de ese estado de desnutrición hay diversas causas, como son, por un lado, la disminución de la ingesta alimentaria y, por otro, el aumento de las necesidades de nutrientes dado el estado de enfermedad de estos pacientes. Asimismo, debido a la situación de inflamación intestinal que acompaña a esta entidad, se produce un aumento de las pérdidas proteicas, además de asociarse a una malabsorción de nutrientes; sin olvidar como otra causa la interacción farmacológica de los distintos medicamentos en la absorción y utilización de los nutrientes.
Mientras que en la EC la afectación nutricional tiene un curso insidioso en forma de anorexia, astenia y estancamiento ponderoestatural, en la CU se produce de forma aguda. De manera que el cribado y seguimiento nutricional se debe realizar a todos los pacientes.
DIETA Y EII
Entre los factores ambientales que juegan un papel en la etiopatogenia de la enfermedad se encuentra la microflora bacteriana y el entorno alimenticio. No existen evidencias claras que justifiquen una relación directa entre dieta y EII; sin embargo, han sido varias las hipótesis que han surgido para intentar demostrar una relación entre la dieta y el aumento de la incidencia de esta enfermedad en los países desarrollados. El aumento del consumo de azúcares y carbohidratos refinados en estos países se ha considerado como un factor de riesgo para desarrollar la enfermedad, mientras que el consumo de frutas y vegetales puede disminuir este riesgo (5). Se ha implicado al omega 6 en el origen de la enfermedad, dado su carácter inflamatorio, ya que afecta al metabolismo del ácido araquidónico y aumenta la producción de leucotrienos B4, lo que favorece la acción inflamatoria. En cambio, estudios en población esquimal, consumidora de ácidos grasos poliinsaturados omega 3, indican que estaría relacionado con una baja prevalencia de EII. Esto ha demostrado la capacidad de los líquidos dietéticos en regular los procesos inflamatorios (6).
INTERVENCIÓN NUTRICIONAL
La EII tiene importantes implicaciones nutricionales y metabólicas, ya que existe una alta prevalencia de malnutrición en esta enfermedad, la dieta puede verse implicada como parte de la etiología y además la intervención nutricional podría tener un papel importante en el tratamiento primario de esta entidad (7).
Los objetivos de un soporte nutricional adecuado incluirían la corrección de las deficiencias de macro y micronutrientes, suministrar las calorías y las proteínas adecuadas para mantener un balance nitrogenado positivo y promover así la cicatrización de la mucosa, además de lograr un crecimiento y desarrollo puberal adecuados. Mientras que en la CU el tratamiento nutricional es básicamente de soporte nutricional, en la EC no solo se emplea como soporte nutricional, sino como tratamiento primario para inducir la remisión (8).
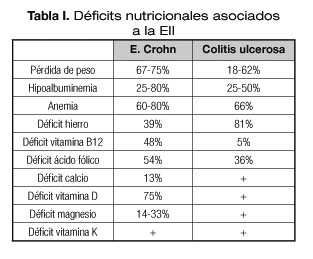
Por ello se recomienda realizar un cribado nutricional adecuado en estos pacientes. En la EII se pueden encontrar déficits nutricionales de: calorías, proteínas, lipoproteínas, alfa y beta carotenos, licopenos, vitaminas hidrosolubles y liposolubles, cobre, magnesio, calcio, hierro y zinc (9) (Tabla I).
Valoración nutricional
Una valoración nutricional adecuada debe comenzar por una anamnesis y exploración física detalladas. Se realizarán mediciones antropométricas y se solicitarán las exploraciones complementarias que sean necesarias para asegurar un aporte calórico suficiente y adaptado a cada paciente (10).
En la anamnesis se deben recoger los antecedentes personales y la evolución de la enfermedad, así como hacer una historia dietética que incluya el recuento de 24 horas, además de la frecuencia de consumo de los principales grupos de alimentos. Idealmente se debería hacer una encuesta dietética de 3 días consecutivos. Con todo ello se pondrán de manifiesto las posibles aversiones y preferencias alimentarias, el patrón y la conducta alimentaria, que nos permitirá comenzar a hacer recomendaciones dietéticas.
En la exploración física intentaremos identificar aquellos cambios que se suponen están relacionados con una ingesta dietética inadecuada; valoraremos los tejidos epiteliales superficiales, como son la piel, el pelo y las uñas; exploraremos la masa muscular y el panículo adiposo, además de inspeccionar tanto la boca como el ano, donde prestaremos especial atención a la presencia de fisuras y fístulas; y deberemos hacer hincapié en la exploración abdominal, buscando puntos dolorosos, zonas de empastamiento o distensión, así como la presencia de masas y megalias.
Con respecto a las mediciones antropométricas, deberemos pesar y tallar al paciente en cada visita y medir el perímetro cefálico a los más pequeños. Cada seis meses se medirá el pliegue subescapular y tricipital. Todas estas mediciones se deben comparar con estándares de referencia, como son las tablas de percentiles (OMS, Orbegozo) y las puntuaciones Z. Con todo ello obtendremos una serie de índices, como el índice de masa corporal (IMC), la relación peso/talla, el % de pérdida de peso y el % de peso ideal.
Disponemos de distintas pruebas complementarias que nos ayudan a realizar la valoración nutricional de forma adecuada. Deberíamos realizar una analítica de sangre que incluya un hemograma, y bioquímica con metabolismo del hierro, zinc, prealbúmina, albúmina, inmunoglobulinas y función hepática. Debido al retraso en el crecimiento que suelen presentar estos pacientes, se puede realizar una radiografía de carpo para valorar la edad ósea del mismo. Además, en función del centro se dispondrá de diversos medios para realizar un análisis de la composición corporal (bioimpedanciometría, absorción DXA), mientras que en aquellos en los que no se disponga de estos medios se utilizarán las mediciones antropométricas. Se recomienda realizar a lo largo del seguimiento de estos pacientes control de osteopenia con densitometría ósea, debido al riesgo elevado que presentan tanto por la situación nutricional como por los tratamientos aplicados.
Se dispone de diversas ecuaciones para el cálculo de los requerimientos nutricionales de estos pacientes (Harris-Benedit [1919], OMS/FAO/ONU [1985] y Schofield [1985]), así como un método de calorimetría tanto directo como indirecto, que estima el gasto energético a partir de la medida de consumo de O2 y de la producción de CO2.
Tratamiento nutricional
Los mecanismos por los que la nutrición enteral ejerce su acción terapéutica primaria no se conocen con exactitud. Se cree que la fuente de proteínas o de grasas podría favorecer la disminución de la carga antigénica en la luz intestinal.
Se han realizado diversos estudios que confirman que la nutrición enteral es una alternativa eficaz al tratamiento farmacológico. Se han obtenido resultados similares en cuanto a la remisión clínica con respecto a los corticosteroides en población infantil (80%), aunque no es tan evidente en población adulta (11,12). Ha demostrado mayor eficacia que los corticosteroides en cuanto a la curación de la mucosa, mejoría de la inflamación, recuperación del crecimiento y mantenimiento de la remisión clínica, aunque se necesitan más estudios que confirmen su utilidad en el mantenimiento para prevenir las recaídas. En población adulta, a diferencia de la infantil, presenta un mayor riesgo de recurrencia precoz tras su suspensión (13).
En los diferentes estudios realizados no se han encontrado diferencias significativas en cuanto al tipo de fórmula utilizada (elemental/semielemental/polimérica). Además, no se ha descrito beneficio en el hecho de suplementar las fórmulas con factores antiinflamatorios ni de factores de crecimiento.
Con respecto a la pauta de administración, la nutrición enteral es más eficaz de forma exclusiva frente a la forma mixta y existen más beneficios si se aplica de forma continua, pero es menos factible y disminuye la calidad de vida, por lo que no es la forma más utilizada.
Aunque no existe una clara influencia en la tasa de remisión, se han obtenido mejores resultados si la afectación es ileocólica o exclusiva a nivel del intestino delgado, siendo discutido su beneficio en la afectación colónica exclusiva.
Por tanto, la nutrición enteral se debería emplear en aquellos brotes de EC leve-moderado, especialmente si la afectación es ileal o ileocólica, obteniéndose mejores resultados cuanto más precoz sea su utilización, recomendándose especialmente en el debut de la enfermedad. Se debería administrar como alimentación exclusiva durante 6-8 semanas, asegurando un aporte calórico adecuado (120-130% de las RDA [cantidad diaria recomendada], debido al estado inflamatorio de la enfermedad), aplicándose ya sea por vía oral, sonda nasogástrica (SNG) o nutrición enteral a débito continuo (NEDC). Con respecto al tipo de fórmula, no existe una recomendación única, empleándose habitualmente fórmulas poliméricas. De forma conjunta al tratamiento nutricional se suele empezar tratamiento de mantenimiento con azatriopina (14). Una vez transcurridas esas 6-8 semanas se inicia la reintroducción de la alimentación de forma gradual, disminuyendo de forma progresiva la nutrición enteral a lo largo de 3-4 semanas. Se considerará que ha fracasado el tratamiento nutricional si no se ha obtenido respuesta en 2 semanas (15).
Conclusiones
La intervención nutricional en pacientes con EII es fundamental por la frecuente asociación de dicha enfermedad con la malnutrición. Se hace necesario hacer un seguimiento nutricional de todos estos pacientes para, de forma individualizada, asegurar un aporte calórico adecuado y personalizado que intente favorecer especialmente en la población infantil un desarrollo tanto a nivel puberal como de crecimiento adecuados, dadas las peculiaridades de este tipo de población en comparación con la población adulta. Además, la nutrición ha demostrado un papel fundamental en el tratamiento de esta entidad y por ello se debe optimizar esta opción. Se deben realizar más estudios que evalúen el papel de la adición de nutrientes inmunomoduladores a las fórmulas actualmente utilizadas.
Bibliografía
1. Guariso G, Gasparetto M, Visonà Dalla Pozza L, D'Inca R, Zancan L, Sturniolo G, et al. Inflammatory bowel disease developing in paediatric and adult age. JPGN 2010;51:698-707. [ Links ]
2. Martín-de-Carpi J, Rodríguez A, Ramos E, Jiménez S, Martínez-Gómez MJ, Medina E; SPIRIT-IBD Working Group of Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica. Increasing incidence of pediatric inflammatory bowel disease in Spain (1996-2009): the SPIRIT Registry. Inflamm Bowel Dis 2013;19(1):73-80. [ Links ]
3. Pérez Tárrago C, Puebla Maestu A, Miján de la Torre. Tratamiento nutricional en la enfermedad inflamatoria intestinal. Nutr Hosp 2008;23(5):417-27. [ Links ]
4. Heuschkel R, Salvestrini C, Beattie RM, Hildebrand H, Walters T, Griffiths A. Guidelines for the management of growth failure in childhood inflammatory bowel disease. Inflamm Bowel Dis 2008;14:839-49. [ Links ]
5. Bernstein CN, Rawsthorne P, Cheang M, Blanchard JF. A population-based case control study of potential risk factors for IBD. Am J Gastroenterol 2006;101:993-1002. [ Links ]
6. Cashman KD, Shanahan F. Is nutrition an aetiological factor for inflammatory bowel disease? Eur J Gastroenterol Hepatol 2003;15:607-13. [ Links ]
7. López Gómez JJ, Urioste Fondo A, Cano Rodríguez. Impacto de la nutrición en la evolución de la enfermedad inflamatoria intestinal. Nutr Hosp 2010;25:181-192. [ Links ]
8. Sierra Salinas C, Navas López VM, Blasco Alonso J. Nutrición en enfermedad inflamatoria intestinal pediátrica (revisión). Nutrición Clínica en Medicina 2008;11(1):36-43. [ Links ]
9. O'Sullivan M, O'Morain C. Nutrition in inflammatory bowel disease. Best Pract Res Clin Gastroenterol 2006;20(3):561-73. [ Links ]
10. Prieto G, Martínez MJ. Crecimiento, maduración sexual y estado nutricional en los pacientes con enfermedad inflamatoria intestinal pediátrica. En: Ricart E, Martín de Carpi J, editores. Enfermedad inflamatoria intestinal pediátrica. Barcelona: Marge; 2013. p. 79-97. [ Links ]
11. Pérez Tárrago C, Puebla Maestu A, Miján de la Torre A. Tratamiento nutricional en la enfermedad inflamatoria intestinal. Nutr Hosp 2008;23(5):418-28. [ Links ]
12. Heuschkel RB, Menache CC, Megerian JT, Baird AE. Enteral nutrition and corticosteroids in the treatment of acute Crohn's disease in children. J Pediatr Gastroenterol Nutr 2000;31(1):8-15. [ Links ]
13. Kleinman RE, Baldassano RN, Caplan A, Griffiths AM, Heyman MB, Issenman RM, et al; North American Society for Pediatric Gastroenterology, Hepatology And Nutrition. Nutrition support for pediatric patients with inflammatory bowel disease: a clinical report of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition. J Pediatr Gastroenterol Nutr 2004;39:15-27. [ Links ]
14. Mossop H, Davies P, Murphy MS. Predicting the need for azathioprine at first presentation in children with inflammatory bowel disease. J Pediatr Gastroenterol Nutr 2008;47:123-9. [ Links ]
15. Critch J, Day AS, Otley A, King-Moore C, Teitelbaum JE, Shashidhar H; NASPGHAN IBD Committee. Use of enteral nutrition for the control of intestinal inflammation in pediatric Crohn disease. J Pediatr Gastroenterol Nutr 2012;54(2):298-305. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
María Josefa Martínez Gómez.
Sección de Gastroenterología y Nutrición.
Hospital Infantil Universitario Niño Jesús.
C/ Menéndez Pelayo, 65. 28009 Madrid
e-mail: mjosemartinez@telefonica.net