INTRODUCCIÓN
La disminución en la ingesta de alimentos en los pacientes oncológicos es uno de los principales obstáculos para mantener un correcto estado nutricio. Además de esto, existen otras anomalías que contribuyen a la desnutrición, como es el caso de la posible malabsorción de los nutrimentos debido a cambios estructurales y funcionales del tracto digestivo. Por otra parte, la misma patología subyacente induce cambios metabólicos, como resistencia a la insulina, intolerancia a la glucosa, lipólisis incrementada y un exacerbado catabolismo proteico (1). La pérdida de la masa magra y grasa, la debilidad, la anorexia y el edema en pacientes con cáncer se conoce como caquexia y se presenta hasta en el 50 % de estos casos. Esta ha sido relacionada con el incremento de complicaciones de la propia enfermedad, así como de los efectos adversos asociados a la terapéutica, lo cual se debe a los mecanismos sistémicos inflamatorios derivados de la propia caquexia a causa de alteraciones hormonales y la presencia de citocinas inflamatorias, que llega a complicar la respuesta anabólica del paciente (1-3).
Asimismo, el músculo esquelético se encuentra en un estado de hiperactivación debido a los factores de transcripción, como el factor nuclear κB (NFκB), el factor de necrosis tumoral α (TNF- α), las interleucinas (IL-1β e IL- 6) (3,4) y la sobreexpresión de miostatina, proteína perteneciente a la familia del factor de crecimiento transformante β (TGF- β), limitando de esta manera el crecimiento de la masa muscular (4). Lo anterior, en conjunto con una baja actividad física y una dieta ineficiente, generará un aumento en la debilidad muscular y una alteración en la realización de actividades de la vida diaria (2).
Ante el contexto señalado, la evaluación e intervención nutricia se ha convertido en un punto crítico para lograr la disminución de la morbimortalidad perioperatoria (5). Algunas de las estrategias terapéuticas implican el uso de suplementación con aminoácidos de cadena ramificada (AACR), particularmente de la leucina (0,2-0,4 g/kg de peso) y sus metabolitos (6). Este aminoácido tiene un impacto positivo en la síntesis proteica, subsanando en parte el catabolismo, independientemente de la vía de administración (7). Por otra parte, los pacientes geriátricos podrían representar el grupo etario mayormente beneficiado ante el incremento de la ingesta proteica. Es por ello que los suplementos como la proteína de suero de leche con alto contenido de AACR han sido utilizados en diversos estudios, en los que han mostrado mejoría en la evolución de estos pacientes (7).
La implementación de proteína de suero de leche en conjunto con terapia de rehabilitación física ha sido estudiada previamente y se han encontrado efectos positivos en indicadores de fuerza de extensión muscular y en funcionalidad valorada por el índice de Barthel (8). La evidencia emergente se dirige a la mejoría de las complicaciones perioperatorias en pacientes con apoyo de suplementación por vía oral (9), reportando resultados favorables en pacientes quirúrgicos con diversas patologías que tomaron proteína de suero de leche en conjunto con el tratamiento médico. Algunos de los beneficios documentados fueron la mejora en los efectos de rehabilitación posterior a resección colorrectal por carcinoma (10) o la mejora del estado nutricional en pacientes sometidos a cirugía bariátrica (11). Resulta fundamental comprender las alternativas que puedan mejorar el panorama del paciente oncológico, por lo cual el objetivo planteado para este estudio fue evaluar el efecto perioperatorio de la proteína de suero de leche y del caseinato de calcio (CaCNT) en pacientes con cáncer sometidos a cirugía electiva.
MATERIAL Y MÉTODOS
PARTICIPANTES
Se realizó un estudio clínico aleatorizado en el periodo de marzo a octubre de 2021, en el Departamento de Cirugía de un hospital de Seguridad Social de segundo nivel de atención hospitalaria. Se incluyeron pacientes adultos de ambos sexos de 18 a 65 años de edad con diagnóstico de cáncer y que requirieron intervención quirúrgica por parte de los servicios de Oncología Quirúrgica, Coloproctología y Oncología Ginecológica. Se excluyeron pacientes con embarazo, falla renal o hepática o con contraindicación para utilizar la vía oral. El estudio fue aprobado por el Comité de Investigación y de Ética en Investigación Hospitalaria con número de registro (R-2021-101-006). A los pacientes candidatos a manejo quirúrgico que aceptaron participar en el estudio se les presentó consentimiento informado para la obtención de firma. Posteriormente, la aleatorización de los grupos se generó por medio de números generados en el software Excel. Los participantes fueron distribuidos en tres grupos de 15 participantes cada uno: el grupo control, el grupo de intervención con CaCNT y el grupo de intervención con proteína aislada de suero de leche (WPI).
ANÁLISIS DE LA COMPOSICIÓN CORPORAL
Se realizaron mediciones de composición corporal y funcionalidad dos semanas antes del procedimiento quirúrgico, así como cuatro semanas después del mismo. La evaluación se llevó a cabo por medio de la técnica de bioimpedancia eléctrica con el equipo Medical Body Composition Analyzer modelo mBCA 525, marca SECA. La talla y el peso fueron evaluados con un estadímetro y báscula marca SECA® modelo 217 y se determinó el índice de masa corporal (IMC) de acuerdo a los criterios de la Organización Mundial de la Salud (OMS). Las variables consideradas para la composición corporal fueron: masa muscular y grasa, agua extracelular (AEC) e intracelular (AIC) y la relación de estas, ángulo de fase, ángulo de fase estandarizado y grasa visceral. Todos los pacientes fueron evaluados bajo las mismas condiciones, marco de tiempo y periodo de ayuno de cuatro horas. Todas las medidas realizadas se basaron en las técnicas y los estándares establecidos por la Sociedad Internacional para el Avance de la Cineantropometría (ISAK) para la toma de las mediciones antropométricas.
EVALUACIÓN DE LA FUNCIONALIDAD
Para la funcionalidad se aplicaron pruebas de fuerza de prensión de mano para evaluar la fuerza muscular, el rendimiento se evaluó a través de la prueba de caminata de seis minutos (P6CM) y para evaluar la masa magra se midió la longitud del recto femoral (LRF) de ambas piernas.
La fuerza de la prensión de mano se realizó con el dinamómetro Medequip Depot® modelo FE-120241. La medición se hizo con el paciente sentado, con los hombros aducidos, el codo flexionado en 90°, el antebrazo colocado neutralmente y la muñeca dorsiflexionada entre 0 y 30°; posteriormente, se le solicitó al participante presionar el mango tan fuerte como le fuese posible. En dicha posición se realizan tres mediciones con un intervalo de un minuto; la medición reportada fue el valor máximo de los tres eventos.
Por otro lado, previo a la evaluación de la P6CM, se le solicitó al participante permanecer descansando por un lapso de 15 minutos. A continuación, se le explicó que caminaría a lo largo de un pasillo de ida y regreso tantas veces fuera posible por un periodo de seis minutos. Se permitía disminuir velocidad o detenerse durante la prueba y continuar posteriormente, de ser posible. Al finalizar los seis minutos, se realizó la medición de acuerdo con la marca de inicio y fin para calcular la distancia por medio de un flexómetro, y al concluir la prueba se realizó medición de signos vitales y oximetría.
Finalmente, para la LRF se utilizó el ultrasonido Esaote MyLab® con sonda lineal (AC2541) en modalidad para músculo esquelético. Para realizar la medición se colocó al paciente en decúbito supino, obteniendo la medición a dos tercios de la distancia existente entre la espina iliaca anterosuperior y el polo superior de la patela en un plano sagital.
SUPLEMENTACIÓN CON PROTEÍNA
Dos grupos recibieron suplementación con proteína (25 g), uno de ellos con CaCNT (n = 15). El caseinato de calcio fue disuelto en ocho onzas de agua purificada cada 24 horas dos semanas previo al evento quirúrgico y cuatro semanas posterior al mismo; la toma de proteína se realizó en el mismo marco temporal en condición de ayuno por las mañanas. En relación con el grupo con WPI (n = 15), la proteína fue otorgada siguiendo los mismos criterios anteriormente mencionados.
REVISIÓN CLÍNICA DEL PACIENTE
Como parte de las medidas de control del estudio, se llevó a cabo un seguimiento del paciente desde el momento del ingreso hospitalario hasta cuatro semanas posterior al mismo para monitorizar la presencia de complicaciones perioperatorias (clasificación de Clavien-Dindo). Previo a la suplementación, se evaluó la ingesta dietética del paciente para complementar el análisis de este. Se registraron el día de ingreso y el de egreso para contabilizar la estancia intrahospitalaria.
ANÁLISIS ESTADÍSTICO
Se analizaron los datos demográficos de manera descriptiva y fueron representados en media y desviación estándar. En el análisis inferencial para el cálculo de la normalidad se utilizó la prueba de Shapiro-Wilk; respecto la evaluación de las diferencias intergrupos, se analizaron por medio de ANOVA y una prueba post hoc de Dunnett; y para diferencias intragrupos se utilizó la prueba de t de Student pareada. Por otro lado, la posible asociación entre variables se analizó a través del test de correlación de Pearson. Los datos fueron analizados con el paquete estadístico SPSS versión 20 (IL, Estados Unidos) y se consideraron un intervalo de confianza del 95 % y una diferencia estadística con un valor de p menor a 0,05 (*p < 0,05, †p < 0,01, ‡p < 0,001).
RESULTADOS
Se evaluaron 45 pacientes de entre 21 y 65 años de edad, con un promedio de 47,62 ± 13,45 años de edad; el 66,7 % de los pacientes fueron mujeres (n = 30) y el 33,3 % fueron hombres (n = 15). La mayoría de los pacientes fueron tratados por parte del Servicio de Oncología Quirúrgica (53,3 %) y la patología más frecuente fue carcinoma mamario (26,7 %), seguida de carcinoma rectal y tiroideo (17,8 %); la información se puede verificar en la tabla I. Respecto a la evolución perioperatoria entre grupos, no se mostraron diferencias de acuerdo a la clasificación Clavien-Dindo para complicaciones quirúrgicas, siendo constante la prevalencia de complicaciones posquirúrgicas no graves. En relación a la estancia intrahospitalaria, el uso de CaCNT o de WPI no mostró una modificación en los días de internamiento respecto al control (3,11 ± 2,7 días, p = 0,19). De igual manera, el sangrado registrado durante la operación mostró un promedio de 279 ± 203,4 ml (p= 0,54) y un tiempo quirúrgico de 2,6 ± 0,8 horas (p = 0,89), sin llegar a ser diferente estadísticamente en ninguno de los grupos.
Tabla I. Características del paciente y relacionadas con el padecimiento.
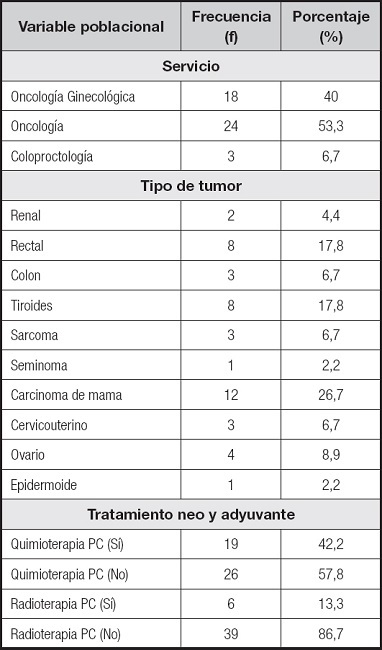
Los datos son representados en frecuencias y porcentajes (n = 45).
PC: previo a cirugía.
Por otro lado, el análisis de las medidas antropométricas fue determinado previamente a la cirugía y posterior a un mes de esta. El IMC predominante entre los grupos fue sobrepeso, con una media de 26,6 ± 4,9 kg/m2 de acuerdo a los criterios de la OMS, sin existir diferencias entre grupos. Respecto al peso corporal, en todos los grupos se presentó una disminución de peso del 0,88 % (0,627 kg); no obstante, es importante mencionar que el grupo con WPI mantuvo su peso posterior a la cirugía (70,4 ± 14 kg vs. 70,4 ± 15 kg). En cuanto a la evaluación de la dieta, los participantes registraron una dieta isocalórica (1.680,18 ± 387,75 Kcal), con una distribución promedio del 56,4 % de hidratos de carbono, 18,3 % de proteínas y 25,3 % de lípidos. No se encontraron diferencias entre los grupos (en la tabla II se puede ver en detalle la distribución de cada grupo).
Tabla II. Características antropométricas y dietéticas por grupo.
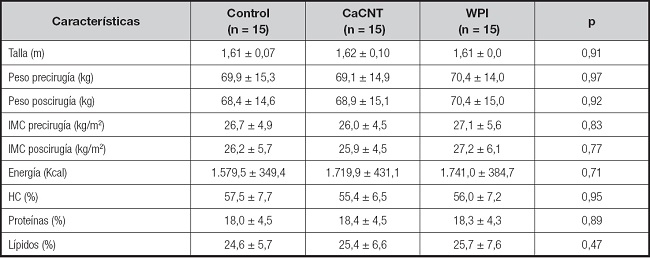
Los datos se representan en media ± DE (n= 45). Prueba estadística utilizada ANOVA post hoc: prueba de Dunnett. CaCNT: caseinato de calcio; WPI: proteína aislada de suero de leche; IMC: índice de masa corporal; HC: hidratos de carbono.
La funcionalidad o recuperación de los pacientes se evaluó por medio de la prueba de caminata de seis minutos, la fuerza de prensión de brazos y la LRF. El rendimiento de los metros reportados en la P6CM (pre: 396,5 ± 104,6 m vs. post: 394,1 ± 97,4 m) entre los grupos no mostró ser diferente en aquellos con suplementación respecto al control. No obstante, en referencia con la fuerza de prensión, el grupo control mostró una disminución de fuerza posterior a la cirugía (-4,4 kg, p = 0,02) (Fig. 1A) en comparación con los grupos suplementados con proteína, que mantuvieron la fuerza inicial registrada. Asimismo, se identificó un aumento en la LRF de ambas piernas en el grupo control posterior a la cirugía, que se incrementó un 32,8 % (pre: 16,35 ± 9,84 mm vs. post: 21,72 ± 11,97 mm; p = 0,005), comparado con los grupos con proteína suplementada, que no registraron cambios.
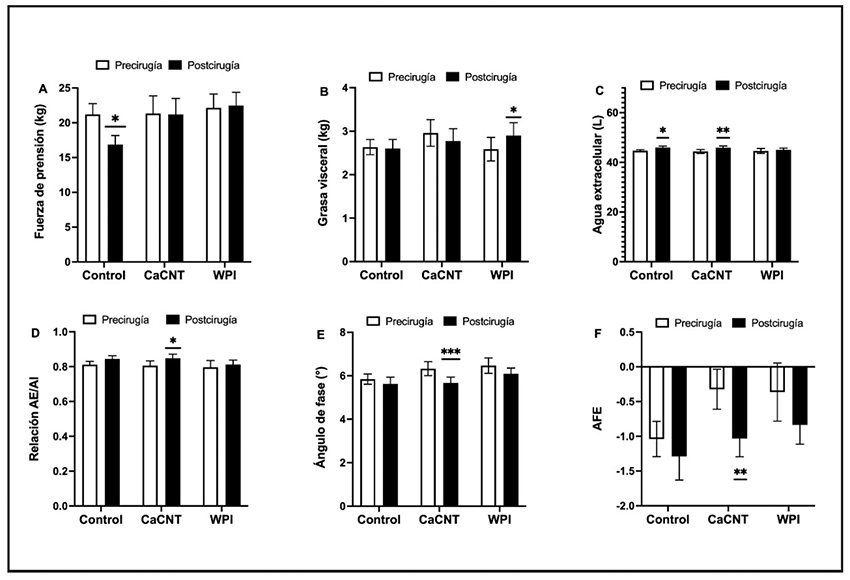
Figura 1. Análisis intragrupos de pruebas de funcionalidad y composición corporal (n = 45). A. Fuerza de prensión precirugía y poscirugía. B. Grasa visceral precirugía y poscirugía. C. Agua extracelular precirugía y poscirugía. D. Relación entre agua extracelular e intracelular precirugía y poscirugía. E. Ángulo de fase precirugía y poscirugía. F. Ángulo de fase estandarizado precirugía y poscirugía (CaCNT: caseinato de calcio; WPI: proteína aislada de suero de leche; AFE: ángulo de fase estandarizado. Prueba estadística utilizada: t de Student pareada. *p < 0,05. **p < 0,01. ***p < 0,001).
La evaluación de la composición corporal no mostró diferencias significativas entre el grupo control y los grupos de intervención (Tabla III). Sin embargo, en la comparación intragrupal se identificó un incremento posquirúrgico de la grasa visceral en el grupo de proteína de suero de leche (2,5 kg vs. 2,9 kg, p = 0,02). De igual manera, el agua extracelular fue mayor tanto en el grupo control como en el grupo de CaCNT (2,6 %, p = 0,04, y 3,3 %, p = 0,001, respectivamente); este último aumentó también su relación de agua en los espacios celulares (AEC/AIC) (p = 0,03). El ángulo de fase y el ángulo de fase estandarizado en el grupo con CaCNT fueron diferentes respecto al control y el grupo con WPI, siendo menor posterior al procedimiento quirúrgico (6,3 ± 1,2 vs. 5,6 ± 1,0, p = 0,002). Los cambios posquirúrgicos pueden ser valorados a detalle en la figura 1B-F.
Tabla III. Análisis de la composición corporal por grupo.
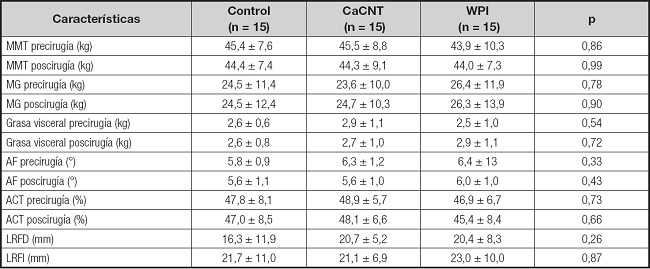
Los datos se representan en media ± DE (n = 45). Prueba estadística utilizada ANOVA post hoc: prueba de Dunnett. CaCNT: caseinato de calcio; WPI: proteína aislada de suero de leche; BIE: bioimpedancia eléctrica; MMT: masa muscular total; MG: masa grasa; AF: ángulo de fase; ACT: agua corporal total; LRFD: longitud del recto femoral derecho; LRFI: longitud del recto femoral izquierdo.
Finalmente, se analizó la correlación entre diversas variables, destacando un mejor resultado en la P6CM con puntajes altos en el ángulo de fase (r = 0,358, p = 0,01) y peores resultados en aquellos con mayores niveles de AEC (r = -0,322, p = 03). Por otro lado, variables de interés perioperatorio como el sangrado durante la operación y la estancia intrahospitalaria se relacionaron de manera inversa con la LRF, el IMC y el ángulo de fase y se asociaron con un mayor sangrado quirúrgico y un mayor número de días de hospitalización cuando los valores de estas características fueron bajos (Fig. 2).
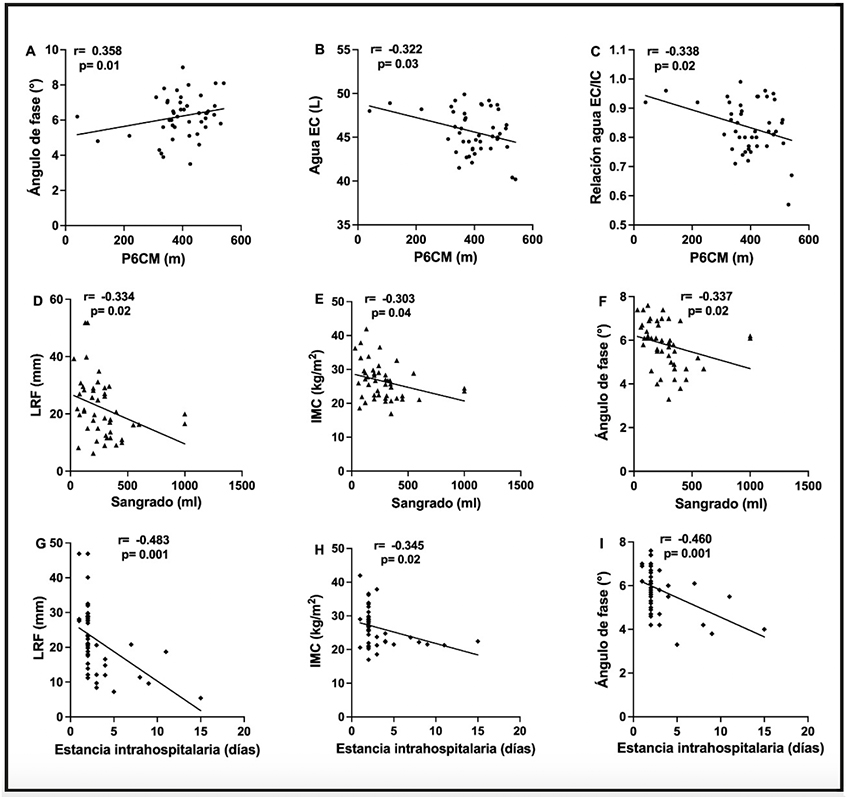
Figura 2. Análisis de correlación (n = 45). A. Ángulo de fase y P6CM. B. Agua extracelular y P6CM. C. Relación de agua extra e intracelular y P6CM. D. Longitud de recto femoral y cantidad de sangrado. E. Índice de masa corporal y cantidad de sangrado. F. Ángulo de fase y cantidad de sangrado. G. Longitud de recto femoral y días de hospitalización. H. Índice de masa corporal y días de hospitalización. I. Ángulo de fase y días de hospitalización (P6CM: prueba de caminata de seis minutos; LRF: longitud de recto femoral; IMC: índice de masa corporal. Prueba estadística utilizada: coeficiente de correlación de Pearson).
DISCUSIÓN
La cirugía en el paciente oncológico continúa siendo el pilar del tratamiento médico (12), sin embargo, el tratamiento tanto nutricional como multidisciplinario se lleva a cabo en pocos pacientes (13). De acuerdo con Bargetzi y cols., (14) la terapia nutricional individualizada permite mejorar la capacidad funcional, así como la calidad de vida de los pacientes oncológicos. Particularmente en el caso de la proteína de suero de leche, sus componentes biológicos, como la lactoferrina, la beta lactoglobulina, la alfa lactoalbúmina y las inmunoglobulinas, contribuyen con los efectos antioxidantes, antitumorales, antivirales y antibacteriales (15).
En este estudio se pretendió evaluar los posibles beneficios posquirúrgicos de la suplementación de proteína en pacientes con cáncer de diferentes parámetros como composición corporal, antropometrías, funcionalidad, tiempo de hospitalización y complicaciones postoperatorias. La estancia intrahospitalaria en la población estudiada no se vio disminuida con el uso de suplementos proteicos. Mientras que Gillis y cols. (13), en su estudio, reportan una disminución en los días de hospitalización, sin embargo, se aprecia una tendencia de disminución en el grupo de proteína de suero de leche, ya que se observa una reducción en promedio de cuatro días, lo cual, en cuestión de costos, podría tener implicaciones positivas en el área administrativa. Esto puede explicarse, en parte, por la variabilidad de los tipos de cáncer entre los grupos de pacientes, así como del tiempo de evolución de los mismos.
Las complicaciones posteriores a la cirugía fueron similares entre grupos, sin denotar diferencias de acuerdo con la clasificación de Clavien-Dindo, lo cual difiere con lo reportado por Srinivasaraghavan y cols., que muestran una disminución de complicaciones en su grupo de intervención con proteína de suero de leche (17). Dicha diferencia puede deberse a factores como la edad, ya que, a mayor edad, será mayor el riesgo de aparición de complicaciones. Asimismo, niveles bajos de hemoglobina y albúmina (18) pueden condicionar la morbimortalidad de estos pacientes, esto sin considerar la progresión de acuerdo al tipo de neoplasia, que es un foco de estudio para elucidar la posible respuesta de la suplementación de proteína ante cada tipo de cáncer.
La fuerza de prensión se considera un marcador de la capacidad funcional. En nuestro estudio no pudo ser incrementada en los grupos de intervención, pero sí mantenida. Yacong Bo y cols. (16) reportan una mejora en la fuerza de prensión de mano posterior a la suplementación en paciente adulto mayor con sarcopenia, sin embargo, además de la proteína de suero de leche, su dieta fue complementada con vitaminas D y E. Otro aspecto que se debe considerar es la presencia del catabolismo proteico que se genera en el paciente oncológico, que por sí solo ha demostrado disminuir la fuerza de prensión de mano en estos pacientes (19), lo que se suma al estrés posquirúrgico. La presencia de citocinas proinflamatorias (IL-6, TNF-α, TGF-β, interferón-γ) (20) puede empeorar este panorama, lo cual podría explicar que, si bien no se presenta un aumento, la fuerza no se pierde y se mantiene, asociándose a una mejor evolución entre los pacientes con suplementación de proteína antes y después de la cirugía.
Por otra parte, la actividad física como terapia de rehabilitación ha demostrado un efecto positivo para incrementar la masa libre de grasa en conjunto con la proteína de suero de leche en pacientes con sarcopenia, lo que parece indicar un efecto sinérgico. En nuestra población, se encontró un aumento en la fuerza muscular en el grupo suplementado con proteína de suero de leche, lo que concuerda con lo reportado en otros estudios (21). Sin embargo, en nuestros grupos de estudio no fue posible implementar el programa de rehabilitación para paciente posquirúrgico dado el periodo de pandemia y la saturación del Servicio de Rehabilitación a favor de pacientes postinfectados de COVID-19.
Se ha documentado un mejor rendimiento en la distancia de la caminata de seis minutos posterior a la suplementación con proteína de suero de leche (17). No obstante, en nuestra población no se pudo observar esa mejora debido, posiblemente, a las diferencias entre grupos en cuanto al tipo y el tiempo de evolución del cáncer, aunque se muestra una tendencia hacia el incremento en metros caminados en ambos grupos de intervención, que es mayor en el grupo suplementado con proteína de suero de leche.
En cuanto a la diferencia en la LRF, su modificación no corresponde con los incrementos de fuerza de prensión de mano o de la distancia de caminata observados en los diversos grupos. Sin embargo, la LRF puede modificarse de manera aguda y está relacionada con la composición corporal. Esto concuerda con las conclusiones de Battaglia y cols. (21), quienes reportaron una reducción en el recto femoral en aquellos pacientes con composición corporal con parámetros por debajo de lo deseable, incluidos la masa muscular y el aumento de agua extracelular, lo que se asocia a mayor edematización y menor rendimiento en las pruebas de funcionalidad, como es el caso de lo reportado en nuestros resultados. Esto representa una ventana de oportunidad para la intervención temprana para el mantenimiento de la masa muscular, considerando el uso de suplementación de proteína posterior a un análisis pertinente de la función renal de los pacientes que pueden ser candidatos a su uso.
A pesar de que se ha documentado que la ingesta de proteína de suero de leche favorece la disminución de la composición corporal a favor de una pérdida de grasa (22-24), en nuestro estudio se observó un incremento de la grasa visceral en el grupo de proteína de suero de leche. Dicho resultado corresponde con revisiones en las cuales se concluye que el efecto de la suplementación con proteína de suero de leche en la grasa corporal es poco claro (25). La disminución de la grasa visceral se ha asociado con la suplementación de dicha proteína en conjunto con actividad física anaeróbica (26). Otra posible explicación es la velocidad de absorción de la proteína de suero de leche en comparación con otro tipo de proteína, lo cual podría favorecer mecanismos anabólicos en estos pacientes. Sin embargo, esto no aún no se comprende en su totalidad (27,28), por lo que es recomendable ahondar en este efecto y en el posible acompañamiento de rehabilitación muscular, que podrían esclarecer este resultado.
En relación con el ángulo de fase y el ángulo de fase estandarizado, ambos presentaron una disminución en el grupo de CaCNT, lo que puede considerarse un marcador de mal pronóstico de acuerdo con diversos autores (29,30), ya que se traduce en una disminución de la calidad de los tejidos secundaria a la afectación de la membrana plasmática (31,32); con ello, además, se genera un incremento tanto del agua extracelular como de la razón de agua extracelular con el agua intracelular. Además de esto, Trommelen y cols. describen la cinética y absorción del CaCNT (33), que tiende a precipitarse en el estómago retrasando el vaciado gástrico, generando sensación de plenitud y disminuyendo su digestión y, por ende, absorción (34). Esto puede generar en los participantes una ingesta menor respecto a los otros grupos que impactaría en su composición corporal, pudiendo explicar dicha relación en nuestros resultados.
La evaluación del estado nutricional requiere ser abordada de manera integral con diversas herramientas desde el punto de vista antropométrico, funcional y metabólico, debido a los múltiples factores que logran repercutir en el mismo, por ejemplo, el periodo de ayuno y el estrés por patología y la terapia implementada. Por lo tanto, es recomendable que la valoración sea multiinstrumental y dinámica en el periodo de tiempo durante el cual se le otorgue la atención médica al paciente. Asimismo, las pruebas de funcionalidad deben ser implementadas como objetivos de desenlace del paciente posquirúrgico con la finalidad de tener parámetros que se vinculen con las actividades de la vida diaria y la independencia del paciente. Dichos parámetros se ven afectados por el ayuno y las alteraciones en el metabolismo proteico de manera sistémica. Por lo anterior, se deben seguir buscando estrategias de suplementación proteica que coadyuven en el mantenimiento de la masa muscular y su funcionamiento.
En relación con las pruebas de análisis de bioimpedancia, no mostraron cambios favorables para el grupo de CaCNT. No obstante, en el grupo de proteína de suero de leche, por los hallazgos relacionados en el mantenimiento del agua celular y el ángulo de fase, se asoció a mejores expectativas en cuanto a complicaciones perioperatorias, cantidad en el sangrado y días de hospitalización, lo que abre la opción a futuras investigaciones para conocer a nivel metabólico el efecto de estos suplementos en pacientes oncológicos. Finalmente, no se encontraron mejoras en pruebas de funcionalidad como la caminata de seis minutos. La cantidad reducida de pacientes reclutados durante el periodo del estudio, correspondiente a las olas de la pandemia por SARS-CoV-2, fue una limitante importante. Otra fue la diversidad de tipos de cáncer entre grupos y, por otro lado, el abordaje quirúrgico de acuerdo con el tipo de tumor podría afectar en mayor o menor grado el efecto de la intervención, por lo que será importante indagar en este tipo de estudios estratificando de acuerdo a estas características y el estadio del cáncer presente en el paciente.
CONCLUSIONES
La proteína aislada de suero de leche mantiene los parámetros de composición corporal como la fuerza de prensión, la masa muscular y el agua celular, lo cual puede generar mejores expectativas y evolución en en pacientes oncológicos sometidos a cirugía electiva. La suplementación nutricional requiere ser abordada desde el punto de vista funcional y metabólico para identificar factores que impacten favorablemente.














