Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Cirugía Plástica Ibero-Latinoamericana
versión On-line ISSN 1989-2055versión impresa ISSN 0376-7892
Cir. plást. iberolatinoam. vol.40 no.4 Madrid oct./dic. 2014
https://dx.doi.org/10.4321/S0376-78922014000400005
Estudio multicéntrico prospectivo observacional sobre implantes PIP® colocados en 12 años
Prospective observational multicenter study on PIP® implants placed in 12 years
Cárdenas-Camarena, L.*; Chung-Gallardo, J.**; Echeverria-Roldán, G.***; León, M.A.****; Oaxaca-Escobar, C.*****; García-Fabian, F.***; Madrid-Basurto, A.******; Encinas-Brambila, J.*******; González-Ulloa, B.******** y Robles-Cervantes, J.A.*********
* Cirujano Plástico, Instituto Jalisciense de Cirugía Plástica "Dr. José Guerrerosantos" e INNOVARE Cirugía Plástica Especializada, Guadalajara, Jalisco, México.
** Cirujano Plástico, INNOVARE Cirugía Plástica Especializada, Guadalajara, Jalisco, México.
*** Cirujano Plástico, RENOVA Centro de Cirugía Plástica, Ciudad de Guatemala, Guatemala.
*** Cirujano Plástico, Hospital Civil de Guadalajara, Guadalajara, Jalisco, México.
***** Cirujano Plástico, Práctica Privada, León, Guanajuato, México.
****** Cirujano Plástico, Práctica Privada, Puebla, Puebla, México
******* Cirujano Plástico, Práctica Privada, La Paz, Baja California, México.
******** Especialista en Radiología, Directora del Departamento de Glándula Mamaria de Diagnóstico Especializado por Imagen, Guadalajara, Jalisco, México.
********* Especialista en Medicina Interna, Instituto Jalisciense de Cirugía Reconstructiva "Dr. José Guerrerosantos" e INNOVARE Cirugía Plástica Especializada, Guadalajara, Jalisco, México.
Dirección para correspondencia
RESUMEN
A pesar de la controversia existente con los implantes PIP® (Poly Implant Prothèse, Francia) son pocos los estudios que existen al respecto, por lo que determinamos realizar un análisis multicéntrico en nuestro entorno para conocer las características y el comportamiento clínico de los mismos.
Planteamos un estudio multicéntrico, prospectivo y observacional, en el que participaron 7 cirujanos plásticos certificados que durante un periodo de 12 años habían colocado implantes PIP®. Analizamos clínicamente y con ultrasonido mamario todas las pacientes que acudieron a revisión, recogimos todos los datos y cuantificamos los hallazgos en aquellas que se intervinieron quirúrgicamente para revisión de los implantes.
Entre enero del 2012 y febrero del 2013 acudieron a consulta 184 pacientes de las 1.315 que habían sido operados entre 1998 y 2010 (14%), evaluando un total de 368 implantes. Solo 39 pacientes (21,2%) presentaban sintomatología. Mediante ultrasonido mamario, 322 implantes (87,5%) fueron informados como íntegros y 46 (12,5%) rotos.
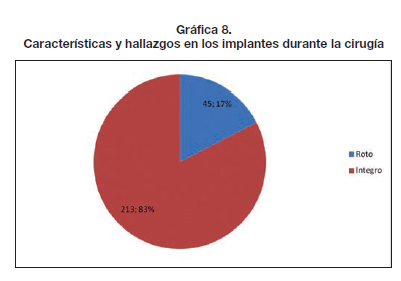
Del total de pacientes revisadas, 55 (30%) no se reoperaron por no tener datos de rotura, mientras que 129 pacientes (70%) decidieron operarse. De ellos, solo 46 presentaban datos de rotura ecográfica (36%). Durante la cirugía se encontraron 213 implantes íntegros (83%) y 45 implantes rotos (17, 8%).
No se encontraron datos de malignidad en las piezas de biopsia tomadas de las cápsulas o en el líquido periprotésico; tampoco crecimiento bacteriano.
El índice de rotura comprobada, 17,8%, fue mayor que el que presentan otros estudios pero que tienen tiempos de seguimiento más cortos.
No se encontró irritación de tejidos o sintomatología mamaria en los implantes íntegros, ni datos de toxicidad en las cápsulas o en el líquido en los implantes rotos. En base a todo ello consideramos que no es mandatorio retirar los implantes PIP® como medida de rutina, sino hacerlo cuando exista evidencia o sospecha de rotura. Creemos que el ultrasonido mamario es un estudio altamente confiable para la evaluación de la integridad de estos implantes.
Palabras clave: Implantes mamarios, Rotura implantes mamarios, Complicaciones implantes mamarios.
Nivel de evidencia científica: II
ABSTRACT
Despite the controversy with PIP® implants (Poly Implant Prothèse, France) there are few studies about it, so we decided to make a multicenter analysis in our environment to determinate the characteristics and clinical behavior of these implants.
A multicenter, prospective, observational study including 7 certified plastic surgeons that for a period of 12 years had placed PIP® implants was performed. All patients attending evaluation were clinical examined and with breast ultrasound. All findings and data in those who underwent surgery for implants review were analyzed.
Between January 2012 and February 2013, 184 patients attended for consultation of 1315 who had been operated between 1998 and 2010 (14%), evaluating a total of 368 implants. Only 39 patients (21.2%) had symptoms. By breast ultrasound, 322 implants (87.5%) were reported as intact and 46 (12.5%) broken. Of the patients reviewed, 55 (30%) were not reoperated for not having evidence of rupture, while 129 patients (70%) decided to be operated. Of these, only 46 had rupture ultrasound data (36%). During surgery 213 implants (83%) were found without damage, and 45 implants were found damaged (17.8%).
There were no data of malignancy in biopsy specimens taken from the capsule or periprosthetic fluid; there was no bacterial growth.
The rupture rate proven, 17.8%, was higher than that presented by other studies but with shorter follow-up time. No irritation symptoms or breast symptoms were found in patients with intact implants. There was no toxicity data in capsules or in the liquid in patients with broken implants.
Based on all this we consider that is not mandatory to remove PIP® implants as a routine measure, but should be done when there is evidence or suspicion of rupture. We believe that breast ultrasound is highly reliable for evaluating the integrity of breast implants.
Key words: Breast implants, Breast implants rupture, Breast implants complications.
Level of evidence: II
Introducción
Los implantes mamarios de silicona fueron introducidos en 1963 por Cronin y Gerow (1). En la actualidad, y tras numerosas modificaciones técnicas, se ha llegado hasta la cuarta generación de implantes (2) en los que lo más importante es el que están provistos de una cubierta más resistente y delgada, y rellenos de gel de silicona cohesiva, característica esta última que evita la migración del gel en caso de rotura del implante.
Existen numerosas variantes de combinación de superficies, cohesividades, formas y tamaños de los implantes mamarios (2) y actualmente, numerosos fabricantes en todo el mundo, de entre los cuales, solo 3 hasta el momento cuentan con la aprobación de la FDA americana (Food and Drug Administration) (3). Para el resto del mundo, cada país cuenta con organismos reguladores que vigilan que las prótesis mamarias cumplan todos los requisitos de su salud para su implantación en seres humanos. Son ejemplos de estos organismos la Medicines and Healthcare Products Regulatory Agency (MHRA), la Australian Government Therapeutic Goods Administration (TGA), la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), y en nuestro país, México, la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS).
En Francia, el organismo encargado de esta vigilancia es la Agence Française de Sécurité Sanitaire des Produits de Santé (AFSSAPS). El 1 de abril del 2010 esta agencia emitió un comunicado señalando la detección de un incremento en la rotura de los implantes mamarios manufacturados por la empresa Poly Implant Prosthese (PIP®) (4). La AFSSAPS determinó que los implantes producidos por esta empresa desde el 2001 habían sido rellenados con un gel de silicona diferente al aprobado sanitariamente para uso en humanos, recomendando a los cirujanos cesar inmediatamente la colocación de estos implantes (4). Posteriormente, en diciembre de 2011, la misma agencia hizo una actualización recomendando como medida preventiva, sin ser emergencia, la retirada quirúrgica de los implantes PIP® en todas la pacientes en las que hubieran sido colocados (5). En este mismo comunicado se aclaró que hasta el momento de su emisión no se había comprobado riesgo incrementado de aparición de cáncer en las pacientes portadoras de esta marca de implantes en comparación con otras marcas de implantes mamarios (5). A pesar de ello, tras estos comunicados, surgieron en todo el mundo numerosas especulaciones creando olas de pánico entre las mujeres afectadas (6-8).
En este trabajo, y a fin de conocer desde un punto de vista científico las características clínicas y por imagen de los implantes PIP® y su relación con posibles complicaciones en relación con el incidente notificado por las autoridades francesas, decidimos recoger datos de las pacientes portadoras de estos implantes mamarios que habían sido intervenidas entre 1998 y 2010 y que fueron revisadas en el transcurso de 14 meses, entre enero de 2012 y febrero de 2013 en diferentes centros quirúrgicos de nuestro entorno, a fin de poder establecer una valoración multicéntrica y una correlación entre los datos clínicos y de imagen obtenidos de las pacientes en revisión clínica con los posibles hallazgos intraoperatorios en aquellas que decidieron someterse a la retirada de los implantes.
Material y método
Para solicitar colaboración multicéntrica, nos pusimos al habla con la empresa distribuidora de los implantes PIP® en México, que nos puso en contacto con los cirujanos a los que les habían suministrado mayor número de implantes de dicha marca. Se trataba de cirujanos de todo México y de Centroamérica, con los cuales nos pusimos en contacto para invitarles a participar en nuestro estudio, de acuerdo con los requisitos de que dispusieran de los datos completos de pacientes e implantes y de tener en su lugar de trabajo un radiólogo especializado en ultrasonido mamario.
Del total de cirujanos plásticos certificados contactados, 7 accedieron a participar en nuestro estudio: 6 en México y 1 en Guatemala. De los 6 mexicanos, 3 trabajaban en la ciudad de Guadalajara (Jalisco), en centros diferentes, y los otros 3 en otras ciudades, 2 del centro del país, León (Guanajuato) y Puebla (Puebla), y el otro al norte del país, Ciudad de La Paz (Baja California).
Desarrollamos un estudio multicéntrico, prospectivo y observacional en que se incluyeron todas aquellas pacientes sometidas a cirugía estética o reconstructiva mamaria en las que se habían colocado implantes PIP® entre los años 1998 y 2010, y que acudieron a consulta para revisión durante el periodo de 14 meses comprendido entre enero de 2012 y febrero de 2013, con los 7 cirujanos que participaron en el estudio.
Elaboramos una hoja especial de recopilación y evaluación de datos para todas las pacientes revisadas. Todas fueron sometidas a revisión clínica por el cirujano plástico que las había operado inicialmente, identificando la presencia de dolor, deformidad mamaria, presencia de parestesias, contractura capsular según escala de Baker, alteraciones cutáneas, presencia de nódulos palpables y fecha de implantación.
A todas ellas se les realizó también estudio mediante ultrasonido mamario por médicos radiólogos especializados en patología mamaria colaboradores de los cirujanos participantes en el estudio. En total fueron 5 radiólogos, ya que los 3 cirujanos de Guadalajara remitieron sus pacientes al mismo especialista. En este estudio ecográfico se evaluó la integridad del implante, la presencia de líquido libre, presencia de nódulos y calcificaciones en tejido mamario según el sistema de clasificación mamaria del Colegio Americano de Radiólogos (BI-RADS), y valoración de las características generales de la cápsula periprotésica.
Del total de pacientes revisadas, en aquellas que decidieron someterse a reintervención para retirada de los implantes PIP®, se llevó a cabo registro de la integridad o rotura de los implantes, características de la cápsula mamaria, presencia y características del líquido periprotésico, presencia de nódulos, y por último, en caso necesario y de ser posible, determinación visual del sitio de rotura de los implantes. Asímismo se tomo biopsia de las cápsulas cuando éstas eran macroscópicamente granulosas y/o calcificadas y se hizo estudio bacteriológico e histológico del líquido periprotésico recogido.
Todas fueron evaluadas clínicamente por su cirujano plástico identificando la presencia de dolor, deformidad, parestesias, contractura según escala de Baker, alteraciones cutáneas, presencia de nódulos palpables y fecha de implantación.
Todos los resultados obtenidos del examen clínico, ecográfico y los hallazgos operatorios se relacionaron para ver si podía existir alguna correlación estadísticamente significativa entre la fecha de implantación y los hallazgos y las características del implante, específicamente con la integridad del mismo.
Los datos fueron sometidos a una prueba estadística con el programa SPSS versión 14 para estadística descriptiva, variables cualitativas y porcentajes. Se calcularon sensibilidad y especificidad, valor predictivo positivo y valor predictivo negativo en relación a los hallazgos ecográficos frente a los quirúrgicos.
RESULTADOS
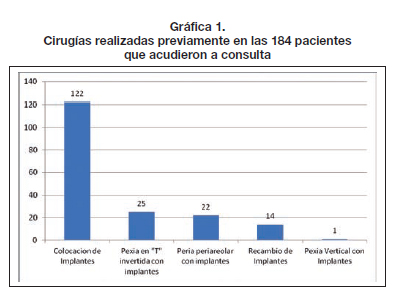
Sobre un total de 1.315 pacientes operadas por los 7 cirujanos participantes en el estudio en 5 ciudades diferentes, acudieron a revisión durante el período de 14 meses comprendido entre enero de 2012 y febrero de 2013 un total de 184, revisándose 368 implantes. La cirugía primaria en estas 184 pacientes consistió en: colocación simple de implantes mamarios en 122 (66,3%); pexia en T con implantes en 25 (13,5%); pexia periareolar con implantes en 22 (11,9%); recambio de implantes en 14 (7,6%) y pexia vertical con implantes en 1 (0,5%) (Gráfica 1).
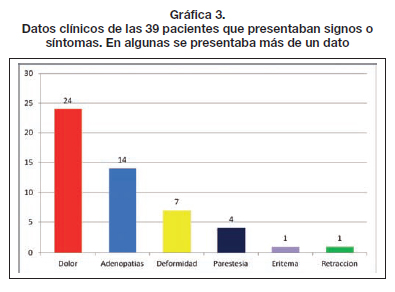
La gran mayoría de estas pacientes acudió a la revisión motivada por la información sobre los implantes PIP® en los medios de comunicación. De estas 184 pacientes, 145 (78,8%) no presentaban signos o síntomas clínicos, mientras que 39 pacientes (21,2%) sí presentaban síntomas (Gráfica 2). De las pacientes sintomáticas, 24 presentaban dolor en alguna de sus mamas; 14 tenían adenopatías; 7 deformidad de alguna de sus mamas; 4 referían parestesias; 1 mostraba eritema y 1 retracción cutánea (Gráfica 3).
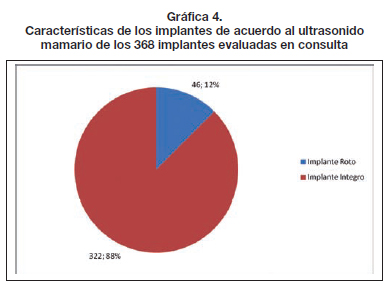
Se sometió a estudio ecográfico mamario a las 184 pacientes (368 implantes). Dentro de los hallazgos ecográficos se determinó: 46 implantes rotos (12,5%) y 322 implantes íntegros (87,5%) (Gráfica 4). Otrtos hallazgos ecográficos en estas mismas pacientes fueron: imagen de capsula periprotésica sin alteraciones en 302 mamas (82%); deformidad del implante en 35 mamas (9,5%); presencia de liquido periprotésico en 30 mamas (8%); capsula gruesa en 29 mamas (7,8%), y calcificación en 11 mamas (3%) (Gráfica 5).
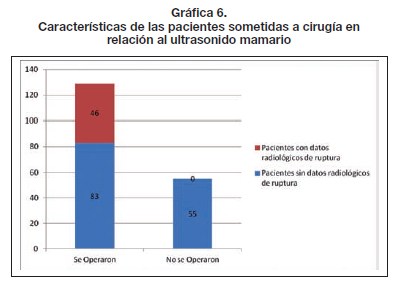
De las 184 pacientes que consultaron, 129 (70%) decidieron operarse para retirada de los implantes PIP®, mientras que 55 (30%) optaron por no operarse ya que se encontraban clínicamente asintomáticas y ecográficamente no presentaban signo alguno de rotura. Es importante hacer notar que de las 129 pacientes operadas, solo 46 (36%) lo hicieron por evidencia clínica y/o radiológica de implante roto, mientras que 83 (64%) decidieron operarse por opción personal ya que no presentaban signos y síntomas clínicos o radiológicos que mostraran rotura de los implantes (Gráfica 6).
De las 129 pacientes operadas, en 102 (79%) solo se practicó retirada y cambio de los implantes; a 13 (10%) cambio de implantes y pexia en T; a 9 (7%) cambio de implantes con pexia periareolar; a 4 (3%) retirada definitiva de los implantes por decisión de las pacientes, y a 1 (1%) cambio del implantes más pexia vertical (Gráfica 7).
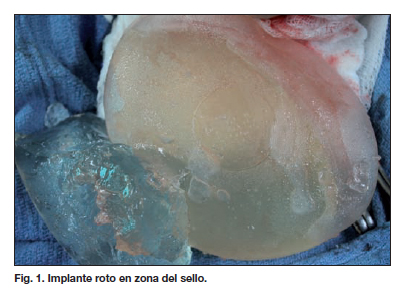
Durante la cirugía se encontraron 213 implantes íntegros (83%) y 45 implantes rotos (17%) (Gráfica 8). Estos resultados se correlacionaron con los informes de las ecografías mamarias de las pacientes. En aquellos implantes cuya integridad lo permitió, se observó rotura en la circunferencia externa del sello del implante (Fig. 1).
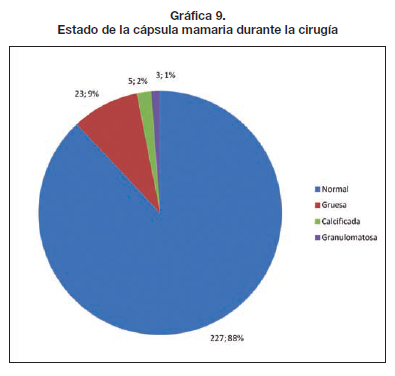
El manejo de la cápsula periprotésica por cada cirujano fue decisión personal de acuerdo a su experiencia e indicación quirúrgica habitual; solamente se les solicitó hacer biopsia si había presencia de cápsula anormal: engrosada, calcificada o con granulomas visibles. También se indicó la recogida para estudio del líquido periprotésico en caso de existir. Los datos recogidos indicaron que 227 de las cápsulas mamarias eran macroscópicamente normales (87%); 23 (8,5%) estaban engrosadas; 5 calcificadas (2,3%) y 3 con aspecto granulomatoso (1%) (Gráfica 9). El estudio anatomopatológico en los casos en que se realizó informó de presencia de granulomas por reacción a silicona y metaplasia de tipo sinovial. El análisis del líquido periprotésico en los casos en que se realizó, presentó histología normal, falta de crecimiento bacteriano por cultivo, sin anomalías en la tinción de Gram.
De los 258 implantes retirados, 46 tenían informe ecográfico previo de rotura, mientras que 212 tenían informe de integridad. Quirúrgicamente 213 implantes se encontraron íntegros y 45 rotos. De estos casos se encontraron 3 implantes que por ultrasonido se informaban como íntegros y que en la cirugía estaban rotos, y 6 que por ultrasonido informaban de rotura pero que en la cirugía aparecieron íntegros. Esto nos arroja una sensibilidad de la ecografía mamaria del 93% y una especificidad de 97%.
En el total de los 368 implantes analizados mediante ecografía mamaria, 46 se informaron como rotos ecográficamente, lo cual nos da un porcentaje del 12,5%.
Los valores predictivo positivo y predictivo negativo tomando en cuenta los informes de los radiólogos y los hallazgos quirúrgicos fueron de 87,5% y 98,5% respectivamente. Esto significa que un informe de implante roto por ultrasonido tiene posibilidades de ser certero en un 87,5%, mientras que un informe de implante íntegro por ultrasonido tiene posibilidades de ser cierto en un 98,5%.
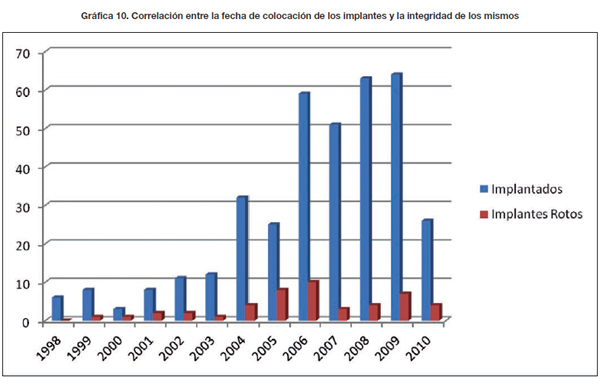
No se encontró correlación con significancia estadística entre el tiempo transcurrido desde la colocación de los implantes y la integridad de los mismos, ya que la dispersión de acuerdo al tiempo de colocación fue muy heterogénea (Gráfica 10).
Discusión
Este estudio es el primero de tipo multicéntrico realizado en nuestro entorno en el que se pretende aportar evidencia clínica sobre las características físicas reales de los implantes PIP®, con recogida de historial de colocación y valoración a largo plazo, así como datos del posible efecto en el cuerpo de las pacientes que los portan, con el objetivo de brindar una orientación adecuada a las pacientes que tienen colocados estos implantes y a la comunidad médica. Creemos que una información científicamente verídica lleva consigo la disminución de la ansiedad de las pacientes provocada en la mayoría de las ocasiones por las informaciones proporcionadas por los medios de comunicación (5-7).
Desde que Cronin y Gerow (1) realizaron su primer implante mamario con prótesis de silicona en 1963, se ha venido evolucionando tecnológicamente en la elaboración de un implante lo menos peligroso posible para el cuerpo de la paciente receptora. Para ello, se han ideado cubiertas más delgadas pero a la vez más resistentes, diferentes tipos de texturas para reducir el grado de contractura capsular y diferentes tipos de geles para evitar que en el caso de una rotura del implante, la silicona pueda migrar al resto del cuerpo (2). Todo esto bajo la supervisión y control de las autoridades gubernamentales locales, regionales e internacionales.
La rotura de un implante mamario puede ser producto de varios factores, tales como defectos de fabricación o deterioro de la cubierta del implante por el paso del tiempo o por traumatismos (8,9). En el caso de los implante PIP®, el fabricante cambió las especificaciones del gel sin la aprobación y la homologación correspondiente por parte de la autoridad reguladora francesa (AFSSAPS) (4). Cuando este hecho se notificó, provocó una alarma mundial producto del posible aumento en la incidencia de rotura de los implantes de esta marca, hasta el punto de llegarse a la recomendación general de la necesidad de retirada de los mismos (4-7).
México no escapo ante la ola de especulaciones. Por tal motivo, la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS) y la Asociación Mexicana de Cirugía Plástica, Estética y Reconstructiva (AMCPER), fijaron su posición con un comunicado en el que se recomendó dejar de colocar implantes marca PIP®, aclarando que dichos implantes solo tenían mayor riesgo de rotura (10).
En 12 años, el grupo de 7 cirujanos plásticos que participó en nuestro trabajo operó un total de 1.315 pacientes, colocando 2.630 implantes de marca PIP®, de las cuales regresaron a la consulta para evaluación al momento de surgir el problema 184 pacientes, valorándose un total de 368 implantes; 145 de estas pacientes no presentaban en ese momento sintomatología alguna y solo consultaron motivadas por la información publicada por los diferentes medios de comunicación. El porcentaje de rotura determinada ecográficamente en estas pacientes fue del 12,5%, muy concordante con los hallazgos quirúrgicos, que fueron del 17,8%.
Sin embargo hemos de señalar que esta cifra representa un mayor índice del recogido por dos de las empresas fabricantes con aprobación FDA, Mentor® (Johnson & Johnson, EE.UU.) y Natrelle® (Allergan Inc. EE.UU.) (11,12), pero menor que el que recogen Maijers y col. (13) quienes hablan de un índice de rotura del 24% en los implantes PIP® colocados 10 años antes. En los CORE estudios para la FDA se encontró necesaria una reoperación por rotura de implantes en el 4,4% de los implantes Natrelle de Allergan® a los 4 años de colocados (11), mientras que para Mentor® fue de 0,9% en 3 años (12). Sin embargo Embrey y col. (9) recogen prevalencias de rotura muy variables en la mayoría de los grupos que revisaron, oscilando entre el 4,5% y el 63,5%, con un seguimiento promedio de 7,8 años. Por lo tanto, el seguimiento de los estudios realizados tanto por Mentor® como por Allergan® parece ser insuficiente, ya que a mayor tiempo de seguimiento parece encontrarse un aumento del índice de rotura (9,13-17).
Maijers y col (13) no encontraron diferencia entre los implantes colocados en 2000 y 2001, momento en el que según los informes de la agencia francesa se hizo el cambio del gel. En su estudio, estos autores plantean la hipótesis de un defecto de la cubierta del implante. Esto podría concordar con nuestros hallazgos, ya que en aquellos implantes retirados en nuestras pacientes del grupo de estudio en los que por su integridad de forma fue posible verificar el sitio de rotura, pudimos comprobar que ésta se produje en el sello de la base del implante. Sin embargo, creemos que se deben realizar estudios de investigación específicos en este aspecto para confirmar dicha hipótesis.
Dentro de los principales síntomas que encontramos entre nuestras pacientes, destacaron la presencia de dolor y adenopatías. Asimismo, ecográficamente encontramos que una cápsula gruesa o la presencia de deformidad fueron los signos más relevantes para la sospecha de un implante roto.
A todas las pacientes se les realizaron estudios ecográficos e histológicos sin evidencia de presencia de alguna lesión sospechosa de malignidad. Solo el 1% presentó calcificación, y postquirúrgicamente el hallazgo más relevante fue la presencia de cápsulas granulomatosas por reacción al material de silicona. Esto concuerda con el informe de Sir Bruce Keogh en un estudio realizado por el Instituto Nacional del Cáncer del Reino Unido y Australia para el National Health Sistem (NHS), en el que el grupo de expertos no encontró evidencia de que los implantes PIP® se asociaran a un mayor riesgo de padecer cáncer que con cualquier otro implante mamario de gel de silicona (7). Asimismo, este grupo de expertos realizó un estudio toxicológico del gel de los implantes PIP® llegando a la conclusión de que el análisis hecho a las muestras recolectadas no mostraba alteraciones ni riesgo para la salud de las pacientes portadoras de estos implantes (7). Esto también concuerda con nuestros hallazgos, ya que la mayoría de nuestras pacientes (79%) no presentaba signo o síntoma alguno, lo cual refuerza la teoría de que los implantes PIP® no presentarían riesgo aumentado de toxicidad local.
Según Embrey y col. (9), el porcentaje de sensibilidad en la detección de anomalías estructurales en implantes mamarios mediante mamografía es del 83%, 75% para la resonancia magnética (RM) y 50% para el ultrasonido, con una especificidad del 43% frente al 71% de la RM y el 40% de la mamografía. Por otro lado, en la Guía de la Primera Conferencia Internacional de Implantes Mamarios celebrada en el 2009 (18,19), se recomienda el ultrasonido mamario como mejor método de estudio postquirúrgico para la evaluación de rotura de los implantes. Este último informe validaría nuestros hallazgos en los que el ultrasonido mamario presentó un 93% de sensibilidad y un 97% de especificidad para evaluar la integridad de los implantes. El ultrasonido sería por tanto un estudio bastante confiable para la determinación de la rotura de implantes mamarios, evitando el riesgo de una rotura de los mismos debida a la presión ejercida durante una mamografía, y el costo excesivo de una RM. Como desventaja, hay que señalar que el ultrasonido es una técnica operador-dependiente, y que por lo tanto es necesario contar con la colaboración de un experto radiólogo para la evaluación de los implantes mamarios. En nuestro estudio, mejoramos esta debilidad buscando en cada uno de los centros quirúrgicos que participaron la colaboración de un especialista en radiología mamaria para que revisara a las pacientes.
Es muy interesante señalar en nuestro estudio, como dato relevante, los valores predictivos obtenidos con el ultrasonido, comprobando que un informe ecográfico de implante integro es mucho más certero que un informe de implante roto.
Actualmente sabemos que no hay evidencia científica de mutagenecidad, toxicidad del gel o riesgo de padecer cáncer por los implantes PIP® (5, 20). Específicamente en nuestro estudio, el 64% de las pacientes que decidieron retirarse los implantes estaban asintomáticas, y de no haber existido miedo por la información ofrecida por los medios de comunicación, no se hubieran operado. Esto concuerda con el estudio definitivo de la NHS (17) en el que un tercio de las pacientes se operaron motivadas por la ansiedad sufrida debido a la desinformación. Igualmente, el Comité Científico de Riesgos de Salud Emergentes y Nuevamente Identificados (SCENIHR), concluyó que de acuerdo a los datos médicos, toxicológicos, o de otro tipo, recogidos hasta la fecha, no es necesario exigir la retirada de los implantes PIP® íntegros como medida de precaución en ausencia de indicaciones clínicas o psicológicas (20).
Conclusiones
El índice de rotura de los implantes PIP® analizados en nuestro entorno geográfico fue del 12,5% mediante ecografía mamaria y del 17,4% comprobado intraoperatoriamente en las pacientes que optaron por la retirada de los mismos. Estas cifras son mayores que las recogidas hasta la fecha por las empresas fabricantes de implantes mamarios con aprobación FDA.
Dado que las autoridades sanitarias informan de que no se ha encontrado mayor riesgo de toxicidad, mutagenicidad o de producir cáncer con estos implantes que con cualquier otro implante de gel de silicona, datos que también concuerdan con nuestros hallazgos, creemos que la indicación para retirada de los mismos debe basarse en la evidencia o sospecha de rotura, como sucede con cualquier otro implante mamario.
Por lo tanto, ante la detección de un mayor porcentaje de roturas, sería recomendable para las pacientes portadoras de implantes PIP® el someterse a una revisión anual por un cirujano plástico, acompañada de un estudio radiológico mamario. El estudio de elección sería el ultrasonido, ya que ha demostrado ser altamente específico y sensible, con un costo muy accesible, pero siempre que sea realizado por un radiólogo especializado en diagnóstico mamario.
Bibliografía
1. Cronin TD, Gerow FJ. Augmentation mammaplasty: New "natural feel" prosthesis. Transactions of the third International Congress of Plastic Surgery, October 13-18, 1963. Amsterdam, the Netherlands. Excerpta Medical Foundation, 1963: 41-49. [ Links ]
2. Bostwick, J. Tratado de Mamoplastia.eD. Amolca. Caracas, Venezuela. 2001. Vol.1. 2o edición, P. 659. [ Links ]
3. http://www.accessdata.fda.gov/cdrh_docs/pdf7/P070004A.pdf. [ Links ]
4. Agencia Francesa de Seguridad de Productos Sanitarios. Comunicado de prensa. Implantes de silicon producidos por PolyImplant Prothesis (PIP). Francia, 1 Abril de 2010. [ Links ]
5. Secretaria a cargo de la Salud. Comunicado de prensa. Actualización de recomendación para mujeres con implantes de silicon PolyImplant Prosthesis (PIP). Paris, 23 de Diciembre de 2011. [ Links ]
6. Williams N. The scandal of device regulation in the UK. Lancet; 2012. 12; 379: 1789-1790. [ Links ]
7. Woods, K. Device regulation in the European Union: response from MHRA. Lancet. 2012. 11; 379: 515. [ Links ]
8. Kwan ChulTark, Hii Sun Jeong, Tae sukRoh, Jong Woo Choi. Analysis of 30 Breast Implant Rupture Cases. Aesth Plast Surg. 2005. 29: 460-469. [ Links ]
9. Embrey M. Adams E., Cunningham B., Peters W., Leroy Young and Carlo G. Factors Associated with Breast Implant Rupture: Pilot of a Retrospective Analysis. Aesth Plast Surg. 1999. 23:207-212. [ Links ]
10. Comisión Federal para la Protección contra riesgos sanitarios. Comunicado de prensa 02/2012. México, 4 de Enero 2012. [ Links ]
11. http://www.accessdata.fda.gov/cdrh_docs/pdf2/P020056b.pdf. [ Links ]
12. http://www.accessdata.fda.gov/cdrh_docs/pdf3/p030053b.pdf. [ Links ]
13. Maijers, MC, Niessen,FB.: Prevalence of rupture in Poly Implant Prothese silicone breast implants, recalled from the european market in 2010. Plast Rec.Surg. 2012. 129(6): 1372-1378. [ Links ]
14. Dowden, RV. Detection of gel implant rupture: A clinical test. Plast Rec Surg 1993. 91 (3) : 548-550. [ Links ]
15. Robinson OG, Bradley EL, Wilson DS. Analysis of explanted silicone implants: A report of 300 patients. Ann Plast Surg 1995, 34 (1): 1-6. [ Links ]
16. Menke H, Grubmeyer H, Biemer E and Olbrisch RR. PIP breast implants after two years: Initials result of a prospective study. Aesth Plast Surg. 2001. 25 (4): 278-282. [ Links ]
17. Keogh, B. Poly Implant Prothesis (PIP) Breast Implants: Final report of the expert Group. National Health Service, UK, Junio, 2012. [ Links ]
18. Stoblen F., Rezai M. and Kummel S. Imaging in patients with breast implants -results of the first International Breast (Implant) Conference 2009. Insights Imaging. 2010. I, 93-97. [ Links ]
19. R. Mann, C. Kuhl, K. Kinkel, C. Boetes. Breast MRI: guidelines from European society of breast imaging. Eur Radio. 2008,18: 1307-1318. [ Links ]
20. Ministerio de Sanidad, Servicios Sociales e Igualdad. Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Nota Informativa. 30 de Octubre del 2013. Actualización de la información y de las recomendaciones sobre prótesis mamarias Poly Implant Prothese (PIP). [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Dr. Lázaro Cárdenas Camarena
INNOVARE Cirugía Plástica Especializada
Av. Verona 7412, Fraccionamiento Villa Verona
Zapopan, Jalisco 45110. México
e-mail: drlazaro@drlazarocardenas.com