Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Enfermedades Digestivas
versión impresa ISSN 1130-0108
Rev. esp. enferm. dig. vol.105 no.10 Madrid nov./dic. 2013
https://dx.doi.org/10.4321/S1130-01082013001000015
CARTAS AL EDITOR
Melanoma maligno en paciente con enfermedad de Crohn y tratamiento con anti-TNF-α
Malignant melanoma in a patient with Crohn's disease and treated with anti-TNF alpha
Palabras clave: Enfermedad de Crohn. Melanoma maligno. Fármacos anti-TNF-α.
Key words: Crohn's disease. Malignant melanoma. Anti-TNF alpha drugs.
Sr. Editor:
Se ha documentado una posible asociación entre los fármacos inhibidores del factor de necrosis tumoral alfa (anti-TNF-α) y el desarrollo de cáncer de piel, fundamentalmente descritos en pacientes afectos de artritis reumatoide y psoriasis.
La mayoría de las neoplasias cutáneas asociadas al tratamiento con anti-TNF-α son del tipo de cáncer de piel no melanomas (CPNM) y, aunque existen casos anecdóticos de melanomas, ninguno se ha descrito en pacientes con enfermedad inflamatoria intestinal (EII).
Nosotros presentamos un caso de melanoma maligno (MM) en paciente con enfermedad de Crohn (EC) y tratamiento con inhibidores del TNF-α, así como una breve revisión de la literatura, para determinar si es necesaria una mayor vigilancia para la detección de estas lesiones en este tipo de pacientes.
Caso clínico
Presentamos un caso de melanoma maligno (MM) en un varón de 29 años con enfermedad de Crohn (EC) ileocólica de 18 años de evolución, intervenida mediante colectomía subtotal y posterior anastomosis íleo-rectal por enterorragia severa asociadas a la enfermedad. Tras la intervención quirúrgica (hace 10 años) y debido a recurrencia de la enfermedad de difícil control, precisa tratamiento con azatioprina (que ya venía utilizando durante 10 años) e infliximab durante 2 años. Tras pérdida de respuesta a este, precisó adalimumab, que ha recibido desde el año 2008, precisando en el último año intensificación del mismo por pérdida de eficacia.
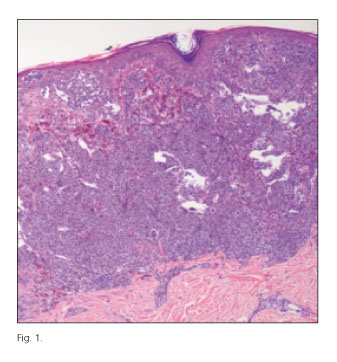
Acude a consulta de dermatología por nevus en espalda, que en los últimos 8 meses experimentó cambios y sangrado con el roce de la ropa. Dada la sugestiva malignidad, se extirpa la lesión, identificándose como un melanoma nodular ulcerado de 7 mm (espesor de Breslow 1,26 mm y nivel de Clark III) sin invasión vascular y/o neural, estadio pT2b de la clasificación TNM (Fig. 1). Biopsia del ganglio centinela negativo.
Discusión
Colectivamente, los fármacos biológicos han sido evaluados en miles de pacientes mostrando un claro beneficio, con una tolerabilidad y seguridad más que aceptables sin embargo, cada vez con más frecuencia, se está relacionando los fármacos anti-TNF-α con la progresión del cáncer de piel (1). Los más frecuentes son los cáncer de piel no melanoma (CPNM), tanto los carcinomas de células basales, como los de células escamosas.
El metaanálisis de Burmester y cols. (2), basado en ensayos clínicos con adalimumab en 23.458 pacientes tratados por diferentes patologías, evidenció que los pacientes con artritis reumatoide (AR), psoriasis y EC, presentan un mayor riesgo de desarrollo de CPNM que la población general. En la AR y la psoriasis, a diferencia de la EC, parece existir un mayor riesgo de MM en los tratados con adalimumab.
En una gran cohorte retrospectiva de pacientes con EC (n 26.403) Long y cols. (3), también encontraron un mayor riesgo de CPNM (n 387) en los pacientes tratados con adalimumab o infliximab, pero no para MM.
Askling y cols. (4), estudiaron los efectos a corto plazo (con una exposición media a los anti-TNF-α menor de 6 meses) de etanercept, infliximab y adalimumab, a través de un metaanálisis que incluye a 15.418 pacientes, encontrando un aumento del riesgo para el desarrollo de CPNM, pero no para los MM. Destacar que el 95 % de los pacientes con infliximab recibían tratamiento inmunosupresor concomitante, por un 71 % y 28 % en los casos de adalimumab y etanercept respectivamente.
Además ese aumento del riesgo de MM en AR o psoriasis también suele acompañarse del uso concomitante de otros tratamientos potencialmente cancerígenos (retinoides, ciclosporina, azatioprina), lo cual dificulta conocer el verdadero papel jugado por estos fármacos en la carcinogénesis de estos tumores.
Además, en nuestro caso el paciente recibió azatioprina concomitantemente, cuyo uso se ha relacionado con un mayor riesgo para CPNM por aumento de la fotosensibilización (3).
De hecho, un reciente estudio prospectivo francés (5) sobre pacientes con enfermedad inflamatoria intestinal encuentra que el uso continuado de azatioprina aumenta el riesgo de CPNM.
Además del aumento de la fotosensibilización, parece que las tiopurinas, a través del metabolito tioguanina-6, provocan un estrés oxidativo con lesiones en el ADN y por tanto, con potencial de desarrollo de cánceres de piel (6).
Se desconoce la biopatología de la iniciación de las neoplasias melanocíticas. En estudios experimentales con ratones se ha observado que TNF-α a través de la activación de moléculas específicas, tales como TNFR1, TNFR2, presenta actividad protumoral (7). Diferentes autores postulan que la participación de los antagonistas del TNF-α probablemente se vinculen a la progresión de la carcinogénesis (8) impulsando la progresión del tumor, lo cual sería de especial interés en los casos de existencia de una lesión precursora subclínica o cánceres in situ.
El papel exacto de los fármacos anti-TNF-α en la carcinogénesis es incierto, pues aunque parecen intervenir en la progresión tumoral, no podemos saber si el desarrollo de un CPNM o MM es por este motivo, o si es por una confluencia de factores como el uso concomitante de otros inmunosupresores, como la azatioprina, o la propia disfunción inmune subyacente en la EC.
En conclusión, presentamos un caso de MM en EC con tratamiento anti-TNF-α asociado a azatioprina de larga evolución. Dado que existen múltiples estudios donde se ha analizado la prevalencia de tumores cutáneos sin hallar casos de MM en pacientes con EC, este caso podría deberse al azar, si bien consideramos que estos pacientes bajo tratamiento inmunosupresor, y más aún en los casos de terapia combinada, deberían llevar a cabo programas de prevención, basados en medidas educacionales respecto a la exposición solar e incluso valoración dermatológica a intervalos regulares en pacientes seleccionados con el fin de detectar nuevas lesiones pigmentadas o vigilar posibles cambios en nevus preexistentes.
Alfonso Alcalde Vargas1, Claudio Trigo Salado1,
Eduardo Leo Carnerero1 y Ana Isabel Lorente Lavirgen2
Servicios de 1Gastroenterología y 2Dermatología.
Hospital Universitario Virgen del Rocío. Sevilla
Bibliografía
1. Pierard-Franchimont C, Pierard GE. Cutaneous adverse reactions to monoclonal antibody treatments. Rev Med Liege 2009;64:339-46. [ Links ]
2. Burmester GR, Panaccione R, Gordon KB, McIlraith MJ, Lacerda AP. Adalimumab: Long-term safety in 23458 patients from global clinical trials in rheumatoid arthritis, juvenile idiopathic arthritis, ankylosing spondylitis, psoriatic arthritis, psoriasis and Crohn's disease. Ann Rheum Dis 2013;72:517-24. [ Links ]
3. Long MD, Herfarth HH, Pipkin CA, Porter CQ, Sandler RS, Kappelman MD. Increased risk for non-melanoma skin cancer in patients with inflammatory bowel disease. Clin Gastroenterol Hepatol 2010;8:268-74. [ Links ]
4. Askling J, Fahrbach K, Nordstrom B, Ross S, Schmid CH, Symmons D. Cancer risk with tumor necrosis factor alpha (TNF) inhibitors: Meta-analysis of randomized controlled trials of adalimumab, etanercept, and infliximab using patient level data. Pharmacoepidemiol Drug Saf 2011;20:119-30. [ Links ]
5. Peyrin-Biroulet L, Khosrotehrani K, Carrat F, Bouvier AM, Chevaux JB, Simon T, et al. Cesame Study Group. Increased risk for nonmelanoma skin cancers in patients who receive thiopurines for inflammatory bowel disease. Gastroenterology 2011;141:1621-8. [ Links ]
6. O'Donovan P, Perrett CM, Zhang X, Montaner B, Xu YZ, Harwood CA, et al. Azathioprine and UVA light generate mutagenic oxidative DNA damage. Science 2005;309:1871-4. [ Links ]
7. Arnott CH, Scott KA, Moore RJ, Robinson SC, Thompson RG, Balkwill FR. Expression of both TNF-alpha receptor subtypes is essential for optimal skin tumour development. Oncogene 2004;23:1902-10. [ Links ]
8. Van Horssen R, Ten Hagen TL, Eggermont AM. TNF-alpha in cancer treatment: Molecular insights, antitumor effects, and clinical utility. Oncologist 2006;11:397-408. [ Links ]











 texto en
texto en