Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Cirugía Oral y Maxilofacial
versión On-line ISSN 2173-9161versión impresa ISSN 1130-0558
Rev Esp Cirug Oral y Maxilofac vol.29 no.1 Madrid ene./feb. 2007
Melanoma cutáneo facial con gánglio centinela en región parotídea. Revisión de la literatura
Cutaneous melanoma of the face with sentinel node in parotid region. Revision of the literature
R. del Rosario Regalado1, Á. Rollón Mayordomo2, C.I. Salazar Fernández2, D. Moreno Ramírez2, T. Creo Martínez3, J.M. Pérez Sánchez4
1 Médico Residente.
2 Médico Adjunto.
3 Médico Residente.
4 Jefe de Servicio. Servicio de Cirugía Oral y Maxilofacial
Hospital Universitario Virgen Macarena. Sevilla, España.
Dirección para correspondencia
RESUMEN
Introducción. La parótida es primer escalón ganglionar en la diseminación regional de los melanomas cutáneos de región frontal, orbitaria y nasal. Aunque la linfografía se ha convertido en una prueba diagnóstica estándar en el estudio del melanoma, no está exenta de inconvenientes.
Material y método. Presentamos el caso de un paciente con melanoma frontal y ganglios centinela parotídeos y discutimos las particularidades, ventajas y desventajas de la técnica en dicha región.
Conclusiones. Aunque se ha demostrado que la afectación del ganglio centinela es el factor predictor más importante de recurrencia y supervivencia, creemos que es una técnica en estudio cuyo efecto en la supervivencia debe ser demostrado frente a la alternativa de seguimiento clínico y que por tanto debe indicarse en casos seleccionados con mayor probabilidad de metástasis.
Palabras clave: Melanoma de cabeza y cuello; Linfografía; Disección cervical; Parotidectomía.
ABSTRACT
Introduction. The parotid gland is the first lymph node echelon in the regional dissemination of frontal, orbital and nasal cutaneous melanomas. Although the lymphoscintigraphy has been become a standard diagnostic technique for studying melanomas, it is not exempt of inconveniences.
Material and methods. We present the case of a patient with frontal melanoma and sentinel nodes in the parotid region, and we discuss the peculiarities, advantages and disadvantages of using this technique in this region.
Conclusions. Although it has been proved that an affected sentinel lymph node is the most important prognostic factor for recurrence and survival, we believe that this is a technique under study, and that its influence on survival should be demonstrated with regard to the alternative of clinical monitoring. It should therefore be indicated in specific cases with greater probabilities of metastases.
Key words: Head and neck melanoma; Lymphoscintigraphy; Neck dissection; Parotidectomy.
Introducción
La mayoría de melanomas cutáneos de cabeza y cuello se localizan en frente y cara.1,2
Las metástasis en ganglios linfáticos regionales se producen entre el 14 y 60% de los pacientes según estadios,3,4 y la región parotídea puede verse afectada en el 2,4% de los casos.5
La introducción de la linfoescintigrafia ha permitido localizar el probable primer escalón de drenaje ganglionar de la lesión, lo cual a su vez permite, mediante su extirpación, el diagnóstico precoz de la metástasis ganglionar con una cirugía relativamente simple, de poca morbilidad e incluso con anestesia local y a continuación, si se confirma la afectación, el tratamiento precoz mediante la linfadenectomía regional.6,7
A pesar de las ventajas que supone la técnica del ganglio centinela, existen opiniones contrarias sobre su utilidad e indicación generalizada,8,9 siendo la región parotídea una de las zonas donde dichas controversias son mayores por sus características clínicas, técnicas y quirúrgicas.5,10
Presentamos el caso de un paciente con melanoma frontal y ganglio centinela parotídeo, y discutimos las particularidades, ventajas e inconvenientes de la técnica en dicha región.
Caso clínico
Paciente de 24 años, sin antecedentes, que es intervenido por el servicio de Dermatología de nuestro hospital por presentar lesión melánica en región frontal. Dicha lesión es informada como melanoma maligno de extensión superficial con Breslow de 2 mm y estadio II.
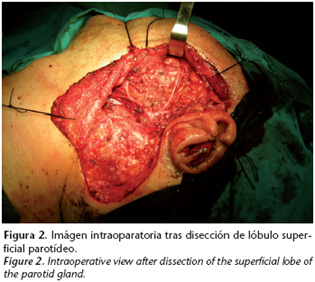
En linfografía preoperatoria se objetivan dos ganglios centinela, uno primario en el seno de la glándula parótida izquierda y otro secundario en cola de dicha glándula. Tras este hallazgo se deriva a nuestro servicio para intervención, practicándose parotidectomía total conservadora y extirpación de tejido graso de polo inferior. El estudio anatomopatológico de la pieza quirúrgica descarta la presencia de metástasis.

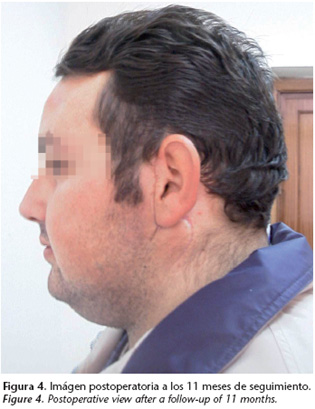
La evolución del paciente es favorable y hasta el momento, tras 24 meses de seguimiento, no se han objetivado recidivas locales, ganglionares ni a distancia.

Discusión
La incidencia de metástasis en ganglios linfáticos parotídeos de melanomas cutáneos de región facial detectados mediante parotidectomía profiláctica es del 2,4%,5 pudiendo llegar al 8%,11 y 13%,12 en estudios realizados con la técnica del ganglio centinela.
Debido a que la probabilidad de aparición de metástasis regionales en melanomas de cabeza y cuello es menor del 20% y que la linfadenectomía profiláctica no aumenta la supervivencia,13 la indicación de la disección ganglionar electiva es controvertida, optando muchos de los autores por realizar seguimiento del paciente y tratamiento de las metástasis en el momento de su detección.14
La disección cervical electiva o profiláctica supone el sobretratamiento o tratamiento no necesario de los pacientes sin metástasis ganglionares que oscilan entre el 95,7 y el 87% de los casos,5,11,12 con lo que implica de aumento en la morbilidad y los costes.
En cabeza y cuello, dicho tratamiento electivo debería incluir en la mayoría de las ocasiones la región parotídea, mediante parotidectomía profiláctica, con los riesgos y secuelas que implica: debilidad temporal del nervio facial en el 15% y definitiva de alguna rama en menos del 5%,15 riesgo que se incrementa en la rama marginal si se asocia disección cervical electiva, síndrome de Frey en un 30% de los casos y secuelas estéticas por hundimiento o cicatriz.11,15
Otra cuestión discutida en el melanoma de cabeza y cuello se refiere a la predicción del camino de drenaje linfático regional para cada paciente.12,14 Mientras que para algunos autores las metástasis linfáticas cervicales siguen un modelo fijo y predecible,14,16,17 acertando en el 92,18 y 97%,19 de los pacientes, para otros, el modelo de distribución es variable.12,20 Sin embargo, dicha predicción solo identifica los niveles cervicales que pueden verse afectados por la diseminación, pero no el lugar exacto ni al paciente con metástasis. Nos permitiría por tanto realizar linfadenectomías regionales profilácticas más selectivas de los posibles niveles afectos, pero sin reducir su número, es decir, el número de pacientes que sobretratamos.

La ventaja que aporta la linfoescintigrafia es la localización del ganglio de drenaje de la lesión, el cual, tras su extirpación y análisis, confirmará aquellos pacientes con metástasis, permitiendo: 1º conocer el patrón de drenaje linfático individual de cada paciente, 2º el estadiaje exacto, 3º la disección ganglionar terapéutica precoz en un segundo tiempo, 4º el tratamiento complementario adyuvante indicado y 5º disponer de información pronóstica referente a supervivencia y recurrencia. Es una técnica quirúrgica diagnóstica indicada en melanomas cuya profundidad sea superior de 1 mm o con nivel de Clark IV.21,22 En los pacientes cuyo ganglio centinela sea negativo, la técnica evita la cirugía agresiva de la disección cervical electiva o la parotidectomía electiva y, por tanto, la morbilidad y coste.8
Sin embargo, la técnica del ganglio centinela también tiene inconvenientes y la información que aporta es controvertida, lo que hace que su justificación pueda ser dudosa frente a la pauta de esperar y ver evolución.9
En el 34% de los pacientes la linfografía detecta ganglios que no concuerdan con los que la predicción clínica establece.10 Dicha discordancia consiste en la identificación como ganglios centinelas de los ganglios retroauriculares en el 13,4% y contralaterales en el 72%, hallazgos contrarios a los observados durante el seguimiento, donde los casos de metástasis en dichos ganglios oscilan entre 1,5-2,9%.10,18,19
La técnica presenta una tasa de falsos negativos menor del 4% si lo determinamos mediante la disección ganglionar realizada concomitantemente.23 Sin embargo, si el criterio es la recurrencia en la zona del ganglio centinela sin disección previa, la tasa de falsos negativos puede variar entre el 0 y el 25% en función del tiempo de seguimiento, el estudio anátomo-patológico realizado (inmunohistoquímico o no), la experiencia del equipo investigador y el método utilizado.9,10,12 Creemos que algunos resultados pueden mejorarse con la utilización de gamma probe (sonda intraoperatoria) como emplean Lin y cols.24
Las complicaciones descritas son bajas e incluyen: seroma (3%), infección de la herida (3%), hematoma (2,5%), reacción alérgica,24,25 y se discute el riesgo de si la inyección de radiofármaco y colorante puede aumentar las metástasis en tránsito.24,26
Finalmente, estamos ante una intervención solo diagnóstica donde no existen datos sobre la eficacia en relación a la supervivencia, es decir, si el tratamiento precoz de estos pacientes una vez se detecte la metástasis mejora su supervivencia.9
Las consideraciones que hay que tener presente ante un ganglio centinela en región parotídea son las generales descritas anteriormente a las que hay que añadir las determinadas por su localización, cuya proximidad al nervio facial hace que su extirpación sea más complicada.10,12
La incidencia de metástasis linfáticas parotídeas en melanoma de cabeza y cuello en estadios iniciales se mantiene entre un 2,4%- 13%,5,11,12 sin embargo la detección de ganglios centinelas preoperatorios en dicha región varia entre el 95 y 35,2%,10-12 lo que se puede explicar por diferencias de aparatología y experiencia del equipo.
Según la localización, los ganglios centinelas de la región parotídea se pueden clasificar en intraparotídeos, que asientan en el interior de la glándula, y periparotideos, que asientan por fuera o en la perifería (estos a su vez se clasifican en anteriores, infraglandulares y supraglandulares).11,12 En las series de Olilla y cols.12 y Fincher y cols.11 la distribución de ganglios intraparotídeos y extraparotídeos es al 50%.
Aunque algunos autores cuestionan la seguridad de realizar la linfadenectomía del ganglio centinela en la región parotídea,5,10 Olilla y cols.12 la realizan en 37 de sus 39 pacientes y Fincher y cols.11 en 12 de sus 18 pacientes (6 con ganglios periparotídeos y 3 intraparotídeos), considerando que los intraparotídeos se pueden extirpar con mínimo riesgo11 y aconsejando una disección meticulosa intraglandular y el uso prudente de electrobisturí.11,12
Ante el riesgo de una lesión definitiva del nervio facial, la alternativa es la de realizar una parotidectomía conservadora, 27 previa localización y disección del nervio facial, extirpando la glándula donde se encuentre el ganglio, lo que realizan Fincher y cols.11 en los 6 pacientes restantes (33% del total) con ganglios intraparotídeos. Esto supone realizar una parotidectomía profiláctica, cirugía de mayor envergadura cuyo tiempo de quirófano y estancia hospitalaria es superior a una simple adenectomía.
El principal inconveniente de la adenectomía aislada es la lesión del nervio durante la extirpación, o en un segundo tiempo si fuese necesario la parotidectomía. Para evitarlo, Lin y cols,24 recomiendan la utilización de sistemas de monitorización intraoperatorios no invasivos. Olilla y cols.12 presentan como única complicación en su serie de 37 linfadenectomías parotídeas un caso (2,6% de los pacientes) de paresia del nervio facial transitoria, incluso extirpando una media de 2-3 ganglios por paciente, Fincher, 11 en su serie de 12 linfadenectomías en parótida, no presenta ninguna complicación al igual que Lin.24
En parótida, la tasa de falsos negativos es del 3,1%-12,5%.10,12,23 La sensibilidad de la técnica es del 64-80%, es decir, de los pacientes que tienen metástasis subclínicas en parótida, un 20-36% no son detectados (falsos negativos), 10,12,24 lo cual se puede explicar por el pequeño tamaño de los ganglios.10,11
Con el fin de mejorar estos resultados se aconseja evitar la inyección abundante de contraste en los melanomas de mejilla, para impedir su extravasación o superposición con la parótida, y levantar colgajos de piel finos, para evitar incluir los ganglios en el colgajo.14
Una vez confirmada la afectación del ganglio parotídeo, la mayoría de autores están de acuerdo en realizar parotidectomía total conservandora y algunos también asocian la disección cervical12,14 ya que el 50% de los pacientes con ganglio parotídeo afectado presentan o presentarán metástasis cervicales.12
La mayoría de los ganglios parotídeos se localizan en la región superficial de la glándula.5,26 Según estudios anatómicos, en el lóbulo superficial pueden asentar hasta 20 ganglios y en el profundo entre 0-5 ganglios. 28,29 Aunque pudiera parecer que la parotidectomía superficial no supone un tratamiento electivo eficaz por no eliminar la totalidad de ganglios intraglandulares, si se realiza sin objetivar ganglios positivos, no se describen recidivas posteriores en lóbulo profundo.5 Sin embargo no está claro si tras una parotidectomía superficial con ganglios positivos es preciso realizar posteriormente una parotidectomía profunda, sobre todo en los casos donde la parotidectomía se haya realizado como técnica de extirpación del ganglio centinela.
Conclusión
Aunque se ha demostrado que la afectación del ganglio centinela es el factor más importante predictor de recurrencia y supervivencia, 23 tenemos la duda de que esta habilidad justifique el que realicemos una prueba diagnóstica-quirúrgica, sin esperar a que esté demostrada su eficacia en la supervivencia frente a la alternativa de seguimiento clínico.
Creemos que debe indicarse selectivamente e individualmente, como técnica experimental o dentro de ensayos clínicos,9 como realizamos en nuestro hospital.
En los casos que se realicen y se detecten ganglios en la región parotídea deberemos analizar la linfografia preoperatoria para distinguir si el/los ganglios son periparotídeos o intraparotídeos y en estos últimos, valorar el grado de profundidad.
En ganglios periparotídeos e intraparotídeos superficiales realizaremos ecografía previa de alta resolución, que permitirá confirmar la existencia y localización de adenopatías de hasta 2,5 mm, que serán confirmadas intraoperatoriamente con la sonda, y adenectomía.
En ganglios intraparotídeos profundos, ante el riesgo de lesión nerviosa, creemos que lo indicado es la parotidectomía superficial conservadora, confirmando tras su extirpación con la sonda, que se han extirpado todos los ganglios, sin dejar restos en el lóbulo profundo o nivel I cervical.
Bibliografía
1. OBrien CJ, Coates AS, Petersen-Schaefer K, Shannon K, Thompson SF, Milton GW, et al. Experience with 998 cutaneous melanomas of the head and neck over 30 years. Am J Surg 1991;162: 310-4. [ Links ]
2. Kane WJ, Yugueros P, Clay RP, Woods JE. Treatment outcome for 424 primary cases of clinical stage I cutaneous malignant melanoma of head and neck. Head Neck 1997;19:457-65. [ Links ]
3. Myers JN. Value of neck disection in the treatment of patients wiyh intermediate- thickness cutaneous malignant melanoma of the head and neck. Arch Otolaryngol Head Neck Surg 1999;125:110-5. [ Links ]
4. Harris C, Bailey J, Blanchaert RH. Surgical management of cutaneous melanoma of the head and neck. Oral Maxillofacial Surg Clin North Am 2005;17:191- 204. [ Links ]
5. O´Brien CJ, Petersen-Schaefer K, Papadopoulos T, Malka V. Evaluation of 107 therapeutic and elective parotidectomies for cutaneous melanoma. Am J Surg 1994;168:400-3. [ Links ]
6. Morton DL, Wen DR, Wong JM, Economou JS, Cagle LA, Storm FK, y cols. Technical details of intraoperative lymphatic mapping for early stage melanoma. Arch surg 1992;127:392-9. [ Links ]
7. Morton DL, Wen DR, Foshag LJ, Essner R, Cochran A. Intraoperative lymphatic mapping and selective cervical lymphadenectomy for early-stage melanomas of the head and neck. J Clin Oncol 1993;11:1751-6. [ Links ]
8. Brobeil A, Cruse CW, Messina JL, Glass LF, Haddad FF, Berman CG, y cols. Cost analysis of sentinel lymph node biopsy as an alternative to elective lymph node dissection in patients with malignant melanoma. Surg Oncol Clin North Am 1999; 8:435-45. [ Links ]
9. Meirion Thomas J, Patocskai EJ. The argument against sentinel node biopsy for malignant melanoma. BMJ 2000;321:3-4. [ Links ]
10. O´Brien CJ, Uren RF, Thompson JF, Howman-Giles RB, Petersen-Schaefer K, Shaw HN, y cols. Prediction of potential metastatic sites in cutaneous head and neck melanoma using lymphoscintigraphy. Am J Surg 1995;170:461-6. [ Links ]
11. Fincher TR, OBrien JC, McCarty TM, Fisher TL, Preskitt JT, Lieberman ZH, y cols. Patters of drainage and recurrence following sentinel lymph node biopsy for cutaneous melanoma of the head and neck. Arch Otolaryngol Head Neck Surg 2004; 130:844-848. [ Links ]
12. Ollila DW, Foshag LJ, Essner R, Stern SL, Morton DL. Parotid region lymphatic mapping and sentinel lymphadenectomy for cutaneous melanoma. Annals of Surgical Oncology 1999;6:150-4. [ Links ]
13. Lens MB, Dawes M, Goodacre T, Newton-Bishop JA. Elective lymph node dissection in patients with melanoma. Arch surg 2002;137:458-61. [ Links ]
14. O´Brien CJ, Shah JP, Balm AJ. Neck dissection and parotidectomy for melanoma. En: Textbook of Melanoma. Ed Thompson JF, Morton DL, Kroon BB. London Libro 2004;296-306. [ Links ]
15. Bron LP, O´Brien CJ. Facial nerve function after parotidectomy. Arch Otolaryngol Head Neck Surg 1997;123:1091-6. [ Links ]
16. Wells KE, Cruce CW, Daniels S, Berman C, Norman J, Reintgen DS. The use of lymphoscintigrafy in melanoma of the head and neck. Plast Reconstr Surg 1994; 93:757-61. [ Links ]
17. Shah JP, Kraus DH, Dubner S, Sarkar S. Patters of regional lymphatic metastases from cutaneous melanomas of the head and neck. Am J Surg 1991;162:320- 3. [ Links ]
18. Pathak I, OBrien CJ, Petersen-Schaeffer K, McNeil EB, McMahon J, Quinn MJ, y cols. Do nodal metastases from cutaneous melanoma of the head and neck follow a clinically predictable pattern? Head Neck 2001;23:785-790. [ Links ]
19. OBrien CJ, Petersen-Schaefer K, Ruark D, Coates AS, Menzie SJ, Harrison RI, y cols. Radical, modified and selective neck dissection for cutaneous malignant melanoma. Head Neck 1995;17:232-41. [ Links ]
20. Norman J, Cruse CW, Espinosa C, Cox C, Berman C, Clark R, y cols. Redefinition of lymphatic drainage with the use of lymphoscintigraphy for cutaneous melanoma. Am J Surg 1991;162:432-7. [ Links ]
21. Balch CM, Mihm MC. Reply to the article "The AJCC staging proposal for cutaneous melanoma: comments by the EORTC Melanoma Group" by DJ Ruiter y cols. (Ann Oncol 2001;12:9-11). Ann Oncol 2002;13:175-6. [ Links ]
22. Morris KT, Stevens JS, Pommier RF, Fletcher WS, Vetto JT. Usefulness of preoperative lymphoscintigraphy for the identification of sentinel lymph nodes in melanoma. Am J surg 2001;181:423-6. [ Links ]
23. Gershenwald JE, Thompson W, Mansfield PF, Lee JE, Colome MI, Tseng C, et al. Multi-institutional melanoma lymphatic mapping experience: the prognostic value of sentinel lymph node status in 612 stage I o II melanoma patients. J Clin Oncol 1999;17:976-83. [ Links ]
24. Lin D, Kashani-Sabet M, Singer MI. Role of the head and neck surgeon in sentinel lymph node biopsy for cutaneous head and neck melanoma. Laryngoscope 2005;115:213-7. [ Links ]
25. Jansen L, Nieweg OE, Peterse JL, Hoefnagel CA, Olmos RA, Kroon BBR. Reliability of sentinel lymph node biopsy for staging melanoma. Br J Surg 2000;87: 484-9. [ Links ]
26. Muller MGS, Van Leeuwen PAM, Pijpers R, Van Diest PJ, Meijer S. Pattern and incidence of first site recurrence following sentinel node procedure in melanoma patients. Eur J Surg Oncol 2000;26:272. [ Links ]
27. Eicher SA, Clayman G, Myers J, Gillenwater A. A prospective study of intraoperative lymphatic mapping for head and neck cutaneous melanoma. Arch Otolaryngol Head Neck Surg 2002;128:241- 6. [ Links ]
28. Barr LC, Skene AI, Fish S, Thomas JM. Superficial parotidectomy in the treatment of cutaneous melanoma of the head and neck. Br J Surg 1994; 81:64-5. [ Links ]
29. McKean ME, Lee K, McGregor IA. The distribution of lymph nodes in and around the parotid gland: an anatomical study. Br J Plast Surg 1985;38:1-5. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Ruth del Rosario Regalado
Avda/ Escultora La Roldana nº11 1º A
41500 Alcalá de Guadaíra. Sevilla, España.
E-mail: ruthdelrosario@eresmas.com
Recibido: 02.11.05
Aceptado: 06.10.06











 texto en
texto en 


