INTRODUCCIÓN
El primer calendario de vacunación, oficial desde 19751, estuvo precedido por la vacunación de la viruela, que comenzó en 18002,3, y las campañas de vacunación, que se iniciaron en 1963 con la administración de la vacuna oral frente a la poliomielitis (VPO)4,5,6. Desde 1965 se fueron añadiendo otras vacunas que debían administrarse a la población diana durante las campañas. Ese primer calendario de vacunación (figura 1), que incluía la vacunación frente a siete enfermedades, se actualizó en el año 19817.
Desde que se produjeron las transferencias de salud pública del Estado a las comunidades autónomas (CCAA), entre los años 1979 y 1985, son ellas las competentes en la gestión del programa de vacunación, desde el establecimiento de sus respectivos calendarios de vacunación hasta la compra, distribución y administración de las vacunas2.
Mediante la Ley General de Sanidad (1986) se creó el Consejo Interterritorial del Sistema Nacional de Salud (CISNS) como un órgano permanente de coordinación, cooperación y comunicación entre la Administración del Estado y las CCAA8. El CISNS acordó un calendario común de vacunación en 1996.
En este artículo se resume el funcionamiento de la Ponencia de Programa y Registro de Vacunaciones y su papel en la evolución de los programas de vacunación en España.
PONENCIA DE PROGRAMA Y REGISTRO DE VACUNACIONES
El CISNS tiene la misión de coordinar y armonizar las estrategias de salud con la finalidad de mantener la equidad y la cohesión en el acceso a las prestaciones sanitarias. La ministra o ministro de Sanidad coordina el Pleno del CISNS, que está formado además por los consejeros de sanidad de las CCAA.
El CISNS se organiza en Comisiones, siendo la Comisión de Salud Pública la que establece acuerdos sobre políticas básicas comunes en temas de Salud Pública. Esta Comisión se creó en 1992, está coordinada por la persona encargada de la Dirección General de Salud Pública del Ministerio de Sanidad y está formada por los Directores Generales responsables de la Salud Pública de las CCAA.
De la Comisión de Salud Pública dependen varios Grupos de Trabajo y Ponencias, siendo una de ellas la Ponencia de Programa y Registro de Vacunaciones (en adelante, Ponencia o Ponencia de Vacunas). Esta Ponencia elabora documentos técnicos basados en la evidencia científica y la epidemiología de enfermedades inmunoprevenibles, que sirven de apoyo a la Comisión de Salud Pública para la toma de decisiones sobre los programas de vacunación para el conjunto del Estado.
En la tabla 1 figuran las instituciones que intervienen en la toma de decisiones sobre el programa de vacunación en España y sus funciones.
Tabla 1. Instituciones que intervienen en la toma de decisiones sobre el programa de vacunación en España y sus funciones.

Fuente: modificada de “Criterios de evaluación para fundamentar modificaciones en el Programa de Vacunación en España”11
Estructura y funcionamiento
La Ponencia de Vacunas se creó en diciembre de 1991 como el órgano científico-técnico de apoyo al CISNS, con la misión de estudiar “la situación de las enfermedades susceptibles de vacunación y la formulación y seguimiento de medidas destinadas a su prevención y control”9.
Desde que comenzó a funcionar el pleno del CISNS en 1987 hasta la creación de esta Ponencia, los asuntos de programas de vacunación se trataban en la Comisión Permanente de Seguimiento de Programas de Salud. Por ejemplo, en el año 1990 se recomendó que las CCAA desarrollaran e implantaran sistemas de registro nominales de las vacunas administradas, incluyendo las recomendadas a grupos de población específicos, como las vacunas frente a la hepatitis B o la gripe10.
La Ponencia de Vacunas está coordinada por la Subdirección General de Promoción de la Salud y Vigilancia en Salud Pública (SGPV) y está formada por un experto o experta de cada comunidad autónoma y de las ciudades de Ceuta y Melilla, nombrados por la persona encargada de la Dirección General de Salud Pública de cada una de ellas. Además, participan expertos o expertas de otras instituciones, como la Agencia Española de Medicamentos y Productos Sanitarios, el Instituto Nacional de Gestión Sanitaria (INGESA), el Instituto de Salud Carlos III, el Ministerio del Interior (Instituciones Penitenciarias), el Ministerio de Defensa, así como del propio Ministerio de Sanidad (Centro de Coordinación de Alertas y Emergencias Sanitarias, Subdirección General de Sanidad Exterior y Dirección General de Cartera Básica de Servicios del SNS y Farmacia, además de la SGPV). La Secretaría y la coordinación de los grupos de trabajo se realizan desde el Área de Programas de Vacunación (SGPV del Ministerio).
Como se ha indicado anteriormente, la finalidad de la Ponencia de Vacunas es asesorar desde un punto de vista científico-técnico a la Comisión de Salud Pública en aspectos relacionados con vacunas y programas de vacunación para la toma de decisiones. Desde su creación, la Ponencia de Vacunas ha desarrollado las siguientes funciones:
- Valoración de las modificaciones en los programas de vacunación vigentes tras la autorización de nuevas vacunas y otros cambios regulatorios en las fichas técnicas.
- Evaluación y propuesta de modificaciones en los programas de vacunación.
- Evaluación de las coberturas de vacunación.
- Discusión y valoración de otros aspectos relacionados con los programas de vacunación.
La elección de los asuntos a trabajar desde la Ponencia de Vacunas se realiza desde la Comisión de Salud Pública, en algunas ocasiones a iniciativa de la propia Ponencia. Generalmente, las propuestas desde la Ponencia incluyen aspectos relacionados con la autorización de nuevas vacunas o modificaciones relevantes en evaluación en la Agencia Europea de Medicamentos (European Medicines Agency, EMA) y estrategias de vacunación tras experiencias en otros países.
En función de la complejidad de cada asunto particular, este se puede resolver directamente en el pleno de la Ponencia o puede formarse un grupo de trabajo ad hoc. En caso de formar un grupo, este elaborará una primera propuesta para valoración y discusión por el pleno de la Ponencia y, tras su aprobación, se eleva a la Comisión de Salud Pública para su discusión y aprobación.
Los grupos de trabajo se forman con miembros de la Ponencia que voluntariamente deseen participar. En función de la complejidad del tema a tratar y del tiempo disponible para la elaboración del trabajo, se puede solicitar la colaboración de otros expertos, que se eligen a propuesta de los miembros de la Ponencia o desde la Secretaría.
La Secretaría de la Ponencia se encarga de coordinar los grupos de trabajo, elaborar propuestas, participar activamente en el desarrollo del trabajo, supervisar los trabajos que se encargan o contratan, así como editar los textos y exponer el borrador a la Ponencia.
El procedimiento utilizado por los grupos de trabajo para elaborar propuestas se describe en el documento “Criterios de Evaluación para fundamentar modificaciones en el programa de vacunación en España”. Este documento técnico, acordado por la Comisión de Salud Pública en 2012, actualizó el inicialmente elaborado en 200411. El procedimiento muestra que la evaluación se realizará en tres pasos, en los que se analizan cinco criterios de manera ordenada:
Carga de enfermedad.
Efectividad y seguridad de la vacuna.
Repercusiones de la modificación.
Aspectos éticos.
Evaluación económica.
En la Ponencia se discuten y acuerdan, además, otros asuntos relacionados con el funcionamiento de los programas de vacunación, como pueden ser la adquisición conjunta de vacunas, actuaciones ante los problemas en el suministro de vacunas, los registros y sistemas de información, etc.
La Ponencia se reúne al menos dos veces al año. En los últimos años se han llevado a cabo reuniones adicionales mediante audio y videoconferencia. Estos recursos se han utilizado ampliamente en los últimos años para tratar aspectos puntuales de los programas de vacunación. Por ejemplo, la Ponencia se reunió en 2015 un total de quince veces, trece de ellas por audioconferencia, y en la mayoría de ocasiones fue para tratar los problemas relacionados con el suministro de vacunas pentavalentes y dTpa, las cuales afectaron de manera importante al buen funcionamiento de los programas de vacunación durante varios años. En 2016, 2017 y 2018 la Ponencia se reunió cinco veces cada año, manteniendo al menos una de esas reuniones carácter presencial y, en 2019 mantuvieron cuatro reuniones, tres de ellas presenciales.
La participación de los miembros en la Ponencia y de otros expertos en los grupos de trabajo se realiza de manera desinteresada y no se remunera la asistencia a las reuniones ni la participación en los grupos. Desde 2016, todos los miembros de la Ponencia deben firmar anualmente un compromiso de confidencialidad y una declaración de intereses. Del mismo modo, estos documentos deben ser firmados por todos y cada uno de los participantes en los grupos de trabajo dependientes de la Ponencia.
Al igual que en el resto de organismos dependientes del CISNS, las decisiones en la Ponencia se toman por consenso.
La Ponencia no tiene un presupuesto concreto establecido. En los últimos años, los trabajos solicitados desde la Ponencia o cualquier otro gasto derivado de las reuniones se han realizado con cargo al presupuesto de la Dirección General de Salud Pública, Calidad e Innovación del Ministerio de Sanidad.
EVOLUCIÓN DEL CALENDARIO DE VACUNACIÓN DESDE 1996 Y PAPEL DE LA PONENCIA DE VACUNAS
Desde su creación, la Ponencia de Vacunas ha realizado recomendaciones sobre aspectos de gestión e incorporación de vacunas en los programas de vacunación. Por ejemplo, en 1992 se acordaron los datos que las comunidades autónomas debían suministrar a nivel central para realizar el cálculo de las coberturas de vacunación12, que se han ido actualizando regularmente. En la tabla 2 se refleja el trabajo realizado por la Ponencia de Vacunas en cuanto al calendario de vacunación desde su creación hasta 1995.
Tabla 2. Trabajo desarrollado por la Ponencia de Programa y Registro de Vacunaciones. Periodo 1991-1996.

(*)Vacunas: VPO, vacuna frente a poliomielitis oral; DTP, vacuna combinada frente a difteria, tétanos y tosferina; TV, triple vírica o vacuna frente a sarampión, rubeola y parotiditis; HB, vacuna frente a hepatitis B. Fuente: modificada de “Criterios de evaluación para fundamentar modificaciones en el Programa de Vacunación en España”11.
En 1995, desde la Ponencia se elaboró un calendario de vacunación infantil que fue aprobado por la Comisión de Salud Pública y el pleno del CISNS. Este primer calendario de vacunación del CISNS, que entró en vigor a lo largo de 1996, era flexible en cuanto a edad de administración de las dosis de vacunas, estableciendo “bandas” o intervalos para cada una de las dosis a administrar. La finalidad de estas “bandas” era facilitar las estrategias de vacunación en las diferentes CCAA. El calendario incorporaba los programas que debían incluirse en todas las CCAA. Un ejemplo es la vacunación frente a la hepatitis B que, aunque se recomendaba desde 1992, todavía no se había incorporado en todas las CCAA. Con el calendario de 1996 todas ellas incorporaron esta vacunación durante la adolescencia (tabla 3).
Tabla 3. Primer calendario de vacunación del Consejo Interterritorial del Sistema Nacional de Salud. Año 1996.
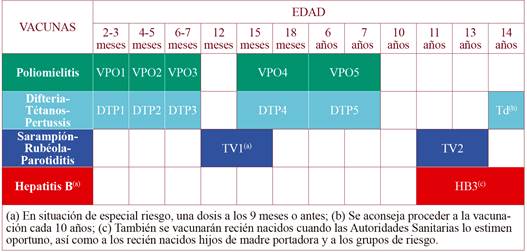
Fuente: Ministerio de Sanidad1.
Desde entonces, se han realizado diversas modificaciones en el calendario, que incluyen nuevas incorporaciones, sustituciones de unas vacunas por otras que protegen frente a la misma enfermedad y cambios de las pautas de administración. En las tablas 4 y 5 se recogen de manera esquemática las modificaciones realizadas en el calendario sistemático de vacunación a partir de 1996 y hasta 2019, por año y por programa de vacunación, respectivamente.
Tabla 4. Modificaciones en el calendario de vacunación (recomendaciones para población general) por años. Periodo 1996-2019.

a: años de edad; m: meses de edad; d: dosis.
(*)Vacunas: Hib, Haemophilus influenzae tipo b; MenC, conjugada frente a meningococo por serogrupo C; VPO, vacuna frente a poliomielitis oral; VPI, vacuna frente a poliomielitis inactivada; DTP, difteria, tétanos y tosferina; Pa, tosferina acelular; TV, triple vírica o vacuna frente a sarampión, rubeola y parotiditis; HB, hepatitis B; VVZ, varicela; VPH, virus de papiloma humano; dTpa, difteria, tétanos y tosferina de baja carga o de adultos; Td, tétanos y difteria de baja carga o de adultos; VNC, vacuna conjugada frente a neumococo.
(**)La recomendación de vacunación a embarazadas con dTpa se ha actualizado recientemente: a partir de la semana 27, preferentemente en las semanas 27 o 2820.
Fuente: modificada de “Revisión del Calendario de Vacunación”15.
Tabla 5. Modificaciones en el calendario de vacunación (recomendaciones para población general) según el programa de vacunación para cada enfermedad o grupo de enfermedades. Periodo 1996-2019.

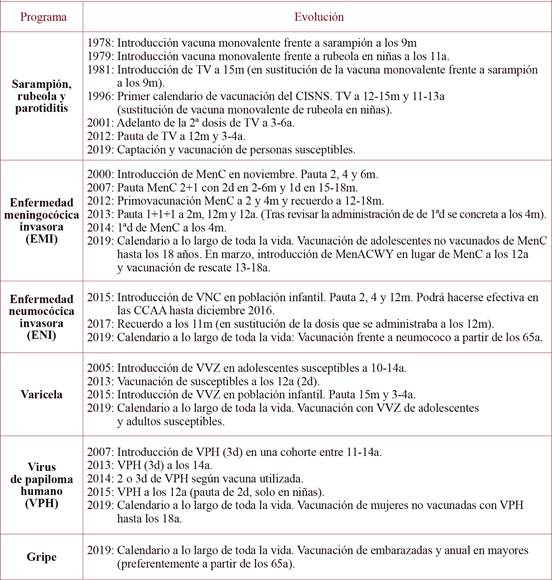
a: años de edad; m: meses de edad; d: dosis.
(*)Vacunas: Hib, Haemophilus influenzae tipo b; MenC, conjugada frente a meningococo por serogrupo C; VPO, vacuna frente a poliomielitis oral; VPI, vacuna frente a poliomielitis inactivada; DTP, difteria, tétanos y tosferina; Pa, tosferina acelular; TV, triple vírica o vacuna frente a sarampión, rubeola y parotiditis; HB, hepatitis B; VVZ, varicela; VPH, virus de papiloma humano; dTpa, difteria, tétanos y tosferina de baja carga o de adultos; Td, tétanos y difteria de baja carga o de adultos; VNC, vacuna conjugada frente a neumococo.
(**)La recomendación de vacunación a embarazadas con dTpa se ha actualizado recientemente: a partir de la semana 27, preferentemente en las semanas 27 o 2820.
En la reunión mantenida el 18 de marzo de 2010 por el Pleno del CISNS, se acordó la adopción de una serie de acciones y medidas para promover la calidad, la equidad, la cohesión y la sostenibilidad del Sistema Nacional de Salud, entre las que se encontraba la aprobación de un calendario único o común de vacunación para España13. La Ponencia de Vacunas propuso una definición de calendario único de vacunación11 y, a partir de 2012, se comenzaron a homogeneizar las edades de administración de las vacunas incluidas en el calendario, alcanzando en 2017 la mayor homogeneidad desde la descentralización de la Salud Pública del Estado en favor de las comunidades autónomas.
Desde 2012 se publica anualmente en la web del Ministerio de Sanidad el calendario recomendado por el CISNS14.
En 2016 se realizó una revisión profunda del calendario de vacunación infantil. La incorporación progresiva de vacunas en el calendario había implicado el aumento en el número de pinchazos, fundamentalmente en los niños más pequeños, lo que podía influir en la aceptación de las vacunaciones por parte de los padres. Además, el conocimiento científico se había ido ampliado con respecto a la respuesta inmune proporcionada por las vacunas y los efectos en el control de las enfermedades inmunoprevenibles en la población. Tras la revisión, se acordó reducir el número de pinchazos en menores de 24 meses, cambiando la primovacunación frente a difteria, tétanos, tosferina, poliomielitis, Haemophilus influenzae tipo b y hepatitis B, que se realizaba con tres dosis a los 2, 4 y 6 meses, a realizarse con dos dosis a los 2 y 4 meses de edad y adelantando la dosis de recuerdo de los 18 a los 11 meses de edad15,16. Este nuevo calendario de vacunación infantil, a pesar de introducir varios cambios, tuvo una buena acogida por parte del personal sanitario y la población.
En 2017 y 2018 se revisaron y actualizaron las recomendaciones de vacunación en la población adulta17 y, junto con las recomendaciones de vacunación infantil acordadas en 2016, se consensuó el primer calendario común de vacunación a lo largo de toda la vida para 201918. Este nuevo calendario incorporó las vacunas recomendadas desde el periodo prenatal, mediante la vacunación de embarazadas, hasta la población mayor, cubriendo todas las edades de la vida. La incorporación en el calendario de las vacunas recomendadas a partir de los 15 años para la población adulta y mayor pretende concienciar de la importancia de la vacunación más allá de la infancia y la adolescencia, así como facilitar la tarea del personal sanitario en la identificación de las vacunas a administrar según la edad de las personas.
Además de evaluar los programas de vacunación sistemática dirigidos a la población general, desde la Ponencia se han elaborado recomendaciones para otros grupos de población. En 2018 se actualizaron las recomendaciones de vacunación para personas de grupos de riesgo de todas las edades, que incluían también el entorno laboral, el embarazo y el puerperio19. En 2019 se elaboraron recomendaciones sobre la vacunación de personas no vacunadas adecuadamente e inmigrantes20 y también para prematuros21. Las recomendaciones de los grupos con más riesgo o más prevalentes se plasmaron también en un formato de calendario, para menores, adolescentes y personas adultas22,23.
Adicionalmente, cada año se elaboran las recomendaciones de vacunación frente a la gripe24. Todas las recomendaciones y documentos técnicos se publican en la web del Ministerio de Sanidad25.
RETOS ACTUALES: GESTIONAR PROBLEMAS DE SUMINISTRO Y MANTENER O AUMENTAR LAS COBERTURAS
Desde comienzos de 2015, la Ponencia de Vacunas ha desarrollado una parte importante de su actividad en la gestión conjunta de los problemas de suministro de vacunas, con el objetivo de que interfieran lo menos posible en el funcionamiento de los programas de vacunación y se mantenga la protección de la población frente a las enfermedades inmunoprevenibles. Las vacunas implicadas en estos problemas de suministro han sido varias: pentavalentes (DTPa/VPI/Hib), difteria, tétanos y tosferina de baja carga (dTpa), tétanos y difteria de adulto (Td), hepatitis A, hepatitis B, rabia y triple vírica. Las causas de estos problemas de suministro han sido diversas, pero el incremento de la demanda de vacunas a nivel mundial sin un desarrollo parejo de la capacidad de producción puede explicar parte del problema26.
Un aspecto fundamental para conservar el control sobre las enfermedades inmunoprevenibles es mantener las coberturas de vacunación en la infancia y aumentarlas en los denominados grupos de riesgo, así como en la población adolescente y adulta. Para ello se debe trabajar en el mantenimiento de la confianza de la población y del personal sanitario en los programas de vacunación, concienciando de su importancia en todas las edades. Fomentar la participación de todos los agentes que intervienen en la vacunación en la elaboración de estrategias de comunicación adecuadas, que difundan información veraz, puede contribuir a unificar los mensajes sobre los beneficios de la vacunación y sobre la seguridad de las vacunas.
AVANZANDO HACIA LA COLABORACIÓN ENTRE LOS COMITÉS ASESORES TÉCNICOS EN LA UNIÓN EUROPEA
La Organización Mundial de la Salud (OMS) recomienda a los Estados miembros que establezcan o refuercen un Comité Técnico Asesor Nacional de Vacunaciones (conocidos por el acrónimo NITAG en inglés, de National Immunization Technical Advisory Group). El objetivo de este Comité es apoyar a los dirigentes en la toma de decisiones sobre vacunación, aportando información basada en criterios técnicos y científicos. Este impulso se plasma en el Plan Mundial de Acción en Vacunas 2011-202027 y en el Plan Europeo de Acción en Vacunas 2015-2020 (objetivo 5)28.
Los Comités de los países de la Unión Europea son heterogéneos en su estructura y en su funcionamiento29.
Teniendo en cuenta las funciones encomendadas a la Ponencia de Vacunas, así como el trabajo que desarrolla desde su creación, se considera que es el Comité Técnico Asesor de Vacunaciones para España. No obstante, deben revisarse y reforzarse algunos aspectos para cumplir con los criterios de evaluación de estos Comités, como son la disponibilidad de un procedimiento normalizado de trabajo donde figuren la estructura y funcionamiento30.
Tanto desde la Organización Mundial de la Salud como desde la Unión Europea se está trabajando para mejorar la toma de decisiones sobre vacunación, recomendando y asesorando sobre el fortalecimiento de estos Comités Técnicos Asesores31,32,36.
Desde el Consejo de la Unión Europea se ha propuesto la necesidad de desarrollar mecanismos de colaboración entre Comités Técnicos Asesores de los Estados miembros33,34,35,36. Recientemente, se ha puesto en marcha un proyecto piloto coordinado desde el Centro Europeo para el Control y Prevención de Enfermedades (European Centre for Disease Prevention and Control, ECDC), en el cual colabora la Ponencia de Vacunas. Esta colaboración puede ayudar a mejorar los procedimientos utilizados para la elaboración de documentos técnicos en España, sobre todo aquéllos que son complicados de implantar porque consumen gran cantidad de recursos, como son la realización de revisiones sistemáticas y la elaboración de modelos matemáticos36.
CONCLUSIÓN
La Ponencia de Programa y Registro de Vacunaciones es el Comité Técnico Asesor de la Comisión de Salud Pública y del Consejo Interterritorial en asuntos relacionados con vacunas y programas de vacunación. Desde 1991 realiza propuestas basadas en la evidencia científica y en la situación epidemiológica de las enfermedades inmunoprevenibles en España, dando soporte para la toma de decisiones.
La evaluación continua de los programas de vacunación realizada por esta Ponencia ha propiciado cambios sustanciales en los mismos, disponiéndose actualmente de un calendario de vacunación a lo largo de toda la vida para la prevención de 14 enfermedades, así como un calendario de vacunación para grupos de riesgo y programas para otras situaciones específicas.















