Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Anales del Sistema Sanitario de Navarra
versión impresa ISSN 1137-6627
Anales Sis San Navarra vol.29 no.3 Pamplona sep./dic. 2006
REVISIONES
Tratamiento de la enfermedad de Crohn perianal
Treatment of perianal Crohns disease
M.A. Ciga, F. Oteiza, J. Marzo, P. Armendáriz, M. De Miguel y H. Ortiz
Unidad de Coloproctología, Servicio de Cirugía General y del Aparato Digestivo.
Hospital Virgen del Camino. Pamplona.
Dirección para correspondencia
RESUMEN
La afectación perianal por enfermedad de Crohn comprende un amplio espectro de lesiones de diferente manejo y pronóstico. Una exploración minuciosa del paciente, si es preciso bajo anestesia, una rectoscopia para valorar la posible afectación del recto por la enfermedad, y en ocasiones la valoración mediante ecografía endoanal o resonancia magnética, son las bases para un correcto enfoque diagnóstico y terapéutico. Farmacología y cirugía han de complementarse en el tratamiento de la enfermedad de Crohn perianal y perseguir un doble objetivo: aliviar la sintomatología del paciente y prevenir posibles complicaciones. Salvo en situaciones de urgencia por sepsis perianal, el tratamiento médico es el primer escalón en el manejo de la enfermedad de Crohn perianal, y en muchas ocasiones se controlará la enfermedad haciendo innecesaria la cirugía. Cuando se precisa de ésta, al propósito de un tratamiento definitivo de la lesión perianal, ha de contraponerse el riesgo de desarrollar complicaciones, muy especialmente incontinencia.
Palabras clave. Enfermedad de Crohn. Enfermedad perianal. Tratamiento médico. Tratamiento quirúrgico.
ABSTRACT
Perianal affectation due to Crohns disease includes a wide spectrum of lesions involving different management and prognosis. A thorough exploration of the patient, under anaesthetic if necessary, a rectoscope to evaluate the possible affectation of the rectum by the disease, and on occasions evaluation through endoanal echography or magnetic resonance, are the bases for a correct diagnostic and therapeutic focus. Pharmacology and surgery must be complementary in the treatment of perianal Crohns disease and must pursue a double aim: to alleviate the symptomology of the patient and prevent possible complications. Except in situations of emergency due to perianal sepsis, medical treatment is the first step in managing perianal Crohns disease, and on many occasions it will control the disease, making surgery unnecessary. When surgery is required, with the aim of a definitive treatment of the perianal lesion, the risk of developing complications, especially incontinence, must be contrasted.
Key words. Crohns disease. Perianal disease. Medical treatment. Surgical treatment.
Introducción
La enfermedad de Crohn perianal se caracteriza por diversas lesiones1; unas son manifestación directa de la enfermedad, como las fisuras anales y las úlceras cavitadas; otras derivan de complicaciones de éstas, como los colgajos cutáneos, los abscesos, las fístulas perianales, anovaginales y rectovaginales, y las estenosis. Además, los pacientes con esta enfermedad pueden presentar lesiones perianales de forma casual o por otras etiologías.
La incidencia de la afectación perianal en la enfermedad de Crohn varía en la literatura entre cifras tan bajas como un 3,8%2 y otras tan elevadas como un 60-80%3,4. Esta incidencia aumenta cuanto más distal es la afectación intestinal: entre el 14 y el 76% cuando sólo está afectado el intestino delgado y entre el 43 y el 94% cuando está afectado el colon2,5-9. Las variaciones tan marcadas en la incidencia son debidas a diferencias en los criterios de definición de enfermedad perianal, a que muchos estudios son retrospectivos y a que las lesiones asintomáticas pueden pasarse por alto si no se buscan10.
En un 20-36% de los casos la afectación perianal es la primera manifestación de la enfermedad y puede preceder a la aparición de síntomas intestinales en varios años2,5. Aunque la etiología es desconocida, se ha identificado un gen en el cromosoma 5 que puede condicionar la susceptibilidad a la enfermedad perianal en la enfermedad de Crohn11.
Lesiones perianales en la enfermedad de Crohn
En la tabla 1 se muestra la frecuencia con que las distintas lesiones perianales aparecen en la enfermedad de Crohn2,5,6,12-20.
Colgajos cutáneos. Son las lesiones perianales más frecuentes en esta enfermedad18 y pueden originarse en un linfedema secundario a obstrucción linfática. Su aspecto suele ser reflejo de la actividad de la enfermedad, apareciendo en las fases agudas con ulceraciones y edema.
Fisuras. Son frecuentemente indoloras1,21,22 y no están asociadas a hipertonía esfinteriana23. Si provocan dolor intenso hay que sospechar una complicación infecciosa (absceso o fístula), hecho que ocurre en un 25% de los casos24. Aunque la localización más frecuente es la posterior25 (Fig. 1) pueden situarse a cualquier nivel de la circunferencia anal y en un tercio de los casos son múltiples24-26.
Úlceras cavitadas. Son úlceras profundas que aparecen en el recto y en el ano; en ocasiones penetran y destruyen el aparato esfinteriano y pueden ser muy dolorosas6,16.
Abscesos y fístulas. Los abscesos son la causa más frecuente de dolor en estos pacientes y habitualmente son el paso previo a la formación de una fístula. Abscesos y fístulas pueden ser de origen criptoglandular o secundarios a complicaciones derivadas de fisuras o úlceras cavitadas1,27,28. La incidencia de fístulas anales se incrementa en los pacientes que tiene el recto afectado por la enfermedad29-31. Siguiendo la clasificación de Parks27, las fístulas transesfinterianas son el tipo más frecuente32,33. Aunque la mayoría de las fístulas son simples, existe una tendencia a desarrollar fístulas complejas30,33: transesfinterianas altas, supraesfinterianas, extraesfinterianas. Con frecuencia existen varios orificios externos, a veces alejados del margen anal18.
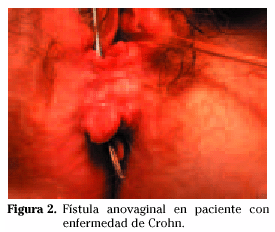
En las mujeres hay que considerar por su frecuencia las fístulas rectovaginales, especialmente si existe enfermedad rectal. Su incidencia ronda el 5-10%6,17. La mayoría son anovaginales (Fig. 2), y en el 85% de los casos el orificio fistuloso se origina en la pared anterior del recto o del ano17.
Las fístulas son también una complicación frecuente de los pacientes con un reservorio ileoanal por colitis indeterminada que posteriormente se diagnostican de enfermedad de Crohn. Las fístulas del reservorio se presentan hasta en un 63% de pacientes y conllevan al fracaso del mismo en el 28-52% de los casos34-37.
Estenosis. Son debidas a la fibrosis extramucosa intensa producida por abscesos de repetición o mal drenados, por fístulas mantenidas o por úlceras cavitadas. La mayoría se localizan en el recto y con frecuencia no ocasionan clínica hasta etapas avanzadas dado que las heces de estos pacientes con frecuencia son blandas o líquidas38.
Hemorroides. No son una lesión específica del Crohn y su incidencia es baja en pacientes con esta enfermedad, pero conviene mencionarlas por las consecuencias que su cirugía puede conllevar16,18,39.
Cáncer de ano. Se han descrito carcinomas epidermoides, carcinomas de células basales y adenocarcinomas, originados en trayectos fistulosos crónicos y sinus persistentes19,20,40-43. Su incidencia no alcanza el 1% y su tratamiento se rige por los principios oncológicos convencionales.
Aunque no tiene una relación directa con la enfermedad de Crohn, es interesante destacar que los pacientes con esta enfermedad pueden presentar incontinencia fecal. Ésta puede ser causada por destrucción de los esfínteres por úlceras profundas, pero es más frecuente la causa iatrogénica secundaria a intervenciones quirúrgicas repetidas sobre la enfermedad perianal6,16,26.
Valoración clínica y diagnóstico
El diagnóstico puede ser difícil si las lesiones perianales son la primera manifestación de la enfermedad. La exploración detallada es imprescindible para poder sospechar el diagnóstico. La presencia de colgajos cutáneos, fisuras asintomáticas, múltiples o de marcada profundidad, fístulas con varios orificios o muy alejados del margen anal y/o la coexistencia de varias lesiones perianales son datos que deben alertar sobre la posibilidad de estar ante un paciente con enfermedad de Crohn perianal33 (Fig. 3). Según los hallazgos se deberá valorar la conveniencia de realizar la exploración anal bajo anestesia. En estas condiciones se podrá examinar a los pacientes con dolor intenso, con fístulas complejas, valorar el recto en busca de proctitis, úlceras o estenosis, drenar abscesos si los hay y tomar biopsias que confirmen el diagnóstico.
Los métodos de imagen son una ayuda inestimable en la valoración del paciente con enfermedad de Crohn perianal. La ecografía endoanal informa sobre abscesos ocultos y trayectos fistulosos, localiza el orificio interno de una fístula, valora la integridad esfinteriana y ofrece datos indirectos de enfermedad inflamatoria como son el engrosamiento de la pared del canal anal a expensas de la mucosa, submucosa y esfínter interno, o la pérdida de las capas de la pared44-46.
En casos de fístula rectovaginal su utilidad es menor47. El dolor y la estenosis pueden ser obstáculos para su realización, debiendo en estos casos realizarla durante la exploración bajo anestesia48, o bien sustituirla, en el caso de mujeres, por una ecografía transvaginal49.
La resonancia magnética puede ser muy útil para valorar la integridad del aparato esfinteriano y parece ser superior a la ecografía endoanal para identificar trayectos fistulosos complejos y abscesos profundos50,51.
En la práctica, la exploración anal bajo anestesia, la ecografía endoanal y la resonancia magnética deben complementarse para una correcta valoración de la enfermedad perianal en la enfermedad de Crohn, especialmente en casos de fístulas perianales. Con la exploración bajo anestesia y una técnica de imagen se debería obtener una precisión diagnóstica próxima al 100%26,52.
Las técnicas de imagen tienen una importancia añadida en la valoración de la respuesta al tratamiento de las fístulas perianales, ya que la respuesta clínica se acompaña en muchas ocasiones de la persistencia de los trayectos en la ecografía o en la resonancia53-55, y este hecho lleva consigo una mayor probabilidad de recidiva56.
La valoración del recto mediante endoscopia es imprescindible, pues el tratamiento de las lesiones perianales, como más adelante se verá, va a estar condicionado según el recto esté afectado o no por la enfermedad inflamatoria. De igual modo se debe conocer la extensión y actividad en el resto del intestino, pues el primer paso en el tratamiento de la enfermedad perianal ha de ser siempre tratar, si existen las lesiones activas a nivel intestinal. En muchos casos este tratamiento será suficiente para mejorar de forma significativa la sintomatología de las lesiones perianales. Por eso una colonoscopia completa y un tránsito baritado son necesarios para un correcto enfoque terapéutico del paciente, además de una tomografía computarizada si la historia clínica y la exploración física nos hacen sospechar complicaciones intraabdominales.
Dada la variedad de lesiones en la enfermedad de Crohn perianal y la frecuente coexistencia de algunas de ellas, es aconsejable utilizar en la valoración del enfermo alguna escala o índice de clasificación que nos permita establecer de una forma objetiva las lesiones que el paciente presenta. Aunque existen varias - clasificación de Cardiff1 (UFS), de Hughes/Cardiff10 (APD), etc - ninguna de ellas está validada; pese a ello es aconsejable utilizar alguna con el fin de unificar criterios en un grupo de trabajo y poder valorar de un modo objetivo la evolución de las lesiones y su respuesta a los distintos tratamientos. Parece de especial utilidad el índice de actividad de la enfermedad de Crohn perianal (PDAI – Tabla 2)57 que además de las lesiones valora de un modo funcional el efecto de la enfermedad perianal sobre aspectos fundamentales de la vida del paciente.
Diagnóstico diferencial
Aunque habitualmente las lesiones perianales en un paciente con enfermedad de Crohn conocida ofrecen pocas dudas diagnósticas, existen una serie de entidades que se deben tener en cuenta a la hora de plantear un diagnóstico diferencial. Estas incluyen: la hidrosadenitis supurativa, las enfermedades de transmisión sexual, la tuberculosis y el cáncer de ano, aunque éste puede considerarse como una lesión asociada.
Tratamiento
El tratamiento de la afectación perianal en la enfermedad de Crohn debe perseguir un doble objetivo: aliviar la sintomatología y prevenir las complicaciones. Como norma general, ha de ser conservador siempre que sea posible, más si se tiene en cuenta que la historia natural de la enfermedad de Crohn lleva en muchas ocasiones a la curación espontánea de las lesiones perianales23. Los colgajos y las fisuras suelen tener un curso benigno y raras veces precisarán un tratamiento quirúrgico; en el caso de las fisuras se han descrito tasas de curación superiores al 80%22,26, aunque muchas veces con estenosis residual. También las fístulas pueden curar espontáneamente en cerca del 40% de los casos23. Sin embargo, las úlceras profundas, las estenosis severas y las fístulas complejas suelen tener un pronóstico peor23 y un elevado porcentaje de pacientes precisarán en su evolución algún tipo de intervención quirúrgica. En general, el curso de la enfermedad perianal es mucho más benigno cuando el recto no está afectado por la enfermedad inflamatoria. También se debe destacar la importancia que el tratamiento médico de la enfermedad intestinal tiene en conseguir un buen resultado con la cirugía de la enfermedad perianal: no se debe intentar un tratamiento quirúrgico electivo sobre lesiones perianales asociadas a la enfermedad de Crohn sin haber conseguido antes que a nivel intestinal la enfermedad esté inactiva.
Tratamiento médico
Aminosalicilatos y corticoides
A pesar de su eficacia incuestionable en el tratamiento sistémico de la enfermedad de Crohn, no existe ningún estudio que demuestre su utilidad en la enfermedad perianal. Por el contrario, los corticoides pueden entorpecer la curación de fístulas y favorecer la formación de abscesos4,58. No obstante, tanto los aminosalicilatos como los corticoides en formas tópicas -enemas, espumas o supositorios- pueden disminuir eficazmente la actividad inflamatoria rectal, aunque no la enfermedad perianal propiamente59-61.
Antibióticos
Su uso se fundamenta en que la flora bacteriana, especialmente la anaerobia, juega un papel importante en la sepsis perianal. Metronidazol y ciprofloxacino son los más usados. El metronidazol a dosis de 10-20 mg/kg/día, ha demostrado su eficacia en varios estudios abiertos en el control de la enfermedad perianal, especialmente en el tratamiento de las fístulas, con cierre completo de éstas en el 34-50% de los casos62-67. La mejoría se observa tras una media de 6-8 semanas. Sin embargo, la disminución de la dosis o la supresión del tratamiento conlleva una recidiva precoz que suele responder bien a la reinstauración del mismo65,67. En tratamientos prolongados deben vigilarse sus efectos secundarios, especialmente la polineuropatía periférica; su incidencia puede alcanzar el 50% y mejora con la disminución de la dosis68,69. El ciprofloxacino, aunque tiene un efecto mínimo sobre anaerobios, es una alternativa al metronidazol70,71 y puede asociarse a éste en pacientes refractarios con mejorías hasta en el 65% de los casos72. Aunque no existen ensayos clínicos controlados parece que la suspensión del tratamiento provoca, al igual que con el metronidazol, una reactivación de la enfermedad perianal.
Inmunosupresores
Azatioprina / 6-mercaptopurina. La eficacia de la azatioprina y de su metabolito, la 6-mercaptopurina en el tratamiento de la enfermedad de Crohn ha sido contrastada en varios estudios controlados. En cinco de ellos se valoró la enfermedad fistulosa en detalle y sus resultados se detallan en un metaanálisis, con un 54% de respuesta en los pacientes tratados frente al 21% en los que recibieron placebo73-78. Sin embargo, ninguno de estos estudios se diseñó para valorar la respuesta específica de la enfermedad perianal a estos fármacos, por lo que los resultados deben interpretarse con cautela. El tratamiento con azatioprina (2,5 mg/kg/día) ó 6-mercaptopurina (1,5 mg/kg/día) en la enfermedad perianal se indica tras el fracaso, la recidiva o la toxicidad del tratamiento antibiótico. El tiempo medio de respuesta al tratamiento es de 3-6 meses; pasados 6 meses se puede abandonar o mantener de forma indefinida dependiendo de la respuesta obtenida. Los pacientes mayores de 40 años con enfermedad perianal de corta evolución y sin fístulas parecen ser los que mejor responden a este tratamiento. Los principales efectos secundarios que se pueden observar son leucopenia, pancreatitis y hepatitis tóxicas, que se presentan en el 9-15% de los pacientes78-79.
Ciclosporina A. No existen estudios controlados que evalúen la ciclosporina en el tratamiento de la enfermedad de Crohn perianal. Los estudios no controlados ofrecen una tasa de respuesta inicial en torno al 80% y una respuesta mantenida del 45-55%80-86. La mejoría clínica suele presentarse de forma rápida, habitualmente en la primera semana. El tratamiento debe iniciarse de forma intravenosa a dosis de 2 mg/kg/día. Si existe respuesta puede pasarse a la administración oral, debiendo ajustar la dosis para alcanzar niveles séricos terapéuticos de 100-200 ng/mL. Las recidivas son frecuentes si se interrumpe el tratamiento. La hipertensión y la nefrotoxicidad son los efectos secundarios más importantes87. Para algunos autores el tratamiento con ciclosporina A sólo debe ser un puente hacia el uso de azatioprina/6-mercaptopurina.
Tacrolimus. La eficacia del tacrolimus en el tratamiento de la enfermedad fistulosa asociada a la enfermedad de Crohn ha sido valorada en un ensayo clínico multicéntrico88, en el que 48 pacientes fueron aleatorizados para recibir placebo o tacrolimus por vía oral a dosis de 0,2 mg/kg/día durante 10 semanas. Aunque la mejoría (cierre de más del 50% de los orificios fistulosos activos) fue significativamente mayor en el grupo del tacrolimus (43% frente al 8%), no hubo diferencias en la curación completa, definida ésta como el cierre de todos los orificios fistulosos durante al menos 4 semanas (10% frente al 8%). Además, los efectos secundarios fueron numerosos (elevación de creatinina, cefaleas, insomnio, etc.). No obstante, en algunos trabajos se ha mostrado eficaz para inducir la remisión y servir de puente hacia el tratamiento con azatioprina / 6-mercaptopurina89-91. El tacrolimus en forma tópica ha sido ensayado en niños con afectación perianal ulcerativa con resultados prometedores92.
Terapia con anticuerpos anti-TNFa
El agente más conocido es el infliximab (cA2 / remicade). Es un anticuerpo quimérico monoclonal contra el factor de necrosis tumoral alfa, que actúa como un inhibidor de la respuesta inflamatoria93-97. A dosis de 5 mg/kg en perfusión intravenosa (2-3 horas), repetida a las 2 y 6 semanas (total 3 dosis), se ha mostrado significativamente superior al placebo tanto en la curación de todas las fístulas que tuviera el paciente (55% frente al 13%) como en la disminución del 50% o más del número de fístulas activas (68% frente al 26%)98. Otros estudios, no controlados, han puesto de manifiesto cifras de respuestas completas del 25-69% y parciales del 20-50%. Sin embargo, estos resultados pueden ser confusos y no comparables porque los criterios de respuesta completa o respuesta parcial no son los mismos en todos ellos.
No se han encontrado factores clínicos o bioquímicos predictivos de respuesta o no al infliximab99-101, sin embargo parece que las fístulas rectovaginales responden peor102 y su uso no está indicado en pacientes con estenosis. La mayoría de pacientes responden tras la primera o segunda dosis, y la mediana de respuesta está en torno a los 4 meses. A partir de esta fecha las recidivas aumentan hasta alcanzar el 90% al cabo de un año. Esta recidiva con el tratamiento convencional de 3 dosis, unido al hecho de que el infliximab es una eficaz terapia de mantenimiento en la enfermedad de Crohn sin fístulas, motivó un ensayo clínico placebo-control, multicéntrico, aleatorizado y doble ciego, para evaluar la eficacia de infliximab como tratamiento de mantenimiento en la enfermedad de Crohn fistulizante (ACCENT II)103. En este estudio, 195 pacientes que habían respondido al tratamiento inicial con infliximab (3 dosis a las 0, 2 y 6 semanas) y 87 pacientes que no habían respondido fueron aleatorizados a recibir bien placebo o bien 5 mg/kg de infliximab cada 8 semanas, a partir de la semana 14 y hasta la 54 (5 dosis más). Aunque la lectura de los resultados es compleja, la principal conclusión del ensayo es que los pacientes que responden al tratamiento de inducción (3 dosis) con infliximab, prolongan la respuesta al tratamiento de forma significativa cuando reciben una nueva dosis cada 8 semanas durante un año (54 semanas) respecto a los que reciben placebo (mediana de tiempo de pérdida de respuesta de 40 semanas en el grupo control frente a 14 semanas en el grupo placebo). Por otra parte, esta prolongación del tratamiento no aumenta la tasa de complicaciones y reacciones adversas descritas con el uso de infliximab. Aunque este ensayo tiene muchos otros puntos interesantes a considerar, (un 67% de pacientes que respondieron a la inducción y fueron aleatorizados a placebo, cuando recayeron respondieron de nuevo al tratamiento; un 57% de pacientes que no respondieron a la dosis de 5 mg/kg lo hicieron al doblar la dosis, etc.) tendremos que esperar a nuevos trabajos basados en la práctica clínica para poder definir mejor el papel del tratamiento de mantenimiento con infliximab en los pacientes con enfermedad de Crohn perianal.
Por último, debemos considerar que aunque la respuesta clínica a infliximab sea prometedora, en un elevado porcentaje de pacientes con respuesta completa persiste la enfermedad fistulosa cuando se examinan con técnicas de imagen, ecografía o resonancia magnética53,54, lo que unido a la alta tasa de recidiva tras el tratamiento de inducción indica que el infliximab al controlar la respuesta inflamatoria de la enfermedad controla el drenaje de las fístulas pero no es capaz de cerrar los trayectos epitelizados.
En general, en la enfermedad perianal se indica el tratamiento con infliximab en los pacientes que no responden al tratamiento con antibióticos ni con inmunosupresores. No obstante, la alta recurrencia tras la inducción lleva a pensar que, por un lado, habrá que ensayar terapias combinadas (con inmunosupresores104, con colocación de sedales105,106) para intentar mejorar los resultados y que, por otro, hoy por hoy el infliximab en modo alguno ha desplazado a la cirugía en el tratamiento de las fístulas en la enfermedad de Crohn perianal107,108.
Los efectos secundarios descritos en el tratamiento con infliximab incluyen reacciones con la infusión, reacciones de hipersensibilidad, infecciones oportunistas (especialmente tuberculosis que debe ser descartada antes de iniciar el tratamiento), formación de anticuerpos antiquiméricos y anti-DNA de doble cadena, y en raros casos, lupus inducido93,109,110.
La eficacia de infliximab se ha demostrado también en las complicaciones del reservorio ileoanal (reservoritis, fístulas...) en pacientes con enfermedad de Crohn a quienes se realizó el reservorio con otro diagnóstico; se han comunicado respuestas iniciales completas en hasta un 62% de los pacientes, pero no hay estudios controlados111,112.
Otros tratamientos
Algunos fármacos - como el metotrexate113,114, el micofenolato mofetil115, la talidomida116, el CDP571117, el oxígeno hiperbárico118,119, las dietas elementales y la nutrición parenteral120, etc, han sido utilizados en la enfermedad de Crohn fistulizante refractaria a otros tratamientos. Aunque en algunos casos ha habido buenos resultados, no existen en la actualidad ensayos clínicos suficientes para apoyar su uso rutinario.
Tratamiento quirúrgico
La variedad de lesiones perianales, la diferente severidad con que se pueden presentar, la frecuencia con la que coexisten lesiones distintas, la diferente respuesta al tratamiento médico, y las implicaciones que en la evolución de la enfermedad puede tener la afectación concomitante de intestino delgado, colon y recto, hace que sea muy difícil establecer unos principios quirúrgicos que se puedan aplicar de forma sistemática; por el contrario, se habrá de individualizar cada caso y en función de un gran número de variables decidir cual puede ser la mejor opción quirúrgica para un determinado paciente.
El rango de opciones quirúrgicas en la enfermedad de Crohn perianal va desde el simple drenaje de abscesos hasta la proctectomía; no obstante, de forma global, las podemos agrupar en cinco categorías:
– Tratamiento quirúrgico electivo de lesiones simples
– Tratamiento quirúrgico urgente de la sepsis perianal
– Tratamientos quirúrgicos puente para delimitar daños
– Tratamientos quirúrgicos definitivos
– Tratamiento quirúrgico de la enfermedad intestinal concomitante
Cirugía electiva de lesiones simples
Colgajos cutáneos. Tienen un curso benigno y excepcionalmente precisarán cirugía. Sólo en casos en que dificulten seriamente la higiene local estará indicada su exéresis bajo anestesia local18.
Fisura anal. Muy frecuentemente son asintomáticas1,21,22 y más del 80% curan espontáneamente22,26. En los casos en que provocan dolor intenso, tras descartar complicaciones infecciosas añadidas (absceso, fístula) se instaurará tratamiento médico conservador. El papel de la nitroglicerina, el diltiacén, la toxina botulínica, y otros tratamientos encaminados a disminuir el tono esfinteriano, no está bien establecido en los pacientes con fisura anal y enfermedad de Crohn. Sólo si las medidas conservadoras fracasan se planteará tratamiento quirúrgico. La esfinterotomía lateral interna es la técnica de elección en estos casos24,121-123. La fisurectomía está contraindicada.
Estenosis. En los casos de estenosis cortas o anulares que provoquen sintomatología, la dilatación digital o con tallos de Hegar será efectiva en la mayoría de casos7,18,124-126. Con frecuencia serán necesarias dilataciones repetidas. Excepcionalmente en estenosis largas y severas será necesaria una proctectomía124,127.
Lesiones concomitantes. En casos de hidrosadenitis supurativas se puede realizar exéresis en las fases no activas, cerrando siempre las heridas128. Si se presentan abscesificadas precisarán drenaje.
Otras consideraciones. Las hemorroides sintomáticas, aunque muy poco frecuentes en la enfermedad de Crohn, deben tratarse de forma conservadora. La hemorroidectomía está contraindicada en estos pacientes por la posibilidad de desencadenar complicaciones a nivel perianal como falta de cicatrización, estenosis residuales, o sepsis severas que un elevado porcentaje pueden abocar en una proctectomía12,17,18,39.
Cirugía urgente de la sepsis perianal
El procedimiento quirúrgico más frecuente es la incisión y drenaje de un absceso2,7,121,126,129. En ocasiones la ecografía endoanal intraoperatoria puede ayudar a localizarlos si son poco evidentes a la exploración44. Es aconsejable asociar tratamiento antibiótico. El objetivo, que no es otro que solucionar el cuadro séptico, no debe hacer olvidar la importancia de no dañar los esfínteres.
Si tras la incisión y drenaje de un absceso se puede poner de manifiesto la existencia de una fístula identificando el orificio interno, estará indicada, independientemente del tipo de fístula pero más si cabe si ésta es compleja, la colocación de un sedal a lo largo del trayecto, anudado de forma laxa, que además de permitir un correcto drenaje del absceso evitará la formación de nuevas colecciones2,15,32,130-136. Por otra parte, en caso de que posteriormente se plantee realizar una cirugía electiva de dicha fístula, tener el trayecto identificado será de una ayuda inestimable cualquiera que sea la técnica que se vaya a utilizar. Debemos comentar no obstante, que no siempre es posible identificar el orificio fistuloso interno en el trascurso del drenaje de un absceso, y aun identificándolo, tutorizar el trayecto puede ser una empresa difícil en la que se puede producir iatrogenia creando nuevos trayectos. Por tanto, aunque se debe intentar, no se debe insistir en colocar un sedal si la tutorización del trayecto no se consigue con maniobras suaves.
La gravedad de la enfermedad perianal por abscesos múltiples, profundos, o por una proctitis severa acompañante, condiciona en ocasiones una mala evolución del cuadro séptico tras el drenaje. En estas condiciones la derivación fecal mediante un estoma, preferentemente una ileostomía, puede hacerse necesaria a fin de controlar la sepsis137.
Cirugías puente para delimitar daños
Tras el drenaje de abscesos perianales es habitual que queden establecidas, si no lo estaban ya, una o varias fístulas. Éstas pueden responder a tratamiento médico, pero una solución puente en casos en que no haya habido respuesta y antes de valorar con cautela la posibilidad de cirugía definitiva, es como ya se ha comentado, la colocación de un sedal laxo a lo largo del trayecto fistuloso, que sirva de drenaje a la fístula y evite la formación de colecciones. La eficacia de esta medida en el control del dolor y la sepsis ha sido ampliamente contrastada independientemente del tipo de fístula en que se coloque2,15,32,130-136. Al evitar el desarrollo de nuevos abscesos, evita también la necesidad de realizar nuevas incisiones y drenajes, con el consiguiente beneficio para el mantenimiento de una correcta función esfinteriana. No está claro cuánto tiempo ha de mantenerse el sedal colocado, pues es frecuente que tras su retirada las fístulas recidiven y se desarrollen nuevos abscesos, posibilidad que aumenta con el paso del tiempo2,32,136. Es por eso que hay autores que optan por mantener estos sedales de forma indefinida, especialmente en pacientes con fístulas complejas.
En casos de enfermedad perianal extensa, o con proctitis asociada, es posible que los sedales no controlen de forma eficaz la sintomatología del paciente o el desarrollo de complicaciones. En estos casos la realización de un estoma derivativo, preferentemente ileostomía, puede ser también un tratamiento puente que mejore la sintomatología y haga remitir el proceso inflamatorio para intentar con posterioridad una cirugía definitiva138. Sin embargo, aunque las remisiones que se obtienen con la derivación son altas (80-90%), es posible que este recurso deba ser abandonado pues existen numerosos estudios que demuestran que la continuidad intestinal no será restaurada en la mayoría de estos pacientes (80-90%) y que muchos acabarán sometidos tarde o temprano a una proctectomía137,139-144. No obstante en estos casos, la derivación fecal puede ofrecer la ventaja de una proctectomía posterior en concidiones más favorables al haberse eliminado con el estoma la sepsis y el proceso inflamatorio local, lo que podría disminuir la alta incidencia (hasta un 30%) de sinus perineales145.
Cirugía definitiva
Como se ha visto la cirugía electiva está bien definida en lesiones simples (colgajos, fisuras...). Sin embargo con las fístulas, la elección de una cirugía definitiva es un tema controvertido, y antes de plantearla será imprescindible asegurar dos hechos fundamentales: la no afectación del recto por la enfermedad inflamatoria y la inactividad de la enfermedad a nivel intestinal18. El antecedente de cirugías previas que hayan podido dejar secuelas anatómicas y/o funcionales en el aparato esfinteriano, y que pueden incrementar la dificultad técnica de una nueva cirugía, es otro hecho importante a considerar antes de decidir la realización de un nuevo procedimiento quirúrgico.
Las fístulas sencillas, con un único orificio externo, un trayecto bajo (subcutáneas, interesfinterianas, transesfinterianas bajas), y sin proctitis asociada, pueden ser tratadas mediante fistulotomía, abriendo el trayecto fistuloso en toda su longitud. Las tasas de curación iniciales van desde el 27 al 95%, y las de recidiva tras haber curado inicialmente del 5 al 41%6,14,15,32,33,39,146-151 (Tabla 3). Sin embargo, puede haber problemas más o menos leves de incontinencia hasta en el 21% de los pacientes15,32. Si existe proctitis activa la tasa de éxito de la fistulotomía es inferior al 30%152, y la curación de la herida puede ser muy tórpida, pudiendo incluso llegarse a una proctectomía entre el 9 y el 29% de los casos15,30,32,146-148,150, por lo que en estas condiciones, la colocación de un sedal laxo es la mejor opción para la mayoría de autores. La fistulotomía tampoco debe realizarse en caso de fístulas bajas cuando se identifican durante el drenaje de un absceso perianal. En estas condiciones de sepsis local el sedal laxo ha de ser nuevamente el tratamiento de elección.
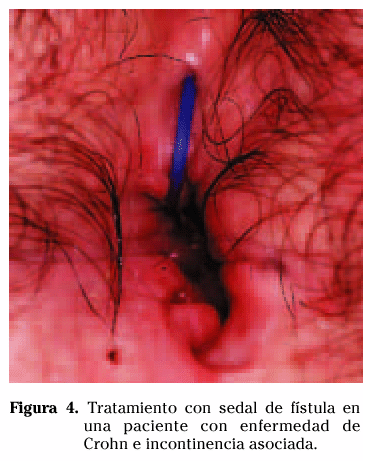
En el caso de fístulas complejas, la afectación concomitante del recto por la enfermedad inflamatoria es un hecho muy frecuente, por lo que la colocación de sedales laxos es la mejor opción quirúrgica153,154 (Figs. 4 y 5); evita el desarrollo de abscesos, evita heridas quirúrgicas amplias, preserva la función esfinteriana, y retrasa la necesidad de medidas más agresivas como el estoma derivativo o la proctectomía32,135.
Dada la elevada recidiva de las fístulas tras la retirada de los sedales a pesar de asociar tratamiento médico, en muchos casos habrá que considerar su uso de forma permanente2,32,136.
La fistulectomía con colgajo de avance endorrectal (Fig. 6) es una alternativa al sedal laxo siempre que no haya proctitis asociada, habiéndose comunicado buenos resultados en el 50-80% de los casos, con recurrencias en el 20-50% de los pacientes155-157 (Tabla 3). El colgajo rectal en manguito también ha sido descrito en el tratamiento de fístulas complejas en la enfermedad de Crohn, con un 62% de curación158. Sin embargo, el fracaso de la técnica puede acabar en proctectomía en un porcentaje elevado de casos.
El tratamiento de las fístulas rectovaginales sigue los mismos principios que las fístulas perianales. La mayoría son bajas, anovaginales, y en los pocos casos en que ocasionan clínica puede realizarse una fistulotomía17,159,160. Para las fístulas rectovaginales se han utilizado distintos procedimientos como el cierre primario17,161,162, colgajo de avance endorrectal151,155,163,164, colgajo de avance en manguito165,166, colgajos anocutáneos164 y colgajos de avance transvaginal167,168. Las tasas de éxito oscilan entre el 25 y el 93%. En caso de fístulas recidivadas puede ser necesaria la interposición muscular, gracilis, recto anterior169, pero hay que considerar que tras cada recidiva la posibilidad de acabar precisando una proctectomía se incrementa, por lo que si la sintomatología es leve el tratamiento conservador puede ser la mejor opción. La derivación fecal puede asegurar una mayor tasa de éxito tras estas técnicas167. Los sedales no son una técnica adecuada en la fístulas rectovaginales. En general, al igual que en el resto de fístulas, la coexistencia de enfermedad rectal debe contraindicar la realización de colgajos.
Los pacientes con un reservorio ileoanal que desarrollan una enfermedad de Crohn tienen un riesgo elevado de formación de fístulas y fallo del reservorio34-37. Si no existe enfermedad pueden intentarse procedimientos locales, un avance del reservorio, o interposición de colgajos musculares. Si existe enfermedad el reservorio será finalmente resecado en un 48% de los pacientes34-37.
La ablación con láser170, la inyección de adhesivos de fibrina171 o de infliximab172 en los trayectos fistulosos, el factor estimulante de colonias de granulocitos173, incluso el trasplante autólogo de células madre174, son otros tratamientos médico-quirúrgicos que han sido utilizados en el tratamiento de las fístulas perianales y rectovaginales en la enfermedad de Crohn. Sin embargo no existen todavía ensayos clínicos que puedan avalar su uso rutinario.
Finalmente, un 10-20% de pacientes con enfermedad de Crohn perianal precisarán una proctectomía (o proctocolectomía) con estoma definitivo13,15,59,133,134,147. La sepsis perianal grave refractaria al tratamiento médico o a medidas quirúrgicas más conservadoras, las úlceras rectales con gran destrucción tisular, las estenosis rectales severas, o cualquier enfermedad perianal asociada a proctitis severa, con sintomatología rectal, tenesmo, urgencia, incontinencia, etc, rebelde a tratamiento, son condiciones que se van a beneficiar únicamente de la resección del recto13,15,59,133,134,147. La proctocolectomía será la técnica de elección cuando existe una proctocolitis con enfermedad perianal grave, pero probablemente también sea la mejor opción cuando existe una pancolitis con enfermedad perianal aunque el recto no esté afectado, pues la morbilidad asociada al remanente rectal es elevada175.
El uso creciente de sedales laxos, y los nuevos avances en el tratamiento médico como el infliximab en terapias de mantenimiento, probablemente consigan reducir las tasas de proctectomía en la enfermedad de Crohn en un futuro próximo.
Cirugía de la enfermedad intestinal concomitante
Parece comprobado que la resección de la enfermedad de Crohn a nivel intestinal, sobre todo si se extirpa toda la enfermedad, mejora y cura la enfermedad perianal hasta en un 50% de los casos29. Igualmente, la recurrencia de la enfermedad perianal tras resección del Crohn enteral es muy superior si existe también recurrencia intestinal que si ésta no se produce9. No obstante la enfermedad perianal por sí sola no es una indicación para realizar una resección proximal.
Tratamiento combinado médico-quirúrgico
Aunque ya se ha comentado, es importante resaltar que habitualmente el tratamiento de la enfermedad de Crohn perianal no es médico o quirúrgico, sino que ambos tratamientos han de combinarse para conseguir los mejores resultados. En algunos casos habrán de aplicarse simultáneamente (abscesos en que se combinará el drenaje quirúrgico con tratamiento antibiótico, fístulas activas que se beneficiarán de combinar tratamiento médico con colocación de sadales, etc), mientras que en otros el tratamiento médico permitirá conseguir las mejores condiciones para llevar a cabo una cirugía definitiva (ya se ha comentado cómo por ejemplo, es imprescindible tratar la actividad intestinal o la proctitis, si existen, antes de plantear una cirugía definitiva a nivel perianal).
Por último y como conclusión, reiterar el hecho de que la enfermedad de Crohn perianal exige, como pocas otras patologías, abordar cada paciente de forma individualizada, para que en función del tipo de lesión o lesiones que presente, la gravedad de las mismas, el antecedente de cirugías previas, el estado de la función esfinteriana, la posible afectación intestinal y rectal concomitante, la respuesta a tratamientos previos, o el impacto que la enfermedad tiene sobre la calidad de vida del paciente, podamos tomar las decisiones terapéuticas más apropiadas para cada enfermo.
Bibliografía
1. Hughes LE. Surgical pathology and management of anorectal Crohns disease. J R Soc Med 1978; 71: 644-651. [ Links ]
2. Sangwan YP, Schoetz DJJr, Murray JJ, Roberts PL, Coller JA. Perianal Crohns disease. Results of local surgical treatment. Dis Colon Rectum 1996; 39: 529-535. [ Links ]
3. Lockhart-Mummery HE. Symposium. Crohns disease: anal lesions. Dis Colon Rectum 1975; 18: 200-202. [ Links ]
4. McClane SJ, Rombeau JL. Anorectal Crohns disease. Surg Clin North Am 2001; 81: 169-183. [ Links ]
5. Williams DR, Coller JA, Corman ML, Nugent FW, Veidenheimer MC. Anal complications in Crohns disease. Dis Colon Rectum 1981; 24: 22-24. [ Links ]
6. Platell C, Mackay J, Collopy B, Fink R, Ryan P, Woods R. Anal pathology in patients with Crohns disease. Aust N Z J Surg 1996; 66: 5-9. [ Links ]
7. Lockhart-Mummery HE. Anal lesions in Crohns disease. Br J Surg 1985; 72 (Suppl): S95-S96. [ Links ]
8. Rankin GB, Watts HD, Melnyk CS, Kelley ML Jr. National Cooperative Crohns Disease Study: extraintestinal manifestations and perianal complications. Gastroenterology 1979; 77: 914-920. [ Links ]
9. Heuman R, Bolin T, Sjodahl R, Tagesson C. The incidence and course of perianal complications and arthralgia after intestinal resection with restoration of continuity for Crohns disease. Br J Surg 1981; 68: 528-530. [ Links ]
10. Hughes LE. Clinical classification of perianal Crohn´s diseases. Dis Colon Rectum 1992; 35: 928-932. [ Links ]
11. Armuzzi A, Ahmad T, Ling KL, de Silva A, Cullen S, van Heel D y col. Genotype-phenotype analysis of the Crohns disease susceptibility haplotype on chromosome 5q31. Gut 2003; 52: 1133-1139. [ Links ]
12. Jeffery PJ, Parks AG, Ritchie JK. Treatment of haemorrhoids in patients with inflammatory bowel disease. Lancet 1977; i: 1084-1085. [ Links ]
13. Wolff BG, Culp CE, Beart RWJr, Ilstrup DM, Ready RL. Anorrectal Crohn´s disease. A long-term perspective. Dis Colon Rectum 1985; 28: 709-711. [ Links ]
14. Marks CG, Ritchie JK, Lockhart-Mummery HE. Anal fistulas in Crohn´s disease. Br J Surg 1981; 68: 525-527. [ Links ]
15. Williams JG, Rothenberger DA, Nemer FD, Goldberg SM. Fistula-in-ano in Crohns disease. Results of aggressive surgical treatment. Dis Colon Rectum 1991; 34: 378-384. [ Links ]
16. Keighley MRB, Williams NS. Surgery of the Anus, Rectum, and Colon. WB Saunders: London, 1993. [ Links ]
17. Radcliffe AG, Ritchie JK, Hawley PR, Lennard-Jones JE, Northover JM. Anovaginal and rectovaginal fistulas in Crohns disease. Dis Colon Rectum 1988; 31: 94-99. [ Links ]
18. Keighley MR, Allan RN. Current status and influence of operation on perianal Crohn´s disease. Int J Colorectal Dis 1986; 1: 104-107. [ Links ]
19. Ky A, Sohn N, Weinstein MA, Korelitz BI. Carcinoma arising in anorectal fistulas of Crohn´s disease. Dis Colon Rectum 1998; 41: 992-996. [ Links ]
20. Church JM, Weakley FL, Fazio VW, Sebek BA, Achkar E, Carwell M. The relationship between fistulas in Crohn´s disease and associated carcinoma. Report of four cases and review of the literature. Dis Colon Rectum 1985; 28: 361-366. [ Links ]
21. Fielding JF. Perianal lesions in Crohn´s disease. J R Coll Surg Edinb 1972; 17: 32-37. [ Links ]
22. Buchmann P, Keighley MR, Allan RN, Thompson H, Alexander-Williams J. Natural history of perianal Crohn´s disease. Ten year follow-up: a plea for conservatism. Am J Surg 1980; 140: 642-644. [ Links ]
23. Alexander-Williams J, Buchmann P. Perianal Crohns disease. World J Surg 1980; 4: 203-208. [ Links ]
24. Fleshner PR, Schoetz DJJr, Roberts PL, Murray JJ, Coller JA, Veidenheimer MC. Anal fissure in Crohns disease: a plea for aggressive management. Dis Colon Rectum 1995; 38: 1137-1143. [ Links ]
25. Sweeney JL, Ritchie JK, Nicholls RJ. Anal fissure in Crohns disease. Br J Surg 1988; 75: 56-57. [ Links ]
26. Allan A, Keighley MRB. Management of perianal Crohn´s disease. World J Surg 1988; 12: 198-202. [ Links ]
27. Parks AG, Gordon PH, Hardcastle JD. A classification of fistula-in-ano. Br J Surg 1976; 63: 1-12. [ Links ]
28. Williams JG, Hughes LE. Abdominoperineal resection for severe perianal Crohn´s disease. Dis Colon Rectum 1990; 33: 402-407. [ Links ]
29. Bergstrand O, Ewerth S, Hellers G, Holmstrom B, Ullman J, Wallberg P. Outcome following treatment of anal fistulae in Crohns disease. Acta Chir Scand Suppl 1980; 500: 43-44. [ Links ]
30. Halme L, Sainio AP. Factors related to frequency, type, and outcome of anal fistulas in Crohns disease. Dis Colon Rectum 1995; 38: 55-59. [ Links ]
31. Hellers G, Bergstrand O, Ewerth S, Holmstrom B. Occurrence and outcome after primary treatment of anal fistulae in Crohn´s disease. Gut 1980; 21: 525-527. [ Links ]
32. Scott HJ, Northover JM. Evaluation of surgery for perianal Crohns fistulas. Dis Colon Rectum 1996; 39: 1039-1043. [ Links ]
33. Williamson PR, Hellinger MD, Larach SW, Ferrara A. Twenty-year review of the surgical management of perianal Crohns disease. Dis Colon Rectum 1995; 38: 389-392. [ Links ]
34. Sagar PM, Dozois RR, Wolff BG. Long-term results of ileal pouch-anal anastomosis in patients with Crohns disease. Dis Colon Rectum 1996; 39: 893-898. [ Links ]
35. Keighley MR. The final diagnosis in pouch patients for presumed ulcerative colitis may change to Crohns disease: patients should be warned of the consequences. Acta Chir Yugosl 2000; 47: 27-31. [ Links ]
36. Hyman NH, Fazio VW, Tuckson WB, Lavery IC. Consequences of ileal pouch-anal anastomosis for Crohns colitis. Dis Colon Rectum 1991; 34: 653-657. [ Links ]
37. Braveman JM, Schoetz DJ, Marcello PW, Roberts PL, Coller JA, Murray JJ y col. The fate of the ileal pouch in patients developing Crohns disease. Dis Colon Rectum 2004; 47: 1613-1619. [ Links ]
38. Alexander-Williams J. Surgical treatment of perianal Crohn´s diseases: the case for conservative treatment. En: Surgery of Inflammatory Bowel Disorders. Eds. Lee ECG, Nolan DJ. Churdhill Livingstone, 1987: 180-183. [ Links ]
39. Morrison JG, Gathright JBJr, Ray JE, Ferrari BT, Hicks YC, Timmcke AE. Surgical management of anorectal fistulas in Crohn´s disease. Dis Colon Rectum 1989; 32: 492-496. [ Links ]
40. Chaikhouni A, Regueyra FI, Stevens JR. Adenocarcinoma in perianal fistulas of Crohn´s disease. Dis Colon Rectum 1981; 24: 639-643. [ Links ]
41. Korelitz BI. Carcinoma arising in Crohn´s disease fistulae: another concern warranting another type of surveillance. Am J Gastroenterol 1999; 94: 2337-2339. [ Links ]
42. Wong NA, Shirazi T, Hamer-Hodges DW, Corfield AP, Lessells AM. Adenocarcinoma arising within a Crohn´s related anorectal fistula: a form of anal gland carcinoma? Histopathology 2002; 40: 302-304. [ Links ]
43. Kulaylat MN, Gallina G, Bem J, Zeid M. Carcinoma arising in anorectal fistulas of Crohn´s disease. Dis Colon Rectum 1999; 42: 826-828. [ Links ]
44. Solomon MJ. Fistulae and abscesses in symptomatic perianal Crohns disease. Int J Colorectal Dis 1996; 11: 222-226. [ Links ]
45. Cho DY. Endosonographic criteria for an internal opening of fistula-in-ano. Dis Colon Rectum 1999; 42: 515-518. [ Links ]
46. Orsoni P, Barthet M, Portier F, Panuel M, Desjeux A, Grimaud JC. Prospective comparision of endosonography, magnetic resonance imaging and surgical findings in anorectal fistula and abscess complicating Crohn´s disease. Br J Surg 1999; 86: 1093-1094. [ Links ]
47. Yee LF, Birnbaum EH, Read TE, Kodner IJ, Fleshman JW. Use of endoanal ultrasound in patients with rectovaginal fistulas. Dis Colon Rectum 1999; 42: 1057-1064. [ Links ]
48. Solomon MJ, McLeod RS, Cohen EK. Reliability and validity studies of endoluminal ultrasonography for anorectal disorders. Dis Colon Rectum 1994; 37: 546-551. [ Links ]
49. Poen AC, Felt-Bersma RJ, Cuesta MA, Meuwissen GM. Vaginal endosonography of the anal sphincter complex is important in the assessment of faecal incontinence and perianal sepsis. Br J Surg 1998; 85: 359-363. [ Links ]
50. Borley NR, Mortensen NJ, Jewell DP. MRI scanning in perianal Crohns disease: an important diagnostic adjunct. Inflamm Bowel Dis 1999; 5: 231-233. [ Links ]
51. Morris J, Spencer JA, Ambrose NS. MR imaging classification of perianal fistulas and its implications for patient mangement. Radiographics 2000; 20: 623-635. [ Links ]
52. Schwartz DA, Wiersema MJ, Dudiak KM, Fletcher JG, Clain JE, Tremaine WJ y col. A comparison of endoscopic ultrasound, magnetic resonance imaging, and exam under anesthesia for evaluation of Crohns perianal fistulas. Gastroenterology 2001; 121: 1064-1072. [ Links ]
53. van Bodegraven AA, Sloots CE, Felt-Bersma RJ, Meuwissen SG. Endosonographic evidence of persistence of Crohns disease-associated fistulas after infliximab treatment, irrespective of clinical response. Dis Colon Rectum 2002; 45: 39-45; discussion 45-46. [ Links ]
54. Van Assche G, Vanbeckevoort D, Bielen D, Coremans G, Aerden I, Noman M y col. Magnetic resonance imaging of the effects of infliximab on perianal fistulizing Crohns disease. Am J Gastroenterol 2003; 98: 332-339. [ Links ]
55. Bell SJ, Halligan S, Windsor AC, Williams AB, Wiesel P, Kamm MA. Response of fistulating Crohn´s disease to infliximab treatment assessed by magnetic resonance imaging. Aliment Pharmacol Ther 2003; 17: 387-393. [ Links ]
56. Loftus EV. Imaging and therapy for perianal Crohn´s disease: On the right track? Am J Gastroenterol 2004; 99: 89-90. [ Links ]
57. Irvine EJ. Usual therapy improves perianal Crohn´s disease as measured by a new disease activity index. McMaster IBD Study Group. J Clin Gastroenterol 1995; 20: 27-32. [ Links ]
58. Lichtenstein GR. Treatment of fistulizing Crohns disease. Gastroenterology 2000; 119: 1132-1147. [ Links ]
59. Basu A, Wexner SD. Perianal Crohns disease. Curr Treat Options Gastroenterol 2002; 5: 197-206. [ Links ]
60. Klotzs U, Maier K, Fischer C, Heinkel K. Therapeutic efficacy of sulphasalazine and its metabolites in patients with ulcerative colitis and Crohn´s disease. N Engl J Med 1980; 303: 1499-1502. [ Links ]
61. Present DH. Perianal fistula. En: Advanced therapy of inflammatory bowel disease. Bayless-Hanauer, eds. London: B.C. Decker Inc 2001: 395-400. [ Links ]
62. Ursing B, Kamme C. Metronidazole for Crohns disease. Lancet 1975; i: 775-777. [ Links ]
63. Bernstein LH, Frank MS, Brandt LJ, Boley SJ. Healing of perineal Crohns disease with metronidazole. Gastroenterology 1980; 79: 357-365. [ Links ]
64. Schneider MU, Strobel S, Riemann JF, Demling L. Treatment of Crohn´s disease with metronidazole. Dtsch Med Wochenschr 1981; 106: 1126-1129. [ Links ]
65. Jakobovits J, Schuster MM. Metronidazole therapy for Crohn´s disease and associated fistulae. Am J Gastroenterol 1984; 79: 533-540. [ Links ]
66. Schneider MU, Laudage G, Guggenmoos-Holzmann I, Riemann JF. Metronidazole in the treatment of Crohn disease. Results of a controlled randomized prospective study. Dtsch Med Wochenschr 1985; 110: 1724-1730. [ Links ]
67. Brandt LJ, Bernstein LH, Boley SJ, Frank MS. Metronidazole therapy for perineal Crohn´s disease: a follow-up study. Gastroenterology 1982; 83: 383-387. [ Links ]
68. Brandt LJ, Bernstein LH, Boley SJ, Frank MS. Metronidazole therapy for perineal Crohns disease: a follow-up study. Gastroenterology 1982; 83: 383-387. [ Links ]
69. Stahlberg D, Barany F, Einarsson K, Ursing B, Elmqvist D, Persson A. Neurophysiologic studies of patients with Crohns disease on long-term treatment with metronidazole. Scand J Gastroenterol 1991; 26: 219-224. [ Links ]
70. Turunen U, Farkkila M, Valtonen V. Long-term outcome of ciprofloxacin treatment in severe perianal or fistulous Crohns disease. Gastroenterology 1993; 104: A793. [ Links ]
71. Wolf JL. Ciprofloxacine may be usefull in Crohn´s disease. Gastroenterology 1990; A212. [ Links ]
72. Prantera C, Kohn A, Zannoni F. Metronidazole plus ciprofloxacin in the treatment of active refractory Crohn´s disease: results of an open study. J Clin Gastroenterol 1994; 19: 79-88. [ Links ]
73. Present DH, Korelitz BI, Wisch N, Glass JL, Sachar DB, Pasternack BS. Treatment of Crohn´s disease with 6-mercaptopurine. A long-term, randomized, double-blind study. N Engl J Med 1980; 302: 981-987. [ Links ]
74. Klein M, Binder HJ, Mitchell M, Aaronson R, Spiro H. Treatment of Crohn´s disease with azathioprine: a controlled evaluation. Gastroenterology 1974; 66: 916-922. [ Links ]
75. Rosenberg JL, Levin B, Wall AJ, Kirsner JB. A controlled trial of azathioprine in Crohn´s disease. Am J Dig Dis 1975; 20: 721-726. [ Links ]
76. Rhodes J, Bainton D, Beck P, Campbell H. Controlled trial of azathioprine in Crohn´s disease. Lancet 1971; 2: 1273-1276. [ Links ]
77. Willoughby JM, Beckett J, Kumar PJ, Dawson AM. Controlled trial of azathioprine in Crohn´s disease. Lancet 1971; 2: 944-947. [ Links ]
78. Pearson DC, May GR, Fick GH, Sutherland LR. Azathioprine and 6-mercaptopurine in Crohn´s disease. A meta-analysis. Ann Intern Med 1995; 123: 132-142. [ Links ]
79. Present DH, Meltzer SJ, Krumholz MP, Wolke A, Korelitz BI. 6-Mercaptopurine in the management of inflammatory bowel disease: short- and long-term toxicity. Ann Intern Med 1989; 111: 641-649. [ Links ]
80. Hanauer SB, Smith MB. Rapid closure of Crohns disease fistulas with continuous intravenous cyclosporin A. Am J Gastroenterol 1993; 88: 646-649. [ Links ]
81. Present DH, Lichtiger S. Efficacy of cyclosporine in treatment of fistula of Crohns disease. Dig Dis Sci 1994; 39: 374-380. [ Links ]
82. O´Neill J, Pathmakanthan S, Goh J. Cyclosporine A induces remission in fistulous Crohn´s disease but relapse occurs upon cessation of treatment. Gastroenterology 1997; 112: A1056. [ Links ]
83. Hinterleitner TA, Petrisch W, Aichbichler B, Fickert P, Ranner G, Krejs GJ. Combination of cyclosporine and prednisolone for perianal fistulas in Crohn´s disease. Z Gastroenterol 1997; 35: 603-608. [ Links ]
84. Egan LJ, Sandborn WJ, Tremaine WJ. Clinical outcome following treatment of refractory inflammatory and fistulizing Crohn´s disease with intravenous cyclosporine. Am J Gastroenterol 1998; 93: 442-448. [ Links ]
85. Gurudu SR, Griffel LH, Gialanella RJ, Das KM. Cyclosporine therapy in inflammatory bowel disease: short-term and log-term results. J Clin Gastroenterol 1999; 29: 151-154. [ Links ]
86. García-Planella E, Domenech E, Cabre E, Bernal MI, Gassull MA. Intravenous cyclosporine A in the treatment of refractory Crohn´s disease. Med Clin (Barc) 2002; 119: 610-612. [ Links ]
87. Sandborn W. A critical review of cyclosporine therapy in inflammatory bowel disease. Inflamm Bowel Dis 1995; 1: 48-63. [ Links ]
88. Sandborn WJ, Present DH, Isaacs KL, Wolf DC, Greenberg E, Hanauer SB y col. Tacrolimus for the treatment of fistulas in patients with Cronh´s disease: a randomized, placebo-controlled trial. Gastroenterology 2003; 125: 380-388. [ Links ]
89. Lowry PW, Weaver AL, Tremaine WJ, Sandborn WJ. Combination therapy with oral tacrolimus (FK506) and azathioprine or 6-mercaptopurine for treatment refractory Crohn´s disease perianal fistulae. Inflamm Bowel Dis 1999; 5: 239-245. [ Links ]
90. Sandborn WJ. Preliminary report on the use of oral tacrolimus (FK506) in the treatment of complicated proximal small bowel and fistulizing Crohn´s disease. Am J Gastroenterol 1997; 92: 876-879. [ Links ]
91. Fellermann K, Ludwig D, Stahl M, David-Walek T, Stange EF. Steroid-unresponsive acute attaks of inflammatory bowel disease: immunomodulation by tacrolimus (FK506). Am J Gastroenterol 1998;93: 1860- 1866. [ Links ]
92. Casson DH, Eltumi M, Tomlin S, Walker-Smith JA, Murch SH. Topical tacrolimus may be effective in the treatment of oral and perianal Crohn´s disease. Gut 2000; 47: 436-440. [ Links ]
93. Targan SR, Hanauer SB, van Deventer SJ, Mayer L, Present DH, Braakman T y col. A short-term study of chimeric monoclonal antibody cA2 to tumor necrosis factor alpha for Crohns disease. Crohns Disease cA2 Study Group. N Engl J Med 1997; 337: 1029-1035. [ Links ]
94. Sandborn WJ, Hanauer SB. Antitumor necrosis factor therapy for inflammatory bowel disease: a review of agents, pharmacology, clinical results, and safety. Inflamm Bowel Dis 1999; 5: 119-133. [ Links ]
95. Braegger CP, Nicholls S, Murch SH, Stephens S, MacDonald TT. Tumour necrosis factor alpha in stool as a marker of intestinal inflammation. Lancet 1992; 339: 89-91. [ Links ]
96. Murch SH, Braegger CP, Walker-Smith JA, MacDonald TT. Location of tumour necrosis factor alpha by immunohistochemistry in chronic inflammatory bowel disease. Gut 1993; 34: 1705-1709. [ Links ]
97. Kam L, Targan S. Infliximab and Croan´s disease. Clin Perspect Gastroenterol 1998; 1: 67-72. [ Links ]
98. Present DH, Rutgeerts P, Targan S, Hanauer SB, Mayer L, van Hogezand RA y col. Infliximab for the treatment of fistulas in patients with Crohns disease. N Engl J Med 1999; 340: 1398-1405. [ Links ]
99. Fefferman D, Lodhavia P, Reinert S y col. Smoking, age, duration of disease, gender, and other clinical factors do not predict response to infliximab in Crohn´s disease patients. Gastroenterology 2001; 120: A619. [ Links ]
100. Louis E, Vermiere S, Rutgeerts P y col. Are systemics inflammatory markers useful in the prediction of response to infliximab in Crohn´s disease? Gastroenterology 2001; 120: A622. [ Links ]
101. Luna-Chadid M, Pérez Calle JL, Mendoza JL, Vera MI, Bermejo AF, Sánchez F y col. Predictors of response to infliximab in patients with fistulizing Crohn´s disease. Rev Esp Enferm Dig 2004; 96: 379-381; discussion 382-384. [ Links ]
102. Parsi MA, Lashner BA, Achkar JP, Connor JT, Brzezinski A. Type of fistula determines response to infliximab in patients with fistulous Crohn´s disease. Am J Gastroenterol 2004; 99: 445-449. [ Links ]
103. Sands BE, Anderson FH, Bernstein CN, Chey WY, Feagan BG, Fedorak RN y col. Infliximab maintenance therapy for fistulizing Cronh´s disease. N Engl J Med 2004; 350: 876-885. [ Links ]
104. Ochsenkuhn T, Goke B, Sackmann M. Combining infliximab with 6-mercaptopurine/azathioprine for fistula therapy in Crohns disease. Am J Gastroenterol 2002; 97: 2022-2025. [ Links ]
105. Topstad DR, Panaccione R, Heine JA, Johnson DRE, MacLean AR, Buie WD. Combined seton placement, infliximab infusion, and maintenance immunosuppressives improve healing rate in fistulizing anorectal Crohn´s disease: a single center experience. Dis Colon Rectum 2003; 46: 577-583. [ Links ]
106. Regueiro M, Mardini H. Treatment of perianal fistulizing Crohn´s disease with infliximab alone an adjunct to exam under anesthesia with seton placement. Inflamm Bowel Dis 2003; 9: 98-103. [ Links ]
107. Poritz LS, Rowe WA, Koltun WA. Remicade does not abolish the need for surgery in fistulizing Crohn´s disease. Dis Colon Rectum 2002; 45: 771-775. [ Links ]
108. McNamara DA, Brophy S, Hyland JM. Perianal Croan´s disease and infliximab therapy. Surgeon 2004; 2: 258-263. [ Links ]
109. Hanauer SB. Safety of infliximab in clinical trials. Aliment Pharmacol Ther 1999; 13 (Suppl 4): 16-22. [ Links ]
110. Colombel JF, Loftus EV Jr, Tremaine WJ, Egan LJ, Harmsen WS, Schleck CD y col. The safety profile of infliximab in patients with Crohn´s disease: the Mayo Clinic experience in 500 patients. Gastroenterology 2004; 126: 19-31. [ Links ]
111. Ricart E, Panaccione R, Loftus EV, Tremaine WJ, Sandborn WJ. Successful management of Crohns disease of the ileoanal pouch with infliximab. Gastroenterology 1999; 117: 429-432. [ Links ]
112. Colombel JF, Ricart E, Loftus EVJr, Tremaine WJ, Young-Fadok T, Dozois EJ y col. Management of Crohn´s disease of the ileoanal pouch with infliximab. Am J Gastroenterol 2003; 98: 2239-2244. [ Links ]
113. Kozarek RA, Patterson DJ, Gelfand MD, Botoman VA, Ball TJ, Wilske KR. Methotrexate induces clinical and histologic remission in patients with refractory inflammatory bowel disease. Ann Intern Med 1989; 110: 353-356. [ Links ]
114. Feagan BG, Rochon J, Fedorak RN, Irvine EJ, Wild G, Sutherland L y col. Methotrexate for the treatment of Crohns disease. The North American Crohns Study Group Investigators. N Engl J Med 1995; 332: 292-297. [ Links ]
115. Fickert P, Hinterleitner TA, Wenzl HH, Aichbichler BW, Petritsch W. Mycophenolate mofetil in patients with Cronh´s disease. Am J Gastroenterol 1998; 93: 2529-2532. [ Links ]
116. Ehrenpreis ED, Kane SV, Cohen LB, Cohen RD, Hanauer SB. Thalidomide therapy for patients with refractory Crohns disease: an open-label trial. Gastroenterology 1999; 117: 1271-1277. [ Links ]
117. Sandborn WJ, Feagan BG, Hanauer SB, Present DH, Sutherland LR, Kamm MA y col. An engineered human antibody to TNF (CDP571) for active Crohns disease: a randomized double-blind placebo-controlled trial. Gastroenterology 2001; 120: 1330-1338. [ Links ]
118. Colombel JF, Mathieu D, Bouault JM, Lesage X, Zavadil P, Quandalle P y col. Hyperbaric oxygenation in severe perineal Crohns disease. Dis Colon Rectum 1995; 38: 609-614. [ Links ]
119. Brady CE III, Cooley BJ, Davis JC. Healing of severe perineal and cutaneous Crohns disease with hyperbaric oxygen. Gastroenterology 1989; 97: 756-760. [ Links ]
120. Calam J, Crooks PE, Walker RJ. Elemental diets in the management of Croan´s perianal fistulae. J Parenter Enteral Nutr 1980; 4: 4-8. [ Links ]
121. Sohn N, Korelitz BI, Weinstein MA. Anorectal Crohn´s disease: definitive surgery for fistulas and recurrent abscesses. Am J Surg 1980; 139: 394-397. [ Links ]
122. Sweeney JL, Ritchie JK, Nicholls RJ. Anal fissure in Crohn´s disease. Br J Surg 1988; 75: 56-57. [ Links ]
123. Fleshner PR, Schoetz DJ Jr, Roberts PL, Murray JJ, Coller JA, Veidenheimer MC. Anal fissure in Crohn´s disease: a plea for aggressive management. Dis Colon Rectum 1995; 38: 1137-1143. [ Links ]
124. Linares L, Moreira LF, Andrews H, Allan RN, Alexander-Williams J, Keighley MR. Natural history and treatment of anorectal strictures complicating Crohn´s disease. Br J Surg 1988; 75: 653-655. [ Links ]
125. Alexander-Williams J, Allan A, Morel P, Hawker PC, Dykes PW, O´Connor H. The therapeutic dilatation of enteric strictures due to Crohn´s disease. Ann R Coll Surg Engl 1986; 68: 95-97. [ Links ]
126. Bernard D, Morgan S, Tasse D. Selective surgical management of Crohn´s disease of the anus. Can J Surg 1986; 29: 318-321. [ Links ]
127. Homan WP, Tang C, Thorgjarnarson B. Anal lesions complicating Crohn disease. Arch Surg 1976; 111: 1333-1335. [ Links ]
128. Church JM, Fazio VW, Lavery IC, Oakley JR, Milsom JW. The differential diagnosis and comorbidity of hidradenitis suppurative and perianal Crohn´s disease. Int J Colorectal Dis 1993; 8: 117-119. [ Links ]
129. Fry RD, Shemesh EI, Kodner IJ, Timmcke A. Techniques and results in the management of anal and perianal Crohns disease. Surg Gynecol Obstet 1989; 168: 42-48. [ Links ]
130. White RA, Eisenstat TE, Rubin RJ, Salvati EP. Seton management of complex anorectal fistulas in patients with Crohn´s disease. Dis Colon Rectum 1990; 3: 587-589. [ Links ]
131. Koganei K, Sugita A, Harada H, Fukushima T, Shimada H. Seton treatment for perianal Crohn´s fistulas. Surg Today 1995; 25: 32-36. [ Links ]
132. Sugita A, Koganei K, Harada H, Yamazaki Y, Fukushima T, Shimada H. Surgery for Crohn´s anal fistulas. J Gastroenterol 1995; 30 (suppl 8): 143-146. [ Links ]
133. Williams JG, MacLeod CA, Rothenberger DA, Goldber SM. Seton treatment of high anal fistulae. Br J Surg 1991; 78: 1159-1161. [ Links ]
134. Faucheron JL, Saint-Marc O, Guibert L, Parc R. Long-term seton drainage for high anal fistulas in Crohn´s disease – a sphincter-saving operation? Dis Colon Rectum 1996; 39: 208-211. [ Links ]
135. Pearl RK, Andrews JR, Orsay CP, Weisman RI, Prasad ML, Nelson RL y col. Role of the seton in the mangement of anorectal fistulas. Dis Colon Rectum 1993; 36: 573-577; discussion 577-579. [ Links ]
136. Buchanan GN, Owen HA, Torkington J, Lunnis PJ, Nicholls RJ, Cohen CR. Long-term outcome following loose-seton technique for external sphincter preservation in complex anal fistula. Br J Surg 2004; 91: 476-480. [ Links ]
137. Yamamoto T, Allan RN, Keighley MR. Effect of fecal diversion alone on perianal Crohn´s disease. World J Surg 2000; 24: 1258-1262; discussion 1262-1263. [ Links ]
138. Edwards CM, George BD, Jewell DP, Warren BF, Mortensen NJ, Kettlewell MG. Role of a defunctioning stoma in the management of large bowel Crohn´s disease. Br J Surg 2000; 87: 1063-1066. [ Links ]
139. Winslet MC, Andrews H, Allan RN, Keighley MRB. Fecal diversion in the management of Crohn´s disease of the colon. Dis Colon Rectum 1993; 36: 757. [ Links ]
140. Harper PH, Kettlewell MG, Lee EC. The effect of split ileostomy on perianal Crohn´s disease. Br J Surg 1982; 69: 608-610. [ Links ]
141. Zelas P, Jagelman DG. Loop ileostomy in the management of Crohn´s colitis in the debilitated patient. Ann Surg 1980; 191: 164-168. [ Links ]
142. Grant DR, Cohen Z, McLeod RS. Loop ileostomy for anorectal Crohn´s disease. Can J Surg 1986; 29: 32-35. [ Links ]
143. Sher ME, Bauer JJ, Gorphine S, Gelernt I. Low Hartmann´s procedure for severe anorectal Crohn´s disease. Dis Colon Rectum 1992; 35: 975-980. [ Links ]
144. Orkin BA, Telander RL. The effect of intra-abdominal resection or fecal diversion on perianal disease in pediatric Crohn´s disease. J Pediatr Surg 1985; 20: 343-347. [ Links ]
145. Yamamoto T, Bain IM, Allan RN, Keighley MR. Persistent perineal sinus after proctocolectomy for Crohns disease. Dis Colon Rectum 1999; 42: 96-101. [ Links ]
146. Hobbiss JH, Schofield PF. Management of perianal Crohn´s disease. J R Soc Med 1982; 75: 414-417. [ Links ]
147. Levien DH, Surrell J, Mazier WP. Surgical treatment of anorectal fistula in patients with Crohn´s disease. Surg Ginecol Obstet 1989; 169: 133-136. [ Links ]
148. Fuhrman GM, Larach SW. Experience with perirectal fistulas in patients with Crohn´s disease. Dis Colon Rectum 1989; 32: 847-848. [ Links ]
149. Winter AM, Banks PA, Petros JG. Healing of transsphincteric perianal fistulas in Crohn´s disease using a new technique. Am J Gastroenterol 1993; 88: 2022-2025. [ Links ]
150. McKee RF, Keenan RA. Perianal Crohn´s disease – is it all bad news? Dis Colon Rectum 1996; 39: 136-142. [ Links ]
151. Michelassi F, Melis M, Rubin M, Hurst RD. Surgical treatment of anorectal complications in Crohn´s disease. Surgery 2000; 128: 597-603. [ Links ]
152. Nordgren S, Fasth S, Hulten L. Anal fistulas in Crohn´s disease: incidence and outcome of surgical treatment. Int J Colorectal Dis 1992; 7: 214-218. [ Links ]
153. Sonoda T, Hull T, Piedmonte MR, Fazio VW. Outcomes of primary repair of anorectal and rectovaginal fistulas using the endorectal advancement flap. Dis Colon Rectum 2002; 45: 1622-1628. [ Links ]
154. Mizrahi N, Wexner SD, Zmora O, Da Silva G, Efron J, Weiss EG y col. Endorectal advancemet flap: are there predictors of failure? Dis Colon Rectum 2002; 45: 1616-1621. [ Links ]
155. Makowiec F, Jehle EC, Becker HD, Starlinger M. Clinical course after transanal advancement flap repair of perianal fistula in patients with Crohn´s disease. Br J Surg 1995; 82: 603-606. [ Links ]
156. Joo JS, Weiss EG, Nogueras JJ, Wexner SD. Endorectal advancement flap in perianal Crohn´s disease. Am Surg 1998; 64: 147-150. [ Links ]
157. Robertson WG, Mangione JS. Cutaneous advancement flap closure: alternative method for treatment of complicated anal fistulas. Dis Colon Rectum 1998; 41: 884-886; discussion 886-887. [ Links ]
158. Marchesa P, Hull TL, Fazio VW. Advancement sleeve flaps for treatment of severe perianal Crohn´s disease. Br J Surg 1998; 85: 1695-1698. [ Links ]
159. Francois Y, Vignal J, Descos L. Outcome of perianal fistulae in Crohn´s disease – value of Hughes´ pathogenic classification. Int J Colorectal Dis 1993; 8: 39-41. [ Links ]
160. Hudson CN. Acquired fistulae between the intestine and the vagina. Ann R Coll Surg Engl 1970; 46: 20-40. [ Links ]
161. Bandy LC, Addison A, Parker RT. Surgical management of rectovaginal fistulas in Crohn´s disease. Am J Obstet Gynecol 1983; 147: 359-363. [ Links ]
162. Cohen JL, Stricker JW, Schoetz DJ Jr, Coller JA, Veidenheimer MC. Rectovaginal fistula in Crohn´s disease. Dis Coln Rectum 1989; 32: 825-828. [ Links ]
163. Jones IT, Fazio VW, Jagelman DG. The use of transanal rectal advancement flaps in the management of fistulas involving the anorectum. Dis Colon Rectum 1987; 30: 919-923. [ Links ]
164. Hesterberg R, Schmidt WU, Muller F, Roher HD. Treatment of anovaginal fistulas with an anocutaneous flap in patients with Crohn´s disease. Int J Colorectal Dis 1993; 8: 51-54. [ Links ]
165. Ozuner G, Hull TL, Cartmill J, Fazio VW. Long-term analysis of the use of transanal rectal advancement flaps for complicated anorectal / vaginal fistulas. Dis Colon Rectum 1996; 39: 10-14. [ Links ]
166. Simmang CL, Lacey SW, Huber PJ Jr. Rectal sleeve advancement: repair of rectovaginal fistula associated with anorectal stricture in Crohn´s disease. Dis Colon Rectum 1998; 41: 787-789. [ Links ]
167. Sher ME, Bauer JJ, Gelernt I. Surgical repair of rectovaginal fistulas in patients with Crohn´s disease: transvaginal approach. Dis Colon Rectum 1991; 34: 641-648. [ Links ]
168. Bauer JJ, Sher ME, Jaffin H, Present D, Gelerent I. Transvaginal approach for repair of rectovaginal fistulae complicating Crohn´s disease. Ann Surg 1991; 213: 151-158. [ Links ]
169. MacRae HM, McLeod RS, Cohen Z, Stern H, Reznick R. Treatment of rectovaginal fistulas that has failed previous repair attempts. Dis Colon Rectum 1995; 38: 921-925. [ Links ]
170. Bodzin JH. Laser ablation of complex perianal fistulas preserves continence and is a rectum-sparing alternative in Crohns disease patients. Am Surg 1998; 64: 627-631; discussion 632. [ Links ]
171. Lindsey I, Smilgin-Humphreys MM, Cunningham C, Mortensen NJ, George BD. A randomized, controlled trial of fibrin glue vs. Conventional treatment for anal fistula. Dis Colon Rectum 2002; 45: 1608-1615. [ Links ]
172. Pogglioli G, Laureti S, Pierangeli F, Rizzello F, Ugolini F, Gionchetti P y col. Local injection of infliximab for the treatment of perianal Crohn´s disease. Dis Colon Rectum 2005; 48: 768-774. [ Links ]
173. Vaughan D, Drumm B. Treatment of fistulas with granulocyte colony-stimulating factor in a patient with Crohns disease. N Engl J Med 1999; 340: 239-240. [ Links ]
174. García-Olmo D, García-Arranz M, García LG, Cuellar ES, Blanco IF, Prianes LA y col. Autologous stem cell transplantation for treatment of rectovaginal fistula in perianal Crohn´s disease: a new cell-based therapy. Int J Colorectal Dis 2003; 18: 451-454. [ Links ]
175. Guillem JG, Roberts PL, Murray JJ, Coller JA, Veidenheimer MC, Schoetz DJ Jr. Factors predictive of persistent or recurrent Crohns disease in excluded rectal segments. Dis Colon Rectum 1992; 35: 768-772. [ Links ]
Miguel Ángel Ciga Lozano
Servicio de Cirugía General y del Aparato Digestivo
Hospital Virgen del Camino
C/ Irunlarrea 4
31008 Pamplona
Tfno. 848 42 95 92 – 848 42 95 02
E-mail: ma.ciga@terra.es
Aceptado: 3 de junio de 2006.