INTRODUCCIÓN
Desde enero de 2020 estamos sufriendo una pandemia mundial que ha provocado más de 2 millones de muertes en todo el mundo. La infección por coronavirus, responsable del síndrome respiratorio grave (SARS-coV-2), ha afectado a casi 100 millones de personas desde entonces. Los casos confirmados se han diagnosticado gracias a diversas pruebas de cribado, en la actualidad el gold standard es el hisopo nasofaríngeo (HN) [1]. Por el momento no se ha informado adecuadamente sobre las posibles complicaciones de este frotis nasal. En este artículo resumimos una complicación de esta prueba como es la fístula traumática de líquido cefalorraquídeo (LCR), así como su tratamiento posterior.
DESCRIPCIÓN DEL CASO
Se presenta el caso de una paciente de 54 años que acudió a consulta de Otorrinolaringología derivada por su médico de cabecera por goteo nasal constante y unilateral izquierdo tras la realización de dos pruebas PCR 2 meses antes. Refería además epistaxis autolimitada posterior a la extracción del exudado nasal. Acudió en dos ocasiones a su médico que pe pautó espray nasal con corticoides por sospecha de rinitis, sin mejoría de la rinorrea. La paciente presentaba además episodios de cefalea moderada intermitente, así como sabor metálico faríngeo. No presentaba antecedentes de traumatismos ni cirugías nasales previas, como único antecedente medico de interés la paciente padecía obesidad. En la exploración ORL mediante nasofibroscopia se apreciaba rinorrea clara en fosa nasal izquierda, sin lesiones aparentes, así como desviación septal izquierda (Vídeo 1. Enlace: https://youtu.be/Dr6jO1oioyE).
En un primer tiempo se realizó un TC de senos paranasales que evidenciaba un defecto posterior en el techo de la fosa nasal izquierda de muy pequeño tamaño (Figuras 1 y 2).

Figura 1. Corte coronal de TC donde se señala (flecha verde) pequeño defecto de la base de cráneo a nivel posterior, en la fosa craneal anterior. Se observa desviación del tabique óseo en la fosa nasal izquierda (fosa afecta).

Figura 2. Corte sagital de TC. Se muestra defecto muy pequeño de base de cráneo a nivel de la lámina cribiforme.
Se tomó muestra del exudado nasal y se solicitó análisis de la proteína B-traza en líquido biológico por nefelometría. El resultado de la presencia de esta proteína en el exudado fue de 27,6 mg/l (valores de referencia 8,89-25,9 mg/L, según nuestro laboratorio), indicando una probable fístula de LCR.
Tras estos hallazgos se propuso cirugía endoscópica nasal para el cierre de fístula de LCR acompañado de septoplastia, con previa administración de fluoresceína intratecal por parte del especialista en anestesiología (Figuras 3 y 4. Vídeo 2, enlace: https://youtu.be/g2be97F8Hqk).
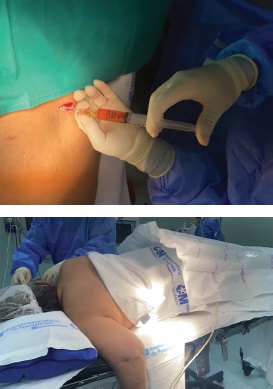
Figura 3. Administración de fluoresceína intratecal por anestesiólogo. Con el paciente sentado o en decúbito lateral en posición fetal se procede a la inyección intratecal o subaracnoidea de la fluoresceína con el paciente despierto. La sustancia para inyectar se obtiene tras añadir 5ml de suero fisiológico a la ampolla de 5ml al 10%, con lo que obtenemos 10 ml de fluoresceína al 5%. De esta disolución cogemos 0,2 cc para introducirlo intratecalmente: se extraen 10 ml de LCR y se mezclan con esos 0,2 cc para a continuación, introducir la mezcla resultante en el espacio subaracnoideo a razón de 1cc por minuto. Tras la inyección de la mezcla se coloca al paciente en decúbito prono con flexión de la cabeza 30º o posición de Flower, que mantendrá entre 30 y 120 minutos. Tiempo necesario para que la fluoresceína penetre en la cavidad intracraneal y posteriormente pueda verse en la fosa nasal.

Figura 4. Localización de fístula de LCR durante el procedimiento quirúrgico (CENS). Se observa salida de fluoresceína a nivel del techo de la fosa nasal, cuyo punto de drenaje nos ayuda a localizar la situación de la fístula. Flecha azul: localización de fístula de LCR señalada.
Se reparó la fístula de LCR mediante técnica multicapa cubriendo el defecto con mucosa nasal de cornete inferior, Surgicel®, Tissucol® (pegamento biológico) y Surgicol®. Al observar que la fluoresceína continuaba siendo visible, se diseñó un colgajo de Hadaad pediculado, se extrajo grasa abdominal y se cubrió la fístula, después se tapó con el colgajo de Hadaad por encima se añadió Surgicel®, Tissucol® y Surgicol® y se verificó la correcta reparación del defecto, frenándose el drenaje de fluoresceína (Vídeo 3, enlace:https://youtu.be/f0ibJOFBG1s).
La paciente estuvo ingresada siete días con una evolución favorable. El tratamiento que recibió durante su estancia fue: amoxicilina clavulánico cómo profilaxis de meningitis, paracetamol y metamizol intravenoso como medicamentos analgésicos, así como laxantes. Como medidas no farmacológicas se le recomendó reposo absoluto. Durante el ingreso presentó una cefalea puntual de 12 horas de duración que precipitó la realización de un TC cerebral a los dos días post quirúrgicos (Figura 5).
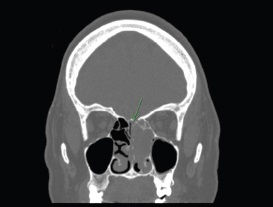
Figura 5. Corte coronal de TC cerebral de la paciente a los dos días posquirúrgicos; Podemos observar cambios secundarios a etmoidectomía izquierda y ocupación por contenido heterogéneo de celdillas etmoidales y fosa nasal izquierda en relación con cambios post quirúrgicos. En el estudio completo no se identifican complicaciones intra ni extracraneales, así como tampoco neumoencéfalo. Al ser un TC realizado en el post operatorio inmediato, aún es posible visualizar el defecto óseo descrito previamente.
El TC seguía mostrando el defecto óseo observado en el TC previo, aunque no se veía neumoencéfalo. Se le realizó una interconsulta al servicio de Neurología, quienes descartaron la hipertensión intracraneal como posible causa de la fístula, viendo más probable el origen traumático de la misma. La rinorrea que refería la paciente antes de la cirugía desapareció y a los siete días fue dada de alta con seguimiento estrecho en nuestras consultas ORL.
Tras cuatro semanas de seguimiento, se realizó un TC craneal de control que mostró una mejor aireación de la fosa nasal izquierda, ausencia de complicaciones intracraneales y reparación del defecto óseo descrito previamente.
DISCUSIÓN
La enfermedad por la COVID-19 ha afectado a millones de personas desde su aparición. En ausencia de tratamientos eficaces o medidas preventivas efectivas para controlar la pandemia, ha sido imprescindible disponer de procedimientos diagnósticos fiables.
El diagnóstico actual de infección aguda por SARS-CoV-2 se basa en pruebas que detectan ARN o antígenos virales [2]. La mayoría de los métodos existentes para las pruebas de la COVID-19 utilizan pruebas de reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR) que detectan secuencias de ácidos nucleicos específicas de SARS-CoV-2.
Estas pruebas son altamente sensibles y específicas cuando se realizan en laboratorios centralizados con protocolos estandarizados, pero requieren una gran cantidad de espacio de laboratorio, equipo complejo, aprobaciones regulatorias para las operaciones del laboratorio y líderes y técnicos de laboratorio capacitados.
Por lo general, los resultados tardan en estar disponibles, con periodos que van de horas a días, y la necesidad de transportar las muestras a un laboratorio central provoca más retrasos. Por esta razón, las pruebas de diagnóstico molecular de baja complejidad y una respuesta rápida tienen ventajas prácticas sustanciales [3].
Este tipo de pruebas que agilizan el diagnostico han recibido la autorización de uso de emergencia (EUA) por parte de la administración de drogas y alimentos(Food and Drug Administration, FDA) [4].
Las pruebas de detección de antígeno funcionan detectando la presencia de proteínas virales y pueden proporcionar resultados rápidos, similar a la forma en que funcionan las pruebas de embarazo [3]. Las pruebas de antígeno pueden ofrecer un rendimiento rápido y escalable, principalmente en atención primaria y servicios de urgencias generales, pero tienen menor sensibilidad que las pruebas que detectan ácidos nucleicos.
La primera semana de julio de 2020, la capacidad diaria de pruebas diagnósticas para la COVID-19 se estimaba entre 520000 y 823000 pruebas. El rendimiento de la prueba (el límite de detección, la sensibilidad, la especificidad y el valor predictivo positivo), el tiempo de respuesta, el costo, la accesibilidad y la aceptación son factores críticos en una estrategia de prueba exitosa que puede satisfacer las necesidades de personas individuales y comunidades en todo el país [5].
La RT-PCR de muestras de las vías respiratorias superiores se considera en la actualidad el gold standard diagnóstico. Esta prueba se obtiene mediante un frotis nasal y orofaríngeo, realizado con un hisopo que se introduce por las narinas siguiendo el suelo de ambas fosas, hasta llegar a la nasofaringe. Aunque el procedimiento de obtención de muestras se considera seguro, en ocasiones la mala colaboración por parte del paciente o la realización de la prueba por personal poco cualificado da lugar a posibles efectos adversos [6].
Algunos efectos adversos descritos en la literatura son epistaxis de gravedad variable, perforaciones septales, ruptura del hisopo y retención en fosa nasal [6,7] e incluso subluxación de la articulación temporomandibular tras la toma de muestra orofaríngea [6]. Aunque son escasas las contraindicaciones para la recogida de muestras nasofaríngeas con hisopo, se debe evitar en pacientes con epistaxis frecuentes por presentar una telangiectasia hemorrágica hereditaria y en pacientes con coagulopatías con antecedentes de sangrados nasales severos previos. Además, debemos tener especial cautela si el paciente presenta antecedentes de traumatismos craneoencefálicos, nasales o una cirugía nasal o craneal reciente. Si el paciente presenta una obstrucción nasal severa, el proceso de recogida de muestra mediante hisopo nasal puede ser complicado, así como peligroso. Las desviaciones septales pueden desplazar el hisopo hacia sitios no deseados como es el caso del techo de la fosa nasal. En niños, la complejidad es mayor debido a la falta de colaboración [8].
La complicación más temida, aunque también infrecuente es la fístula de LCR tras la obtención del frotis nasal con el hisopo [9-12]. La causa de aparición de dicha fístula suele ser la disrupción de la aracnoides y la duramadre, frecuentemente asociada a un defecto óseo [17]. Actualmente en la literatura encontramos pocos casos descritos con fistula de LCR tras PCR, varios de ellos ya presentaban un defecto de la base de cráneo. El primer caso publicado describía un encefalocele previo, observado ya en TC de 2017. Tras introducir el hisopo nasal se produjo la ruptura de dicho encefalocele [10]. En otro caso publicado posteriormente (mayo de 2021) se presenta un paciente de mediana edad que debuta con meningitis tras referir rinorrea unilateral y cefalea días después de la realización de un test PCR con hisopo nasal. Este paciente sufría un meningocele congénito ya conocido [11]. En otros casos reportados no se disponía de TC previo, por lo que se desconoce la preexistencia de lesiones a nivel de la base del cráneo [9,12]. Nuestra paciente no se había realizado ningún TC craneal previo, por lo que desconocemos la existencia de erosión de la base de cráneo a este nivel.
El compromiso traumático del revestimiento dural con fístula de LCR puede aumentar la probabilidad de que un paciente desarrolle meningitis con tasas de mortalidad posteriores del 10% si las infecciones o fístulas no se reconocen. En las fístulas de LCR postraumáticas, especialmente de la base anterior del cráneo, del 10 al 25% de los pacientes desarrollarán meningitis. El tratamiento de estas fístulas de LCR postraumáticas puede variar considerablemente en función de las lesiones intracraneales asociadas, el sitio de la fuga y la extensión del defecto [13].
La reparación de la rinorrea del LCR ha evolucionado drásticamente en los últimos 30 años. Antes de la llegada del abordaje endoscópico, se utilizaba la craneotomía para las reparaciones, lo que conllevaba una tasa de éxito y una morbilidad variables. Más recientemente, se han descrito varias series de casos e informes que explican diversos métodos endoscópicos y materiales para llevar a cabo la reparación de la fístula, con una tasa de éxito media del 90% (rango: 60-100%). El sitio más común de fuga de LCR es la región del techo etmoidal o la placa cribiforme [14]. La fístula traumática de LCR, en particular iatrogénica, sigue siendo la causa más común. La obtención de imágenes con CT y RMN sigue siendo el estándar de oro para la localización de fugas de LCR.
Las fistulas de líquido cefalorraquídeo, pequeñas y de bajo gasto, pueden reconstruirse de manera endoscópica mediante una gran variedad de técnicas. En las que se usan colgajos libres, la tasa de éxito que se logra es mayor de 95% [15]. Sin embargo, cuando se aplican estas técnicas en defectos grandes que implican alto gasto, el resultado continúa siendo poco satisfactorio. Esta situación ha dado lugar a la necesidad de desarrollar colgajos pediculados vascularizados, que promueven una cicatrización rápida y completa. El colgajo nasoseptal pediculado (Hadaad) ha demostrado ser el más efectivo en el control de fistulas de LCR de alto gasto, que los colgajos libres tradicionales (grasa, fascia y músculo) [15]. Sin embargo, el uso de un colgajo para prevenir la fuga de LCR no es suficiente. Esto se debe a que hay muchos factores que pueden precipitar el fallo del cierre; como son la movilización del colgajo cuando encontramos fugas masivas de LCR, la formación de válvulas unidireccionales con el desarrollo posterior de neumoencéfalo relacionados con la presión del aire o la necrosis del colgajo que surge de un daño pedicular accidental. Por estos motivos, la mayoría de los centros utilizan un cierre multicapa en el que, antes de colocar un colgajo autólogo, colocan un parche de colágeno heterólogo (DuraGen®, Duramatrix Onlay®) [16]. También ha demostrado ser útil el TachoSil®, una esponja de colágeno equino recubierto de trombina humana y fibrinógeno que, en contacto con los fluidos, desarrolla una reacción química que permite una fuerte unión entre la esponja de colágeno y la superficie de la herida [16].
La inyección intratecal de fluoresceína es un método que se utiliza en las cirugías de reparación de fistulas de líquido cefalorraquídeo. El procedimiento quirúrgico más frecuente es la endoscopia endonasal y el propósito de la inyección de este colorante es la localización del área de la fístula. La participación en el proceso anestésico y quirúrgico del anestesiólogo (facultativo que habitualmente realiza la punción) hace indispensable la revisión de este método y la puntualización de algunas consideraciones anestésicas. Para este uso médico, el fármaco debe ser preparado por el servicio de Farmacia para asegurar la ausencia de gérmenes y sustancias tóxicas. El primer hecho a tener en cuenta será, por lo tanto, descartar el preparado oftalmológico y escoger el fármaco de concentración y uso adecuados para administración intratecal [17].
Existen diversos protocolos de administración de fluoresceína, coincidiendo en la suma importancia de la administración lenta de la disolución, aproximadamente a velocidad de 1cc por minuto [18]. Además de requerir unas condiciones de asepsia adecuadas, monitorización constante y exploración neurológica posterior del paciente.
CONCLUSIONES
Aunque la prueba de hisopo nasal para diagnóstico de la COVID-19 se considera segura, en ocasiones puede conllevar complicaciones. La aparición de rinorrea clara unilateral o goteo post nasal de sabor salado o metálico tras la realización de un HN nos debe poner en alerta a la hora de diagnosticar una posible fístula de LCR.
Es de suma importancia instruir adecuadamente al personal sanitario que realiza el test, indicando la dirección y orientación correcta del hisopo. Además, se debe informar al paciente sobre los síntomas y signos de alarma.
En pacientes con alteraciones previas de la base del cráneo, distorsión de la anatomía nasal o cirugías previas nasosinusales puede ser recomendable utilizar en ellos otro tipo de pruebas disponibles para diagnosticar la COVID-19.














