INTRODUCCIÓN
La ecografía es una técnica de imagen que no emplea radiaciones ionizantes y no requiere instalaciones específicas. Esta es una de las razones por las que desde hace décadas no es exclusiva de los servicios de Radiodiagnóstico. Especialidades como Cardiología o Ginecología la tienen ampliamente integrada en su práctica diaria.
Además, en los últimos años ha crecido el interés por parte de otras muchas especialidades. Diferentes factores han contribuido a este hecho, por un lado, el abaratamiento de los equipos, cada vez más compactos, por otro lado, el crecimiento de la demanda de exploraciones, que los servicios de radiodiagnóstico tienen dificultades para satisfacer en una coyuntura de escasez de profesionales.
El hecho de que la ecografía sea la técnica de imagen de elección para la valoración de la glándula tiroidea ha despertado el interés de profesionales relacionados como médicos de familia, endocrinólogos y otorrinolaringólogos.
Por nuestro lado, los radiólogos estamos realizando esfuerzos por cubrir la demanda de exploraciones, por ejemplo, mediante el sistema de delegación de exploraciones en técnicos de radiodiagnóstico, un proceso que requiere un esfuerzo de formación y cambio de mentalidad.
Lejos de polemizar sobre quién debe de realizar esta técnica, nuestra opinión es que quién la realice debe de hacerlo en las mejores condiciones para garantizar el resultado óptimo para el paciente.
En nuestro centro, desde hace unos años, hemos ofrecido nuestra colaboración al servicio de ORL en este proceso, con resultados satisfactorios para ambos servicios. Por un lado, los profesionales de ORL han ganado autonomía, y por otro, los radiólogos hemos reforzado nuestro papel como referentes en imagen. Sin duda, es el paciente el mayor beneficiario.
En este artículo, repasaremos los puntos de partida que un especialista no radiólogo debe asimilar antes de enfrentarse a la tarea de integrar la ecografía de tiroides a su práctica diaria.
MATERIAL Y MÉTODO
Hemos realizado una revisión sistemática de tipo narrativo con búsqueda bibliográfica en la base de datos Pubmed. Nos hemos basado asimismo en documentación disponible en la web de sociedades de imagen médica como la Sociedad Española de Ultrasonografía (SEUS) y el American College of Radiology (ACR).
DISCUSIÓN
Trataremos varios puntos esenciales. En primer lugar, describiremos como ha de ser el proceso ecográfico en sentido amplio. Después abordaremos aspectos técnicos básicos que es imprescindible conocer. Finalmente, nos centraremos en la interpretación de las imágenes, para lo cual, explicaremos el estudio sistemático de la glándula y daremos unas pinceladas de la patología tiroidea más frecuente: el nódulo tiroideo bajo la perspectiva del sistema Ti-RADS y la enfermedad tiroidea difusa.
1) El proceso ecográfico
La posibilidad de realizar ecografías comienza necesariamente con la formación y experiencia del ecografista. A lo largo de la residencia de radiodiagnóstico, por ejemplo, el residente realiza innumerables ecografías de todo tipo. El BOE estipula un número mínimo de 500 ecografías solamente durante la rotación de Abdomen de 6 a 9 meses [1].
De igual manera algunas especialidades se plantean incorporar la ecografía en los planes formativos del sistema MIR. Actualmente existen multitud de cursos para especialistas no radiólogos, aunque no existe una vía única de formación acreditada multinivel como ya existe en otros países como el Reino Unido. Será por lo tanto la propia especialidad la que tenga que valorar esta necesidad y su regulación [2,3].
El proceso ecográfico, además, no se limita al acto de realizar la ecografía. Debe de existir un trabajo previo y otro posterior que culmina en la asunción de las consecuencias derivadas de los hallazgos, por partes del paciente y del médico prescriptor.
En abril de 2013 las SEUS publicó el documento «Requisitos de calidad del proceso ecográfico» en el que se describe los puntos esenciales que debe de cumplir el proceso [4]. Si bien el documento ha sido redactado por una asociación radiológica y estemos tentados en afirmar que no se puede aplicar en el ámbito clínico, el proceso no debe de distar significativamente tanto si la ecografía ha sido prescrita por otro especialista y realizada por un radiólogo, como si la ha realizado el clínico por autoderivación.
Destacamos los que son algunos puntos de especial importancia bajo nuestro punto de vista:
Es imprescindible que exista una idoneidad y justificación de la prueba. La indicación médica es el presupuesto inicial de toda prueba de imagen. Responde a las preguntas ¿Por qué lo hago? y ¿Qué espero encontrar?. Es útil disponer de criterios definidos y consensuados de indicación.
Es útil la realización en base a instrucciones escritas con manual de procedimiento y protocolos para determinadas patologías.
La exploración debe de ser registrada y archivada, a ser posible en servidores, preferiblemente en el sistema PACS del hospital (Picture Archiving and Communication System), de tal manera que puedan ser accesibles a otros profesionales, en concreto a los radiólogos, para proceder a comparar y realizar seguimiento de lesiones.
Todas las exploraciones deben de ser informadas, contando con una impresión diagnóstica y decisiones derivadas. La ausencia de este incurre en mala praxis ya que es en este acto donde asumimos nuestra responsabilidad sobre el proceso (Tabla 1) [5,6].
2) Algunos aspectos técnicos básicos
Excede el propósito de esta revisión tratar en profundidad los aspectos técnicos de la ecografía. Es útil, sin embargo, para obtener un mayor rendimiento de la técnica, conocer las bases físicas, estar familiarizado con el dispositivo y saber manipular algunos parámetros.
El elemento principal de un equipo de ultrasonidos es la sonda, que actúa como emisor y receptor de ultrasonidos. De manera muy esquemática e intuitiva la energía sonora del ultrasonido enviado y recogido por la sonda se transforma en una imagen bidimensional que depende de la cantidad de energía recibida y del tiempo transcurrido en este proceso. Tenemos por lo tanto información sobre cómo se comporta el ultrasonido al chocar con una estructura y a qué profundidad se localiza [7].
Existen multitud de sondas en el mercado, de diferentes morfologías y frecuencia de emisión de ultrasonido. Para el estudio del cuello se recomienda emplear una sonda lineal de 10 MHz (7-15 MHz) [7].
La elección de la frecuencia adecuada para cada región es importante, ya que esta frecuencia está directamente relacionada con la resolución de la imagen, pero es inversamente proporcional a la profundidad de visualización. Es decir, a mayor frecuencia, mejor resolución, pero menor penetración [8].
Para obtener una imagen óptima en escala de grises (modo B), es importante tener amplio contacto entre sonda y la piel, eliminando cámaras de aire con ayuda de gel transductor y mantener un ángulo lo más cerca de la perpendicular.
El foco y la ganancia son otros parámetros que podemos manipular para optimizar la imagen.
A la hora de interpretar y describir las imágenes, hablaremos de ecogenicidad. Los términos isoecoico, hiperecoico, hipoecoico o ecogénico son relativos a las estructuras circundantes.
No todo lo que vemos en la pantalla se corresponde con estructuras reales. Las imágenes que no se corresponden con verdaderas estructuras se denominamos artefactos. Aunque generalmente degradan la imagen y nos pueden inducir a error, algunos son útiles para interpretar los hallazgos. Los efectos posteriores, por ejemplo, es decir, lo que pasa por detrás de una estructura, nos ayuda a comprender su composición: si la ecogenicidad aumenta por detrás, se denomina refuerzo y sugiere elevado contenido agua, posiblemente quístico, si por el contrario disminuye, hablaremos de sombra y sugiere, entre otras posibilidades gas o calcificación.
Emplear la técnica Doppler, disponible en muchos equipos, nos ayuda a obtener más información. Someramente, esta técnica detecta la dirección y sentido del movimiento por lo que nos ayuda a detectar vasos permeables y vascularización intraparenquimatosa. Por convención en el modo Doppler Color, en rojo vemos el movimiento hacia el transductor y en azul en dirección opuesta. En el caso del Doppler, debemos de disminuir la frecuencia del pulso para detectar flujo lento y el ángulo óptimo es menor de 60º.
3) Exploración del tiroides por ecografía: Sistemática y patología más frecuente
Las principales indicaciones para realizar una ecografía tiroidea son: Valoración de lesiones focales (diferenciar nódulo tiroideo de otras masas cervicales, confirmar presencia de nódulo tiroideo sospechado en la exploración, caracterizar nódulo y valorar criterios de agresividad), valorar cambios difusos en el parénquima tiroideo, guiar punciones y hacer cribado en pacientes con alto riesgo de neoplasia tiroidea [9].
En primer lugar, comentaremos la exploración sistemática del tiroides mediante ecografía. Abordaremos a continuación el nódulo tiroideo con su manejo, y la enfermedad tiroidea difusa.
A) Sistemática de la exploración
El tiroides es una glándula formada por dos lóbulos unidos por un fino istmo y situada en el espacio visceral del cuello. El lóbulo piramidal es un fino puente de tejido ascendente desde el istmo, presente sólo en algunos pacientes y generalmente no visualizado en ecografía.
El volumen de cada lóbulo puede fácilmente medirse mediante ecografía utilizando la fórmula del elipsoide. Los límites de la normalidad en mujeres son 10-15 ml y en hombres 12-18 ml [9].
Es importante hacer siempre una exploración sistemática de la glándula para no pasar por alto hallazgos relevantes [7-9].
La exploración se realiza en decúbito supino, con hiperextensión del cuello. Una leve rotación lateral nos permite realizar un abordaje más perpendicular de ambos lóbulos.
La exploración comienza con un corte axial de línea media donde valoramos tamaño, simetría y ecoestructura. En este plano medimos también el espesor del istmo. Podemos a continuación medir el volumen de cada lóbulo (Figura 1). Continuamos con barridos ortogonales en los planos axial y longitudinal de los lóbulos en modo B y modo Doppler Color, con el fin de detectar lesiones focales y valorar ecoestructura y vascularización.
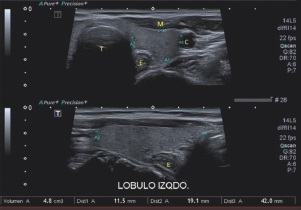
Figura 1. Tres medidas del lóbulo tiroideo izquierdo y cálculo de volumen en tiroides normal. Señalamos las relaciones anatómicas de interés: T: Tráquea. E: Esófago. C: Carótida común. M: musculatura prelaríngea.
Los nódulos deben de medirse cuidadosamente en los tres planos, mediante dos imágenes vinculadas, una axial donde se mide el eje máximo y su perpendicular y otra con la medida en el plano longitudinal. Debemos aportar suficientes imágenes para ilustrar los hallazgos que nos permitan caracterizarlos (bordes, composición, morfología, presencia de calcio...) y localización precisa. Si la lesión tiene halo, los puntos de medida deben de localizarse en el margen externo del mismo, incluyéndolo por lo tanto en la medida [11].
Terminaremos con barridos laterales desde celdas submaxilares a huecos supraclaviculares, y de línea media anterior, con el fin de detectar adenopatías sospechosas u otras lesiones. Las adenopatías también deben de medirse, al menos en su eje menor, y aportar imágenes para su valoración (morfología, ecoestructura, patrón vascular y localización precisa) [12,13].
B) El nódulo tiroideo
La presencia de nódulos tiroideos es muy frecuente, con una incidencia aproximada del 5% de nódulos detectables a la palpación, del 50% en las autopsias [14] y de hasta de 68% en la ecografía [15].
El diagnóstico definitivo de estos nódulos requiere métodos invasivos como la punción-aspiración con aguja fina (PAAF) [16], siendo la inmensa mayoría de los nódulos benignos, con una incidencia de malignidad estimada total del 3-7%, [17-19] y que afecta en estimaciones poblacionales, al 1,6 % de los pacientes con nódulos [20]. De estos nódulos malignos, la gran mayoría son además neoplasias de tipo papilar, con comportamiento indolente [18].
En los últimos años el uso masivo de la ecografía cervical y tiroidea ha elevado significativamente, por un lado, la detección de nódulos, y por otro la incidencia del cáncer de tiroides en pacientes asintomáticos, sin por ello disminuir la mortalidad global por cáncer de tiroides [21]. Estos hechos, constatados en series históricas de Corea y EE. UU., ha supuesto un problema de salud pública y ha llevado a definir los fenómenos denominados como sobrediagnóstico o sobretratamiento (diagnóstico o tratamiento respectivamente de cáncer de tiroides que, de no haber sido detectado o tratado, no hubiera llevado a síntomas ni a la muerte) [15,21,22].
Para tratar de frenar estos fenómenos se han creado diferentes sistemas de estratificación de riesgo que pretenden predecir, en base a las características de imagen de los nódulos por ecografía, la probabilidad de malignidad para así seleccionar únicamente como candidatos a biopsia aquellos más clínicamente significativos.
Múltiples sistemas han sido propuestos en la literatura reciente, generalmente denominados TI-RADS (Thyroid Imaging reporting and Data System): europeo (EU-TIRADS), Coreano (K-TIRADS), de la American Thyroid Association (ATA classification system). Aunque son todos similares y efectivos, nos centraremos en el del Colegio Americano de Radiología (ACR TI-RADS) [15].
Divide la valoración del nódulo tiroideo en la valoración de cinco descriptores, cada uno con varias posibilidades que generan una diferente puntuación: Composición, ecogenicidad, forma, márgenes y presencia de focos ecogénicos. El sumatorio final se sitúa en una categoría TIRADS determinada, desde TIRADS 1 (0 puntos) a TIRADS 5 (7 puntos o más), cada uno resultando en una recomendación que tiene en cuenta además el tamaño del nódulo (Tabla 2, Figuras 2 y 3).
Tabla 2. Descriptores ACR-TIRADS, opciones y puntuación entre paréntesis.
|
Descriptor ACR-TIRADS |
Opciones |
|---|---|
|
Composición |
Quístico o casi (0), Espongiforme (0), Mixto sólido-quístico (1), Sólido o casi (2) |
|
Ecogenicidad |
Anecoico (0), Hiper o isoecoico (1), Hipoecoico (2), Muy hipoecoico (3) |
|
Forma |
Más ancho que alto (0), Más alto que ancho (3) |
|
Márgenes |
Lisos (0), Mal definidos (0), Lobulados o irregulares (2), Extensión extratiroidea (3) |
|
Focos ecogénicos |
Ninguno o con artefacto en cola de cometa (0), Macrocalcificaciones (1), Calcificaciones periféricas (2), Focos ecogénicos puntiformes (3) |
Un nódulo muy ecogénico se define como aquel con ecogenicidad menor o igual a la musculatura prelaríngea. El descriptor Focos ecogénicos es el único que permite elegir simultáneamente varias opciones cuyas puntuaciones se añaden al sumatorio final.
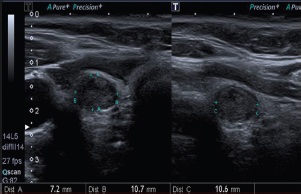
Figura 2. Correcta medición en tres planos de nódulo sólido (2 puntos), hipoecoico (2 puntos), más ancho que alto (0 puntos), de contornos lisos (0 puntos) y sin focos ecogénicos (0 puntos). Puntuación final: 4 puntos, categoría ACR-TIRADS 4. Recomendación ACR en nódulos > 10 mm: Seguimiento.

Figura 3. Nódulo sólido (2 puntos), hipoecoico (2 puntos), más alto que ancho (3 puntos), con contornos irregulares (2 puntos). Puntuación final: 9, categoría ACR-TIRADS 5. Recomendación ACR: Seguimiento. Se decidió biopsiar con resultado: Atipia de significado incierto, Bethesda III.
TIRADS 1 y 2: No PAAF.
TIRADS 3, 4 y 5: Punción si tamaño superior a 2,5 cm, 1,5 cm o 1 cm respectivamente y seguimiento si mayores de 1,5 cm, 1 cm y 0,5 cm respectivamente.
Es destacable el hecho de que la técnica Doppler no está incluida en este sistema, aunque nos puede ser de ayuda para detectar y caracterizar la porción sólida de un nódulo mixto [18].
Esta herramienta nos ha ayudado a sistematizar el manejo del nódulo, así como a comunicarnos mejor entre los diferentes especialistas que intervenimos en su manejo. Después de algunos años de aplicación, está demostrando su eficacia con respecto al manejo previo en dos puntos clave: mejor descripción de nódulos e inclusión de recomendaciones de manejo [23]. Con respecto a otros sistemas, ACR-TIRADS ha demostrado ser además más específico y reducir la tasa de biopsias de entre 19,9 a 46,5% [24]. El seguimiento recomendado permite además rescatar neoplasias significativas inicialmente no biopsiadas.
En el futuro podremos ver modificaciones que mejoren aún su precisión. Nuevos estudios indagan sobre el papel que pudieran tener otras técnicas y aplicaciones, como la ecografía con contraste, la elastografía o la inteligencia artificial [25,26] (Figura 4).

Figura 4. Elastografía con el método Shear-Wave 2D (2D-SWE) de nódulo tiroideo categorizado como TIRADS 3 con elevada rigidez, señalada en rojo en el mapa de color con respecto a la escala lateral, y cuantificada en 117,2kPa. Este hallazgo aumenta la sospecha de malignidad con respecto a nódulos de aspecto similar pero más elásticos.
C) Enfermedad tiroidea difusa
Este grupo de patologías tiene en común un proceso inflamatorio subyacente que va a alterar la ecogenicidad de la glándula y frecuentemente sus contornos, vascularización y tamaño.
La ecografía es por lo tanto una herramienta útil para su valoración por su sensibilidad, aunque es poco específica, con importante solapamiento de los hallazgos, que generalmente deben de interpretarse en función de la clínica [9,10].
Podemos encontrar, además, lesiones focales, como pseudonódulos inflamatorios o verdaderos nódulos como enfermedad concomitante que tendrán que ser valorados específicamente.
Repasaremos las enfermedades difusas más frecuentes y relevantes.
Tiroiditis crónica linfocitaria (Tiroiditis de Hashimoto). Esta enfermedad de origen autoinmune es con diferencia la tiroiditis más frecuente. Se trata de una enfermedad evolutiva en la que en las fases iniciales la presencia de infiltrados linfocitarios se va a traducir en ecografía por áreas parcheadas hipoecoicas milimétricas y aumento de la vascularización. En fases más avanzadas se va a instaurar progresivamente una fibrosis con distorsión arquitectural y pseudonódulos, generalmente hiperecogénicos. Esta enfermedad asocia con mayor frecuencia de neoplasias como carcinoma papilar y linfoma tiroideo, por lo que hay que realizar una valoración minuciosa de cualquier nódulo con características sospechosas. Son frecuentes las adenopatías peritiroideas de carácter reactivo (Figura5).

Figura 5. Tiroiditis autoinmune de Hashimoto. Tiroides de tamaño normal con contornos lobulados, tractos fibrosos (*) y pseudonódulos (+). Áreas hipoecoicas parchedas y confluentes (x).
Enfermedad de Graves. Tiene también un origen autoinmune. En ecografía vemos una glándula aumentada de tamaño con parénquima relativamente homogéneo y escasa fibrosis. Característicamente muestra un aumento de la vascularización en el estudio Doppler denominado Infierno tiroideo.
Tiroiditis granulomatosa subaguda (Tiroiditis de De Quervain): Enfermedad autoinmune y autolimitada, supuestamente desencadenada por infección vírica del tracto respiratorio superior. Cursa con dolor cervical de inicio brusco. En ecografía vemos bocio heterogéno, con áreas parcheadas hipoecoicas e hipovasculares.
Tiroiditis crónica evolucionada. Estadio final e inespecífico de tiroiditis y tratamientos como radioterapia o radioyodo. La glándula muestra característicamente pérdida de volumen, disminución de la vascularización, con contornos lobulados y ecogenicidad difusamente disminuida y grosera.
Enfermedad neoplásica infiltrativa. Algunas neoplasias pueden infiltrar difusamente la glándula, sin nódulos circunscritos, lo que puede hacer que se confunda con otras enfermedades difusas no neoplásicas y dificultar su diagnóstico. Típicamente se comportan de forma agresiva y la anatomía patológica suele corresponderse con linfoma, carcinoma anaplásico o algunas variantes de carcinoma papilar de tiroides. Ante esta sospecha, habrá que valorar realizar PAAF.
CONCLUSIONES
La ecografía es una técnica de imagen actualmente accesible para muchas especialidades. El hecho de ser la técnica de elección en la valoración de la patología tiroidea ha despertado el interés en otorrinolaringología.
Aunque iniciarse en una técnica nueva puede ser arduo, el esfuerzo puede verse recompensado con un manejo más ágil de la patología tiroidea y mayor autonomía del especialista ORL. Como especialistas en imagen, debemos sin embargo señalar la necesidad de realizarlo con rigor y responsabilidad, con correcto archivo de imágenes e informes asociados. Es importante también conocer los límites de la técnica y contar con el respaldo de un servicio de radiología para casos complejos y completar seguimiento de hallazgos.
Cursos y talleres son una buena herramienta para mejorar la curva de aprendizaje, y plantear en el futuro la posibilidad de tener una formación reglada.
La exploración del tiroides ha de ser sistemática y completa. Nos va a permitir detectar patología focal y difusa.
En la valoración del nódulo tiroideo, el sistema TIRADS nos ha permitido sistematizar el manejo y mejorar la comunicación entre especialistas. Los hallazgos de la enfermedad tiroidea difusa por ecografía son frecuentemente inespecíficos y requieren en muchas ocasiones la correlación con la clínica.














