Introducción
La prevalencia de la obstrucción intestinal maligna (OIM) en el mundo varía entre el 3 y el 15%, dependiendo de las series revisadas. Entre el 5 y el 51% se presentan en pacientes con tumores de ovario, y del 10-28%, en pacientes con tumores gastrointestinales. Otros tumores relacionados incluyen: gástrico (6-19%), de páncreas (6-13%), de vejiga (3-10%) y de endometrio (3-11%). El tiempo medio entre el diagnóstico del cáncer y la obstrucción intestinal maligna es de 14 meses, pero puede ser la primera manifestación de la enfermedad tumoral en el 2% de los casos, y hasta en el 22%, en series quirúrgicas. Esta enfermedad compromete el intestino delgado en el 61% de los casos; el intestino grueso, en el 33%, y en el 20%, ambos sitios, simultáneamente. Pueden observarse múltiples niveles de obstrucción hasta en el 80% de los casos1-3. Los criterios de OIM se basan en el compromiso intestinal debajo del ángulo de Treitz, asociado a neoplasia maligna y sin evidencia de curación4.
La falta de estudios contundentes que sirvan para el desarrollo de protocolos concretos para el abordaje de esta entidad hace que la obstrucción intestinal se maneje empíricamente, existiendo marcadas variaciones en la práctica clínica5. En este sentido, resulta complicado hacer estudios de buena calidad en este tipo de pacientes, dada la dificultad de un reclutamiento adecuado, una esperanza de vida corta y las dificultades éticas para el uso de grupos control. Además, la escasa respuesta a los tratamientos utilizados sumado al mal pronóstico, con un rápido deterioro del estado general, son factores que hacen de esta patología uno de los mayores retos para los servicios de cuidados paliativos, con un alto impacto sobre la calidad de vida del paciente y sus cuidadores(1-3, 6).
La OIM se trata de una patología compleja, que produce un alto grado de disconfort, debido a los síntomas ocasionados por las alteraciones mecánicas y funcionales a través de distintos mecanismos fisiopatológicos y que puede responder peor a las medidas convencionales de reposo intestinal, descompresión nasogástrica y líquidos intravenosos7-9. Entre estos mecanismos se encuentran la oclusión del lumen intestinal, las alteraciones en la motilidad y la acumulación de secreciones. Estos mecanismos propuestos confirman la hipótesis de que una combinación de agentes propulsores, antiinflamatorios y antisecreceptores deberían producir mejorías clínicas en los pacientes con OIM10. Esta combinación es conocida por los médicos de cuidados paliativos y puede resolver la obstrucción y los síntomas asociados. Medicamentos como la octreotide, que puede reducir la hiperemia, las secreciones intestinales y la presión intraluminal; la dexametasona dirigida a la reducción del edema de la pared intestinal; y la motilidad gastrointestinal que promueve la metoclopramida son ampliamente usados7-9. Además, el amidotrizoato, medio de contraste hiperosmolar soluble en agua, diluye el contenido intestinal, disminuyendo el edema de pared, lo cual, a su vez, facilita el tránsito intestinal3. En un metaanálisis con 15 estudios, Mercadante et al, evaluaron la eficacia del uso de octreotide en comparación con escopolamina butilbromuro. Los autores hallaron tasas de respuesta total de entre el 60-90%, así como una mayor y más rápida eficacia con el uso de octreotide, al igual que una disminución en el uso de drenaje por sonda nasogástrica (SNG) e, incluso, en diferir su utilización6,8.
Este tratamiento farmacológico, aplicado de forma temprana e intensiva, ha demostrado ser eficaz no sólo para controlar los síntomas gastrointestinales en pacientes inoperables sino también para revertir la obstrucción intestinal maligna, lo que permite una clara mejoría tanto en la calidad de vida como en la supervivencia de estos pacientes7,10. Aunque tales medicamentos se han utilizado con cierto éxito para paliar los síntomas, existen datos clínicos limitados sobre la efectividad de estos agentes, particularmente en combinación. En la Tabla 1 resumen se presenta el manejo farmacológico detallado en una revisión de la literatura3.
Tabla 1: Manejo farmacológico de la obstrucción intestinal maligna
| Principales manifestaciones OIM y su tratamiento | |
|---|---|
| Dolor nociceptivo somático continuo | Uso de analgésicos opioides potentes en dosis tituladas |
| Dolor visceral cólico | Butilbromuro de escopolamina 20-40 mg cada 8 horas (100mg dosis máxima) |
| Aumento de secreciones gastrointestinales | Butilbromuro de escopolamina 20-40 mg cada 8 horas (100mg dosis máxima) Octreotida 100-300 µg cada 8horas |
| Náuseas y vómito | Haloperidol 5-15mg /día Metoclopramida 40-240 mg/día Ondansetrón 12-24 mg/día Olanzapina 2,5-20 mg/día |
| Actividad inflamatoria local | Dexametasona 6-16 mg/día |
Desarrollo de la experiència
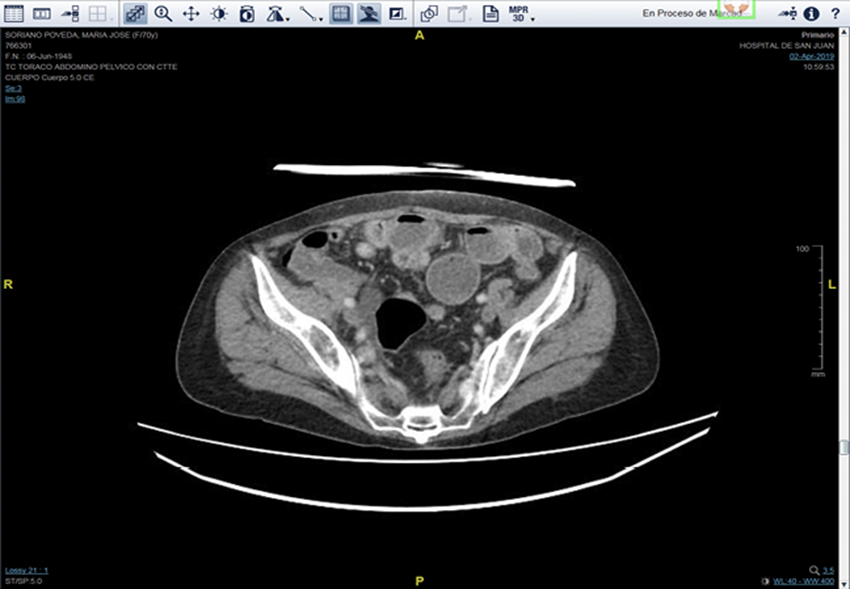
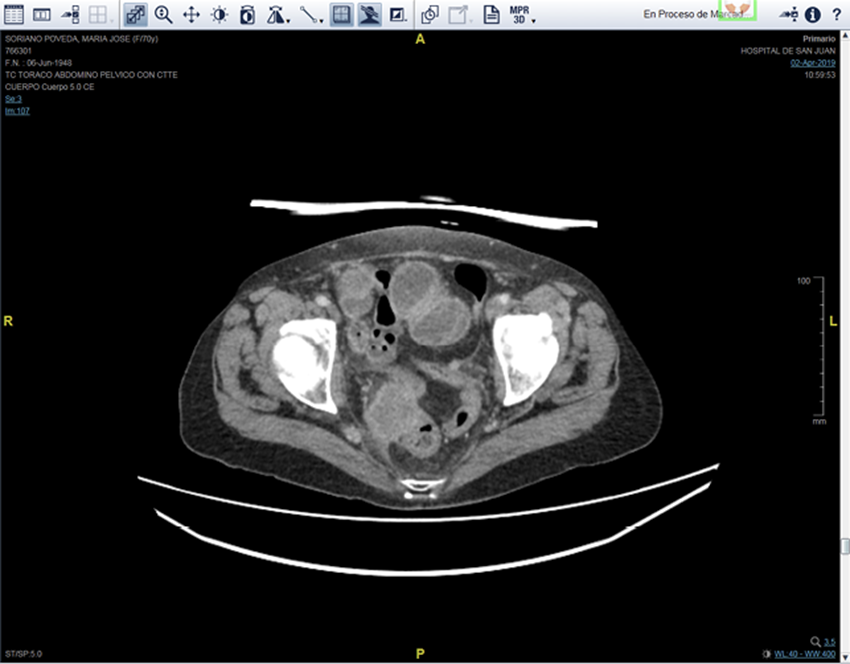
Informamos sobre un caso clínico de un paciente de 70 años, con antecedentes de adenocarcinoma de colon derecho, diagnosticado en junio de 2014, que precisó de hemicolectomia derecha. Actualmente con progresión de enfermedad por metástasis pulmonares y peritoneales de nueva aparición. Es remitido por el servicio de Oncología Médica a la Unidad de Hospitalización a Domicilio de San Juan de Alicante para tratamiento en fase paliativa terminal. El paciente presenta cuadro de oclusión de intestino delgado debido a implante mesentérico en cuadrante inferior derecho, que fue tratado con perfusión de 4 mg de dexametasona y 30 mg de metoclopramida (Figura 1 y Figura 2).
Por persistencia de sintomatología clínica de la OIM se decide iniciar en nuestra unidad perfusión de 1000cc SF a los que añadimos 12 mg de ondasetron, 60 mg de butilbromuro de escopolamina, 30 mg de metoclorpamida y 50 microgramos de octreotide subcutánea a pasar en 24 horas. Se le añaden 500ml de suero glucosado y 12 mg dexametasona por el reservorio. Además de 40 pantoprazol intravenoso.
A la valoración del día siguiente el paciente comienza a presentar aparición de ruidos hidroaéreos con expulsión de gases, manteniendo ingesta adecuada de líquidos. Sin nauseas y con una pequeña deposición. El paciente refiere además control adecuado del dolor con parches de fentanilo transdérmico. Al tercer día, se obtienen deposiciones suficientes, disminuyendo la distensión abdominal y el timpanismo a la exploración. Manteniendo dicha mejoría clínica durante 20 días.
A la tercera semana de comienzo de la perfusión, el paciente presenta empeoramiento clínico, con sensación nauseosa y vómitos fecaloides. Ante deterioro clínico y mínima respuesta al tratamiento agresivo de la oclusión intestinal, y dada la situación irreversible, se comenta dicho escenario con el paciente y los familiares, quien, de consenso tras entender y asumir etapa final de la vida, están conformes con adecuar el esfuerzo terapéutico y no colocar SNG. Al vigésimo tercer día de comenzar con la perfusión combinada de medicamentos, se acuerda con paciente y familiares iniciar sedación reglada añadiendo Midazolam 25 mg/día consiguiendo que el paciente quede dormido y en ausencia a estímulos (nivel 6 escala de sedación de Ramsay a las 6 horas) que se mantiene hasta el exitus del paciente en domicilio al vigésimo quinto día de iniciada la perfusión.
Discusión
Controlar los síntomas y mejorar la calidad de vida son objetivos fundamentales de los cuidados paliativos. En el presente caso, la estrategia de tratamiento utilizada demostró ser altamente efectiva en un paciente con OIM inoperable, no sólo para reducir los síntomas gastrointestinales, es decir, los vómitos, sino también para prolongar el tiempo medio de supervivencia. Siendo en nuestro caso de 25 días desde iniciada la perfusión.
Este caso sugiere que la combinación de agentes propulsores y antisecretivos puede actuar sinérgicamente favoreciendo una rápida recuperación del tránsito intestinal sin inducir cólicos desagradables y mejorando la sintomatología del paciente. Este hecho se justificaría en que el mecanismo más importante de la OIM, en este contexto, es funcional y puede ser reversible incluso en pacientes con cáncer avanzado, si se inicia un tratamiento agresivo temprano antes de que la impactación fecal y el edema hagan irreversible la OIM.