INTRODUCCIÓN
El cuerpo o corpúsculo carotídeo es una pequeña estructura (2-5 mm de tamaño y 5-20 mg de peso) situado en la cara posterior de la bifurcación carotídea (en su adventicia). Inervado por el nervio glosofaríngeo e irrigado por vasos dependientes de la carótida externa, es un receptor químico que detecta los cambios sanguíneos del pCO2, pO2 y pH para regular así la ventilación, la frecuencia cardiaca y la presión arterial (su estimulación induce taquipnea, taquicardia e hipertensión arterial). Para evitar confusión recordamos que el seno carotídeo es un receptor de presión arterial cuya estimulación provoca bradicardia e hipotensión.
Los tumores que se asientan sobre el cuerpo carotídeo son muy poco frecuentes y existen controversias respecto a su terminología, etiología, historia natural (comportamiento biológico) y otras de interés más práctico, como su diagnóstico y tratamiento.
Estos tumores se han denominado de diversas maneras según su localización (tumor del cuerpo o corpúsculo carotídeo o glomo carotídeo), embriología (paragangliomas carotídeos, paragangliomas no cromafines o no funcionales) y función (quemo- o quimidectomas carotídeos). El término paraganglioma carotídeo (PGC) es el más aceptado en la actualidad.
La cirugía (resección del tumor) es el tratamiento de elección de los PGC.
RECUERDO HISTÓRICO
La primera resección de un PGC se atribuye a Riegner en 1880, cuando todavía no se habían caracterizado bien estos tumores. El paciente no sobrevivió. Sí lo hizo el paciente intervenido por Mayld (1886), aunque presentó una hemiplejía y una afasia. Un paciente fue operado sin secuelas por Albert en 1889. En 1937 Lubbers describió la realidad de esta época: cita a un paciente de 58 años que fallece cuatro días después de la cirugía por un sangrado excesivo y al que se le llegó a ligar la carótida común.
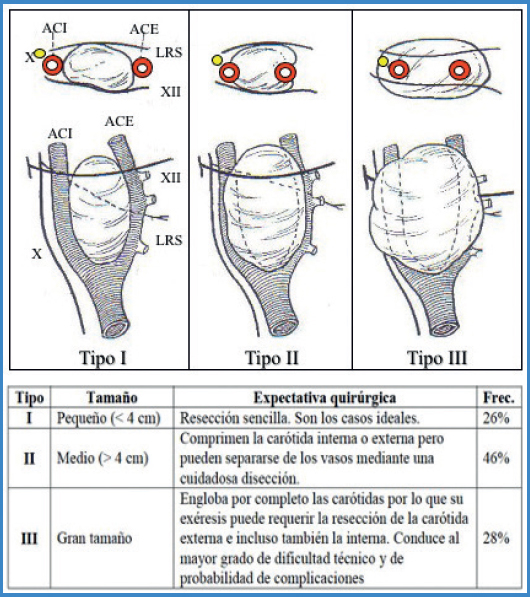
Para tratar estos tumores en 1953 Morfit incluyó las técnicas de reconstrucción arterial. La década de los setenta del siglo xx fue especialmente útil para el diagnóstico y el tratamiento de los PGC. En este sentido, la TC comenzó a aportar información fundamental para la cirugía. En 1971 Shamblin propuso una clasificación de interés quirúrgico que, con modificaciones, permanece vigente (1) (Fig. 1). En 1973 Hekster introdujo la técnica de embolización preoperatoria mediante abordaje transfemoral hasta la carótida externa, que demuestra su utilidad en disminuir el sangrado durante la cirugía, con lo que mejoran las posibilidades de resección de estos tumores.
Más recientemente los estudios genéticos y otras investigaciones han profundizado en el conocimiento de los paragangliomas. En 2002 Al-Mefty y Teixeira introdujeron el término paragangliomas complex ante la presencia de tumores gigantes, bilaterales, múltiples, malignos, secretores, asociados a otras enfermedades, tratamiento previo con mal resultado, tratamiento con radioterapia o efectos adversos con la embolización.
ASPECTOS DE INTERÉS
Mientras en la década de los setenta del siglo xx las publicaciones decían que “muchos cirujanos vasculares no tendrán la oportunidad de tratar un PGC en toda su vida profesional”, en la actualidad las cosas han cambiado al constatarse una mayor incidencia real o aparente (mayor diagnóstico) de PGC. Por ello podemos afirmar que muchos cirujanos vasculares tendrán la oportunidad durante su vida profesional de diagnosticar y tratar al menos 1 o 2 casos cada 5-10 años.
Posiblemente la baja frecuencia de los PGC explica que en la mayoría de los Atlas of Vascular Surgery and Endovascular Therapy. Anatomy and Technique no traten el tema que nos ocupa, por lo que se hace pertinente este artículo.
Unos consejos iniciales para aquellos con escasa experiencia en esta patología:
Individualizar las indicaciones quirúrgicas mediante algoritmos (teniendo en cuenta diversos factores) y adaptarlos a cada medio (2).
Hay que recordar que los PGC son tumores muy vascularizados que, aunque delimitados, no están encapsulados, poseen un lento crecimiento y habitualmente son benignos, únicos y no funcionantes. En estas situaciones, la resección de un PGC para un cirujano con cierta experiencia suele ser relativamente sencilla y conlleva muy buenos resultados.
No obstante, en algunas ocasiones estos tumores invaden la adventicia, e incluso la media, de las arterias carótidas. En estas circunstancias se precisan técnicas de reconstrucción vascular (actualmente, alrededor del 12 % de los casos).
Junto a estos casos irresecables existen paragangliomas gigantes, bilaterales, multicéntricos, secretores, etc. En todos estos casos los resultados quirúrgicos (fundamentalmente por morbilidad neurológica [pares craneales]) son bien diferentes y exigen un mayor rigor en la indicación y una mayor experiencia quirúrgica.
En la cirugía de los PGC, máxime en casos complex, es importante el conocimiento anatómico de la zona quirúrgica. En nuestra opinión, los cirujanos de cabeza y cuello (en nuestro centro, los otorrinolaringólogos) son excelentes colaboradores o viceversa (lo somos nosotros de ellos en la reparación vascular) en casos complejos (3).
CÓMO LO HAGO (HOW I DO IT)
Hace años, a petición del editor de una monografía sobre los paragangliomas cervicocefálicos, escribimos un capítulo sobre el “Tratamiento quirúrgico de los paragangliomas carotídeos” (4). En ese artículo se revisaba ampliamente el estado actual del tratamiento quirúrgico de los PGC. Las indicaciones quirúrgicas y los aspectos preoperatorios (clasificación de Shamblin, valor del estudio genético, el consentimiento informado, la utilidad de la embolización, etc.) iniciaban la revisión. Los aspectos intraoperatorios (equipo quirúrgico) y de técnica quirúrgica (posición del paciente, incisión y exposición, control de los vasos e identificación de los nervios, la extirpación del tumor de manera subadventicial o periadventicial, la necesidad de resección arterial y su reconstrucción, etc.) se trataban en profundidad. Los aspectos posoperatorios, los resultados de morbilidad (neurológica y vascular) y mortalidad, junto al seguimiento de estos pacientes, finalizaban la primera parte del artículo. Una segunda parte se dedicaba a situaciones especiales: PGC no resecables, malignos, residuales (persistentes) o recurrentes, bilaterales, múltiples y patologías asociadas, en niños, etc.
Seguimos estando de acuerdo con la gran mayoría de lo entonces allí redactado y en este momento pretendemos aportar una visión más personal (y práctica), ya que hemos tratado más de medio centenar de pacientes durante más de tres décadas en el Hospital Universitario de Salamanca (3,5).
Aspectos preoperatorios
Una vez realizados los preceptivos estudios diagnósticos y preoperatorios de un PGC (que no incluyen las mismas pruebas, aunque muchas de ellas sean válidas para ambos objetivos), las siguientes fases son la de la indicación quirúrgica (la entrevista con el paciente y su familia es muy importante) y la posterior planificación táctica y técnica anestesicoquirúrgica. En este sentido, desde hace años solicitamos sistemáticamente estudios genéticos a todos nuestros pacientes, y en las formas familiares solemos conocer los resultados antes de la cirugía. Aunque nunca hemos encontrado un PGC funcionante, es obligado sistematizar su investigación dentro del protocolo preoperatorio.
Momentos antes de la intervención nos gusta recordar fundamentalmente el angio TC, realizado en diversas proyecciones y con reconstrucciones 3D, que para nosotros es la prueba de imagen que aporta la información más valiosa sobre la anatomía de la tumoración (fundamentalmente su extensión craneal) y sus relaciones con las estructuras adyacentes (yugular interna, nervio vago, arteria carótida, etc.). En nuestra opinión la gradación Shamblin debe tenerse en cuenta, pero la creemos relativa, pues en la práctica hemos encontrado grados III relativamente fáciles de resecar, y por el contrario, grados II que infiltran y no pueden resecarse sin sacrificar el eje carotídeo en algún sector.
No somos partidarios de la prueba de tolerancia a la oclusión de la carótida interna y nunca la hemos practicado. Respecto a la embolización preoperatoria, actualmente solo la indicamos en tumores mayores de 4 cm (en los que puede ser más beneficiosa), la cual se practica exactamente 48 horas antes de la cirugía. Con estas pautas selectivas la embolización preoperatoria no es para nosotros un tema controvertido.
Aspectos intraoperatorios
Como ya hemos señalado, en ciertos casos es útil operar con compañeros experimentados de otras especialidades, ya que aporta seguridad y buena práctica quirúrgica. Puede ser necesaria incluso la intervención adicional de un cirujano maxilofacial en los excepcionales casos en los que se precise luxar la articulación temporomandibular para ampliar el campo operatorio (en nuestra experiencia únicamente en un caso).
Siempre hemos practicado la cirugía mediante anestesia general con intubación orotraqueal (nasotraqueal si se sospechara la necesidad de luxar la mandíbula). En nuestros primeros casos, inyectábamos a modo profiláctico lidocaína o novocaína en las proximidades del seno carotídeo. Actualmente es el anestesista quien controla farmacológicamente esta eventualidad. La vigilancia continua de la perfusión cerebral es otro aspecto destacable, que realizamos mediante un INVOS™ 5100C (oxímetro cerebral/somático).
Técnica quirúrgica
Inicialmente debemos resaltar que el objetivo de la cirugía es la extirpación íntegra del PGC preservando el sistema carotídeo y los nervios adyacentes, con la menor pérdida de sangre y dejando una cicatriz lo más cosmética posible. Esto requiere cierta experiencia (identificar nervios, controlar vasos, realizar una correcta disección o, si es preciso, insertar un shunt y reemplazar un segmento arterial por un injerto o una prótesis). A diferencia de la endarterectomía carotídea (EC), en esta patología (probablemente debido a su baja frecuencia) no existen datos sobre el volumen de cirugía/resultados, aunque es lógico pensar que estos sean también cirujano-dependientes. Con esto queremos expresar que aquellos cirujanos que practican frecuentemente EC mostrarán una mayor habilidad a la hora de practicar la resección de un PGC con éxito, pero también debemos señalar que los campos operatorios no son exactamente similares.
La cirugía de los PGC consiste, la mayoría de las veces, en la resección de la lesión sin afectar para nada a la vascularización carotídea (habitualmente casos Shamblin de tipo I y II). Sin embargo, cuando existe un tumor grande que envuelve totalmente los vasos e incluso los infiltra (habitualmente casos Shamblin III, pero no exclusivamente), puede ser imposible la extirpación de la tumoración sin resecar parte de las arterias carótidas, lo que obliga a su reparación posterior (sutura, plastia, interposición venosa o protésica).
Como en toda cirugía del cuello, posicionamos y colocamos personalmente al paciente (decúbito supino con el cuello rotado e hiperextendido). Preparamos un campo amplio. La pierna ipsilateral también debe prepararse si pensamos en la obtención de un segmento de safena interna.
Realizamos una incisión cervical oblicua a nivel del borde anterior del músculo esternocleidomastoideo (algo más extensa que para practicar un EC), evitando en lo posible lesionar las ramas del nervio auricular mayor (Fig. 2). Para esta cirugía no es aconsejable la cervicotomía transversa. Realizada la incisión cutánea, se divide el músculo platisma (en ocasiones es necesario ligar y dividir la vena yugular anterior) e identificamos la vena yugular interna, en ocasiones oculta por la tumoración. Después de ligar-seccionar la vena facial, se lateraliza la vena yugular interna y se accede al plano carotídeo. Aparece entonces el tumor firmemente adherido y aparentemente encapsulado, que, según el grado Shamblin, deja ver más o menos la bifurcación carotídea y las arterias carótidas interna y externa.
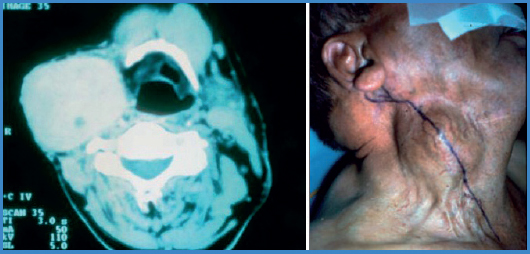
Figura 2. Caso personal nº 5. Paraganglioma carotídeo unilateral gigante (7 cm de diámetro transversal) extirpado a través de una cervicotomía estándar. Con permiso de: Lozano y Muñoz en: Acta Otorrinolaringol Esp 2009;60(Supl.1):80-96.
En accesos distales (para controlar la carótida interna) puede dividirse el vientre posterior del músculo digástrico e incluso el músculo estilomastoideo y movilizar la parótida. En una sola ocasión hemos practicado la subluxación anterior de la mandíbula y una mandibulotomía para obtener mayor exposición distal. La adopción de estas actuaciones tiene sus inconvenientes y en cualquier caso es preciso saber que existen tumores de tal magnitud que pueden considerarse inoperables.
Una vez realizado el acceso lo primero es identificar la carótida común (2 cm por debajo del tumor), que controlamos con cintas de Silastic™ (vessel loops). La carótida interna y la externa distal se tratan de la misma manera. Hay que ser consciente de que no siempre es fácil realizar un control arterial distal al inicio de la intervención, pero ello no debe preocuparnos, pues con el trascurso de la cirugía llegaremos a su control.
Los nervios vago e hipogloso los identificamos sistemáticamente, y si es necesario, los separamos del tumor con vessel loops. El asa del hipogloso puede seccionarse si facilita la disección. Dependiendo del tamaño del tumor puede ser necesario identificar otros nervios: laríngeo superior, espinal accesorio, glosofaríngeo, etc. Muchos de ellos solo se visualizan cuando evoluciona la movilización-exéresis del tumor. Es en esta situación en la que la experiencia anatómica cobra gran valor (Fig. 3).
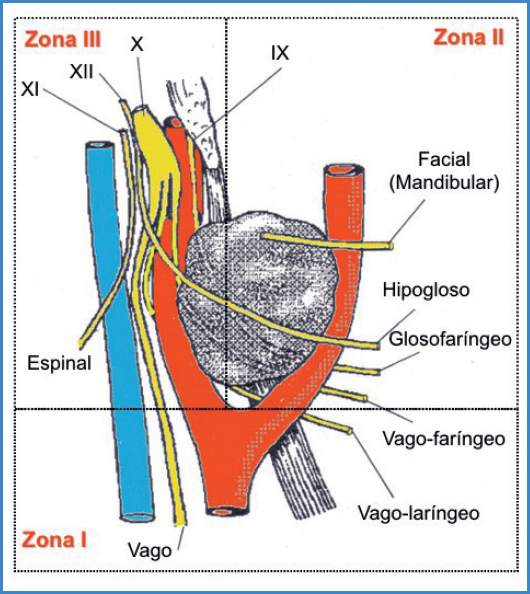
Figura 3. Zonas quirúrgicas. La mayor complejidad es propia de la zona III. Con permiso de: Lozano y Muñoz en: Acta Otorrinolaringol Esp 2009;60(Supl.1):80-96.
Llegados a este punto comenzamos con la resección del PGC. Es bien conocido cómo Gordon-Taylor, en 1940, observó la presencia de un plano de disección subadventicial relativamente hemostático que denominó línea blanca. Fue un gran avance en su tiempo, ya que permitió extirpar el PGC preservando las arterias carótidas. Frente a ello, cirujanos de la Clínica Mayo se inclinaron por una disección periadventicial y alegan a su favor una menor tasa de lesiones arteriales durante la intervención. Para nosotros, la elección viene determinada por la complejidad del caso durante la cirugía y procuramos mantenernos en un plano de disección relativamente cómodo (avascular), peri- o subadventicial. Nunca hemos perforado la pared arterial (Fig. 4).
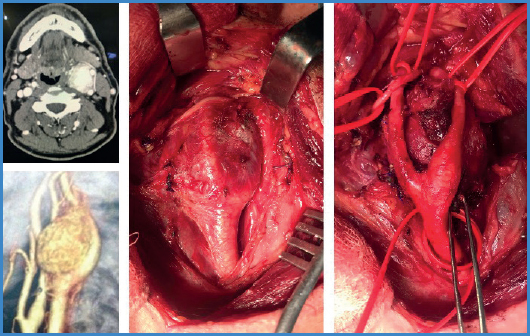
Figura 4. Caso personal nº 51. TC (imagen coronal y reconstrucción 3D en color). Imagen intraoperatoria antes y después de la resección del paraganglioma carotídeo.
Realizamos esta fase de la cirugía con ayuda de lupas de magnificación (× 2,5). Comenzamos con la disección de la cara anterior de la arteria carótida común y desde allí progresamos longitudinalmente hacia arriba para buscar primero la carótida externa y después, la carótida interna. Con tijeras, con disectores de Mayo y bisturí eléctrico bipolar vamos avanzando poco a poco (haciendo hemostasia) para abrir toda la cara anterior como si fuera un libro y dejamos para un segundo momento la cara posterior. Las ramas de la arteria carótida externa pueden ligarse y dividirse si esto facilita la movilización del tumor a la vez que disminuye la vascularización del PGC.
La disección progresa más tarde de forma posteromedial (collar del tumor). Debemos prestar especial atención al separar el tumor de la cara posterior de la bifurcación carotídea debido a la posible hemorragia al desprender la tumoración de la zona originaria del corpúsculo o glomo. Esta fase, por una mayor adherencia, muchas veces debe hacerse a punta de tijera.
Aunque un experto grupo holandés propone (por una menor morbilidad neurológica de su serie) una exéresis cráneo-caudal (de la base del cráneo hacía carótida común) en lugar de la estándar (de carótida común hacia arriba), nosotros seguimos la técnica convencional, pero no tenemos inconveniente en modificarla según las circunstancias.
Regularmente irrigamos el campo con suero salino para evitar la desecación de las estructuras. Para evitar el espasmo arterial aplicamos localmente papaverina (gasa empapada en dicha sustancia). Nunca hemos usado el autotransfusor (aunque nuestro hospital dispone de uno).
Una vez extirpada la tumoración es importante reconfirmar la anatomía. Comprobamos el latido distal de la carótida interna, la integridad de la yugular interna y de los nervios referidos (hipogloso, vago, etc.).
Antes del cierre de la herida operatoria realizamos una hemostasia cuidadosa. De forma rutinaria dejamos un drenaje aspirativo que mantenemos al menos 24 horas. Se cierra la pared en dos planos (fascia y subcutáneo) con Vicryl® 2-0 y colocamos un apósito simple.