INTRODUCCIÓN
La desnutrición aparece con frecuencia en los pacientes con cáncer debido a su proceso oncológico y a los tratamientos recibidos, como la cirugía, la radioterapia o la quimioterapia (1). Esta desnutrición se asocia a un exceso de morbilidad y mortalidad (2), mayor riesgo de complicaciones (3), prolongación de la estancia en el hospital (4), peores respuestas a los tratamientos coadyuvantes previamente mencionados (4) y disminución en la calidad de vida (QoL) (5).
Los pacientes oncológicos tienen, por tanto, un mayor riesgo de desarrollar caquexia, con empeoramiento de todos los parámetros previamente mencionados (6). La pérdida de peso es un componente de este síndrome, con gran degradación de las proteínas musculares, inflamación sistémica, incremento de la resistencia a la insulina y anorexia (7-9). En este contexto, los efectos inmunomoduladores y antiinflamatorios de los ácidos poliinsaturados de cadena larga (PUFA) están bien descritos (10). Los PUFA ω-3 y ω-6 juegan un papel importante en la regulación inmunológica, y el equilibrio entre ellos puede afectar la severidad de las enfermedades inflamatorias (11). Los PUFA son precursores de la producción de diferentes series de eicosanoides (12), entre las que la prostaglandina E2 (PGE2) (13) es un metabolito principal. La PGE2 tiene propiedades proinflamatorias y puede producir diferentes efectores inmunológicos (14). Sin embargo, los eicosanoides derivados de los PUFA ω-3 difieren en estructura y función, y generalmente se consideran menos inflamatorios que los eicosanoides derivados de los PUFA ω-6 (15).
En algunos trabajos en pacientes oncológicos, el asesoramiento nutricional ha demostrado mejorar significativamente la ingesta de energía y de proteínas, y también la puntuación de calidad de vida (16), en este caso en pacientes con cáncer de colon en radioterapia. Las guías de la European Society of Parenteral and Enteral Nutrition (ESPEN) (17,18) recomiendan el uso de fórmulas inmunomoduladoras en los pacientes oncológicos. No obstante, estas guías (18), en los pacientes oncológicos, recomiendan de forma débil y con un nivel de evidencia bajo el empleo de los ácidos grasos omega-3 de cadena larga parar mejorar el apetito y el peso corporal, y sugieren su empleo en los pacientes con cáncer avanzado sometidos a quimioterapia y con riesgo de presentar pérdida de peso o desnutrición con el fin de estabilizar o mejorar el apetito, la ingesta alimentaria, la masa magra y el peso corporal. El uso en pacientes oncológicos sin un tratamiento activo no está claro y es un área de interés donde evaluar resultados. Por otra parte, aunque los suplementos orales nutricionales (SON) se han mostrado útiles en la práctica clínica habitual (19), son escasos los estudios que evalúan específicamente el papel de los suplementos orales nutricionales (SON) con PUFA ω-3 a nivel ambulatorio, siendo este otro grupo de pacientes en los que es necesario evaluar al menos su efectividad (20-22). Además, no existen en la literatura estudios con pacientes oncológicos ambulatorios que utilicen la herramienta EuroQol-5D (EQ5D) (20) para evaluar el impacto de los SON enriquecidos con ω-3 sobre la calidad de vida.
El objetivo de nuestro estudio fue evaluar, en un estudio en condiciones de vida real (EVR), la efectividad sobre los parámetros nutricionales y la calidad de vida de un SON enriquecido con ω-3 en pacientes ambulatorios oncológicos.
MATERIAL Y MÉTODOS
SUJETOS
Los datos se recogieron de manera prospectiva y el estudio se realizó en un solo hospital con pacientes oncológicos ambulatorios durante 12 semanas, sin tratamientos coadyuvantes activos durante ese tiempo (quimioterapia/radioterapia/cirugía). Se incluyeron 35 pacientes oncológicos con riesgo nutricional intermedio o alto. Antes de recoger todos los datos clínicos, bioquímicos y de calidad de vida de los pacientes, se comprobaron los criterios de inclusión y se descartó la presencia de criterios de exclusión. Se incluyeron pacientes de ambos sexos de entre 30 y 70 años de edad, con riesgo nutricional intermedio o alto, determinado por el test Malnutrition Universal Screening Tool (MUST). Además era necesario que el sujeto aceptara participar en el estudio y leyera y firmara el consentimiento informado. Se excluyeron los pacientes con contraindicación formal de nutrición oral, los pacientes con expectativa de vida inferior a los 6 meses, los pacientes que tuvieran indicación de terapia coadyuvante (quimioterapia/radioterapia/cirugía) durante los 3 meses del estudio y aquellos con cualquier afección psicológica que pudiera interferir con el consumo de los productos del estudio, con alergia o intolerancia a alguno de los ingredientes de la fórmula, y con cualquier otra patología o condición no especificada que el investigador considerara capaz de interferir con la evaluación de la fórmula o de poner en riesgo innecesario al paciente. El estudio fue aprobado por el Comité de Ensayos Clínicos del HCUV (pi17-491) y los pacientes firmaron un consentimiento informado antes de iniciar el protocolo del estudio.
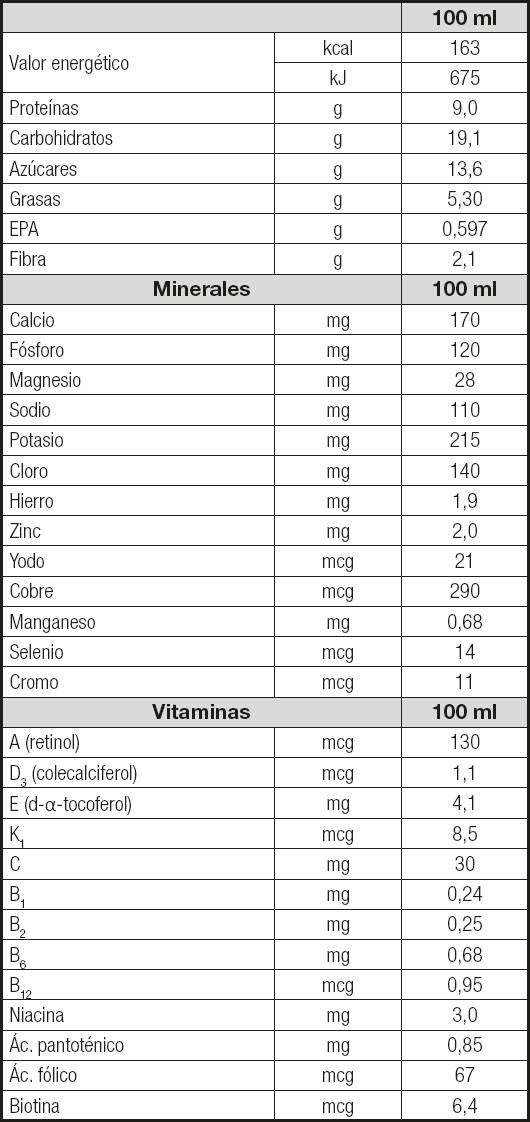
A todos los pacientes se les administraron, de manera ambulatoria, 2 envases al día de Forticare® (Nutricia Danone, Madrid, España). En la tabla I se muestra la composición de este SON (125 ml), en formato listo para consumir, que contiene 1,6 kcal/ml. Las proteínas de este SON son en un 30 % del suero con un 70 % de caseína. La mezcla de grasas contiene un 50 % de grasas polinsaturadas con 590 mg de eicosapentaenoico (EPA) en 100 ml, y fibra en dosis de 2,1 g por 100 ml (81 % soluble y 19 % insoluble).
Al inicio del reclutamiento en el estudio y tras los 3 meses de intervención se recogieron las siguientes variables: peso, talla, índice de masa corporal (IMC), Malnutrition Universal Screening Tool (MUST), bioquímica nutricional, encuesta nutricional de 3 días, efectos adversos generados por la fórmula, cumplimentación y calidad de vida con el test EuroQol-5D (EQ-5D) (23).
ANTROPOMETRÍA Y VALORACIÓN ANALÍTICA
A todos los pacientes se les pesó, se les talló (Modelo Omron®, LA, CA, EUA) y se les calculó el índice de masa corporal (IMC) con la siguiente fórmula: peso en kg / talla en m2. Se realizó una impedanciometría para determinar la masa grasa total y la masa magra total (Akern EFG, Pisa, Italia). También se recogió el peso habitual y se les realizó el test MUST, clasificando a los pacientes en: puntuación 0 (bajo riesgo nutricional), puntuación 1 (riesgo nutricional intermedio) y puntuación 2 o más (alto riesgo nutricional). En el momento basal y tras 12 semanas de la intervención nutricional se extrajeron muestras de sangre en ayunas para la determinación de glucosa, sodio, potasio, creatinina, proteína C-reactiva (PCR), albúmina, prealbúmina y transferrina (Hitachi, ATM, Manheim, Alemania).
VALORACIÓN DE LA INGESTA Y DE LA CALIDAD DE VIDA
En el momento basal se indicó a los pacientes que consumieran dos envases al día del SON (Tabla I). Los diarios de ingesta dietética de 3 días (dos días de lunes a viernes y uno de fin de semana) se completaron al inicio del estudio y a los 3 meses, y se utilizaron para evaluar la ingesta del paciente. La ingesta media total de energía y macronutrientes se calculó utilizando el programa DietSource 3.0 (Nestlé®, Suiza) con tablas de composición de alimentos nacionales (24). La ingesta dietética total se calculó sumando el consumo de SON a la ingesta espontánea de alimentos, solicitándose que se registrara el número de los envases o partes de los mismos consumidos dentro del diario. El número de envases de SON se recogió a diario por parte del paciente para evaluar la cumplimentación.
Durante el estudio, los eventos adversos (EA) se registraron a través de un registro diario. También se registraron los problemas gastrointestinales relacionados con el consumo del SON (diarrea, náuseas y vómitos) de manera dicotómica.
El EQ-5D se realizó en el momento basal y a los 3 meses. Es un test no especifico de ninguna patología, validado y estandarizado para describir y evaluar la calidad de vida. Este cuestionario describe el estado de salud en términos de cinco dimensiones: movilidad, autocuidado, actividades diarias, dolor o malestar y ansiedad o depresión. Cada una de estas dimensiones se divide en tres niveles de gravedad (sin problemas, algunos problemas y problemas extremos). Estos datos posteriormente se convierten a una única puntuación general (índice EQ-5D) utilizando una tabla de valores predefinida (23). El índice varía entre un valor de 1 (mejor estado de salud) y 0 (peor estado de salud).
ANÁLISIS ESTADÍSTICO
Se realizó un cálculo del tamaño muestral teniendo en cuenta una mejoría de la calidad de vida general de 0,20 puntos, obteniéndose un tamaño muestral de (n = 35), con un error de tipo I < 0,05 y una potencia estadística del 80 %. Las pruebas estadísticas fueron de dos colas y se realizaron al nivel de significancia de 0,05. Las variables cuantitativas con distribución normal se analizaron con la prueba de la “t” de Student de dos colas, emparejadas o no emparejadas. Las variables no paramétricas se analizaron con la prueba de Wilcoxon. Las variables cualitativas se analizaron con la prueba del chi cuadrado, usando la corrección de Fischer cuando fue necesario (casillas con n < 5). El paquete estadístico utilizado fue el SPSS 23.0, (IBM, IL, EUA) y los valores de p < 0,05 se tomaron como significativos.
RESULTADOS
En total se reclutaron 35 pacientes en el estudio. La edad media fue de 65,4 ± 10,7 años (18 mujeres/17 hombres). La patología oncológica se localizó en 4 áreas: tubo digestivo, 17 pacientes (48,5 %); cabeza y cuello, 9 pacientes (25,7 %); pulmón, 7 pacientes (20,0 %); y otros, 5 (16,4 %) pacientes.
La tabla II muestra la evolución en las variables antropométricas y bioquímicas tras la intervención nutricional. Con respecto a las variables antropométricas, el aumento del IMC, el peso, la masa magra y la masa grasa no alcanzó la significación estadística. Con respecto a las variables bioquímicas, aumentaron los niveles séricos de proteínas totales (1,5 ± 0,2 g/dl; p = 0,01), albúmina (0,9 ± 0,1 mg/dl; p = 0,04) y transferrina (53,9 ± 21,1 mg/dl; p = 0,02), manteniéndose sin modificaciones significativas el resto de parámetros analizados.
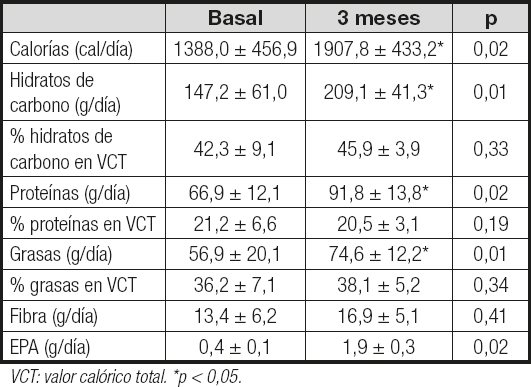
En la tabla III se muestra la modificación de la ingesta tras la intervención nutricional en un registro de alimentos de 3 días, incluyendo los dos envases de Forticare® al día. Esta valoración de la ingesta mostró un aumento significativo de la ingesta de calorías (599,1 ± 33,1 cal/día; p = 0,02), la ingesta de hidratos de carbono (62,5 ± 14,1 g/día; p = 0,02), la ingesta de proteínas (25,1 ± 9,2 g/día; p = 0,01), la ingesta de grasas totales (18,3 ± 3,1 g/día; p = 0,02) y la ingesta de EPA (1,4 ± 0,2 g/día; p = 0,02). No existieron modificaciones en el porcentaje de calorías que representaba cada macronutriente en el aporte calórico total tras los 3 meses de intervención. La toma del SON representó a los 3 meses un 21,2 % del aporte calórico total de la dieta, un 38,1 % de los hidratos de carbono, un 22,3 % de las proteínas y un 29,1 % de las grasas. Con respecto a la cumplimentación de la toma del SON, el 100 % de los pacientes finalizaron el protocolo tomando 2 envases del suplemento de manera diaria. La cumplimentación media del grupo fue de un 81,7 ± 7,2 % de las tomas prescritas para esos 3 meses (181 ± 21 envases/trimestre).
En el análisis del riesgo nutricional, al inicio del estudio, un 100 % (n = 35) de los pacientes presentaban en el test MUST la categoría de alto riesgo nutricional (2 o más puntos). Tras la intervención, un 34,3 % (n = 12) de los pacientes presentaban la categoría de bajo riesgo nutricional, un 51,4 % (n = 18) presentaban en el test MUST la categoría de moderado riesgo nutricional y un 14,3 % (n = 5) la categoría de alto riesgo nutricional (≥ 2 puntos), siendo estadísticamente significativa la diferencia entre antes y después de la intervención (p = 0,02). La tolerancia gastrointestinal (diarrea, náuseas y vómitos) con este SON fue buena. Solo 3 pacientes (8,5 %) presentaron durante el tratamiento náuseas y vómitos, y 2 pacientes presentaron diarrea (5,7 %). No hubo abandonos por intolerancia.
Con respecto al test de calidad de vida, la puntuación total de las 5 dimensiones aumentó significativamente a los 3 meses (0,51 ± 0,06 vs. 0,84 ± 0,03 puntos; p = 0,01). Analizando las cinco dimensiones, tras la toma del SON, todas ellas aumentaron el porcentaje de pacientes que pasaron a la categoría “sin problemas”: movilidad (69,4 % vs. 91,4 %; p = 0,03), autocuidado (74,2 % vs. 91,4 %; p = 0,04), actividades diarias (74,2 % vs. 91,4 %; p = 0,04), dolor o malestar (74,2 % vs. 88,5 %; p = 0,02) y ansiedad o depresión (80,0 % vs. 94,1 %; p = 0,04).
DISCUSIÓN
Nuestro trabajo muestra cómo la suplementación ambulatoria con un SON enriquecido con ω-3 durante 3 meses en pacientes oncológicos aumenta los niveles séricos de proteínas viscerales, el estado nutricional y la calidad de vida.
La desnutrición y la inmunosupresión son dos factores de los pacientes con cáncer. Existe evidencia que sugiere que la alimentación enteral, suplementada con ácidos grasos ω-3, arginina y otros inmunonutrientes, reduce las complicaciones posoperatorias (25). Una limitación de estos estudios es que la mayoría de los diseños se han realizado con alimentación por sonda y pocos estudios han evaluado solo pacientes ambulatorios con SON enriquecidos con ω-3 (20-22). En parte porque la mayoría de los SON existentes en el mercado que están diseñados específicamente para pacientes oncológicos presentan una mezcla de varios inmunonutrientes, y en parte por los problemas éticos y logísticos de realizar estudios con un diseño de ensayo clínico en pacientes oncológicos, sobre todo en la rama de control. Por todo ello, los estudios en vida real (EVR) nos pueden proporcionar información adicional. Estos EVR, en Medicina, generan una evidencia obtenida de datos del mundo real, es decir, de datos obtenidos fuera del contexto de ensayos controlados aleatorios y generados durante la práctica clínica habitual (26). Para evaluar los resultados de los pacientes y garantizar que estos reciban el tratamiento adecuado para ellos, es necesario utilizar datos del mundo real, aproximándose mucho más a la realidad cotidiana de nuestra practica clínica.
Nuestro hallazgo muestra cómo este SON enriquecido con ω-3 mejoró las concentraciones de proteína en sangre en pacientes oncológicos ambulatorios, sin una mejoría del peso pero tampoco con disminución del peso durante los 3 meses de seguimiento. A pesar de la no existencia de un grupo de control que permita validar esta hipótesis, en nuestra muestra, en la práctica clínica real, estos son los hallazgos que nos hemos encontrado. Teniendo en cuenta que todos los pacientes presentaban más de un 5 % de pérdida en los meses anteriores al estudio según el MUST, todos ellos dejaron de perder peso tras la intervención. Nuestros datos concuerdan con los de estudios previos en pacientes con cáncer de páncreas, que sugirieron que el EPA solo, en una dosis cercana a los 2 g/día, se asoció con la estabilidad del peso (27) y con una ganancia neta de masa corporal magra (dosis promedio de 2,1 g/día de EPA). En nuestros pacientes, el consumo medio mostró una ingesta de EPA de 1,9 g/día. En otro estudio de pacientes con cáncer de cabeza y cuello sin radioterapia (28), una ingesta de suplementos enriquecidos con omega-3 (0,6 g de EPA por día) mejoró también los niveles de proteínas sin afectar al peso.
La cumplimentación de SON en condiciones de vida real fue buena, observándose un incremento significativo de la ingesta de calorías y macronutrientes. En algunos ensayos clínicos de SON enriquecidos con ω-3 (29) no se han mostrado efectos significativos sobre la ingesta. Estos se deben en parte a la presencia de tratamientos coadyuvantes durante el diseño, como, por ejemplo, la quimioterapia, que disminuye ostensiblemente la ingesta. Sin embargo, en otros estudios con radioterapia durante la intervención (16) sí se demostró un aumento en la ingesta. Esta mejoría también se tradujo en mayor calidad de vida en el estudio de Ravasco y cols. (16) y, sin embargo, el estudio de Poulsen (29) mostró un nulo incremento de la ingesta y tampoco demostró ninguna mejoría de la calidad de vida.
La calidad de vida es un concepto multidimensional que incluye dominios relacionados con el estado de salud y las expectativas vitales. Por tanto, la calidad de vida depende tanto de la situación física como psicológica de los pacientes, y ambos factores pueden influir a su vez en la situación nutricional (30). Por otra parte, la propia situación nutricional juega un papel importante en el estado físico y las expectativas de vida. Como observamos en nuestro estudio, la mejoría de la situación nutricional (test MUST) y las variables bioquímicas se acompaña en la vida real de una mejoría de la calidad de vida en todas sus dimensiones. Probablemente, uno de los factores que explica la efectividad encontrada en nuestro trabajo sobre la situación nutricional podría ser la buena tasa de cumplimentación con el tratamiento, que permite el óptimo efecto de este soporte nutricional. Por otra parte, el buen cumplimiento de la toma del SON, a su vez, es probable que esté influenciado por la mejora del estado de salud (nutricional, peso corporal) y la calidad de vida, lo que estimula aun más a los pacientes a seguir cumpliendo su tratamiento nutricional y mejorando todos los parámetros.
Una limitación de nuestro estudio es la corta duración de la intervención (3 meses). En segundo lugar, la heterogeneidad de las patologías oncológicas que presentaban los pacientes y la subjetividad a la hora de valorar la ingesta nutricional a través de encuestas de 3 días, así como la ausencia de un grupo control sin intervención. En tercer lugar, la intervención nutricional parece mejorar los parámetros proteicos y el estado nutricional, etc., pero no se pueden atribuir estos resultados al aporte de omega-3 de la fórmula porque no existe un grupo comparador normocalórico y normoproteico sin omega-3. En cuarto lugar, aunque la herramienta utilizada para valorar la calidad de vida, el EuroQol-5D (EQ-5D), no es un test validado en pacientes oncológicos, nos parece una herramienta útil en este tipo de pacientes al presentar un corto número de preguntas y ser rápido de realizar. No obstante, este estudio en vida real nos muestra la efectividad de este suplemento enriquecido con ω-3, su buena tolerancia y la alta cumplimentación por parte de estos pacientes, con un efecto importante en la calidad de vida. Todo esto hace que sus datos sean fácilmente generalizables a la rutina asistencial habitual de nuestras consultas.
CONCLUSIÓN
En conclusión, la utilización de un SON enriquecido con ω-3 en pacientes oncológicos ambulatorios en un estudio con diseño en vida real muestra un efecto beneficioso sobre los parámetros nutricionales y la calidad de vida. Son necesarios más estudios que evalúen el efecto de los SON en diferentes patologías, no solo sobre los parámetros nutricionales sino también sobre la calidad de vida (31)