INTRODUCCIÓN
Desde su introducción en la década de 1970, la nutrición enteral domiciliaria (NED) se ha afianzado como una intervención nutricional fiable y eficaz, algo especialmente relevante dada la confianza creciente en la atención ambulatoria. La NED se inicia generalmente durante una estancia en el hospital y se continúa después como terapia domiciliaria a largo plazo. En general, las diferencias en cuanto a la indicación de la nutrición enteral (NE) hospitalaria y domiciliaria son mínimas. Sin embargo, en el caso de la NED hay que considerar criterios adicionales, como el pronóstico, la calidad de vida relacionada con la salud (CVRS) y aspectos éticos. Para iniciar la NED, el principio que se debería seguir es que sin la NE sería esperable un deterioro significativo del estado nutricional del paciente, que afectaría al pronóstico y a la CVRS, lo que supone una decisión compleja, especialmente si no existe un tratamiento eficaz para la enfermedad subyacente.
El tratamiento nutricional enteral es un tratamiento médico, pero las decisiones en cuanto a la vía, la composición y la gestión del tratamiento nutricional se toman mejor desde los equipos de soporte nutricional multidisciplinares.
Esta guía proporciona información basada en la evidencia sobre el uso de la NED. Hay numerosas enfermedades, a menudo complejas, que pueden hacer necesaria una NED. Su descripción no forma parte de la presente guía, pero se incluyen:
– Trastornos de la deglución por enfermedades neurológicas.
– Obstrucciones por tumores malignos.
– Caquexia por cáncer.
– Enfermedad pulmonar obstructiva crónica.
– Enfermedades cardiacas.
– Infecciones crónicas.
– Malabsorción/maldigestión a causa de enfermedades hepáticas, pancreáticas o intestinales.
Los requerimientos nutricionales específicos de estas enfermedades se describen detalladamente en otras guías de la European Society for Clinical Nutrition and Metabolism (ESPEN) recientemente publicadas (véase la web de la ESPEN y la revista Clinical Nutrition). La presente guía se centra en la metodología y la práctica clínica de la NED, el seguimiento correspondiente y las estrategias para evitar complicaciones.
METODOLOGÍA
La presente guía práctica consta de 61 recomendaciones y se basa en la guía de la ESPEN sobre NED, la versión práctica (1) y la versión científica (2). En este caso, la guía original se ha acortado al restringir los comentarios a la evidencia recopilada y la bibliografía en las que se basan las recomendaciones. Las recomendaciones no se han modificado, pero se ha transformado la presentación del contenido en una presentación gráfica, con diagramas de flujo para la toma de decisiones, siempre que ha sido posible. La guía original se elaboró según el procedimiento operativo estándar (POE) para las guías ESPEN (3). Este POE está basado en la metodología de la Scottish Intercollegiate Guidelines Network (SIGN). Se han realizado búsquedas en la literatura y se han clasificado del 1 al 4 según la evidencia. Asimismo, se crearon recomendaciones que se clasificaron en cuatro clases (A/B/0/GPP). Entre paréntesis se indican los números de la recomendación original (R1, R2, etc.) y la clasificación. El grupo de trabajo incluía médicos, un farmacéutico, una enfermera y dietistas, así como un representante de los pacientes. El proceso de elaboración de la guía fue financiado exclusivamente por la ESPEN. La guía abreviada y la difusión fueron financiadas en parte por la sociedad United European Gastroenterology (UEG) y también por la ESPEN. Para obtener más detalles sobre la metodología, véanse la versión completa de la guía ESPEN (2) y el POE de la ESPEN (3).
RECOMENDACIONES
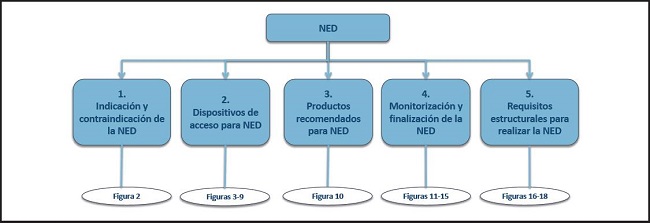
Esta guía práctica incluye 61 recomendaciones estructuradas en cinco capítulos principales y diversos subcapítulos (Fig. 1).
INDICACIÓN Y CONTRAINDICACIÓN DE LA NED (Fig. 2)

Figura 2. Indicación y contraindicación de la NED. NED: nutrición enteral domiciliaria; CVRS: calidad de vida relacionada con la salud.
¿CUÁLES SON LAS INDICACIONES DE LA NED?
1. Se debería ofrecer tratamiento con NED a los pacientes con riesgo nutricional o desnutridos que no puedan alcanzar sus necesidades de nutrientes mediante una ingesta dietética normal, que tengan un tracto gastrointestinal funcionante, que puedan recibir la terapia fuera de un entorno de cuidados de agudos y que estén de acuerdo y sean capaces de cumplir el tratamiento con NED, con el objetivo de mejorar el peso corporal, el estado funcional o la CVRS.
(Recomendación 1, grado GPP, consenso fuerte, 97 % de acuerdo)
Comentario
La NED está indicada en pacientes con alto riesgo nutricional o desnutridos, que no pueden satisfacer sus requerimientos nutricionales por vía oral y que presentan un tracto gastrointestinal funcionante (4). Así, la NED puede definirse como una terapia de mantenimiento de la vida y debería plantearse si se considera probable que la ingesta nutricional de un paciente sea cualitativa o cuantitativamente insuficiente durante una semana o más.
Se considera que un estado nutricional es inadecuado cuando el paciente no puede comer durante una semana o si la ingesta energética es inferior al 60 % de sus necesidades estimadas durante 1-2 semanas (normalmente, inferior a 10 kcal/kg/d o un déficit de 600-800 kcal/d) (5-8). Se presume que la ingesta nutricional es deficiente cuando no se puede realizar una ingesta de alimentos normal, que alcanzaría las necesidades individuales, a pesar de la optimización del tratamiento médico y dietético. En esta situación, la NE se debería iniciar en la primera semana. Se debe asumir que existe un deterioro significativo del estado nutricional cuando el paciente ha perdido > 5 % de su peso corporal en 1-3 meses (9). El estado nutricional puede deteriorarse si la absorción de alimentos es inferior al 75 % de las necesidades diarias (10,11), si ha habido una pérdida de peso previa o procesos catabólicos concomitantes o si está implicado un tratamiento con quimioterapia (12).
Un ensayo controlado aleatorizado (ECA) multicéntrico en el que se evaluaron pacientes sometidos a esofagectomía o gastrectomía total demostró que la NED a través de una yeyunostomía como práctica habitual era factible, segura y aceptable para los pacientes y sus cuidadores. Además, los autores demostraron un incremento sustancial de los parámetros antropométricos y funcionales, así como del coste eficiencia tras seis meses de seguimiento (13). En dos estudios que incluían pacientes con cáncer y con enfermedad de Crohn se demostró la eficacia de la NED en los resultados clínicos (14,15).
2. Antes del alta hospitalaria debería considerarse la posibilidad de administrar suplementos nutricionales orales o NED a los pacientes en riesgo de desnutrición (por ejemplo, pacientes con enfermedad neurológica, traumatismo craneoencefálico, cáncer de cabeza y cuello, enfermedades malignas gastrointestinales y de otro tipo y enfermedades gastrointestinales no neoplásicas, incluidos los síndromes de malabsorción).
(Recomendación 2, grado B, consenso fuerte, 96 % de acuerdo)
Comentario
En los datos epidemiológicos recogidos de 3.246 pacientes italianos a lo largo de un periodo de once años, se pudo observar un incremento anual progresivo del tratamiento con NED (16). La incidencia media fue de 406 ± 58 pacientes/millón de habitantes/año para los pacientes que vivían en su domicilio y de 319 ± 44 para los pacientes que vivían en residencias de ancianos (tasa de prevalencia media ± DE: 464 ± 129 casos/millón de habitantes en domicilio frente a 478 ± 164 en residencias de ancianos) (16).
Según varios estudios epidemiológicos y registros nacionales europeos, las indicaciones más frecuentes de la NED en adultos son las enfermedades neurológicas (neurovasculares y degenerativas), el cáncer de cabeza y cuello, el cáncer gastrointestinal y otros cánceres, la parálisis cerebral, las enfermedades gastrointestinales no neoplásicas (por ejemplo, fístulas, estenosis esofágica, enfermedad inflamatoria intestinal), traumatismos craneales, síndromes de malabsorción (por ejemplo, síndrome de intestino corto), trastornos graves de la motilidad intestinal, enfermedades metabólicas hereditarias y fibrosis quística (4,14,16-24).
Un estudio retrospectivo italiano encontró que la duración media de la NED era de unos 196 días (22). Desglosada por patologías, la duración fue de 261 días para la enfermedad neurovascular, 251,5 días para la enfermedad neurodegenerativa, 118 días para el cáncer de cabeza y cuello, 82,5 días para el cáncer abdominal, 788 días para los traumatismos craneales y 387 días para las enfermedades congénitas. Solo el 7,9 % de los pacientes reanudaron la nutrición oral y la mediana de supervivencia fue de 9,1 meses (22).
¿CUÁNDO NO SE DEBE RECOMENDAR LA NED? (CONTRAINDICACIÓN)
(Recomendación 3, grado GPP, consenso, 78 % de acuerdo)
Comentario
Esta recomendación se basa en una recomendación previa de la Sociedad Alemana de Nutrición Clínica (25). Para garantizar una atención óptima, se debería hacer un esfuerzo para estimar la esperanza de vida (26). Para más recomendaciones sobre la NED, se debería consultar la guía de la ESPEN sobre los aspectos éticos de la nutrición e hidratación artificial (27) y la guía de nutrición clínica en Neurología (28).
4. La NED no se administrará a pacientes con contraindicaciones como alteraciones funcionales graves del intestino, obstrucción gastrointestinal, hemorragia del tracto gastrointestinal, malabsorción grave o alteraciones metabólicas graves.
(Recomendación 4, grado GPP, consenso, 84 % de acuerdo)
Comentario
Esta recomendación se basa en la buena práctica clínica y no es específica para la NED. Se aplica de forma similar a la nutrición enteral en general.
5. Si el paciente y/o sus tutores legales no están de acuerdo con el programa de NED o es improbable que lo cumplan y/o si hay problemas organizativos/logísticos que no se pueden resolver, no se debe ofrecer la NED.
(Recomendación 5, grado GPP, consenso fuerte, 97 % de acuerdo)
DISPOSITIVOS DE ACCESO PARA NED (Fig. 3)

Figura 3. Dispositivos de acceso para la NED: una visión general. NED: nutrición enteral domiciliaria.
DISPOSITIVOS DE ACCESO (FIG. 4)
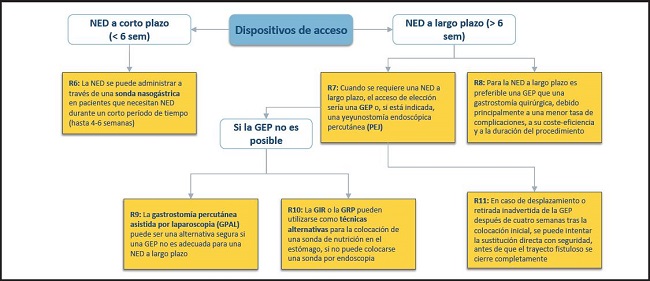
Figura 4. Dispositivos de acceso para la NED a corto y largo plazo. NED: nutrición enteral domiciliaria; GEP: gastrostomía endoscópica percutánea; PEJ: yeyunostomía endoscópica percutánea; GPAL: gastrostomía asistida por laparoscopia percutánea; GRP: gastrostomía radiológica percutánea; GIR: gastrostomía insertada radiológicamente.
NED DE CORTA DURACIÓN (< 6 SEMANAS)
6. La NED se puede administrar a través de una sonda nasogástrica en pacientes que necesitan NED durante un corto periodo de tiempo (hasta 4-6 semanas).
(Recomendación 6, grado 0, consenso, 90 % de acuerdo)
Comentario
La vía más adecuada para el tratamiento nutricional ambulatorio depende del funcionamiento, la accesibilidad y la capacidad digestiva y/o de absorción del tracto gastrointestinal. La vía de administración de la nutrición debería seleccionarse cuidadosamente (teniendo en cuenta las contraindicaciones). Si la NED es necesaria durante un tiempo limitado (hasta seis semanas), puede utilizarse una sonda nasogástrica. Dichas sondas, sobre todo las de pequeño calibre, se podrían utilizar durante periodos más largos, cuando la gastrostomía endoscópica percutánea (PEG) o la gastrostomía insertada radiológicamente (GIR) (22,29) no son una opción adecuada a largo plazo. Si ya existe un acceso in situ que pueda utilizarse para la administración de NE, debe considerarse su uso.
NED de larga duración (> 6 semanas)
7. Cuando se requiere una NED a largo plazo, el acceso de elección sería una PEG o, si está indicada, una yeyunostomía endoscópica percutánea (JEP).
(Recomendación 7, grado B, consenso fuerte, 93 % de acuerdo)
Comentario
La recomendación de utilizar una PEG o una JEP para NED a largo plazo se basa en un ECA (30) citado en la guía de la ESPEN sobre el cáncer (5), en el que se compararon las PEG y las sondas nasogástricas en pacientes con cáncer de cabeza y cuello, tres revisiones sistemáticas sobre el mismo tema (31-33) y una revisión sistemática que comparaba las PEG con las sondas nasogástricas en pacientes con disfagia (34). El peso corporal se mantenía de forma similar tanto con la PEG como con la sonda nasogástrica (33), mientras que el riesgo de pérdida de la sonda era menor (33,34) y la CVRS era probablemente mejor (30), aunque las sondas nasogástricas se asociaron con menos disfagia (33) y un destete más temprano tras la finalización de la radioterapia (31,33). Estas ventajas suponen una limitación frente a la clara recomendación de la PEG sugerida por los estudios anteriores y conducen al grado de recomendación B en lugar de A. Una revisión sistemática que incluía once ECA reportaba un menor número de fracasos de la intervención y una mejoría superior del estado nutricional en el grupo de PEG en comparación con el grupo de sonda nasogástrica (34). Además, la CVRS (por ejemplo, las molestias, la incomodidad, la alteración de la imagen corporal y de las actividades sociales) fue favorable a la PEG. No hubo diferencias significativas en las tasas de mortalidad y de neumonía por aspiración entre los dos grupos. Otra revisión sistemática no permitió extraer conclusiones firmes sobre si la nutrición con PEG era beneficiosa o no en comparación con la nutrición a través de sonda nasogástrica en pacientes mayores con disfagia no asociada a accidente cerebrovascular (35). En ancianos hospitalizados, el uso de la PEG se asoció a una mayor supervivencia, fue mejor tolerada y se asoció a una menor incidencia de aspiración (36) en comparación con la nutrición por sonda nasogástrica. El uso de una sonda JEP o PEG/J (PEG con extensión yeyunal) para la NED puede ser adecuado en caso de trastornos de la motilidad gastroduodenal, estenosis de la salida gástrica o alto riesgo de aspiración (37,38).
8. La gastrostomía percutánea asistida por laparoscopia (GPAL) puede ser una alternativa segura si una PEG no es adecuada para una NED a largo plazo.
(Recomendación 9, grado 0, consenso fuerte, 93 % de acuerdo)
Comentario
Existe una gran aceptación de la PEG frente a la gastrostomía quirúrgica convencional como técnica de inserción de elección debido a su menor coste, simplicidad, tiempo de procedimiento y menos complicaciones (39,41). Sin embargo, hay pacientes que no son candidatos apropiados para una PEG o en los que hay intentos fallidos de colocación de la misma (42). Una revisión sistemática y un metaanálisis solo pudieron demostrar que la PEG tiene menos complicaciones que la gastrostomía quirúrgica en los estudios aleatorizados incluidos en el análisis (39). Un gran estudio observacional en el que se compararon la GPAL, la PEG, la gastrostomía radiológica percutánea (GRP) y la gastrostomía quirúrgica convencional demostró que la tasa de complicaciones más baja correspondía al grupo de la GPAL (43).
En una revisión sistemática de Yuan y cols. (44) tanto la PEG como la GRP fueron eficaces para la NE a largo plazo en individuos seleccionados, aunque otra revisión indicó que la PEG se asociaba a una menor mortalidad a los 30 días en comparación con la GIR, lo que sugiere que la PEG debería considerarse como de primera elección para la NE a largo plazo (45). Por último, una revisión retrospectiva reveló que las tasas de pérdida de la sonda eran significativamente mayores en el grupo de GIR en comparación con el grupo de PEG (46).
9. La GIR o la GRP pueden utilizarse como técnicas alternativas para la colocación de una sonda de nutrición en el estómago, si no puede colocarse una sonda por endoscopia.
(Recomendación 10, grado 0, consenso fuerte, 97 % de acuerdo)
Comentario
El riesgo de peritonitis y mortalidad disminuye si la gastrostomía se coloca mediante una técnica endoscópica en lugar de radiológica (46-48). Las técnicas radiológicas deberían reservarse para aquellos pacientes en los que no es posible una técnica endoscópica. Sin embargo, tanto la PEG como la GRP son eficaces para la NE a largo plazo en individuos seleccionados (44).
10. En caso de desplazamiento o retirada inadvertida de la PEG después de cuatro semanas tras la colocación inicial, se puede intentar la sustitución directa con seguridad antes de que el trayecto fistuloso se cierre completamente.
(Recomendación 11, grado GPP, consenso fuerte, 93 % de acuerdo)
Comentario
Un trayecto fistuloso maduro es un requisito para la sustitución de una PEG después de su retirada inadvertida, extracción, oclusión o rotura. Los pacientes con riesgo de extracción involuntaria (por ejemplo, con demencia o delirio) requieren medidas preventivas para proteger la sonda. La adhesión del estómago a la pared abdominal se produce normalmente en un plazo de siete a 14 días, pero puede retrasarse en pacientes con problemas de cicatrización (49). La retirada involuntaria de una sonda de gastrostomía percutánea colocada recientemente (menos de cuatro semanas) es una urgencia.
En las dos primeras semanas, el recambio se realizará por vía endoscópica o radiológica a través de la misma ubicación. Entre dos y cuatro semanas después de la colocación inicial, se puede intentar la reposición a ciegas (por decisión médica), además de la sustitución endoscópica, si se comprueba posteriormente la posición adecuada de la sonda mediante un estudio con contraste hidrosoluble (50). La reposición debe realizarse rápidamente para mantener la permeabilidad y evitar el cierre del trayecto (37). Para el recambio a ciegas se utilizan generalmente las sondas de balón. Si se puede planificar el primer recambio de sonda, se recomienda realizarlo en un hospital. Los posteriores podrían ser realizados por una enfermera en el domicilio o en una residencia de ancianos, si los pacientes no son capaces de hacerlo (51).
Si no se dispone de una sonda de gastrostomía de diámetro similar para la sustitución inmediata, se puede utilizar temporalmente una sonda Foley de balón del mismo diámetro para mantener el trayecto abierto y, si es necesario, administrar NE, líquidos o medicamentos, aunque actualmente es más difícil con los conectores universales de seguridad (por ejemplo, ENFit®) (51). Si existe alguna duda sobre la adecuada ubicación tras el recambio a ciegas, debería confirmarse endoscópica o radiológicamente la posición correcta, utilizando un contraste hidrosoluble, antes de utilizar la sonda. Las técnicas alternativas para comprobar la posición correcta son la confirmación del pH del contenido gástrico (pH 5 o inferior), la irrigación de la sonda con 3-50 ml de agua estéril sin resistencia ni fugas alrededor del estoma, la evaluación de la longitud externa de la sonda y la manipulación de la sonda mediante rotación y movimientos de entrada y salida (59,60).
11. Para la NED a largo plazo es preferible una PEG que una gastrostomía quirúrgica, debido principalmente a una menor tasa de complicaciones, a su coste-eficiencia y a la duración del procedimiento.
(Recomendación 8, grado B, consenso fuerte, 100 % de acuerdo)
MANIPULACIÓN DE SONDAS, PUNTOS DE SALIDA Y FUNGIBLES
Aspectos de enfermería (Fig. 5)
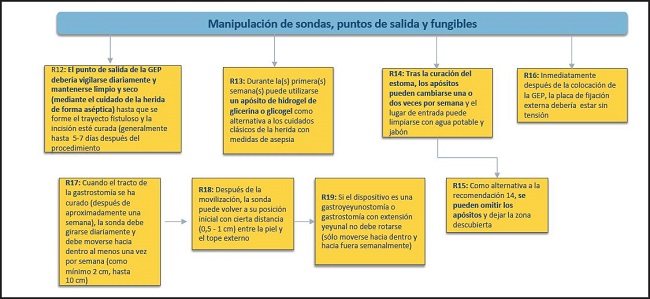
Figura 5. Manipulación de sondas, puntos de salida y fungibles. Aspectos de enfermería. GEP: gastrostomía endoscópica percutánea.
12. El punto de salida de la PEG debería vigilarse diariamente y mantenerse limpio y seco (mediante el cuidado de la herida de forma aséptica) hasta que se forme el trayecto fistuloso y la incisión esté curada (generalmente, hasta 5-7 días después del procedimiento).
(Recomendación 12, grado B, consenso fuerte, 100 % de acuerdo)
Comentario
Durante la primera semana tras la inserción de la PEG, uno de los objetivos es prevenir la infección del tracto del estoma. No es necesario aplicar tracción durante las primeras 24 horas al sistema de sonda PEG recién insertado para lograr una mejor adaptación de la sonda gástrica a la pared abdominal (52). Debe vigilarse diariamente el punto de salida de la PEG (para detectar signos de sangrado, dolor, eritema, induración, fugas e inflamación) y limpiarse con cloruro sódico al 0,9 %, agua estéril o agua recién hervida y enfriada (para eliminar cualquier resto). Se suele utilizar una gasa estéril (que no desprenda fibras) en Y para comprimir, colocada bajo la placa de disco externa, con un apósito transpirable respetuoso con la piel. Cuando la gasa se coloca bajo el disco externo, hay que evitar la tensión (51,53). Deben evitarse los apósitos oclusivos porque favorecen un ambiente húmedo y pueden provocar la maceración de la piel (52,53).
De acuerdo con las guías anteriores (61,62), la calificación de la recomendación 12 se ha elevado a una B, aunque la evidencia bibliográfica previa utilizada se ajusta más bien a un 0. Dentro de estas guías, falta una comparación directa de “sin cuidados” con “cuidados asépticos”; y en su lugar solo se examinó la “limpieza” frente a la “desinfección” por razones obvias (éticas).
13. Cuando el tracto de la gastrostomía se ha curado (después de, aproximadamente, una semana), la sonda debe girarse diariamente y debe moverse hacia dentro al menos una vez por semana (como mínimo 2 cm, hasta 10 cm).
(Recomendación 17, grado GPP, consenso, 87 % de acuerdo).
Comentario
El síndrome de enterramiento del tope interno de la gastrostomía (BBS) es una complicación grave en la que el dispositivo de fijación interna migra a lo largo del trayecto fistuloso hacia el exterior del estómago. El dispositivo puede acabar en cualquier localización entre la mucosa del estómago y la superficie de la piel (54). El BBS es generalmente una complicación a largo plazo, infrecuente y grave, pero que se puede prevenir con unos cuidados de enfermería adecuados. Las señales de alarma son cualquier dificultad para movilizar la sonda, las fugas alrededor del lugar de inserción cuando se intenta lavar la sonda, las alarmas frecuentes de la bomba de infusión (que pueden indicar obstrucción), el dolor abdominal, las infecciones crónicas de la zona o la resistencia a la administración de NE o líquidos (38). El factor de riesgo más importante para un BBS es la compresión excesiva del tejido entre el dispositivo de fijación interno y el externo (con mayor frecuencia en el caso de los dispositivos internos rígidos o semirrígidos) (55). La distancia entre los dos topes no debe ser ni demasiado holgada ni demasiado ajustada. La sonda debe avanzar en el estómago un mínimo de unos 2-3 cm, pero con pequeños movimientos se corre el riesgo de que solo se mueva la pared abdominal, por lo que lo ideal sería llegar hasta 5-10 cm (56). Esto puede hacerse, como pronto, cuando haya pasado aproximadamente una semana tras la inserción ya que antes podría provocar dolor local y dañar la formación del trayecto fistuloso. Una PEG también puede “incrustarse” en la mucosa gástrica y permitir igualmente girar la PEG. Esto puede ocurrir cuando una “bolsa” de mucosa gástrica ha crecido por encima y alrededor del tope interno (56). Cuando hay puntos de sutura porque el estómago está fijado a la pared abdominal (gastropexia), la movilización de la sonda puede retrasarse hasta que se hayan retirado las suturas (normalmente, después de dos semanas). Si hay una extensión yeyunal dentro de la sonda o si la sonda es una gastroyeyunostomía, el dispositivo no debe girarse (sino solo moverse hacia dentro y hacia fuera) (53,57).
14. Después de la movilización, la sonda puede volver a su posición inicial con cierta distancia (0,5-1 cm) entre la piel y el tope externo.
(Recomendación 18, grado 0, consenso fuerte, 93 % de acuerdo)
Comentario
Véase el comentario a la recomendación 13.
15. Si el dispositivo es una gastroyeyunostomía o gastrostomía con extensión yeyunal no debe rotarse (solo moverse hacia dentro y hacia fuera semanalmente).
(Recomendación 19, grado GPP, consenso fuerte, 92 % de acuerdo)
Comentario
Véase el comentario a la recomendación 13.
16. Durante la(s) primera(s) semana(s) puede utilizarse un apósito de hidrogel de glicerina o glicogel como alternativa a los cuidados clásicos de la herida con medidas de asepsia.
(Recomendación 13, grado B, consenso fuerte, 97 % de acuerdo)
Comentario
Dos ECA en adultos compararon unos apósitos diferentes para heridas con los apósitos estándar. El estudio más reciente demostró una reducción estadísticamente significativa de la infección al final de la primera y la segunda semana, utilizando un apósito para heridas de hidrogel de glicerina (aplicado al día siguiente de su colocación y cambiado semanalmente durante cuatro semanas) (52,58). Sin embargo, el otro estudio no demostró ninguna ventaja de un apósito de glicogel en cuanto a la infección periestomal después de una semana de uso (59). Ambos estudios concluyeron que, al evitar los cambios diarios de los apósitos habituales, esta otra técnica puede ser una alternativa coste-efectiva. Los resultados se confirmaron en un ECA muy reciente en el que se utilizó un hidrogel en niños (60).
De acuerdo con las guías anteriores (61,62), la calificación de la recomendación 16 se ha elevado a una B, aunque la evidencia bibliográfica previa utilizada se ajusta más bien a un 0.
17. Tras la curación del estoma, los apósitos pueden cambiarse una o dos veces por semana y el lugar de entrada puede limpiarse con agua potable y jabón.
(Recomendación 14, grado 0, consenso fuerte, 90 % de acuerdo)
Comentario
Después de una semana aproximadamente (o si está bien curado), el área del estoma puede limpiarse dos veces por semana con una toalla limpia, utilizando agua fresca del grifo y jabón y secando la piel después suave y completamente. Si el orificio del estoma está bien curado, también es posible ducharse, bañarse y nadar (es aconsejable cubrir la zona con un apósito impermeable cuando se nade en piscinas públicas) al cabo de unas semanas. Para algunos pacientes puede ser aconsejable utilizar una fijación o sujeción adicional para minimizar la tracción en el lugar del estoma (53). Una vez que el paciente es dado de alta, es importante garantizar una atención posterior competente y de alta calidad mediante una comunicación verbal clara y materiales escritos o visuales para los cuidadores y/o los pacientes. También debe señalarse a qué servicio o departamento se puede acudir en caso de urgencia (61).
18. Como alternativa a la recomendación 14, se pueden omitir los apósitos y dejar la zona descubierta.
(Recomendación 15, grado GPP, consenso fuerte, 92 % de acuerdo)
Comentario
Véase el comentario a la recomendación 17.
19. Inmediatamente después de la colocación de la PEG, la placa de fijación externa debe estar sin tensión.
(Recomendación 16, grado GPP, consenso fuerte, 93 % de acuerdo)
Complicaciones (Fig. 6)
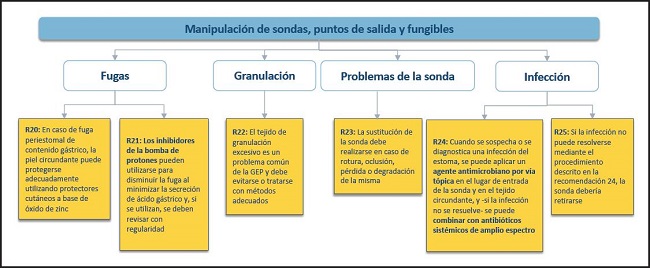
Figura 6. Manipulación de sondas, puntos de salida y fungibles: complicaciones. GEP: gastrostomía endoscópica percutánea.
Fugas
20. En caso de fuga periestomal de contenido gástrico, la piel circundante puede protegerse adecuadamente utilizando protectores cutáneos a base de óxido de zinc.
(Recomendación 20, grado 0, consenso fuerte, 93 % de acuerdo)
Comentario
En la primera semana tras la colocación puede producirse una pequeña salida de líquido periestomal, pero la fuga de contenido gástrico (muy a menudo en combinación con signos de infección periestomal o ensanchamiento de la gastrostomía) puede provocar problemas graves e incluso la pérdida de la sonda. Los factores de riesgo de fuga periestomal incluyen la infección de la piel, el aumento de la secreción de ácido gástrico, la gastroparesia, el aumento de la presión abdominal, el estreñimiento, la torsión lateral de la sonda, el aumento de la tensión entre el tope interno y externo, el BBS y la presencia de tejido de granuloma en el trayecto fistuloso (51,62,63). Además, los factores relacionados con el paciente pueden dificultar la cicatrización de la herida, como la diabetes, la inmunosupresión y la desnutrición.
En cualquier caso, para minimizar el daño de la piel debido a las fugas, se puede aplicar un producto tópico como un agente absorbente en polvo o una película de barrera, pasta o crema (que contenga óxido de zinc) (64). Asimismo, pueden utilizarse apósitos de espuma en vez de gasas para reducir la irritación local de la piel (la espuma separa el líquido de la piel, mientras que las gasas pueden contribuir a una mayor maceración). Las infecciones locales por hongos también pueden estar asociadas a fugas y pueden tratarse con agentes antifúngicos tópicos. Es importante verificar que la tensión entre los dos topes sea adecuada, evitando el movimiento innecesario de la sonda o la excesiva presión. La torsión lateral, que da lugar a un trayecto del estoma demasiado grande, se puede corregir estabilizando la sonda mediante un dispositivo de sujeción o cambiando a una sonda de bajo perfil (49). Si se trata de una sonda con balón como sistema de retención, el volumen del balón se debe ajustar a las recomendaciones del fabricante y comprobar regularmente (por ejemplo, una vez por semana). En el caso de una gastrostomía de botón, hay que asegurarse de que el tamaño del globo y la longitud de la sonda son correctos (53). En algunos casos refractarios se puede intentar retirar la sonda durante 24-48 horas, lo que permitiría un ligero cierre espontáneo del trayecto, con el objetivo de que la sonda de sustitución se ajuste mejor (65). Si todas las medidas mencionadas fracasan, hay que colocar una nueva gastrostomía en una nueva ubicación.
21. Los inhibidores de la bomba de protones pueden utilizarse para disminuir la fuga al minimizar la secreción de ácido gástrico y, si se utilizan, se deben revisar con regularidad.
(Recomendación 21, grado 0, consenso fuerte, 96 % de acuerdo)
Comentario
La descompresión gástrica y el inicio de los inhibidores de la bomba de protones y/o los procinéticos pueden ser útiles mientras se optimiza simultáneamente el estado nutricional (por ejemplo, con el inicio de la NP) y la situación médica (66).
Granulación
22. El tejido de granulación excesivo es un problema común de la PEG y debe evitarse o tratarse con métodos adecuados.
(Recomendación 22, grado GPP, consenso fuerte, 93 % de acuerdo)
Comentario
El desarrollo de un exceso de tejido de granulación alrededor de la sonda de gastrostomía es una complicación común en pacientes con una sonda PEG. El tejido de granulación es vascular, por lo que sangra fácilmente y a veces es doloroso. Las causas más comunes de su desarrollo son un exceso de humedad, mucha fricción o movimiento de una sonda mal fijada y la colonización crítica, la fuga o la infección (recomendaciones 22 y 24). Se puede utilizar una película o crema de barrera para proteger la piel circundante si el tejido de granulación es exudativo. La piel afectada debería limpiarse con un antimicrobiano como mínimo una vez al día. Además, existe una gran variedad de opciones de tratamiento, como la aplicación de un agente antimicrobiano tópico bajo el dispositivo de fijación, o un apósito de espuma o de plata sobre la zona afectada que debería cambiarse solo si hay exudación significativa (pero al menos, semanalmente). Otra opción es cauterizar directamente el tejido de granulación en exceso con nitrato de plata. Como alternativa, se puede administrar una crema o pomada tópica de corticoides durante 7-10 días en combinación con un apósito de espuma. Por último, se han descrito en la literatura la resección quirúrgica y la coagulación con argón. Si los pasos anteriores resultan ineficaces, puede probarse una marca comercial diferente o un tipo alternativo de sonda de gastrostomía (38,53,67).
Problemas de la sonda
23. La sustitución de la sonda debe realizarse en caso de rotura, oclusión, pérdida o degradación de la misma.
(Recomendación 23, grado GPP, consenso fuerte, 93 % de acuerdo)
Comentario
La mayoría de las sondas de gastrostomía colocadas por vía transoral pueden durar muchos años. La duración de una sonda PEG se relaciona fundamentalmente con un manejo cuidadoso de la misma. No es necesario cambiar la sonda regularmente (52). En algún momento habrá que sustituirla por rotura, oclusión, pérdida de la misma o degradación (38). Un dispositivo de acceso enteral percutáneo que muestre signos de colonización fúngica con deterioro del material y compromiso de la integridad estructural debería ser sustituido de forma no urgente (37). En el caso de una sonda con tope interno, la retirada se realiza cortando la sonda a nivel de la piel abdominal y empujando el tope interno hacia la luz intestinal (técnica de “cortar y empujar”) (68). La migración no suele presentar problemas, incluso en el caso de las sondas de gran calibre (69). No obstante, se recomienda la extracción endoscópica del tope interno en los casos de cirugía intestinal previa y en los pacientes con riesgo de estenosis o íleo, que podrían dificultar la migración espontánea y la eliminación del fragmento seccionado (38). La sustitución puede realizarse de muchas maneras: por vía endoscópica, radiológica, quirúrgica o a pie de cama (según el tipo de sonda de gastrostomía que se sustituya) (53). Las sondas de balón son las que se utilizan principalmente para la sustitución a ciegas a través del mismo trayecto fistuloso maduro. El balón se infla con agua estéril (no suero salino) (normalmente, de 5 a 10 ml) y se comprueba el volumen de agua cada semana para prevenir que el balón se desinfle espontáneamente por pérdida de agua. Este tipo de sonda puede necesitar su sustitución cada tres o cuatro meses debido a la degradación del balón (38,70).
Infección
24. Cuando se sospecha o se diagnostica una infección del estoma, se puede aplicar un agente antimicrobiano por vía tópica en el lugar de entrada de la sonda y en el tejido circundante, y si la infección no se resuelve, se puede combinar con antibióticos sistémicos de amplio espectro.
(Recomendación 24, grado 0, consenso fuerte, 93 % de acuerdo)
Comentario
La infección del estoma es una complicación común después de la colocación de la gastrostomía por vía transoral (71). Los pacientes con diabetes, obesidad, mal estado nutricional y los que reciben tratamiento crónico con corticosteroides u otra terapia inmunosupresora tienen un mayor riesgo de infección (72). Además, la piel hiperhidratada o inflamada, debido a las fugas, puede favorecer el crecimiento de microorganismos (véanse las recomendaciones 20 y 21). La prevención consiste en un buen cuidado de la herida con técnica aséptica tras su colocación y en la detección temprana de signos y síntomas de infección, como pérdida de la integridad de la piel, eritema, exudado purulento y/o maloliente, fiebre y dolor (73). Hay que asegurarse de que el tope externo no está demasiado apretado, causando demasiada presión entre el tope interno y el externo. Se puede realizar un frotis de la zona para detectar infecciones bacterianas y fúngicas. Se puede utilizar una pomada antimicrobiana o un apósito con un agente antimicrobiano de liberación sostenida en el estoma de la gastrostomía: estos apósitos suelen obtener su actividad antimicrobiana de la plata, el yodo o el polihexametileno biguanida y están disponibles en diferentes formas (por ejemplo, espumas, hidrocoloides o alginatos). Hay que tener en cuenta las alergias a cualquiera de los componentes del producto y que los apósitos de plata no pueden usarse durante la realización de una resonancia magnética. Pueden utilizarse antibióticos sistémicos o (si se ha comprobado) agentes antifúngicos, en combinación con el tratamiento tópico local. No deben utilizarse antibióticos tópicos.
25. Si la infección no puede resolverse mediante el procedimiento descrito en la recomendación 24, la sonda debería retirarse.
(Recomendación 25, grado GPP, consenso, 86 % de acuerdo)
Comentario
En caso de obstrucción, de infección periestomal que persiste a pesar del tratamiento antimicrobiano adecuado, de excoriación de la piel o de una infección por hongos (especialmente si se trata de una sonda de silicona) es aconsejable retirar y/o sustituir la sonda de gastrostomía (53,73).
INICIO DE LA NED (FIG. 7)

Figura 7. Requisitos previos al inicio y calendario de la NED. NED: nutrición enteral domiciliaria; NE: nutrición enteral.
26. La NED puede iniciarse cuando el paciente esté médicamente estable y: a) se verifique la posición correcta de la sonda; b) se demuestre la tolerancia a la nutrición enteral prescrita (volumen y fórmula); y c) el paciente y/o quien administre la nutrición tenga los conocimientos y habilidades adecuadas para manejar la NED.
(Recomendación 26, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
Los pacientes hospitalizados que inician la nutrición enteral deberían recibir ya un tratamiento nutricional estable antes del alta hospitalaria. Debe confirmarse que el paciente tolera el volumen y el tipo de nutrición que se le administrará en su domicilio. Si el paciente ha ingresado para un procedimiento de un día con el fin de (re)colocar una sonda, se debe comprobar la función gastrointestinal antes del alta para garantizar la seguridad. El inicio de la NED depende del tipo y la posición de la sonda. Debe verificarse la posición correcta de todos los tipos de sonda y, si se ha realizado un procedimiento intervencionista (por ejemplo, la inserción de una gastrostomía o yeyunostomía), es necesario un periodo de observación para garantizar que no haya ninguna complicación quirúrgica. Los pacientes con NED y sus cuidadores necesitan formación en el manejo de la NE por parte de un equipo multidisciplinar (74). Antes de ser dados de alta, deben ser capaces de demostrar su competencia en la administración de la nutrición, el manejo del equipo y la resolución de problemas básicos en caso de fallo de la sonda o del equipo (75).
27. El paciente con una sonda nasogástrica puede iniciar la NED inmediatamente, una vez se haya confirmado la adecuada colocación de la sonda, según el plan de cuidados nutricionales previamente establecido.
(Recomendación 27, grado GPP, consenso fuerte, 96 % de acuerdo)
Comentario
Una vez se haya confirmado la posición de la sonda nasogástrica, la NED puede comenzar o continuar según el plan de cuidados nutricionales previamente establecido. No hay evidencia de que la fórmula nutricional deba diluirse al inicio de la NED solo por motivos de dilución, a menos que se necesite líquido adicional en forma de agua (76). Cualquiera que sea el acceso por sonda que se utilice, debe tenerse precaución si se sospecha un síndrome de realimentación. En estos casos, deberían seguirse las guías adecuadas para evitar complicaciones metabólicas.
28. Los adultos a los que se les ha colocado una sonda de gastrostomía sin complicaciones pueden iniciar la NE entre dos y cuatro horas después del procedimiento.
(Recomendación 28, grado A, consenso fuerte, 100 % de acuerdo)
Comentario
Tradicionalmente, tras la inserción de la gastrostomía, la NE se iniciaba con agua o solución salina lentamente y con un incremento gradual, y posteriormente se iniciaba la fórmula enteral. Un metaanálisis reciente de ECA no mostró diferencias en cuanto a las complicaciones cuando se iniciaba en menos de cuatro horas o se iniciaba tardíamente o al día siguiente (38). No hay evidencia que apoye la administración de agua antes de comenzar la NE a través de la gastrostomía (52,77,78).
(Recomendación 29, Grado B, consenso fuerte, 93 % de acuerdo)
Comentario
Los estudios recomiendan una infusión inicial de 10 ml/h de cloruro sódico al 0,9 % en las primeras 24 horas tras la inserción de la sonda, seguida del inicio de la NE a 10 ml/h durante 24 horas y luego del aumento de la velocidad en 20 ml/h hasta que se alcance el objetivo nutricional, generalmente al sexto día (79). En un ensayo prospectivo aleatorizado realizado por Han-Geurts en 2007 se utilizó una pauta de inicio de 1,0 kcal/ml administrada en infusión continua por bomba, iniciando a 30 ml/h el primer día postoperatorio y aumentando a 84 ml/h el tercer día, según tolerancia (80). El 90 % de los pacientes toleraron esta pauta nutricional y alcanzaron completamente sus objetivos nutricionales.
Una revisión sistemática de las vías para nutrición precoz tras una esofagectomía informó de que la NE que se iniciaba en el primer día postoperatorio y se incrementaba gradualmente para satisfacer las necesidades nutricionales al tercer día era bien tolerada (81). No obstante, en algunos centros las pautas de progresión de la nutrición hacían que solo la mitad de los pacientes alcanzasen su objetivo al octavo día. Cuando no se ha realizado ningún procedimiento quirúrgico, no están bien definidas en la literatura las pautas de inicio de la nutrición yeyunal, sin embargo, dado que no hay resección del tracto gastrointestinal y posiblemente menos posibilidad de íleo, las pautas de inicio tienden a ser más liberales.
ADMINISTRACIÓN (FIG. 8)
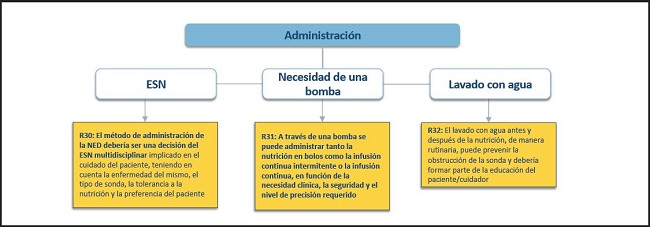
Figura 8. Administración de la NED. NED: nutrición enteral domiciliaria; ESN: equipo de soporte nutricional.
Equipo de soporte nutricional
30. El método de administración de la NED debería ser una decisión del equipo de soporte nutricional (ESN) multidisciplinar implicado en el cuidado del paciente, teniendo en cuenta la enfermedad del mismo, el tipo de sonda, la tolerancia a la nutrición y la preferencia del paciente.
(Recomendación 30, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
El nivel de actividad del paciente, su entorno social y sus capacidades individuales deberían tenerse en cuenta a la hora de elegir el método de administración (82). En algunas situaciones hay que tener en cuenta los costes atribuibles al tratamiento con NED, ya que podrían influir en la elección del método de administración.
Necesidad de una bomba
31. A través de una bomba se puede administrar tanto la nutrición en bolos como la infusión continua intermitente o la infusión continua, en función de la necesidad clínica, la seguridad y el nivel de precisión requerido.
(Recomendación 31, grado GPP, consenso fuerte, 92 % de acuerdo)
Comentario
El procedimiento de infusión en bolos supone dividir el volumen total de nutrición entre cuatro y seis tomas a lo largo del día. El volumen de infusión suele estar entre 200 y 400 ml administrados durante un periodo de 15 a 60 minutos, en función de su tolerancia y las necesidades de nutrientes del paciente. Las infusiones en bolos se utilizan cuando el paciente tiene una sonda nasogástrica in situ o una sonda de gastrostomía. Las tomas se administran con una jeringa de 50 ml, con o sin émbolo. La nutrición en bolos en el estómago se considera la más fisiológica (83). La infusión continua de fórmula enteral suele realizarse a través de una bomba. Las bombas de nutrición enteral pueden infundir soluciones con precisión (84). El uso de una bomba de nutrición enteral permite infundir con seguridad pequeños volúmenes de solución durante periodos de tiempo variables (85). Esto se considera una ventaja en la nutrición yeyunal, ya que el yeyuno depende del suministro controlado de sustratos isotónicos. Los bolos de nutrición de fórmula hipercalórica deberían administrarse preferentemente mediante una bomba de nutrición. La infusión nocturna de la nutrición mediante una bomba permite a los pacientes estar activos durante el día para realizar trabajos/estudios y otras actividades sociales. La nutrición nocturna mediante bomba permite a los pacientes tener un sueño ininterrumpido sin necesidad de ajustar los flujos durante la noche. Las bombas de nutrición pueden ser estáticas o móviles, colocando el dispositivo en una mochila especialmente diseñada. Pueden colocarse en la espalda del paciente o acoplarse, por ejemplo, a una silla de ruedas. Las bombas de nutrición han evolucionado para ser más ligeras y más intuitivas en su manejo, lo que permite una mayor facilidad en la administración de NED por los pacientes y los cuidadores (84).
Lavado con agua
32. El lavado con agua antes y después de la nutrición de manera rutinaria puede prevenir la obstrucción de la sonda y debería formar parte de la educación del paciente/cuidador.
(Recomendación 32, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
Independientemente de la vía de administración (gástrica o yeyunal), las sondas de nutrición son proclives a obstruirse, principalmente por la composición química de las soluciones ricas en proteínas, la viscosidad del fluido y el pequeño diámetro de la luz de la sonda. Este problema se agrava aún más cuanto más larga sea la sonda de nutrición y si se administran medicamentos a través de ella. Las sondas deberían lavarse con al menos 30 ml de agua potable antes de empezar y después de terminar la nutrición en caso de administración en bolos o cada cuatro horas si la nutrición es en infusión continua (86).
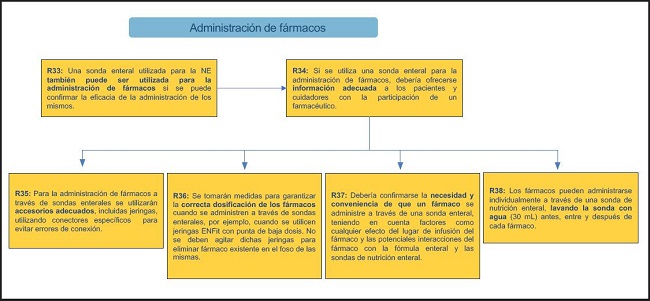
ADMINISTRACIÓN DE FÁRMACOS (FIG. 9)
33. Una sonda enteral utilizada para la NE también puede ser utilizada para la administración de fármacos si se puede confirmar la eficacia de la administración de los mismos.
(Recomendación 33, grado GPP, consenso fuerte, 92 % de acuerdo)
Comentario
La administración de medicamentos a través de sondas de nutrición enteral es una práctica muy extendida, pero una encuesta reciente realizada en Reino Unido (87) descubrió que más del 30 % de los cuidadores de pacientes que requieren la administración de medicamentos a través de sondas de nutrición enteral no recibieron información. Además, esa encuesta se llevó a cabo a través de un grupo nacional de apoyo a los pacientes, por lo que podría ser que en una población más amplia incluso menos cuidadores recibieran dicha información. Cuando se utiliza una sonda de nutrición enteral para la administración de medicamentos, es importante que la sonda no se obstruya y que quienes prescriban, suministren y administren los medicamentos sean conscientes de su responsabilidad ante cualquier acontecimiento adverso derivado del uso de medicamentos no autorizados o del uso de medicamentos autorizados fuera de ficha técnica.
Debería consultarse el correspondiente resumen de las características del producto para ayudar a comprender la situación legal en relación a cada una de las prescripciones y formas farmacéuticas. El uso de un producto fuera de los términos del resumen de las características del producto conlleva una responsabilidad adicional que debería ser aceptada antes de la prescripción, suministro o administración del medicamento. Siempre que sea posible, debe evitarse triturar los medicamentos dados los riesgos potenciales de exposición al fármaco y a las imprecisiones en la dosificación del mismo. La elección de la forma de dosificación para la administración a través de una sonda de nutrición enteral también presenta consideraciones prácticas. Por ejemplo, aunque es posible que haya una incidencia generalmente mayor de oclusiones de la sonda cuando se utilizan formas farmacéuticas sólidas a través de sondas nasogástricas y GEP de silicona, hay que tener cuidado con los medicamentos líquidos, ya que pueden contener sorbitol, que se ha notificado que contribuye a la diarrea (48 % de los casos de diarrea osmótica, n = 14) (88) o a tener una osmolaridad > 500-600 mOsm/kg, lo suficientemente alta como para provocar alteraciones intestinales (73).
34. Si se utiliza una sonda enteral para la administración de fármacos, debería ofrecerse información adecuada a los pacientes y cuidadores con la participación de un farmacéutico.
(Recomendación 34, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
Un farmacéutico está en una posición ideal para asesorar sobre la administración de medicamentos a través de sondas de nutrición enteral y, de hecho, en las guías nacionales se ha recomendado la participación de los farmacéuticos (73). El farmacéutico puede sugerir medicamentos alternativos u otras opciones de tratamiento del paciente cuando se le pide que asesore sobre la administración de un medicamento concreto a través de una sonda de nutrición enteral.
35. Para la administración de fármacos a través de sondas enterales se utilizarán accesorios adecuados, incluidas jeringas, utilizando conectores específicos para evitar errores de conexión.
(Recomendación 35, grado A, consenso fuerte, 100 % de acuerdo)
Comentario
Véase el comentario a la recomendación 36.
36. Se tomarán medidas para garantizar la correcta dosificación de los fármacos cuando se administren a través de sondas enterales, por ejemplo, cuando se utilicen jeringas con punta de baja dosis ENFit®. No se deben agitar dichas jeringas para eliminar fármaco existente en el foso de las mismas.
(Recomendación 36, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
La reconocida norma ISO 80369-3 para sondas enterales (ENFit®) se ha introducido a raíz de errores de conexión, que incluían errores fatales. Esta norma exige que las sondas y los accesorios, incluidas las jeringas, tengan un diseño específico para que no puedan conectarse con sondas y accesorios destinados a la administración por una vía diferente.
Dada la preocupación por la exactitud de la administración de fármacos con las jeringas ENFit® y, en particular, con las jeringas con punta de baja dosis ENFit®, se actualizó el diseño de las jeringas de 1 ml y 3 ml para incorporar una punta de jeringa de baja dosis. Aunque la punta de baja dosis podría mejorar la precisión de la dosis, también podría dar lugar a un remanente de fármaco en el foso de la jeringa que podría alterar inadvertidamente la cantidad de fármaco administrado. Por lo tanto, se deben tomar medidas para evitar una dosificación inexacta cuando se utilicen jeringas ENFit® de baja dosis para administrar medicamentos a través de sondas enterales. Agitar una jeringa para eliminar el fármaco del foso de la jeringa expone el ambiente y a las personas al fármaco y podría afectar a la dosis administrada, por lo que, en ausencia de evidencia, no es una práctica recomendada.
37. Debería confirmarse la necesidad y conveniencia de que un fármaco se administre a través de una sonda enteral, teniendo en cuenta factores como cualquier efecto del lugar de infusión del fármaco y las potenciales interacciones del fármaco con la fórmula enteral y las sondas de nutrición enteral.
(Recomendación 37, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
El lugar de la punta de la sonda enteral y, por tanto, el lugar de infusión del fármaco es un factor importante a la hora de establecer la eficacia probable del fármaco. Por ejemplo, un estudio sobre la trovafloxacina administrada en estómago mostró una eficacia similar con o sin la administración simultánea de la fórmula enteral, pero la infusión a través de una sonda directamente en el duodeno en lugar del estómago condujo a una menor disponibilidad del fármaco (89). Desgraciadamente, en esta publicación no se indica el tipo o el material de la sonda nasogástrica utilizada.
No se ha notificado ninguna diferencia entre la NE en bolos o continua en relación a la obstrucción de la sonda (p = 0,33) (88) cuando se utiliza una sonda de nutrición enteral para la administración de medicamentos. Sin embargo, la elección entre nutrición en bolos y continua podría afectar a la administración en la práctica de determinados medicamentos, como los que se unen a la fórmula enteral y, por tanto, algunos medicamentos administrados a través de una sonda de nutrición enteral podrían tener que ser administrados separados de la fórmula enteral. Se han notificado interacciones entre medicamentos específicos y la fórmula enteral que reducen la eficacia de los mismos, así como interacciones directas entre medicamentos y sondas de nutrición enteral. Por ejemplo, se ha reportado que la fenitoína se une directamente a la fórmula enteral, así como a las sondas de nutrición enteral de poliuretano lubricadas con polivinilpirrolidona (siendo el pH un factor importante) (90). También se ha sugerido que las PEG de poliuretano son preferibles a las de silicona cuando se considera la administración de medicamentos a través de una sonda de nutrición enteral, debido al mayor mantenimiento de la permeabilidad y la consiguiente posibilidad de seguir utilizando la sonda (88).
38. Los fármacos pueden administrarse individualmente a través de una sonda de nutrición enteral, lavando la sonda con agua (30 ml) antes, entre y después de cada fármaco.
(Recomendación 38, grado 0, consenso fuerte, 100 % de acuerdo)
Comentario
Está casi universalmente aceptado que los medicamentos no deben mezclarse antes de su administración a través de una sonda de nutrición enteral debido a los riesgos que conlleva, entre ellos, las interacciones farmacológicas, y que es necesario un lavado adecuado de la sonda entre la nutrición y/o los medicamentos. El uso de al menos 30 ml de agua para la irrigación cuando se administran medicamentos o cuando se lavan las sondas nasogástricas de pequeño diámetro puede reducir el número de obstrucciones de la sonda (88). Una encuesta realizada a 105 farmacéuticos belgas de la comunidad reveló que tenían un conocimiento limitado sobre la administración de medicamentos a través de sondas de nutrición enteral. Por ejemplo, menos de la mitad sabía si los medicamentos debían mezclarse o no antes de su administración (91). Otra encuesta similar (92) realizada por el mismo grupo, pero esta vez en centros residenciales belgas para personas con discapacidad intelectual, reveló que menos del 40 % del personal sabía si los medicamentos podían mezclarse antes de su administración. Además, en el mismo tipo de centro se constató que no se seguían las recomendaciones para la administración de medicamentos a través de sondas de nutrición enteral (93). En la práctica, más de dos tercios de los medicamentos preparados se mezclaban antes de su administración, y en algunos casos hasta ocho medicamentos a la vez, a pesar de que casi la mitad del total de los registros de medicación contenían al menos una interacción farmacológica (94). La administración inadecuada de medicamentos se atribuyó a factores como la falta de tiempo y unos conocimientos limitados (95).
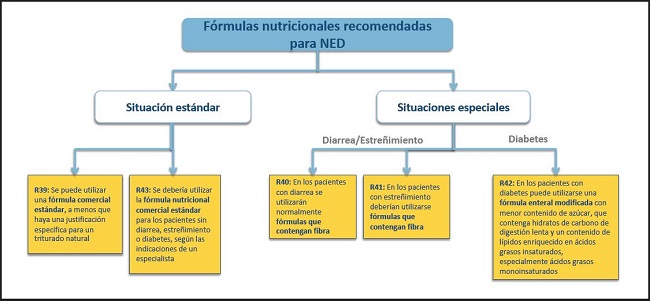
FÓRMULAS NUTRICIONALES RECOMENDADAS PARA NED (FIG. 10)
SITUACIÓN BASAL
39. Se puede utilizar una fórmula comercial estándar, a menos que haya una justificación específica para un triturado natural.
(Recomendación 39, grado 0, consenso fuerte, 92 % de acuerdo)
Comentario
No hay diferencias fundamentales en cuanto a los productos nutricionales preferibles en NED para pacientes que pueden tener una enfermedad benigna o maligna. Frecuentemente se han utilizado alimentos naturales a través de la sonda en lugar de fórmulas comerciales. Se ha considerado que la nutrición por sonda con alimentos naturales requiere mucho tiempo y, por lo tanto, es laboriosa, y un estudio encontró que el tiempo y los costes no nutricionales podían suponer más del 50 % del coste total de la nutrición (96). El mismo estudio también concluyó que la estandarización de los alimentos naturales por sonda era deficiente y que existía riesgo de contaminación microbiana e inestabilidad del producto. Cabe destacar que cuatro de los cinco autores de este estudio en particular estaban relacionados con empresas de nutrición enteral comercial. Sin embargo, otros también han expresado su preocupación por la mayor contaminación microbiana de los alimentos naturales en comparación con las fórmulas enterales comerciales (97,98). Además, cuando 203 pacientes polacos pasaron de la nutrición por sonda con alimentos naturales administrada en bolos de 50-100 ml entre cinco y seis veces al día a la nutrición por sonda con formula comercial administrada en bolos o en infusión continua bajo el control de un especialista, presentaron menos ingresos en el hospital y en Cuidados Intensivos, y una menor frecuencia de neumonía, infección del tracto urinario y anemia que requiriera hospitalización (99). En este estudio, además de la fórmula comercial por sonda, se proporcionó a los pacientes información sobre cuidados, lo que complica la interpretación de los resultados comunicados (99). En otro estudio, se observó durante un periodo de ocho meses, en pacientes con cáncer de cabeza y cuello, que la fórmula comercial era relativamente más beneficiosa en comparación con preparados con alimentos naturales por sonda o la dieta triturada utilizada como nutrición por sonda (100). La nutrición con triturados naturales, aunque sin un beneficio claro en comparación con la nutrición comercial, se sigue utilizando ocasionalmente en pacientes crónicos en casa, pero no en los hospitales. Si se utiliza, debería administrarse a través de una sonda grande (14 de diámetro) o una PEG para evitar que se obstruya.
40. Se debería utilizar la formula nutricional comercial estándar para los pacientes sin diarrea, estreñimiento o diabetes, según las indicaciones de un especialista.
(Recomendación 43, grado GPP, consenso fuerte, 96 % de acuerdo)
Comentario
Hay información más limitada sobre otras situaciones especiales, que incluyen un papel potencial de la dieta baja en yodo para nutrición enteral hecha en casa para la preparación para la exploración y el manejo del carcinoma diferenciado de tiroides (101). En un estudio de NE en pacientes con enfermedad de Crohn (que se complica porque a todos los participantes en el estudio se les administraron 200 ml de lípidos de soja al 10 % por vía intravenosa diariamente durante un periodo indeterminado), la fórmula elemental fue beneficiosa para la remisión de la enfermedad, así como para el mantenimiento de la remisión, en comparación con la fórmula elemental más tratamiento farmacológico (prednisolona o sulfasalazina), solo tratamiento farmacológico (y una dieta baja en residuos) o ninguna intervención (102). Se ha lanzado un mensaje general en relación a garantizar la claridad por parte del prescriptor de los objetivos nutricionales si se utilizan módulos proteicos, ya que los diferentes productos no son clínicamente equivalentes para la misma cantidad de aminoácidos (103). Otros informes parecen ser actualmente menos relevantes desde el punto de vista clínico. Por ejemplo, la nutrición enteral estándar por sonda resultó beneficiosa en 14 pacientes HIV positivos con emaciación, sin grupo control (104); la suplementación de la nutrición enteral con enzimas digestivas no tuvo efectos significativos en las concentraciones totales de proteínas y albúmina en 16 ancianos residentes en un centro de cuidados (105); y la disponibilidad únicamente de información limitada sobre los intentos de modificar la microflora intestinal mediante la incorporación de fructooligosacáridos a la nutrición por sonda (106).
SITUACIONES ESPECIALES
Diarrea/estreñimiento
(Recomendación 40, grado A, consenso fuerte, 92 % de acuerdo)
Comentario
En un estudio cruzado en el que se investigaba el efecto de la fibra en NE en diez residentes de un centro de cuidados crónicos médicamente estables, se descubrió que con la fibra casi se duplicaban tanto la frecuencia deposicional como el peso húmedo de las heces (ambos p < 0,05), sin diarrea (107). Cuando los residentes israelíes de centros de cuidados de larga estancia recibieron durante un periodo de ocho semanas una nutrición por sonda que contenía fibra, en lugar de una que no la contenía, se observó una reducción en la glucosa y un aumento de la albúmina y la hemoglobina, aunque las dos fórmulas tenían otras diferencias más allá de la fibra, por ejemplo, en la densidad de aminoácidos y micronutrientes (108). Además, los residentes no fueron aleatorizados a una u otra fórmula nutricional. Más recientemente, en una revisión sistemática y un metaanálisis sobre los efectos de la fórmula enteral con fibra tanto en un entorno de enfermedad aguda como de crónicos, se observaron beneficios estadísticamente significativos de la fórmula enteral que contenía fibra (especialmente, mezclas de fibra) para los pacientes con diarrea, así como una tendencia de beneficio de la fórmula enteral que contenía fibra para los pacientes con estreñimiento (109).
(Recomendación 41, grado B, consenso fuerte, 96 % de acuerdo)
Diabetes
43. En los pacientes con diabetes puede utilizarse una fórmula enteral modificada con menor contenido de azúcar, que contenga hidratos de carbono de digestión lenta y un contenido de lípidos enriquecido en ácidos grasos insaturados, especialmente ácidos grasos monoinsaturados.
(Recomendación 42, grado 0, acuerdo mayoritario, 60 % de acuerdo)
Comentario
En los pacientes con diabetes se pueden utilizar formulas específicas con un menor contenido de azúcar, que son comparables a las fórmulas estándar en tolerancia (110). Por ejemplo, se observó una mejoría del control glucémico de los residentes de un centro de larga estancia con diabetes tipo 2 que recibieron una fórmula enteral con un tercio menos de energía procedente de los azúcares (111). Una limitación de este estudio (111) que ya se ha planteado previamente (110) es que no se informó de la proporción de fórmula enteral recibida por cada grupo del estudio. En otro estudio de NE específica para diabetes se observó una disminución tanto en las necesidades de insulina como en la HbA1c tras 84 días en pacientes con diabetes tipo 2 con disfagia neurológica (112). Uno de los pacientes del grupo de nutrición enteral con menos azúcar tuvo diarrea en relación a la fórmula enteral y uno de los pacientes del grupo con formula estándar tuvo una hiperglucemia grave “posiblemente relacionada con el tratamiento”. Una revisión sistemática de fórmulas enterales específicas para diabetes (definidas como suplementos orales o fórmulas enterales que contienen una alta proporción [> 60 %] de lípidos, fructosa y fibra) encontró mejoría del control glucémico en comparación con la fórmula enteral estándar (113).
Para un contenido fijo de azúcar, el aumento del contenido de lípidos y proteínas de la fórmula enteral específica para diabetes puede afectar al control glucémico. Por ejemplo, en una revisión sistemática de los efectos de distintos macronutrientes sobre la glucemia posprandial, se vio que se necesitaba más insulina después de las ingestas ricas en grasas/proteínas (114).
MONITORIZACIÓN Y FINALIZACIÓN DE LA NED (FIG. 11)

Figura 11. Monitorización y finalización de la NED: una visión general. NED: nutrición enteral domiciliaria; CVRS: calidad de vida relacionada con la salud.
¿CUÁNDO Y CÓMO DEBERÍAN SER MONITORIZADOS LOS PACIENTES CON NED? (FIG. 12)
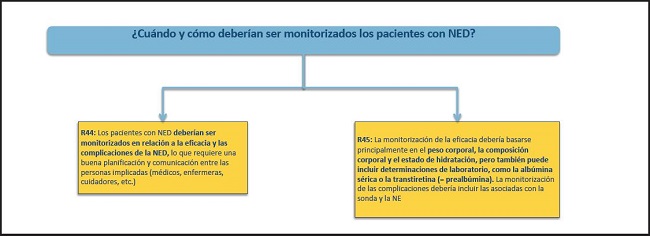
Figura 12. Monitorización y finalización de la NED: ¿cuándo y cómo? NE: nutrición enteral; NED: nutrición enteral domiciliaria.
44. Los pacientes con NED deberían ser monitorizados en relación a la eficacia y las complicaciones de la NED, lo que requiere una buena planificación y comunicación entre las personas implicadas (médicos, enfermeras, cuidadores, etc.).
(Recomendación 44, grado GPP, consenso fuerte, 96 % de acuerdo)
Comentario
La monitorización debería depender de muchos factores, relacionados con el paciente (enfermedad subyacente, estado nutricional al alta, tratamiento activo o cuidados paliativos) y relacionados con la estructura (presencia o ausencia de un equipo multidisciplinar encargado del seguimiento, legislación del país sobre la atención domiciliaria que exige la renovación de la prescripción a determinados intervalos, etc.).
Puede implicar al equipo multidisciplinar prescriptor (médico, dietista, enfermero, farmacéutico), al médico y al enfermero de Atención Primaria, a los cuidadores en domicilio, así como al propio paciente, reforzando la importancia de formar a los pacientes y/o cuidadores en el cuidado de la sonda, en temas de higiene y seguridad y en la resolución de problemas básicos.
45. La monitorización de la eficacia debería basarse principalmente en el peso corporal, la composición corporal y el estado de hidratación, pero también puede incluir determinaciones de laboratorio, como la albúmina sérica o la transtiretina (= prealbúmina). La monitorización de las complicaciones debería incluir las asociadas con la sonda y la NE.
(Recomendación 45, grado GPP, consenso, 83 % de acuerdo)
Comentario
La monitorización se llevará a cabo en el domicilio o en el lugar donde se originó la prescripción. Puede incluir:
– Para la eficacia: peso corporal, composición corporal (masa libre de grasa o masa muscular), hidratación, fuerza y rendimiento muscular, ingesta de alimentos y transtiretina sérica (debido a una vida media mucho más corta que la de la albúmina).
– Para la tolerancia: complicaciones relacionadas con la sonda (fugas, obstrucción, desplazamiento, complicaciones locales del estoma) y tolerancia respiratoria y digestiva.
El seguimiento prospectivo sistemático de una cohorte española de 365 pacientes con NED por diversos motivos mostró, tras un promedio de 148 ± 104 (media ± DE) días, una mejoría de todos los parámetros antropométricos (peso, circunferencia del brazo) y bioquímicos (albúmina, transtiretina, transferrina, linfocitos) (18). En un estudio prospectivo de 150 pacientes de 70 ± 8 años (media ± DE) a los que se les colocó una PEG por varias enfermedades, entre los 72 que sobrevivieron al menos 60 días no hubo cambios significativos en el peso o la albúmina sérica después de cuatro meses (115). Entre los 80 pacientes que fueron aleatorizados para recibir NED complementaria, nutrición parenteral domiciliaria (NPD) o nada después de una cirugía abdominal mayor y que fueron evaluados hasta un año después del alta, hubo una disminución global del peso corporal (aunque con mantenimiento de la masa magra corporal) y un aumento de la albúmina sérica con el tiempo, sin diferencias entre los grupos (116). Un seguimiento a distancia puede resultar útil: un estudio prospectivo de 188 pacientes con NED mayores de 65 años mostró que la incorporación de una consulta telemática con el equipo del hospital a la visita mensual a domicilio permitió reducir las complicaciones metabólicas (117).
FINALIZACIÓN (FIG. 13)
46. La NED debería finalizarse cuando se haya alcanzado el peso deseado y la ingesta oral del paciente se ajuste a sus necesidades de mantenimiento.
(Recomendación 46, grado GPP, consenso fuerte, 92 % de acuerdo)
Comentario
Aparte de los casos de cuidados al final de la vida, hay varias situaciones en las que finalizará la NED:
– Restablecimiento de la nutrición oral.
– Complicación grave (diarrea intratable, neumonía por aspiración), que conlleva una contraindicación prolongada para la NED.
– Traslado a un centro de cuidados de larga estancia.
– Finalización de la NED indicada como nutrición trófica (síndrome del intestino corto).
La primera situación es la más frecuente. Los pacientes pueden evolucionar de la NE total a la NE complementaria y a la autonomía oral completa. Una cohorte de 417 pacientes con NED se sometió a seguimiento durante un periodo de 24 a 103 meses. La NED se había finalizado por fallecimiento en el 75,2 %, por retirada en el 32,6 % y por otros motivos en el 6,7 %; solo el 5,5 % era todavía dependiente de la NED (23). En una cohorte española se observó en 365 pacientes con NED seguidos durante 148 ± 104 días (media ± DE) que era el mismo número de pacientes (47,2 %) el que había recuperado la autonomía oral que el que seguía necesitando la NE (47,8 %) (18). Dos estudios de cohortes regionales reportaron que era mucho más frecuente la recuperación de la autonomía oral en pacientes con enfermedades digestivas que en pacientes con cáncer o enfermedades neurológicas (4,23).
La situación de los cuidados al final de la vida ha sido abordada por la reciente guía de la ESPEN sobre los aspectos éticos de la nutrición e hidratación artificial (27), en la que se dice que “en caso de que la viabilidad o eficacia de la nutrición artificial sea incierta, es aconsejable administrar el tratamiento a modo de prueba. En caso de complicaciones o si no se consigue el éxito deseado, debería suspenderse el intento”.
MANEJO DE LAS COMPLICACIONES (FIG. 14)
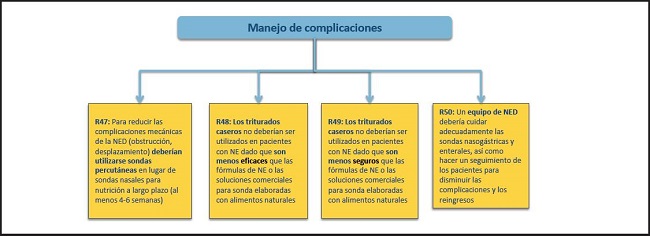
Figura 14. Monitorización y finalización de la NED. Manejo de complicaciones. NE: nutrición enteral; NED: nutrición enteral domiciliaria.
47. Para reducir las complicaciones mecánicas de la NED (obstrucción, desplazamiento) deberían utilizarse sondas percutáneas en lugar de sondas nasales para nutrición a largo plazo (al menos 4-6 semanas).
(Recomendación 47, grado B, consenso fuerte, 98 % de acuerdo)
Comentario
Las complicaciones de la NE en general se aplican a los pacientes con NED y pueden ser clasificadas como complicaciones mecánicas, aspirativas, gastrointestinales, metabólicas y del estoma. La frecuencia de estas complicaciones se ha evaluado en varios estudios retrospectivos y prospectivos que han incluido diferentes tipos de pacientes y de accesos enterales (118-121). En una revisión sistemática Cochrane, la nutrición a través de una PEG demostró una menor probabilidad de fracaso de intervención (definida como interrupción de la nutrición, obstrucción o fuga de la sonda, o falta de adherencia al tratamiento), lo que sugiere que el procedimiento endoscópico es más eficaz y seguro que la nutrición por sonda nasogástrica (121).
Las complicaciones mecánicas tales como el desplazamiento y la obstrucción de las sondas son más frecuentes en las sondas nasales, especialmente en las nasoyeyunales, que en las sondas PEG (118). En los casos de obstrucción persistente, algunos expertos, pero no todos, recomiendan la infusión con bebidas carbonatadas que contienen cola o enzimas pancreáticos para desobstruir la sonda (122). Sin embargo, esta maniobra no es recomendable por varias razones; una de ellas es que el contenido de azúcar de los refrescos aumenta el riesgo de contaminación bacteriana de la sonda. Otros recomiendan el uso de una solución de bicarbonato sódico al 8,4 % para desobstruir la sonda; sin embargo, esto tampoco es medicina basada en la evidencia. Si es necesario, y en manos expertas, se podría utilizar una guía metálica o un dispositivo comercial para desobstruir en el caso de sondas PEG (38). La aspiración puede ocurrir en pacientes que no son capaces de proteger sus vías respiratorias, especialmente los pacientes con problemas neurológicos. Se ha informado que la incidencia de aspiración alcanza el 20 % y se han estudiado varias estrategias para reducir la aspiración. Estas incluyen la elevación de la cabecera de la cama, la nutrición pospilórica (por vía nasoyeyunal, gastroyeyunostomía percutánea o PEJ) y la administración de agentes procinéticos para estimular el vaciado gástrico (38,122). Las complicaciones gastrointestinales incluyen estreñimiento, diarrea, vómitos y dolor abdominal. Estas complicaciones pueden estar causadas por la enfermedad subyacente, el tratamiento farmacológico, la fórmula enteral y el método de administración (38,122). Las complicaciones metabólicas incluyen hiperglucemia, alteraciones electrolíticas, deficiencia de micronutrientes y síndrome de realimentación (38,122). Las complicaciones del estoma son frecuentes en los pacientes con gastrostomía e incluyen exceso de tejido de granulación, fugas, infección periestomal y BBS (38,52).
48. No deberían utilizarse triturados caseros en pacientes con NE dado que son menos eficaces que las fórmulas de NE o las soluciones comerciales para sonda elaboradas con alimentos naturales.
(Recomendación 48, grado GPP, acuerdo mayoritario, 63 % de acuerdo)
Comentario
Véase el comentario a la recomendación 49.
49. No deberían utilizarse triturados caseros en pacientes con NE dado que son menos seguros que las fórmulas de NE o las soluciones comerciales para sonda elaboradas con alimentos naturales.
(Recomendación 49, grado GPP, consenso, 76 % de acuerdo)
Comentario
Las soluciones de triturados caseros son todavía populares en muchos países debido a su bajo coste en comparación con la fórmula enteral. Sin embargo, dichas soluciones no están estandarizadas en cuanto a la composición de macronutrientes y micronutrientes y pueden suponer un mayor riesgo de contaminación, así como una manipulación y una administración más engorrosas (123). En un estudio observacional, el uso de una fórmula enteral y de un ESN en comparación con las soluciones de triturados mejoró el peso y disminuyó las complicaciones infecciosas, los ingresos hospitalarios y los costes, pero no tuvo ningún efecto sobre otras complicaciones (124).
Véase también la recomendación 39.
50. Un equipo de NED debería cuidar adecuadamente las sondas nasogástricas y enterales, así como hacer un seguimiento de los pacientes para disminuir las complicaciones y los reingresos.
(Recomendación 50, grado B, consenso fuerte, 100 % de acuerdo)
Comentario
La formación adecuada del paciente/cuidador y la continuidad de los cuidados tras el alta hospitalaria son factores clave para el éxito de la NED (125). La mayoría de las complicaciones potenciales a largo plazo dependen exclusivamente de la calidad de los cuidados posteriores de las sondas y pueden evitarse eficazmente si se toman las medidas adecuadas. En un estudio prospectivo que incluyó a 108 pacientes de edad avanzada en Italia, con un seguimiento de 12 meses, los autores constataron una baja tasa de complicaciones, la mayoría de ellas leves. La mortalidad tras el primer mes y al año fue del 7,4 % y 23,1 %, respectivamente, con una supervivencia media de 674 días, que es casi tres veces mayor que la de la literatura. Los autores atribuyen sus mejores resultados respecto a otras series de pacientes a la continuidad de los cuidados por parte del mismo equipo de nutrición (126). En una investigación cuasi experimental realizada en Taiwán con evaluaciones antes y después en 233 pacientes con nutrición por sonda nasogástrica, la intervención sistemática de enfermería, que incluía folletos educativos detallados y educación a través de vídeos, en comparación con la educación habitual mejoró significativamente los conocimientos y las habilidades de los cuidadores principales y disminuyó la incidencia de complicaciones a los tres meses (127). En ausencia de un cuidado adecuado de la gastrostomía, las tasas de reingreso hospitalario a los seis meses alcanzaban el 23 %. En un estudio prospectivo de 313 pacientes con gastrostomía seguidos por un equipo de NED, se presentaron 371 complicaciones y la mayoría se resolvieron sin hospitalización. Los reingresos hospitalarios relacionados con la gastrostomía se redujeron significativamente del 23 al 2 % (p < 0,0001) (128).
EVALUACIÓN DE LA CVRS (FIG. 15)

Figura 15. Monitorización y finalización de la NED. Evaluación de la CVRS. NED: nutrición enteral domiciliaria; CVRS: calidad de vida relacionada con la salud.
(Recomendación 51, grado GPP, consenso fuerte, 92 % de acuerdo)
Comentario
La CVRS es uno de los resultados relacionados con el paciente necesarios para evaluar el efecto de los tratamientos. La NED tiene un efecto considerable física, social y psicológicamente en la vida de los pacientes y sus cuidadores. El apoyo en el momento de la colocación de la sonda, y de manera regular y continua, puede ayudar a minimizar el impacto en ambos, permitiéndoles aprovechar al máximo su vida diaria, dormir mejor y disfrutar de una mayor CVRS en general (129).
La CVRS debería medirse al inicio de la NED y periódicamente durante el tratamiento para evaluar el impacto de esta intervención. En estos pacientes se ha investigado la CVRS utilizando principalmente cuestionarios genéricos, como el SF-36, el SF-12, el CVRS-BREF de la Organización Mundial de la Salud (OMS) y el EQ-5D, con un resultado inferior al de la población general. Entre los principales factores que pueden influir en la CVRS del paciente con NED se encuentran la enfermedad subyacente, la edad, el sexo y la presencia del cuidador. Además, la evaluación del cuidador puede ser útil para tener una aproximación a la percepción del paciente cuando este no tiene capacidad de comunicarse (130).
52. Para evaluar la CVRS de los pacientes con NED, deberían utilizarse cuestionarios específicos validados.
(Recomendación 52, grado GPP, consenso, 88 % de acuerdo)
Comentario
Las Medidas de Resultados Comunicadas por los Pacientes deberían desarrollarse mediante un proceso estandarizado (131). El proceso de validación de estas herramientas conlleva la medición de las siguientes propiedades psicométricas (viabilidad, fiabilidad o reproductibilidad, respuesta, determinación de la diferencia mínima clínicamente significativa y validez). Para medir la CVRS en pacientes con NED podemos utilizar cuestionarios genéricos o específicos. Las herramientas genéricas carecen de sensibilidad para reflejar los problemas de los pacientes y las diferencias en la CVRS entre subgrupos según las enfermedades o durante el seguimiento. Los cuestionarios específicos se elaboran a partir de los síntomas, limitaciones y problemas de los pacientes en su vida diaria y son más sensibles a los cambios. Para estudiar la CVRS en la NED, algunos autores han utilizado cuestionarios específicos para diferentes patologías como el IBDQ, el QOL-EF de cáncer de cabeza y cuello y el EORTC QLQ-C30 (132,133). Existen otros cuestionarios específicos para la PEG, pero con algunas limitaciones metodológicas. En un estudio multicéntrico en población española que incluyó 355 sujetos, se validó un cuestionario específico para evaluar la CVRS en pacientes con NED. Este cuestionario, NutriQoL®, consta de 17 ítems y evalúa la CVRS en dos dimensiones (rendimiento físico, actividades de la vida diaria y aspectos sociales). Este cuestionario es válido, fiable y, aunque poco sensible al cambio, parece ser útil para medir la CVRS en esta población (134,135).
REQUISITOS ESTRUCTURALES PARA REALIZAR LA NED (FIG. 16)

Figura 16. Necesidades estructurales para llevar a cabo la NED: una visión general. NED: nutrición enteral domiciliaria; ESN: equipo de soporte nutricional.
EDUCACIÓN Y ESN (FIG. 17)
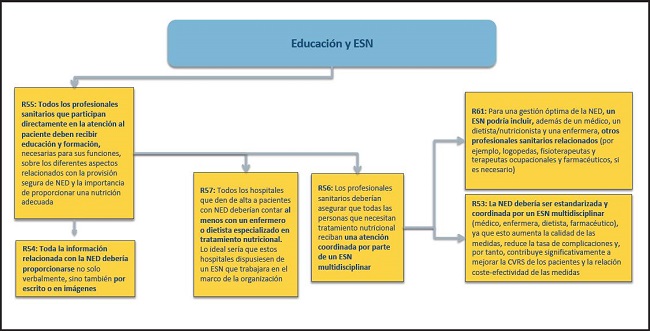
Figura 17. Necesidades estructurales. Educación y ESN. NED: nutrición enteral domiciliaria; ESN: equipo de soporte nutricional; CVRS: calidad de vida relacionada con la salud.
53. Todos los profesionales sanitarios que participan directamente en la atención al paciente deben recibir educación y formación, necesaria para sus funciones, sobre los diferentes aspectos relacionados con la provisión segura de NED y la importancia de proporcionar una nutrición adecuada.
(Recomendación 55, grado B, consenso fuerte, 100 % de acuerdo)
Comentario
El número de pacientes que reciben NED ha aumentado considerablemente en los últimos años (75). Se calcula que actualmente hay más del doble de pacientes que reciben NE en la comunidad que los que la reciben en el hospital (136). La NED es una terapia compleja y debería ser monitorizada de manera próxima (136); de no ser así, se podrían producir complicaciones graves, como neumonía por aspiración, desplazamiento de la sonda, complicaciones gastrointestinales, etc. El tratamiento suele iniciarse en Atención Especializada, pero los médicos de Atención Primaria también pueden remitir pacientes para NED electiva con inserción de una sonda de nutrición de forma ambulatoria. Las sondas de gastrostomía son las vías de acceso más fáciles de manejar en la comunidad. Todos los hospitales que den de alta a pacientes con NED deberían disponer de al menos una enfermera especializada en tratamiento nutricional y una dietista (137). Estos hospitales deberían contar con una comisión de nutrición que proporcionase protocolos para una NED segura. La composición de este equipo puede variar según el entorno y las disposiciones locales, pero debería estar formado al menos por un médico, un dietista, una enfermera de soporte nutricional y, si es posible, un farmacéutico y un fisioterapeuta. La estrecha colaboración con el médico de Atención Primaria es importante para el seguimiento y en caso de complicaciones. Es recomendable la intervención educativa (por ejemplo, tres cursos modulares de una semana durante seis meses) (125) para todos los profesionales sanitarios, en particular, personal médico, dietistas y enfermeras, incluidos aquellos que trabajan con personas con demencia. El efecto sobre el cuidado de los pacientes (estado nutricional, duración de la estancia en el hospital, frecuencia de las visitas del médico de Atención Primaria, complicaciones y CVRS) debería compararse con la ausencia de educación formal (129). La mayoría de los países cuentan con empresas de servicios (“proveedores de atención domiciliaria”) que proporcionan a los pacientes en domicilio las fórmulas enterales, las bombas y el material fungible (138). El reembolso de los productos enterales, los fungibles y el alquiler de las bombas debería discutirse con las compañías de seguros o con el Gobierno para poder proporcionar la NED a todos los pacientes (138,139).
54. Toda la información relacionada con la NED debería proporcionarse no solo verbalmente, sino también por escrito o en imágenes.
(Recomendación 54, grado B, consenso fuerte, 100 % de acuerdo)
Comentario
Cada vez es mayor el número de pacientes adultos que necesitan continuar la nutrición enteral tras el alta hospitalaria (75,136). La NED hace referencia a la nutrición proporcionada en el domicilio del paciente a través de una sonda de nutrición directamente en el tracto gastrointestinal cuando un individuo no puede ingerir, masticar o tragar alimentos, pero puede digerir y absorber los nutrientes. Permite al paciente volver a su entorno familiar, en el que el propio paciente puede continuar la nutrición enteral y donde la familia, los amigos o los cuidadores profesionales pueden prestarle apoyo (84,85). La prescripción debería realizarse en el entorno hospitalario o en el domicilio. Se debería proporcionar información escrita que incluya vías de contacto en caso de que se produzcan complicaciones y/o se necesiten más aclaraciones (129,137-140).
55. Todos los hospitales que den de alta a pacientes con NED deberían contar al menos con un enfermero o dietista especializado en tratamiento nutricional. Lo ideal sería que estos hospitales dispusiesen de un ESN que trabajara en el marco de la organización.
(Recomendación 57, grado B, consenso fuerte, 96 % de acuerdo)
Comentario
Véase el comentario a la recomendación 53.
56. Los profesionales sanitarios deberían asegurar que todas las personas que necesitan tratamiento nutricional reciban una atención coordinada por parte de un ESN multidisciplinar.
(Recomendación 56, grado B, consenso fuerte, 100 % de acuerdo)
Comentario
Véase el comentario a la recomendación 53.
57. Para una gestión óptima de la NED, un ESN podría incluir, además de un médico, un dietista/nutricionista y una enfermera, otros profesionales sanitarios relacionados (por ejemplo, logopedas, fisioterapeutas y terapeutas ocupacionales y farmacéuticos, si es necesario).
(Recomendación 61, grado GPP, consenso fuerte, 97 % de acuerdo)
Comentario
El equipo de NED da apoyo a los pacientes que se alimentan a través de una sonda de nutrición enteral en la comunidad. Sin embargo, la organización de los servicios de apoyo al creciente número de personas que reciben NED varía según las regiones. Las guías del National Institute for Health and Care Excellencce (NICE) de Reino Unido señalan que las personas que reciben NED en la comunidad deberían “recibir el soporte de un equipo multidisciplinar coordinado” (136). Parece que un modelo de coordinación de cuidados estandarizado que incluya un equipo multidisciplinar podría mejorar los resultados y reducir los costes relacionados con la atención sanitaria. No obstante, no se dispone de datos suficientes para determinar específicamente el grado de eficacia de dicha intervención o la composición del equipo. Los beneficios de introducir en la comunidad los ESN vienen principalmente de trabajo observacional, que ha permitido contemplar beneficios (por ejemplo, las auditorías realizadas tras la introducción de control por expertos de la NED) en cuanto a reducción de costes y mejoría de los resultados. Los miembros del equipo multidisciplinar más mencionados en diferentes países fueron las enfermeras y las dietistas, mientras que también se incluyeron en la mayoría de los diferentes enfoques de un equipo multidisciplinar los médicos de Atención Primaria y médicos especialistas. En algunos casos, también se consideraron logopedas y otros trabajadores sanitarios (141).
58. La NED debería ser estandarizada y coordinada por un ESN multidisciplinar (médico, enfermera, dietista, farmacéutico), ya que esto aumenta la calidad de las medidas, reduce la tasa de complicaciones y, por tanto, contribuye significativamente a mejorar la CVRS de los pacientes y la relación coste-efectividad de las medidas.
(Recomendación 53, grado B, consenso fuerte, 96 % de acuerdo)
INFRAESTRUCTURA (FIG. 18)
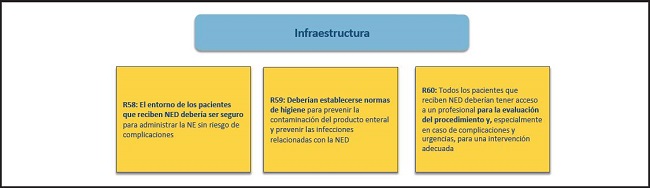
Figura 18. Necesidades estructurales. Infraestructura. NE: nutrición enteral; NED: nutrición enteral domiciliaria.
59. El entorno de los pacientes que reciben NED debería ser seguro para administrar la NE sin riesgo de complicaciones.
(Recomendación 58, grado B, consenso fuerte, 100 % de acuerdo)
Comentario
Véase el comentario a la recomendación 53.
60. Deberían establecerse normas de higiene para prevenir la contaminación del producto enteral y prevenir las infecciones relacionadas con la NED.
(Recomendación 59, grado GPP, consenso fuerte, 100 % de acuerdo)
Comentario
Véase el comentario a la recomendación 53.
61. Todos los pacientes que reciben NED deberían tener acceso a un profesional para la evaluación del procedimiento y, especialmente en caso de complicaciones y urgencias, para una intervención adecuada.
(Recomendación 60, grado GPP, consenso fuerte, 100 % de acuerdo)