Introducción
Las particularidades anatómicas de las falanges de la mano de cara a un procedimiento quirúrgico reconstructivo representan un reto muy importante cuando se intenta como objetivo primordial la rehabilitación funcional temprana empleando maniobras técnicas lo más anatómicas posible para solventar el defecto creado. La limitada cobertura periósea de partes blandas disponible en los dedos, la contigüidad con los paquetes neurovasculares y las estructuras mecánicas funcionales, requieren de una identificación fina y precisa con instrumentación y, lo que aún es más importante, de su preservación durante el procedimiento quirúrgico para conseguir la mejor oportunidad de una rehabilitación postoperatoria temprana.
Entre los tumores que pueden afectar a las falanges, el encondroma es el tumor primario que representa hasta alrededor de los dos tercios de las lesiones óseas en manos y dedos. Casi siempre son tumores únicos, pero se pueden encontrar 2 o más falanges afectadas, siendo las proximales y medias las más frecuentes afectadas. Es relativamente más común en hombres que en mujeres y con frecuencia aparece entre la primera y la cuarta décadas de la vida, aunque no necesariamente ocurre en la etapa de crecimiento.(1,2)
Entre las características clínicas habituales de presentación de un encondroma está un crecimiento gradual asintomático, habitualmente en metáfisis o diáfisis de la falange proximal y adyacente a la placa epifisiaria considerada como fuente de cartílago del origen fenotípico tumoral. Se acompaña de la sustitución del tejido óseo medular de la falange afectada por un tejido de tipo mixoide que adelgaza y expande la estructura cortical que la rodea sin invadir tejidos circundantes y que constituye frecuentemente la evidencia histopatológica obtenida en casi todos los casos. Adicionalmente, también puede presentarse clínicamente como una fractura patológica por la debilidad estructural de la cortical de la falange, en cuyo caso se acompaña de dolor e incapacidad funcional.
El diagnóstico suele hacerse mediante una radiografía simple que muestra la lesión lítica medular, expansiva. con cortical preservada y sin invasión de la misma ni de los tejidos blandos circundantes, característica que lo distingue de su contraparte histológica, la de un raro tumor maligno, el condrosarcoma.
Los encondromas tienen gran actividad mitótica en la parte sólida de la deformidad tumoral y suele ser difícil la diferencia aparente con el tejido óseo no afectado, por lo que no resulta tan fácil la resección tumoral precisa. En el interior del encondroma aparece un tejido de tipo mixoide muy característico, con elementos celulares de fenotipo cartilaginoso con escasa celularidad en los márgenes del tumor, donde el tejido fibrótico de septums y márgenes establece la diferencia con la normalidad del tejido óseo no afectado.(3)
El abordaje quirúrgico más aceptado en los defectos mayores, hasta el momento, es la resección del tumor sólido incluyendo márgenes tumorales adecuados y el curetaje medular meticuloso, extrayendo todo el tejido tumoral de sustitución medular.(2,4)
Presentamos en este artículo la técnica quirúrgica de resección tumoral y reconstrucción posterior de falange que hemos empleado en 2 casos clínicos representativos de encondroma en dedo de mano, resueltos satisfactoriamente con la sistematización técnica que proponemos a base de: resección tumoral adecuada y curetaje, manejo de la inestabilidad residual mediante injerto óseo autólogo y osteosíntesis rígida, e integración temprana del tejido óseo autólogo de reemplazo utilizando factores de crecimiento de origen plaquetario, todo ello con vistas a conseguir una recuperación funcional temprana del paciente sin los inconvenientes conocidos de la inmovilización prolongada.(5)
Material y método
Técnica quirúrgica
Realizamos el abordaje quirúrgico del encondroma digital sobre el aspecto dorsal de la falange afectada, siguiendo un diseño individualizado para cada paciente que permita preservar las venas de drenaje con el fin de evitar la congestión venosa distal en el área quirúrgica; tenemos la misma consideración para la circulación arterial circunfleja periarticular. Continuamos con disección subperióstica de acuerdo a la región afectada por el tumor, con liberación amplia del aparato extensor dorsal. La resección tumoral, planificada de acuerdo con las imágenes diagnósticas, la llevamos a cabo de manera muy precisa con sierra neumática oscilatoria y gubia fina, preservando, cuando las condiciones encontradas lo permiten, un remanente de cortical palmar sin compromiso tumoral macroscópico para orientación del injerto óseo a emplear en la reconstrucción ulterior de la falange, y preservando el mecanismo de los tendones flexores y extensores no afectados por la lesión tumoral. Proseguimos con un curetaje exhaustivo de la cavidad, retirando todo el tejido mixoide tumoral hasta encontrar cortical de aspecto macroscópico aparentemente no comprometido.
Medimos el defecto creado quirúrgicamente y la longitud que consideramos apropiada para la reconstrucción de sustitución, y diseñamos con iguales medidas y forma sobre la cortical externa del hueso ilíaco como fuente donadora de un injerto óseo monocortical. Tomamos el injerto óseo levantando un segmento articulado medialmente de la cresta ilíaca y por debajo del borde superior para no crear deformidad residual en el área donante, manteniendo en el injerto una sola cortical, la externa, para la estabilización ósea posterior con placa y tornillos de un sistema de titanio de fijación rígida de mano, en el cual los tornillos característicamente se introducen dentro de la placa para no afectar a los desplazamientos tendinosos. Finalmente, dejamos en el sitio donante un drenaje aspirativo muy fino construido con perforaciones a partir del tubo plástico de una mariposa o aguja hipodérmica y una jeringa con vacío sostenido. Tras vaciar el drenaje al final del procedimiento, introducimos a través del mismo una solución anestésica y vasoconstrictora para reducir el sangrado y las molestias postoperatorias durante 1 o 2 días, cuando los analgésicos orales serán ya suficientes. Practicamos perforaciones en la cortical del injerto por fuera del sitio de aplicación de la placa de osteosíntesis para favorecer la conexión microvascular con el hueso esponjoso subyacente a la cortical del injerto. Colocamos el injerto en el defecto entre los dos remanentes, proximal y distal, resultantes después de la resección tumoral y realizamos la osteosíntesis rígida entre los 3 componentes para conseguir una condición estable y funcional inmediata.
Una vez estabilizada la falange reconstruida, aplicamos el plasma rico en plaquetas (PRP) previamente obtenido de 10 cc de sangre periférica del paciente que producen aproximadamente 5-6 cc de PRP. Empleamos para ello los tubos y el sistema de centrifugación RegenLab® (Lausanne, Suiza): 3500 revoluciones por minuto (rpm) durante 5 minutos, con una inclinación de 45°. De esta forma agregamos al ambiente tisular del injerto los factores de crecimiento coadyuvantes para propiciar el proceso de integración del injerto óseo y su permanencia posterior.
Finalmente examinamos la funcionalidad del dedo afectado y procedemos a reconstruir adecuadamente los ligamentos de estabilidad articular. Reparamos la incisión de abordaje en dos planos de sutura. En el postoperatorio inmediato mantenemos la mano en posición elevada durante 5 días antes de iniciar la movilización gradual pasiva y activa de flexión y extensión de las articulaciones metacarpo-falángica e interfalángica proximal. Conseguimos de esta forma una recuperación funcional suficiente antes de los 2 meses de postoperatorio.
Casos clínicos
Presentamos a modo de ilustración del procedimiento descrito, 2 casos clínicos de reconstrucción autóloga de falange tras resección por encondroma.
Caso 1
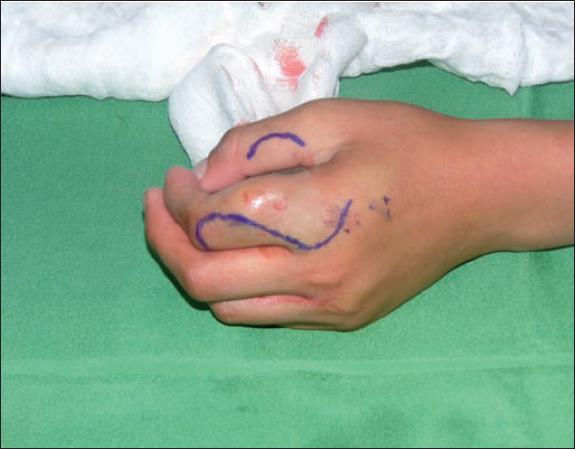
Varón de 56 años de edad que acude a consulta con un inmovilizador de mano. Tenía antecedente de tumoración de falange proximal del segundo dedo de la mano izquierda, no dominante, que había sido tratada de forma conservadora por un médico ortopeda durante 3 años sin justificación terapéutica alguna (Fig. 1). La tumoración presentaba en ese momento unas dimensiones de aproximadamente 38 x 20 mm de diámetro mayor longitudinal, que afectaba prácticamente a las tres cuartas partes de falange. El crecimiento había sido gradual hasta que se produjo una fractura patológica durante un esfuerzo menor de prensión, la cual fue confirmada por radiografía simple. Dado que se trataba de una fractura patológica, que no podía curar por el problema de base, programamos al paciente para intervención quirúrgica planificada (Fig. 2).
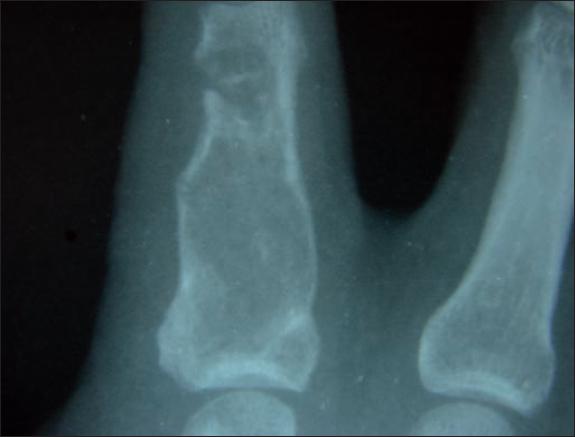
Fig. 1 Caso 1. Varón de 56 años de edad. Tumoración lítica medular sin afectación de partes blandas en falange proximal de segundo dedo mano izquierda.
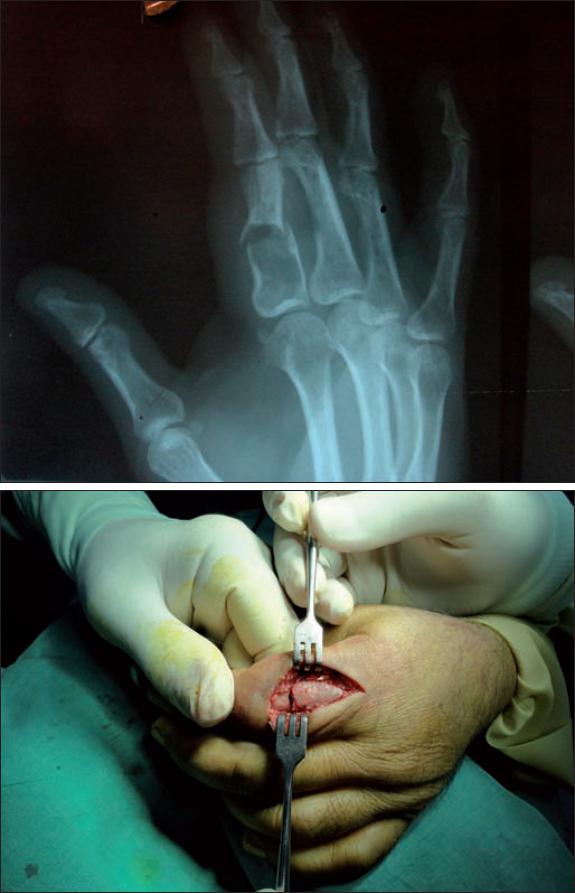
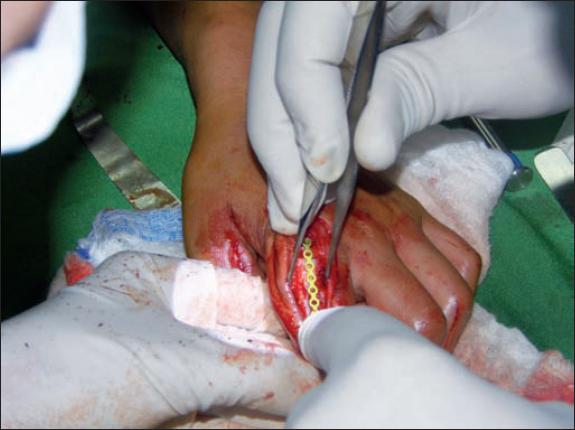
Fig. 2 A) Imagen radiológica de la fractura patológica. B) Disección subperióstica e identificación de la fractura diafisiaria de la falange proximal.
Mediante sedación intravenosa a demanda, isquemia con torniquete sin exanguinación que se mantuvo durante 35 minutos y bloqueo proximal de nervios radial y mediano, llevamos a cabo el procedimiento quirúrgico descrito. El defecto óseo resultante fue de 43 x 25 mm (Fig. 3).
Para la obtención del injerto óseo de hueso ilíaco empleamos infiltración local de solución anestésica vasoconstrictora con bloqueo proximal de inervación periférica sensitiva. Conseguimos la osteosíntesis con una placa de mano de titanio en forma de L de 6 orificios y 5 tornillos que proporcionó la estabilidad necesaria entre los 3 elementos óseos: remanente óseo proximal, injerto óseo interpuesto y remanente óseo distal, obteniendo así una reconstrucción anatómica de la falange proximal.
Una vez estabilizada la falange inyectamos 5 cc de PRP introduciéndolo con aguja a través de las perforaciones de la cortical del injerto y aplicándolo también en el área quirúrgica circundante al injerto.
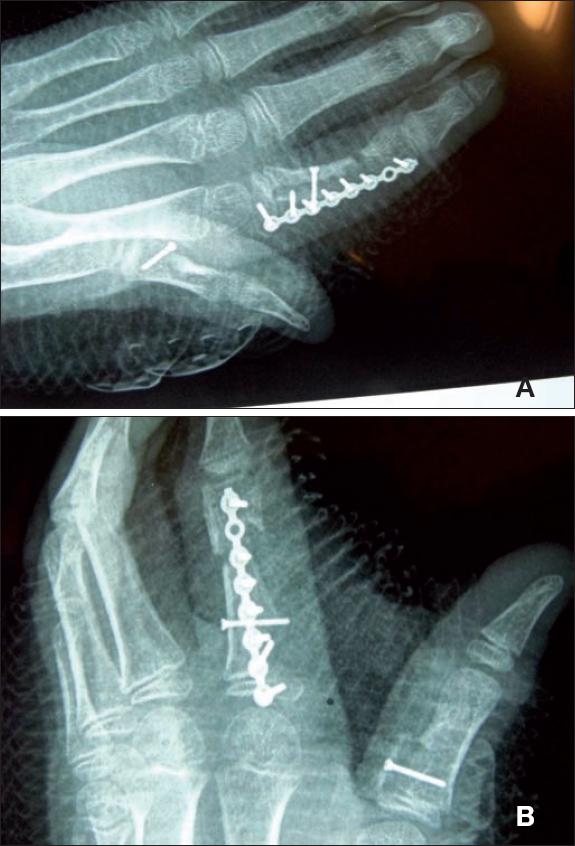
El control radiológico postoperatorio inmediato y a los 12 meses mostró consolidación adecuada e imágenes de trabeculación ósea de aspecto normal, lo que es suficientemente demostrativo de la integración del injerto para ese momento (Fig. 4).
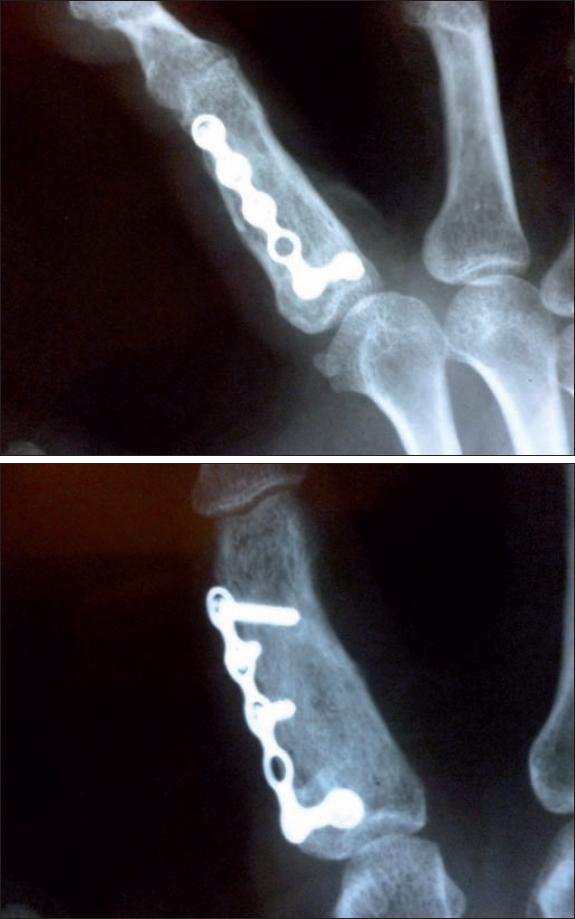
Fig. 4 A) Vista dorsal de la placa de osteosíntesis. B) Vista lateral. Ambas muestran integración completa del injerto óseo a los 12 meses de postoperatorio.
El informe del estudio anatolopatológico comprobó el diagnóstico de encondroma. El examen físico de la mano reveló un resultado funcional satisfactorio antes de los 2 meses de la intervención, El seguimiento de 2 años de postoperatorio se mantiene sin evidencia de recidiva tumoral ni de alteraciones funcionales.
Caso 2
Varón de 12 años de edad evaluado durante una brigada humanitaria de Cirugía Reconstructiva, que presentaba crecimiento tumoral de la falange proximal del dedo índice izquierdo de aproximadamente 2 años de evolución, a quien previamente en otro hospital se le había ofrecido una amputación del segundo rayo como único tratamiento posible.
La radiografía simple mostró evidencia de una tumoración lítica medular compatible con encondroma que afectaba a la mayoría anatómica de la falange proximal del segundo dedo, de 33 mm en sentido longitudinal y 22 mm en sentido transversal. La tumoración mostraba crecimiento mayor hacia los aspectos radial y dorsal, con acortamiento comparativo con el dedo índice del lado sano de 3-4 mm y con considerable afectación medular de la falange. La segunda imagen tumoral detectada afectaba únicamente a la cortical ulnar y tenía de 7 a 9 mm de diámetro, sin aparente sustitución tumoral medular (Fig. 5).
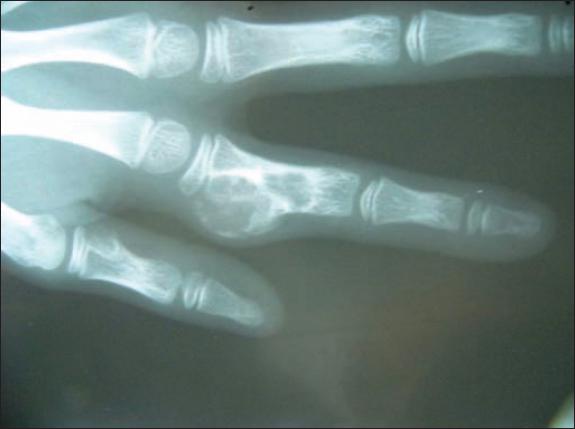
Fig. 5 Caso 2. Varón de 12 años de edad. Imagen radiológica de las tumoraciones de falange proximal del primer y segundo dedos mano izquierda.
Bajo anestesia general y bloqueo de los nervios radial y mediano, con isquemia de 45 minutos, realizamos disección y resección planificada y precisa de la masa tumoral que se originaba de la placa epifisaria en sus lados dorsal y radial y se extendía hasta la metáfisis distal de la falange proximal del segundo dedo; empleamos para ello una sierra neumática oscilatoria de hoja fina por sus ventajas técnicas de precisión. A continuación practicamos curetaje meticuloso del tejido de sustitución medular de tipo mixoide, y en el remanente cortical ulnar palmar practicamos una osteotomía transversal para conseguir elongación con el injerto óseo debido al acortamiento de 3 mm diagnosticado en el preoperatorio, que consideramos provocaba una importante afectación funcional. El defecto originado fue en total de unos 38 mm (Fig. 6 y 7).
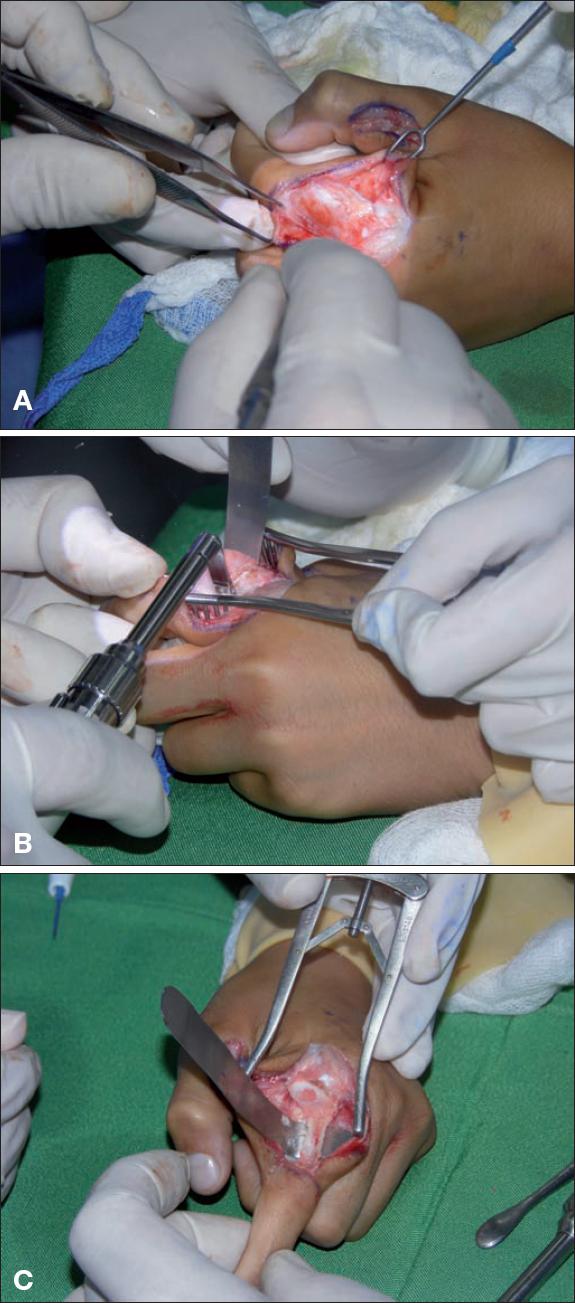
Fig. 7 A) Disección subperióstica y preservación del aparato extensor. B) Resección tumoral con sierra oscilatoria. C) Resección completa con preservación de la cortical del lado ulnar para guía de colocación del injerto óseo de cresta ilíaca con FCOP.
Llevamos a cabo la estabilización del conjunto óseo mediante una placa lineal de 8 orificios y 7 tornillos, ya que el volumen óseo residual de la epífisis tras la resección permitía colocar 1 solo tornillo en situación proximal al defecto. Adicionalmente colocamos 1 tornillo en orientación transversal con técnica de compresión interfragmentaria para lograr una mayor estabilización entre el injerto y el remanente cortical proximal del lado radial preservado como guía direccional. Colocamos también un injerto óseo estabilizado en la tumoración de la base de la falange proximal del primer dedo, empleando os-teosíntesis mediante técnica de compresión interfragmentaria con 1 solo tornillo. Finalmente colocamos entre 5- 6 cc de PRP dentro y alrededor de los injertos óseos y finalizamos la reconstrucción de forma similar a lo descrito en el caso anterior (Fig. 8 y 9).
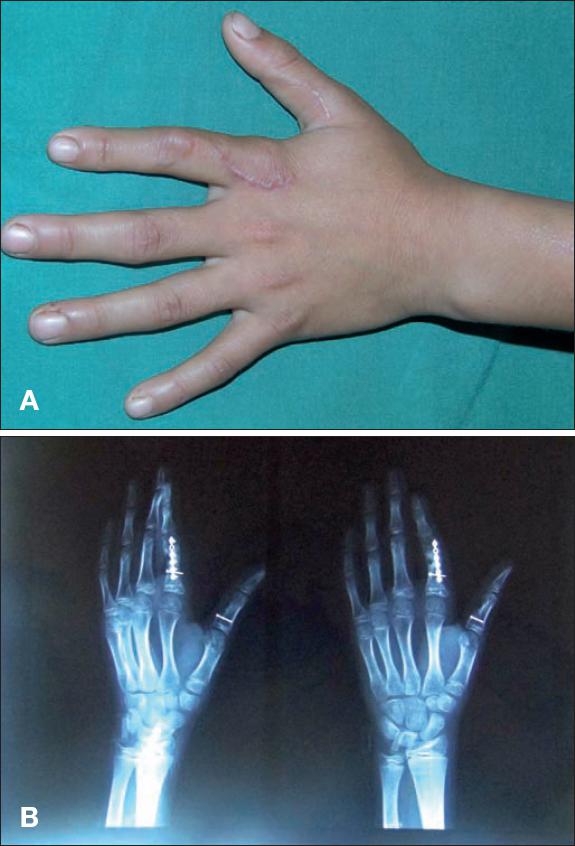
Dado que el paciente estaba en etapa de crecimiento, en un segundo tiempo quirúrgico, a los 15 meses de post-operatorio y una vez comprobada tanto clínica como radiológicamente la integración del injerto óseo que proveía suficiente estabilidad, decidimos retirar el tornillo de la epífisis porque frenaba la posibilidad de crecimiento de la falange. A pesar de una discreta angulación radial del dedo, que no pudimos corregir, la funcionalidad a los 2 meses de postoperatorio resultó ser suficientemente satisfactoria y el paciente precisó de poco tiempo para su rehabilitación. El seguimiento a los 2 años sigue siendo también satisfactorio y sin recidivas (Fig. 10).
Discusión
El defecto mayor creado por la resección de un encondroma benigno de falange proximal, cuando es necesario sacrificar la mayoría de la masa estructural ósea por un compromiso mayor, es altamente disfuncional y plantea difíciles alternativas reconstructivas. Presentamos a consideración un protocolo sencillo, viable y sistematizado, basado en 3 maniobras técnicas que en conjunto proporcionan la posibilidad de obtener resultados favorables de reconstrucción en condiciones clínicas difíciles y similares.
En primer lugar, consideramos determinante planificar estrictamente la resección tumoral de acuerdo con las imágenes diagnósticas obtenidas, que no necesariamente coinciden con la manifestación clínica de apariencia macroscópica transoperatoria de la lesión. Los encondromas tienen una gran actividad mitótica en la parte sólida de la deformidad tumoral y suele ser difícil la diferencia aparente con el tejido óseo no afectado; por ello no resulta tan fácil su resección tumoral precisa. En el interior del encondroma existe un tejido de tipo mixoide muy característico, con elementos celulares de fenotipo cartilaginoso con escasa celularidad en los márgenes del tumor, donde el tejido fibrótico de septums y márgenes establece la diferencia con la normalidad del tejido óseo no afectado.(3) La resección del tumor sólido, incluyendo márgenes tumorales adecuados y el curetaje medular meticuloso para extraer todo el tejido tumoral de sustitución medular, es el abordaje quirúrgico más aceptado hasta el momento para los defectos mayores.(2,4) Sin embargo, al realizar este procedimiento resulta invariablemente un remanente de estructura ósea muy debilitado o sin la rigidez funcional suficiente de soporte, por lo que se hace necesario un injerto óseo con características reconstructivas de reemplazo apropiadas. Este injerto puede ser de volumen y longitud considerables para lograr una sustitución completa dentro del defecto creado, y dentro de nuestro protocolo integral de cuidados específicos, creemos que debe ser estabilizado de forma rígida para permitir la integración tisular ósea y la rehabilitación funcional temprana del paciente, a diferencia del pobre resultado que proporciona una prolongada inmovilización y de sus conocidas consecuencias.(5)
Actualmente se acepta que la angiogénesis de reconstrucción tisular es la base de la integración de un injerto óseo dentro del lecho receptor, el cual debe ofrecer un ambiente bioquímico tisular con condiciones apropiadas para que el proceso natural de curación se efectúe en su primera y segunda fases.(6) El bajo metabolismo tisular del injerto libre no revascularizado de tejido óseo sobrevivirá inicialmente por imbibición, y en los primeros días, en circunstancias apropiadas, se establecen las conexiones de la microcirculación, condicionadas por la presencia de los factores de crecimiento tisular existentes.(7) Sabemos con certeza suficiente que el fenómeno de la angiogénesis se puede ver facilitado con la aplicación de Factores de Crecimiento de Origen Plaquetario (FCOP) obtenidos con la apropiada separación de plasma sanguíneo autólogo, preferentemente y de manera fundamental sin la presencia de glóbulos blancos, ya que estos desencadenan un proceso inflamatorio innecesario en estas condiciones.(8-10) Esto se consigue con un tubo de procesamiento que particularmente contenga un gel selectivo mediante el cual, al centrifugar la sangre, se separen de forma efectiva los componentes de importancia biológica, los glóbulos rojos y blancos, pero sin un arrastre mecánico de las plaquetas que por su bajo peso no pueden atravesarlo en la fuerza G establecida y permanecen aisladas en el plasma como elemento individualmente necesario para la señal celular de cambio buscada.(11)
La reconstrucción estructural se consigue mediante la osteosíntesis rígida interna entre el injerto óseo adicionado y los remanentes postresección de la falange afectada. La adición los FCOP constituye un complemento terapéutico para mejorar la viabilidad de la integración ósea. Ambos procedimientos se consiguen con relativa facilidad, dentro del tiempo quirúrgico empleado. El tamaño clínico del defecto y la inestabilidad resultante no son limitantes para conseguir la reconstrucción quirúrgica requerida. El curetaje exhaustivo intramedular y el fresado cortical permiten retirar el material de característica mixoide.
En la reconstrucción del defecto óseo resultante en los 2 casos clínicos que presentamos utilizamos con muy buen resultado un injerto interpuesto de hueso ilíaco monocortical, no solo hueso esponjoso, para favorecer el contacto de las 3 superficies de hueso esponjoso con el lecho receptor y al mismo tiempo poder estabilizarlo utilizando la monocortical existente mediante material de osteosíntesis rígida interna con placa y tornillos de titanio de un sistema específico para mano y dedos. Añadimos FCOP como elemento coadyuvante de angiogénesis al proceso inicial de curación y consecuentemente para obtener una adecuada integración tanto temprana como mantenida del tejido óseo de injerto de reemplazo.
La aplicación conjunta de estos 3 pilares técnicos utilizados con resultados satisfactorios como sistematización técnica, nos ha permitido en nuestra práctica cambiar el curso de propuestas previas para los casos presentados, como la amputación del dedo afecto, que evidentemente no estaban justificadas por carencia de fundamentos básicos reconstructivos.
Conclusiones
Consideramos que en el tratamiento quirúrgico de los encondromas de falange, la realización de una adecuada y precisa resección tumoral con instrumentación quirúrgica adecuada marca la diferencia para manejar las estructuras óseas de mano y dedos; la adición de dos elementos coadyuvantes como son la osteosíntesis rígida interna como estándar de tratamiento reconstructivo óseo de la mano, y el uso de injerto óseo monocortical más FCOP, ambos endógenos, son suficientes para propiciar una angiogénesis temprana que facilitará una rápida estabilización ósea y una recuperación funcional del paciente.
Esta sistematización, que hemos mostrado en los dos casos presentados, es técnicamente sencilla y no tiene contraindicaciones evidentes.
Debemos hacer énfasis sobre la necesidad de una detección temprana de este tipo de tumores para reducir el tamaño de la resección quirúrgica necesaria y, consecuentemente, del tejido autólogo de reemplazo.