Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.42 no.6 Toledo nov./dic. 2018 Epub 09-Nov-2020
https://dx.doi.org/10.7399/fh.11004
ORIGINALES
Análisis bioquímico como método eficiente para aumentar la seguridad de la nutrición parenteral en neonatos
1Servicio de Farmacia, Hospital Clínic, Barcelona. España.
2Laboratorio CORE, CDB, Hospital Clínic, Barcelona. España.
Objetivo:
Se describe el proceso de validación del control bioquímico de las bolsas de nutrición parenteral para verificar la correcta composición de ingredientes críticos antes de la administración, así como su impacto en la seguridad tras dos años desde la implantación en una población de recién nacidos prematuros.
Método:
Para la validación de la técnica se usaron 35 muestras de nutrición parenteral sin lípidos, que se procesaron en el laboratorio de Urgencias, siguiendo los procedimientos rutinarios utilizados para medir las concentraciones de glucosa y electrolitos en plasma y orina. Para analizar su impacto en la seguridad se realizaron análisis pre y post implantación mediante análisis modal de falla, efectos y criticidad. También se evaluaron los resultados fuera de rango y sus potenciales repercusiones en la seguridad del paciente.
Resultados:
El análisis de regresión no muestra error sistemático de medida para glucosa, calcio y potasio; en cambio, para el sodio y el magnesio sí existe un error sistemático, por lo que ambos fueron descartados para los análisis rutinarios. Los resultados del análisis modal de fallos y efectos, atribuibles a la implantación del control bioquímico, mostraron una disminución del riesgo del proceso del 11%.
Se analizaron 1.734 nutriciones, correspondientes a 218 neonatos prematuros; se encontraron 58 (3,3%) resultados fuera del rango de aceptación, de los cuales 7 se consideraron errores de preparación potencialmente peligrosos.
Conclusiones:
El control bioquímico de glucosa y electrolitos es un método eficiente y reproducible que evita que posibles errores de preparación afecten al paciente.
PALABRAS CLAVE: Análisis modal de fallos y efectos; Análisis químico; Control de calidad; Nutrición parenteral; Prematuro; Seguridad
Introducción
La nutrición parenteral (NP) es esencial para la supervivencia de los recién nacidos prematuros cuyos requerimientos nutricionales no pueden ser cubiertos a través del tracto gastrointestinal.
Sociedades científicas como la European Society of Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN) y la European Society of Clinical Nutrition and Metabolism (ESPEN) proporcionan guías específicas para la prescripción de los aportes nutricionales en este grupo de pacientes1,2. Sin embargo, la NP también se asocia a un elevado riesgo de efectos adversos, como infecciones o desequilibrios metabólicos, que pueden poner en riesgo a un paciente intrínsecamente muy vulnerable3. Por este motivo, cualquier error de prescripción, preparación o contaminación microbiológica podría ser fatal.
Por otra parte, la complejidad de la formulación constituye un riesgo en sí misma. Las causas principales de esta complejidad son: la manipulación de un elevado número de ingredientes con volúmenes muy pequeños, los problemas de estabilidad fisicoquímica y el elevado riesgo de contaminación durante la preparación4.
En los últimos años, la introducción de sistemas semiautomatizados para la preparación de las mezclas de NP ha constituido un avance importante en la mejora de la trazabilidad y la seguridad del proceso5 6-7; sin embargo, la implementación de estos sistemas en la elaboración de nutriciones para prematuros de bajo peso es complicada, debido al manejo de volúmenes inferiores a 1 ml en la mayoría de los componentes. Por este motivo, la preparación de NP en recién nacidos prematuros es un proceso esencialmente manual, siendo imprescindible la implantación de controles de calidad que disminuyan la probabilidad de errores y garanticen la seguridad de los pacientes. Controles en proceso, como el doble chequeo o algún sistema que asegure la trazabilidad de los ingredientes, son alternativas válidas en ausencia de los sistemas semiautomatizados de preparación8. El control microbiológico también es una práctica necesaria para asegurar la idoneidad de la técnica aséptica durante la elaboración de la nutrición. En cuanto al producto acabado, el control gravimétrico, valorando el peso final de las bolsas con un margen de aceptación del 5%, es el más extendido8 9-10; sin embargo, su utilidad es bastante limitada para la detección de errores de preparación, teniendo en cuenta el pequeño volumen de la mayoría de los componentes.
Las NP contienen habitualmente aminoácidos, glucosa, lípidos, electrolitos (sodio, potasio, calcio, fósforo y magnesio), oligoelementos y vitaminas, además de fármacos como carnitina y heparina. El análisis bioquímico de la composición de las NP podría ser un adecuado método de control, ya que aseguraría, en caso de error en la fabricación, la correcta composición de ingredientes críticos como la glucosa o algunos electrolitos potencialmente peligrosos. La medición en NP de la concentración de estos componentes se puede hacer mediante adaptaciones de las técnicas convencionales usadas en el laboratorio clínico para medir dichas concentraciones en muestras biológicas, siendo una alternativa sencilla al alcance de casi todos los hospitales. El uso de los procedimientos de medida de un laboratorio de Urgencias, que ya está habituado a trabajar con tiempos de respuesta cortos, permitiría la obtención de los resultados rápidamente y con un coste muy bajo.
El objetivo de este estudio es describir la validación analítica de la técnica utilizada en el control bioquímico de las NP de recién nacidos prematuros y evaluar el impacto en la seguridad del paciente tras su implantación en un hospital de tercer nivel.
Métodos
Validación de la técnica
Los ingredientes clínicamente más relevantes que se midieron por este procedimiento fueron glucosa, sodio, potasio, magnesio y calcio.
Las mediciones se llevaron a cabo mediante el analizador automático Dimension EXL (Siemens®Diagnostics) del laboratorio de Urgencias de nuestro hospital, que permite, entre otros parámetros, medir las concentraciones de glucosa y electrolitos en plasma y orina.
Las técnicas empleadas para medir la glucosa y el calcio fueron la espectrometría de absorción molecular GLUC Dimension®Ref. DF40 y CA Dimension®Ref. DF23A, respectivamente. Para medir la concentración de sodio y potasio se usó el procedimiento de potenciometría indirecta Quic-kLYTE Dimension®Ref. S600. Estos procedimientos se usaron sin modificaciones para medir en NP las concentraciones de calcio, magnesio, sodio y potasio, mientras que para la glucosa las muestras de NP se diluyeron previamente 1:20 con agua destilada.
Para la validación de los procedimientos de medida se usaron 35 muestras de NP sin lípidos, que fueron réplicas de muestras reales y que se fabricaron con doble chequeo como garantía de su correcta elaboración. Debido al uso de este doble chequeo y a la utilización de material volumétrico y de pesada que tiene una incertidumbre de medida muy pequeña, se consideró que la fabricación de las muestras usadas para la validación estaba exenta de error. Para calcular la inexactitud de los procedimientos de medida se analizó la diferencia entre la concentración teórica de las muestras y la concentración medida usando el procedimiento de regresión lineal no paramétrico de Passing-Bablok11,12.
Al mismo tiempo, y con el fin de hacer interpretables los resultados obtenidos en la práctica diaria, se consensuaron con los neonatólogos cuáles debían ser los márgenes de error clínicamente aceptables para cada componente.
Evaluación de la implementación
Análisis de riesgo
Se realizó un análisis de riesgo siguiendo el método failure mode, effect and criticality analysis (FMECA) a fin de cuantificar el riesgo del proceso antes y después de la implantación.
Este análisis se hizo sobre la base de un rediseño global del proceso de prescripción y preparación de la NP pediátrica en el que, además de la instauración del control bioquímico de las mezclas, se puso en marcha un programa de prescripción electrónica y un sistema de doble chequeo en la preparación.
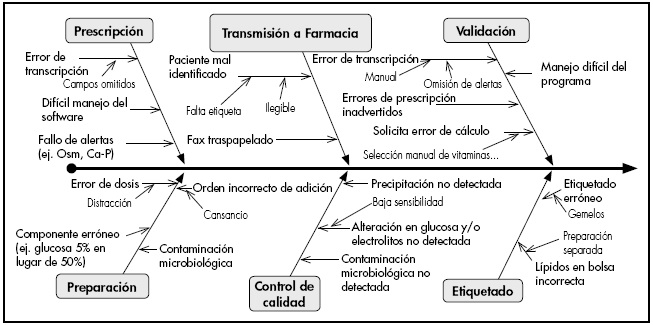
Un equipo multidisciplinar, formado por farmacéuticos y técnicos de farmacia implicados en el proceso de preparación de NP pediátricas, identificó mediante un diagrama de Ishikawa todos los posibles errores durante la prescripción, validación y elaboración de las mezclas. A continuación, asignaron un valor a cada posible error en cuanto a su probabilidad de ocurrir (de 1 a 10), gravedad de las consecuencias para el paciente en caso de ocurrir (de 1 a 10) y dificultad de detección del error durante el proceso (de 10 a 1). Tras la multiplicación de estos tres ítems se obtiene el índice de criticidad (IC), que cuantifica la magnitud del riesgo del proceso.
La diferencia entre el IC antes y después de la implantación del control nos da una idea del impacto en la reducción del riesgo global.
Valoración de la efectividad
Se evaluaron todas las nutriciones pediátricas realizadas en el período de 2 años postimplantación. Las mezclas analizadas no contenían lípidos, ya que en nuestro centro se administran de forma separada. Se registraron las siguientes variables relativas a los pacientes: peso el día de inicio de la NP, edad gestacional y duración de la nutrición. Por otro lado, se cuantificó el tiempo de respuesta desde la solicitud del análisis al laboratorio hasta su validación en el aplicativo informático del hospital y el coste medio por determinación. Finalmente, se evaluaron todas las preparaciones con resultados fuera del rango de aceptación, analizando las causas y el posible impacto en la seguridad del paciente.
Resultados
Validación de la técnica
Los neonatólogos consideraron un ± 10% sobre la concentración teórica como rango clínicamente aceptable para los componentes analizados, aunque desviaciones superiores podían ser aceptables en función de las características y situación clínica del prematuro.
LaTablas 1y laTabla 2muestran la concentración media de los ingredientes medidos en las muestras utilizadas para la validación y las rectas de regresión de cada componente.
Tabla 2. Rectas de regresión correspondientes a la inexactitud relativa de los distintos procedimientos de medida y sus coeficientes de correlación.

a: error proporcional; b: error constante; Conc esp: concentración específica; Conc med: concentración medida; IC: intervalo de confianza.
En el análisis de regresión se observa para todos los parámetros un coeficiente de correlación superior a 0,975. Los resultados de las rectas de regresión indican que para la glucosa y el calcio los procedimientos no muestran errores sistemáticos de medida. Para el potasio se observa un error sistemático proporcional positivo del 3,7%, que no se consideró clínicamente relevante. Para el sodio existe un error sistemático constante positivo de 3 mmol/l, irrelevante a concentraciones elevadas, pero que puede ser significativo a concentraciones pequeñas, por lo que se desestimó para el control. El magnesio presenta un error sistemático mixto, siendo el error proporcional del 11,3% y, por tanto, superior al rango de aceptación (± 10%), por lo que también se eliminó de las determinaciones.
Las inexactitudes relativas observadas para el magnesio, sodio y potasio podrían deberse al efecto de la distinta matriz usada en las muestras (solución parenteral versus plasma), y se consideró que podrían corregirse con el uso de calibradores adecuados. Sin embargo, esta medida correctora se ha pospuesto, ya que el objetivo buscado con la implantación de este método de control era disponer de una técnica fácilmente integrable a la rutina del laboratorio de Urgencias del hospital, sin tener que realizar demasiadas manipulaciones a las muestras para proceder a su análisis. De esta manera, en la medida de lo posible, se usa el mismo procedimiento que el que se utiliza en las muestras biológicas. Por otro lado, la correlación de glucosa, calcio y potasio, considerados los ingredientes más críticos, era perfectamente aceptable.
Para la implementación del control en la rutina del Servicio de Farmacia y el laboratorio se creó un sistema automático de cálculo en el aplicativo informático del hospital (SAP®). En la solicitud se indica el volumen de cada uno de los ingredientes a determinar y el volumen total de la bolsa. A partir de estos datos y de la concentración de las soluciones de partida, se calcula automáticamente la concentración teórica de los ingredientes. Los resultados de medida obtenidos en el analizador se integran automáticamente en el aplicativo del hospital, de manera que se visualiza la diferencia porcentual entre la concentración medida y la esperada (Figura 1).
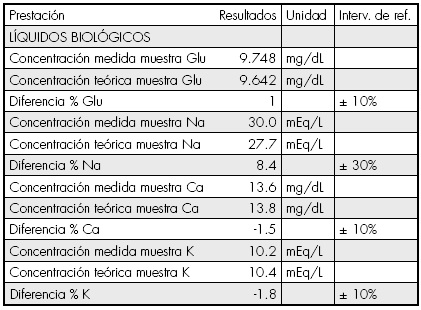
Figura 1. Ejemplo de resultados que se muestran a través del sistema informático del hospital. Glu: glucosa; Na: sodio; Ca: calcio; K: potasio.
Evaluación de la implementación
Análisis de riesgo
Se identificaron 31 posibles errores a lo largo del proceso, como se muestra en el diagrama de Ishikawa representado en laFigura 2. Para los 31 posibles fallos se calculó el IC, en base a su probabilidad de ocurrir, gravedad y dificultad de detección. El IC global antes de los cambios fue 4.964, mientras que tras las medidas instauradas se redujo a 1.715; ello supone una reducción del 65,5% en el riesgo global, del cual un 11% se atribuye a la implantación del control bioquímico.
Valoración de la efectividad
Se analizaron un total de 1.734 bolsas de NP, correspondientes a 218 neonatos, de edad gestacional 30 ± 4 semanas. El peso medio el primer día de la NP fue 1,35 ± 0,8 kg, siendo < 1 kg en 94 pacientes (43%). La duración media de la NP fue de 7,95 días.
Las mezclas utilizadas tenían una media de 12,4 ± 1,1 ingredientes, de los cuales el 50% tenía un volumen inferior a 1 ml. El volumen total medio de las bolsas de NP analizadas fue de 162,2 ± 27,1 ml. Este volumen incluye 50 ml de volumen de purga que se añaden en cada bolsa. Se analizaron todas las NP preparadas, enviando al laboratorio de Urgencias una muestra de 5 ml.
El tiempo medio de respuesta medido desde la recepción de la muestra en el laboratorio hasta la validación del resultado en el programa informático fue de 55,3 ± 7,4 minutos. El coste por determinación se estimó en 0,25 €.
De las 1.734 muestras analizadas, se encontraron 58 (3,3%) resultados fuera del rango de aceptación para glucosa, calcio y potasio (± 10%).
En 34 de los 58 casos, la desviación estuvo ligeramente por encima del rango de aceptación (entre el 10 y el 15%) y los neonatólogos no consideraron que tuviera ninguna repercusión clínica, por lo que se aceptó la preparación como correcta. En 17 casos, el resultado fuera de rango se identificó como un error de transcripción al hacer la solicitud en el programa informático, o bien a un error de identificación de los pacientes al hacer la solicitud. Por último, los 7 casos restantes se identificaron como errores de preparación potencialmente peligrosos, por lo que se desecharon las bolsas y se procedió a la repetición de las mismas. De estos, 3 errores estuvieron relacionados con la concentración de calcio en la muestra, otros 3 con la concentración de potasio, y un caso con la de glucosa.
Discusión
La complejidad de las mezclas y la fragilidad del paciente hacen de la prescripción y elaboración de NP pediátricas en recién nacidos prematuros un proceso crítico que requiere revisión continua para garantizar la seguridad.
El análisis bioquímico de las nutriciones puede aportar un gran valor añadido al proceso, al asegurar la correcta composición de ingredientes críticos como la glucosa o el potasio. El hecho de que no sea una práctica habitual en nuestros hospitales puede ser debido a la dificultad de integrarlo en la rutina diaria o a su elevado coste, según los instrumentos de medida que se utilicen.
Por otro lado, en muchas ocasiones se establecen controles aleatorios en un porcentaje definido de preparaciones. Este estudio demuestra que es factible implementar el control bioquímico de todas las bolsas elaboradas a un coste realmente asequible, gracias a la colaboración interdisciplinar entre el laboratorio de Urgencias y el Servicio de Farmacia. El tiempo de respuesta, inferior a 1 hora en la mayoría de los casos, permite detectar posibles errores antes del momento de la administración y repetir la preparación en caso necesario.
El análisis de riesgos mostró que, aunque la implementación del control bioquímico tiene influencia en la disminución global del riesgo del proceso, otras medidas, como la prescripción electrónica o la introducción de controles en proceso, como el doble chequeo en nuestro caso, pudieron tener igual o incluso más peso específico en la reducción del riesgo.
También fue útil para mostrar que, pese a las medidas introducidas, siempre queda un riesgo remanente (un 34% en nuestro caso) que debe estudiarse, valorando adecuadamente sus causas, para poner en marcha las medidas oportunas, con el objetivo de disminuirlo o eliminarlo.
Aunque los resultados del FMECA no son extrapolables a otros centros, el hecho de integrar el análisis de riesgos de nuestros procesos a la práctica habitual de nuestro entorno es una actividad recomendada por diversas organizaciones, como la Joint Commission o el Consejo de Europa13,14, como herramienta de soporte a la mejora continua.
A pesar de no disponer de información sobre errores de medicación relacionados con la NP que llegasen al paciente antes y después de la implantación del control bioquímico, consideramos que los datos presentados, en cuanto a disminución del riesgo del proceso y errores evitados, avalan los beneficios de la intervención.
Como muestran los resultados, nuestra población estaba formada fundamentalmente por recién nacidos prematuros con peso inferior a 1,5 kg, cuya indicación de NP es precisamente su condición de prematuridad. El elevado número de ingredientes y el pequeño volumen de la mayoría de ellos hacen evidente la dificultad que entraña la preparación de estas mezclas. Este es un problema ampliamente reconocido, que se ha intentado paliar de diversas formas. La adecuada formación y evaluación periódica de los preparadores es una de ellas, aunque otros autores han explorado las ventajas de la automatización en la preparación, o el uso de mezclas estandarizadas15 16-17. Sin duda, próximas investigaciones deberán aclarar el papel de estas opciones en la práctica clínica. Mientras tanto, y siempre desde una perspectiva interdisciplinar, los equipos responsables de la NP en neonatos deberán seguir luchando por mejorar la seguridad a través de la innovación y la mejora continua del proceso.
Como conclusión, el control bioquímico de glucosa y electrolitos es un método eficiente y reproducible que permite el análisis de ingredientes críticos en todas las nutriciones. Los resultados se conocen antes de la administración, lo que permite evitar que posibles errores de preparación lleguen al paciente. En nuestra experiencia de dos años, permitió detectar siete errores de preparación de consecuencias potencialmente graves en estos pacientes neonatos.
REFERENCIAS
Lapillonne A, Carnielli VP, David Embleton N, Mihatsch W. Quality of newborn care: adherence to guidelines for parenteral nutrition in preterm infants in four European countries. BMJ Open. 2013;3(9):e003478. [ Links ]
Koletzko B, Goulet O, Hunt J, Krohn K, Shamir R; Parenteral Nutrition Guidelines Working Group; European Society for Clinical Nutrition and Metabolism; European Society of Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN); European Society of Paediatric Research (ESPR). 1. Guidelines on Paediatric Parenteral Nutrition of the European Society of Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN) and the European Society for Clinical Nutrition and Metabolism (ESPEN), Supported by the European Society of Paediatric Research (ESPR). J Pediatr Gastroenterol Nutr. 2005;41(Suppl 2):S1-87. [ Links ]
Zingg W, Tomaske M, Martin M. Risk of Parenteral Nutrition in Neonates: An Overview. Nutrients. 2012;4(10):1490-503. [ Links ]
Flynn EA, Pearson RE, Barker KN. Observational study of accuracy in compounding iv admixtures at five hospitals. Am J Health-Syst Pharm. 1997;54:904-12. [ Links ]
Raimbault M, Thibault M, Lebel D, Bussières JF. Automated compounding of parenteral nutrition for pediatric patients: characterization of workload and costs. J Pediatr Pharmacol Ther. 2012;17(4):389-94. [ Links ]
Bethune K, Duncombe R. The use of automated compounding devices. Hosp Pharm Eur. 2002;1:39-40. [ Links ]
Crill CM, Hak EB, Helms RA. Accuracy of parenteral nutrition solutions compounded with automated systems and by hand. Am J Health Syst Pharm. 2005;62(22):2345-8. [ Links ]
Cardona Pera D, Cervera Peris M, Fernández Arévalo M, Gomis Muñoz P, Martínez Tutor MJ, Piñeiro Corrales G, et al. Consenso español sobre preparación de mezclas nutrientes parenterales. Farm Hosp. 2009;33(Supl 1):81-107. [ Links ]
Muñoz PG, López LG, Costa CM, Villares JM, Giner CP, Maristany CP, et al. Documento de consenso SENPE/SEGHNP/SEFH sobre nutrición parenteral pediátrica. Nutr Hosp. 2007;22(6):710-9. [ Links ]
Quintana I, Martínez G, López Sáez A, Pérez Ruixo JJ, Jiménez Torres NV. Control gravimétrico en la nutrición parenteral. Nutr Hosp. 2003;18(4):215-21. [ Links ]
Bablok W, Passing H, Bender R, Schneider B. A general regression procedure for method transformation. J Clin Chem Clin Biochem. 1988;26(11):783-90. [ Links ]
Clinical and Laboratory Standards Institute. Method Comparison and Bias Estimation Using Patients Samples; Approved Guideline, Second Edition. Document EP09-A2-IR. Pennsylvania, USA: CLSI; 2010. [ Links ]
Adachi W, Lodolce AE. Use of failure mode and effects analysis in improving the safety of i.v. drug administration. Am J Health Sys Pharm. 2005;62(9):917. [ Links ]
Resolution CM/ResAP(2011)1 on quality and safety assurance requirements for medicinal products prepared in pharmacies for the special needs of patients (consultado diciembre 2016). Disponible en: https://wcd.coe.int/ViewDoc.jsp?id=1734101&Site=CM [ Links ]
Lenclen R, Crauste-Manciet S, Narcy P, Boukhouna S, Geffray A, Guerrault MN, et al. Assessment of implementation of a standardized parenteral formulation for early nutritional support of very preterm infants. Eur J Pediatr. 2006;165(8):512-8. [ Links ]
Krohn K, Babl J, Reiter K, Koletzko B. Parenteral nutrition with standard solutions in paediatric intensive care patients. Clin Nutr. 2005;24(2):274-80. [ Links ]
Kreissl A, Repa A, Binder C, Thanhaeuser M, Jilma B, Berger A, et al. Clinical Experience With Numeta in Preterm Infants: Impact on Nutrient Intake and Costs. JPEN J Parenter Enteral Nutr. 2016;40:536-42. [ Links ]
Agradecimientos
Nuestro agradecimiento a José Luis Bedini, María Lombraña, Mireia Mensa, Susana Ceamanos y Rodolfo Juncos. Todos ellos contribuyeron, de una u otra forma, al éxito del proyecto.
Cómo citar este artículo:Salazar-Santander C, Miana-Mena MT, González-de-la-Presa B, López-Cabezas C. Biochemical test as an efficient system to improve safety in parenteral nutrition for premature infants. Farm Hosp. 2018;42(6):239-243.
Aportación a la literatura científicaCon este estudio se pretende dar a conocer una técnica que permite reducir el riesgo inherente al proceso de elaboración de nutriciones parenterales destinadas a pacientes sumamente vulnerables, como son los neonatos. El control bioquímico se incorpora a controles de calidad ya existentes en este proceso, como el microbiológico y gravimétrico, pero con valor añadido, en cuanto a que permite detectar errores en la composición de la mezcla, a diferencia de los anteriores. En nuestro entorno, el análisis bioquímico de las bolsas de NP ha hecho posible la identificación de siete errores potencialmente peligrosos antes de su llegada al paciente. Además, de forma previa a su incorporación se llevó a cabo un análisis de riesgos que permitió mejorar la seguridad del proceso mediante la identificación de los puntos críticos del mismo. La descripción de los pasos seguidos para la implantación del control bioquímico en nuestra institución podría facilitar la tarea a otros servicios de farmacia hospitalaria que quisieran incorporarla a sus procesos habituales.
Recibido: 28 de Febrero de 2018; Aprobado: 22 de Junio de 2018











 texto en
texto en