INTRODUCCIÓN
Las terapias biológicas y dirigidas han sido diseñadas para actuar específicamente sobre una diana terapéutica considerada importante en un proceso patogénico de diferentes enfermedades reumáticas, de forma que pueden mejorar la calidad de vida de los pacientes (ofrecen mayor control de los síntomas y evitan la aparición de la discapacidad), y, en muchos casos, aumentan las expectativas de vida y frenan la progresión de la enfermedad.
Como contrapartida, su alto impacto económico resalta la necesidad de un uso eficiente de los recursos sanitarios y la conveniencia de establecer una estrategia terapéutica integral de estas enfermedades1.
Los medicamentos biosimilares son fármacos biológicos producidos según las exigencias específicas de la EMA, que deben demostrar similitud con su fármaco de referencia en cuanto a calidad, actividad biológica, seguridad y eficacia, en el marco de ensayos clínicos de comparación directa aleatorizados doble ciego2. Dado su menor coste, su utilización puede contribuir a la eficiencia del gasto farmacéutico y a la sostenibilidad del sistema sanitario. Pero, a pesar de cumplir con las exigencias reseñadas anteriormente, hay reticencias y resistencia en cuanto a su uso.
Etanercept es un fármaco antirreumático biológico modificador de la enfermedad que inhibe de manera competitiva la unión del factor de necrosis tisular (TNF) a sus receptores de superficie celular y, por ello, inhibe la actividad biológica del TNF. Etanercept se utiliza en el tratamiento de diferentes enfermedades reumáticas, como la artritis reumatoide, artritis idiopática juvenil, artritis psoriásica y espondilitis anquilosante.
Desde finales de 2016 disponemos del biosimilar de etanercept, indicado para el tratamiento de las mismas enfermedades reumáticas que el medicamento de referencia.
Los objetivos de este estudio son: 1.- Conocer la respuesta a etanercept biosimilar (E-BS) en pacientes naive diagnosticados de artritis reumatoide, artritis psoriásica y espondilitis anquilosante, así como en pacientes con estas mismas patologías a los que se les realizó cambio desde etanercept de referencia (E-R) a E-BS (switch). Y, 2.- Evaluar el impacto económico de estas actuaciones.
MATERIAL Y MÉTODOS
Se realizó un estudio observacional retrospectivo de pacientes adultos diagnosticados de artritis reumatoide, espondilitis anquilosante y artritis psoriásica en tratamiento con etanercept, de referencia y/o biosimilar, en un hospital de tercer nivel, entre enero de 2017 y diciembre de 2019.
Antes de iniciar el estudio se solicitó autorización al Comité Ético de Investigación con medicamentos del hospital, que aprobó el planteamiento desde el punto de vista metodológico y ético.
Los datos se recogieron de la historia clínica electrónica (Selene®) y del programa de dispensación de medicamentos del Servicio de Farmacia (Farmatools®). El tratamiento de los datos se realizó de acuerdo con la legislación vigente sobre protección de datos de carácter personal3. Los datos clínicos de los pacientes fueron anonimizados para su inclusión en la base de datos.
Se analizaron dos grupos de pacientes:
Aquellos que iniciaron tratamiento con E-BS (etanercept biosimilar) como primera terapia biológica (naive).
Pacientes a los que se les realizó cambio (switch) desde E-R (etanercept de referencia) a E-BS (etanercept biosimilar).
Como grupos control de los anteriores, se incluyeron pares de pacientes, ajustados por edad, sexo y diagnóstico, en los que se mantuvo el E-R.
Las variables analizadas fueron: edad en el momento del estudio, sexo, diagnóstico, tratamiento (medicamento, pauta, duración), unidades de etanercept dispensadas, modificaciones del tratamiento durante el periodo del estudio, motivo que causó la suspensión o el cambio de tratamiento, fecha de suspensión de etanercept y tiempo de seguimiento. El mantenimiento del tratamiento se valoró como respuesta adecuada al mismo.
Se calculó el impacto en el coste del tratamiento comparando la diferencia entre el coste de la utilización de E-BS (precio neto x unidades dispensadas en el periodo de seguimiento) y el que hubiera supuesto el mantenimiento del E-R (precio neto x unidades dispensadas en el periodo de seguimiento).
Se calculó el ahorro en cada uno de los grupos de estudio (naive y switch) y el ahorro total.
Se realizó análisis descriptivo de las variables para conocer las características generales de la población en estudio. Las variables cualitativas se presentaron con su distribución de frecuencias absolutas y porcentajes. De las variables cuantitativas se calculó su media y su desviación estándar. Se evaluó la asociación entre variables cualitativas con el test X2 y con las cuantitativas mediante la prueba no paramétrica U de Mann-Whitney. El nivel de significación se fijó en 0,05.
RESULTADOS
Durante el periodo comprendido entre enero de 2017 y diciembre de 2019, 110 pacientes diagnosticados de artropatías se trataron con E-BS (etanercept biosimilar) en nuestro hospital:
- 62 iniciaron tratamiento con E-BS como primer fármaco biológico (naive).
- En 48, que estaban en tratamiento con E-R (etanercept de referencia), se realizó cambio a E-BS de manera electiva. Se seleccionaron pacientes que se mantenían estables y con buena respuesta al principio activo durante al menos seis meses. El cambio a E-BS se realizó tras informar al paciente y de acuerdo con el mismo.
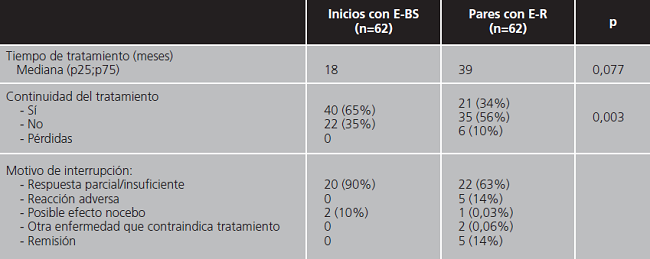
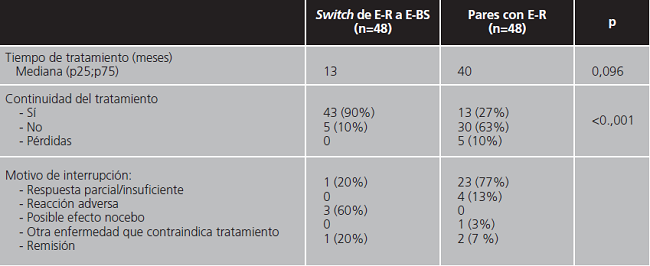
Se analizaron cada uno de estos grupos por separado y se compararon entre sí (tabla 1) y con una población control pareada por edad, sexo y diagnóstico (tablas 2 y 3).
Tabla 1. Pacientes tratados con E-BS: inicios y switch.
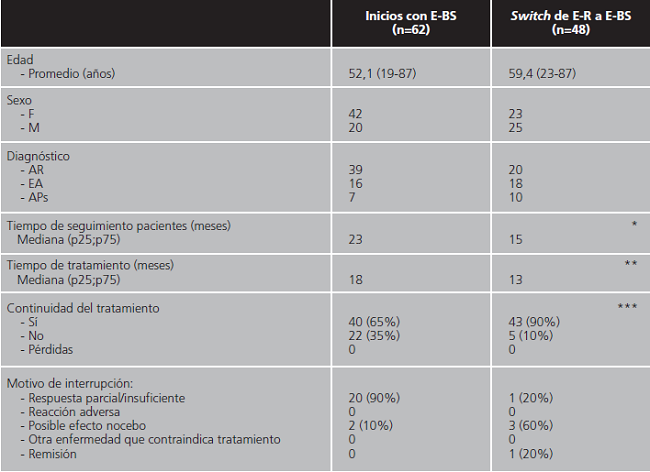
APs: artritis psoriásica; AR: artritis reumatoide; EA: espondilitis anquilosante;
*p<0,001;
**p=0,0012;
***p=0,002.
Las características de los pacientes que iniciaron tratamiento con E-BS se recogen en la tabla 1. No se registraron reacciones adversas. En los casos en los que fue necesario interrumpir el tratamiento con etanercept, éste se sustituyó por otro fármaco biológico diferente.
La comparación de este grupo con la población pareada de pacientes que iniciaron tratamiento con E-R se resume en la tabla 2. La principal diferencia está en la proporción de pacientes en los que se mantiene el tratamiento con E-BS frente a E-R (65% vs 34%; p=0,003).
Las características de los pacientes a los que se realizó cambio de E-R a E-BS se recogen en la tabla 1. Estos pacientes llevaban en tratamiento con E-R una media de 86 meses antes de que se les realizara el cambio. La principal causa de interrupción del tratamiento fue un posible efecto nocebo (3 casos, 60%), volviendo todos ellos al tratamiento con el fármaco de referencia, E-R.
La comparación de este grupo con la población pareada de pacientes en tratamiento con E-R se resume en la tabla 3. La principal diferencia entre estos grupos está en la proporción de pacientes en los que se mantiene el tratamiento con E-BS frente a E-R (90% vs 27%; p<0,0001).
Esto también queda de manifiesto en la comparación entre los inicios con E-BS y los switch (tabla 1): estos últimos permanecen en tratamiento con E-BS en mayor proporción que los inicios (90% vs 65%; p=0,002). Entre estos 2 grupos también hay diferencia en los tiempos de seguimiento y tratamiento, dado que los switch empezaron a realizarse con posterioridad a la introducción del biosimilar en pacientes nuevos.
En todos los grupos estudiados, las reacciones adversas observadas fueron leves.
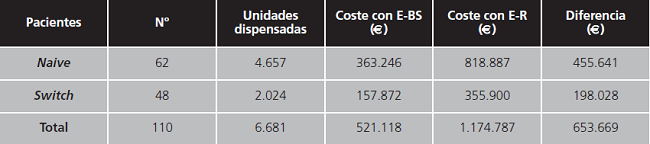
Los costes de etanercept BS en pacientes naive y switch se recogen en la tabla 4. En el caso que se hubiese administrado el de referencia, el coste hubiese supuesto un incremento de 653.668 € durante los 3 años que abarcó.
DISCUSIÓN
Se presenta un estudio observacional retrospectivo en el que se pone de manifiesto que el uso de etanercept biosimilar en enfermedades reumáticas es seguro y eficaz y ha supuesto una reducción de los costes en un hospital de tercer nivel.
Los agentes biológicos han permitido un gran avance en el tratamiento de patologías complejas, como la artritis reumatoide, la psoriasis, la esclerosis múltiple, la enfermedad de Crohn y el cáncer1. Sin embargo, estos fármacos tienen un alto impacto en el gasto hospitalario de nuestro sistema sanitario, impacto que va creciendo con los años.
Los biosimilares son tan seguros y eficaces como los medicamentos de referencia para las indicaciones para las que están autorizados y además tienen un coste sensiblemente menor. Por ello, su utilización puede contribuir en la sostenibilidad del sistema sanitario4,5,6,7. Sin embargo, su utilización es objeto de cierta controversia8.
En 2015 la Sociedad Española de Reumatología publicó un documento de posicionamiento sobre fármacos biosimilares en el que manifiesta su compromiso inequívoco con la sostenibilidad del sistema sanitario y apoya medidas que, sin reducir la calidad asistencial, estén encaminadas a asegurar su continuidad9. Asimismo, en este escenario de incremento en la oferta terapéutica de biológicos, considera imprescindible preservar la libertad de prescripción de los médicos que realizan la indicación de los fármacos según las características y circunstancias individuales de cada paciente.
Etanercept biosimilar se introdujo en el hospital a finales de 2016. Durante los 3 años que comprenden el estudio, se ha utilizado como agente biológico de inicio y en sustitución del etanercept de referencia para el tratamiento de diferentes enfermedades reumáticas en 110 pacientes.
Las tasas de retención observadas fueron del 90% en los pacientes a los que se les realizó switch y del 65% en los naive (tabla 1). Esta mayor persistencia en el tratamiento en los switch pudo estar influida por el largo tiempo que estos pacientes llevaban con buena respuesta clínica a este principio activo antes del cambio. En pacientes estables, bien controlados con un biológico, el cambio a un BS parece ser una estrategia razonable. Por otra parte, como ocurre con otros biológicos, en los inicios no hay tanta seguridad de que se vaya a obtener buena respuesta a un fármaco y puede ser necesario realizar cambios hasta conseguir controlar la enfermedad10-11. Las tasas de retención observadas en los switch son similares a las publicadas por el registro danés de terapias biológicas después de un año del cambio12. En un metaanálisis realizado se observaron tasas de retención de al menos el 75%13. Estos datos se asemejan a los encontrados en nuestro estudio; si bien la tasa de retención en pacientes naive fue algo inferior, la de los pacientes a los que se les cambió desde el de referencia fue superior.
Al comparar los dos grupos de pacientes analizados (inicios y switch) con una población control se observó una mayor necesidad de cambios de tratamiento en éstas últimas. En el caso de los pacientes que iniciaron tratamiento con etanercept biosimilar, este hecho pudo estar asociado a unos periodos de seguimiento y tratamiento más prolongados en la población control (tabla 2). Aunque no podemos concluir una mejor respuesta al tratamiento con etanercept BS, los resultados observados en los inicios no son inferiores a los que se obtienen con el tratamiento con etanercept de referencia. La mayor persistencia en los switch (tabla 3) pudo venir condicionada a que dichos pacientes llevaban estables y con buena respuesta al principio activo un largo periodo de tiempo antes del cambio.
Un aspecto a destacar en nuestra experiencia es el hecho de que las reacciones adversas no motivaran la interrupción del tratamiento con etanercept BS ni en pacientes naive ni en los switch. Sin embargo, sí lo fueron en los pacientes de las poblaciones control, lo que pudo ser debido a mayores tiempos de tratamiento en éstos últimos (tablas 2 y 3). Otros estudios con mayores periodos de tratamiento sí han asociado las reacciones adversas como causa de interrupción del tratamiento con etanercept BS14.
Las causas de interrupción más frecuentemente observadas fueron respuesta parcial o insuficiente al tratamiento en los pacientes naive y posible efecto nocebo en los switch. Cuando se inicia tratamiento con un medicamento biológico, no es extraño tener que realizar cambios a otros fármacos. El efecto nocebo ha sido observado en diferentes estudios al realizar switch14. Sin embargo, es un aspecto difícil de cuantificar, especialmente en estudios retrospectivos como el nuestro15. En este sentido, es importante disponer de programas de formación dirigidos tanto a los profesionales sanitarios como a los pacientes a fin de generar confianza en el uso de los BS1,16. Por otra parte, es verosímil pensar que la información previa al switch al paciente y realizarlo de acuerdo con el mismo minimiza la probabilidad de este efecto nocebo.
La aparición de medicamentos biosimilares, según han ido finalizando las patentes de medicamentos de referencia, contribuye a la sostenibilidad y eficiencia del gasto farmacéutico, a la vez que promueven de forma indirecta la investigación de otros medicamentos y la incorporación de otros fármacos innovadores8,10,17,18. Todo ello permite el acceso de mayor número de pacientes a los medicamentos biológicos y aumenta las alternativas en situación de fallo terapéutico1.
Aunque los efectos de los biosimilares en la disminución de los costes sanitarios no se conocen con exactitud, un análisis realizado por el RAND Corporation estimó que su introducción podría reducir los costes directos en 54 billones de doláres entre 2017 y 2026 en EE.UU.19.
Analizando el impacto económico en nuestro estudio, se observó una importante disminución de coste por paciente en tratamiento con etanercept, tanto en pacientes naive como en switch (tabla 4). Este hecho coincide con el observado en otros estudios17.