Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista de Bioética y Derecho
versión On-line ISSN 1886-5887
Rev. Bioética y Derecho no.31 Barcelona 2014
https://dx.doi.org/10.4321/S1886-58872014000200004
ARTÍCULO
Evaluación ética de proyectos de investigación financiados por la Comisión Nacional de Investigación Científica y Tecnológica, Chile 2012
Ethical evaluation of research projects funded by the National Commission for Scientific and Technological Research, Chile 2012
Maura Sara Castañeda Iñiguez*, Viviana Huspenina**, Sandra Lucía Montaño*** y Eliana Maribel Quintero Roa****
*Programa de Posgrado de Ética de la Investigación Biomédica y Psicosocial del Centro Interdisciplinario de Estudios en Bioética de la Universidad de Chile. maviz_castaneda@yahoo.com.mx
**Programa de Posgrado de Ética de la Investigación Biomédica y Psicosocial del Centro Interdisciplinario de Estudios en Bioética de la Universidad de Chile. vhuspenina@gmail.com
***Programa de Posgrado de Ética de la Investigación Biomédica y Psicosocial del Centro Interdisciplinario de Estudios en Bioética de la Universidad de Chile. sandra_lumr@hotmail.com
****Programa de Posgrado de Ética de la Investigación Biomédica y Psicosocial del Centro Interdisciplinario de Estudios en Bioética de la Universidad de Chile. equintero@unab.edu.co
RESUMEN
Objetivo: Evaluar las diferencias en la aplicación de pautas éticas locales e internacionales en proyectos de investigación en seres humanos y área de medicina, financiados por la Comisión Nacional de Investigación Científica y Tecnológica (CONICYT) 2006-2008 en Chile.
Metodología: Estudio de tipo descriptivo y observacional. Los criterios de selección fueron: proyectos desarrollados en seres humanos en el área de Medicina, realizados en el período 2006-2008 y con documentación completa. La información se recolectó a través de dos instrumentos. El primero instrumento evaluó la validez científica de los proyectos y el segundo instrumento se enfocó hacia los aspectos éticos de los mismos.
Resultados: Se evaluaron 52 proyectos Fondecyt-Fonis aprobados en el período 2006-2008. La duración media de los proyectos financiados por Fondecyt fue de 3.27 años versus 1.63 años de aquellos apoyados por Fonis. Sólo en alrededor del 40% de ellos (ambos) explícitamente manifestó su adherencia a normas éticas locales e internacionales. Aunque el 100% de los proyectos contaba con un documento de consentimiento informado, sólo 62.1 y 63.6% de los proyectos Fondecyt y Fonis, respectivamente, tenían la constancia de que el participante o su representante legal habían recibido suficiente información y que la información se había entendido completamente.
Conclusiones: Los proyectos Fondecyt y Fonis evaluados presentaron deficiencias en algunos aspectos éticos y metodológicos, en particular, en lo relativo al consentimiento informado.
Palabras clave: evaluación ética; pautas éticas internacionales; proyectos de investigación; Chile.
ABSTRACT
Aim: To evaluate the differences in the application of local and International ethical guidelines in research projects involving humans and medicine area, funded by the National Commission for Scientific and Technological Research (CONICYT) Chile 2006-2008.
Methods: The study was descriptive and observational. The selection criteria used were: projects developed in humans in Medicine area, conducted in the period of 2006-2008 and with full documentation. The information was collected through two instruments. The first instrument evaluated the scientific validity of the project and the second instrument was focused towards ethical aspects thereof.
Results: 52 projects Fondecyt-Fonis approved in 2006-2008 were evaluated. The average duration of the projects funded by Fondecyt was 3.27 years versus 1.63 and to those supported by Fonis. Only about 40% of them (both) explicitly expressed its adherence to local and international ethical standards. Although 100% of projects had an informed consent document, only 62.1 % and 63.6 % of the Fondecyt y Fonis projects, respectively, had the certificate that the participant or his legal representative had received enough information and that the information had been fully understood.
Conclusions: Fondecyt and Fonis projects assessed presented deficiencies in some ethical and methodological aspects, in particular with regard to the informed consent.
Key words: ethical assessment; international ethical guidelines; research projects; Chile.
Introducción
Desde finales de los años cuarenta, la necesidad de someter la investigación en seres humanos a ciertos principios éticos básicos ha sido tema de diversos Códigos como el de Nuremberg o Declaraciones como la de Helsinki entre otras(1). En los años setenta, el Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS) y la Organización Mundial de la Salud (OMS) comienzan a trabajar alrededor de la ética de la investigación biomédica. Como producto de este trabajo surge, en 1982, la propuesta de Pautas Éticas Internacionales para la Investigación Biomédica en Seres Humanos, concretándose éstas con la revisión y actualización de 1993 y 1998 hasta la actualmente vigente realizada en 2002(2). Las aportaciones que hacen dichas pautas alrededor de las bases éticas mínimas exigibles que regulen y dirijan el actuar científico han sido muy importantes. Orientan a quienes trabajan en investigación a respetar los principios éticos fundamentales como son el respeto por la persona sujeto de la investigación, la no maleficencia, la positiva relación riesgo-beneficio, la evaluación independiente y el consentimiento informado, entre otros.
En Chile, la Norma General Técnica No 57 constituye el principal marco de referencia en el sector público para la evaluación ética de proyectos de investigación en los que participan seres humanos y para el funcionamiento de los comités Ético-Científicos(3). Asimismo, la Ley No 20.120 "Sobre investigación en seres humanos, su genoma y prohíbe la clonación humana" regula la investigación biomédica(4). Ambos instrumentos fundamentan la evaluación ética de los proyectos de investigación que se llevan a cabo en el país.
La Comisión Nacional de Investigación Científica y Tecnológica (CONICYT) tiene como objetivo primordial promover la investigación científica en áreas prioritarias, con dicho fin fueron creados el Fondo Nacional de Desarrollo Científico y Tecnológico (FONDECYT) y Fondo Nacional de Investigación y Desarrollo en Salud (FONIS)(5). Ambos financian proyectos de investigación y para aquellos en los que participan sujetos humanos cuenta con un Comité Asesor de Bioética que revisa los aspectos éticos de los proyectos aprobados(6).
En la década de los noventa, Lavados et al, reportaron "problemas éticos" en prácticamente la mitad de los proyectos revisados por el Comité de Ética de la Escuela de Medicina de la Universidad Católica(7) y más recientemente Téllez et al, 2010(8), realizaron una evaluación de la experiencia del Comité Ético-Científico del Servicio de Salud Metropolitano Sur Oriente en la revisión de proyectos de investigación, encontrando deficiencias en la estructuración del consentimiento informado, omisión de información sobre posibles riesgos molestias e inconvenientes entre otros.
Los avances de la ciencia y la tecnología en el mundo actual, así como la importancia que tiene hoy en día la investigación científica, han dado como resultado el surgimiento de un nuevo debate sobre la importancia de la evaluación de los aspectos éticos de la investigación que se realiza en sujetos humanos(9). Es por eso que se planteó realizar un estudio que evaluara la aplicación de pautas éticas locales e internacionales en proyectos de investigación en seres humanos, financiados por Fondecyt y Fonis en Chile.
Material y Métodos
Estudio de tipo descriptivo, observacional. El universo de estudio lo constituyeron los proyectos aprobados por el FONDECYT y el FONIS en el período 2006-2008. Los criterios de selección utilizados fueron: Proyectos desarrollados en seres humanos, en el área de Medicina, realizados en dicho período y con documentación completa. Para la recolección de la información se utilizaron dos instrumentos, el primero para evaluar la validez científica y la pertinencia social de los proyectos y el segundo enfocado hacia los aspectos éticos de los mismos. Se tomaron como base para su elaboración normas éticas nacionales e internacionales (Declaración de Helsinki, Pautas éticas internacionales para la investigación Biomédica en seres humanos del Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS), Conferencia Internacional de Armonización para las Buenas Prácticas Médicas, Ley 20.120 del 2006, Norma técnica No. 57). Utilizando una lista de cotejo tipo checklist se evaluó la validez científica y la pertinencia social de los proyectos a través de variables como la formación académica del investigador principal, protocolo claramente formulado, tipo de diseño de estudio utilizado, objetivos claros, criterios de inclusión y exclusión de pacientes sin discriminación arbitraria, además de métodos de análisis de datos claramente establecidos y garantía de confidencialidad. En el segundo instrumento se evaluaba el documento de consentimiento informado y se incluyeron variables tales como: información clara, comprensible y completa sobre: objetivos, posibles beneficios y riesgos, efectos adversos, duración del estudio, derecho explícito para la persona a no participar o a retirarse del estudio en cualquier momento sin ningún tipo de perjuicio, confidencialidad de datos personales explícitamente garantizada, identificación clara del(os) investigador(es) responsable(s) y de la institución y/o personas a contactar en caso de necesidad (dirección y teléfono, correo electrónico), constancia que el paciente/sujeto de investigación o su representante legal y el testigo han recibido información suficiente acerca del estudio y que la han comprendido y mención de que se entregó un ejemplar del consentimiento firmado al paciente. Todos los análisis se efectuaron con el programa estadístico STATA para Windows versión 8.1.
Resultados
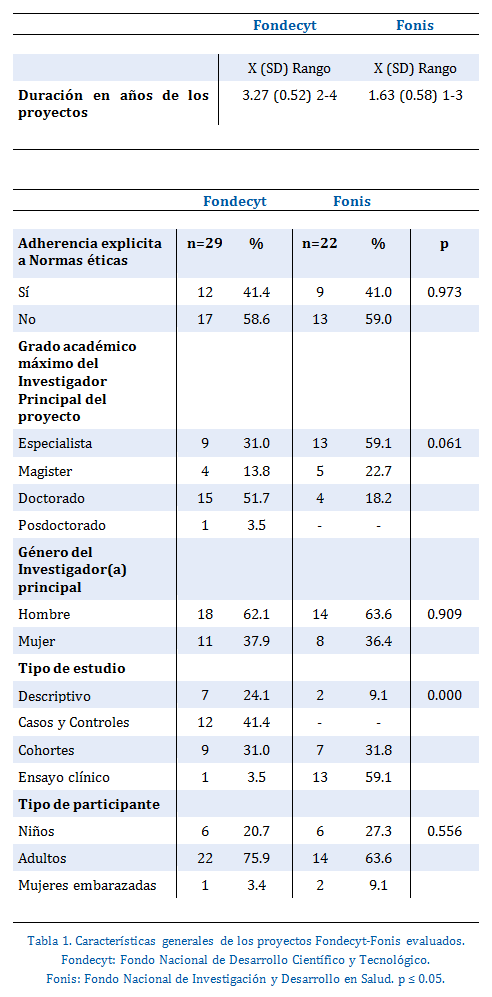
Fueron evaluados un total de 51 proyectos, de los cuales el 56.9% (29) correspondían a los financiados por Fondecyt y el 43.1% (22) a los de Fonis. En relación a las características generales de los mismos, la duración media en años de dichos proyectos fue de 3.27 (SD 0.52) y 1.63 (SD 0.58), respectivamente. Sólo 12 de los 29 proyectos de Fondecyt explicitaban en el documento que se adherían a alguna norma ética vigente (41.4%) contra 41.0% de los de Fonis (9 de 22). El grado académico máximo alcanzado por el investigador principal en los proyectos Fondecyt fue el de doctorado (51.7%) contra el 18.2% de los de Fonis. Un porcentaje menor alcanzaron el grado de magister (13.8 y 22.7% respectivamente). Más del 60% de los investigadores principales fueron hombres en ambos tipos de proyectos. En cuanto al tipo de estudio, en los proyectos Fondecyt, el más frecuentemente utilizado fue el de casos y controles (41.4%), en cambio, en los Fonis un importante porcentaje de ellos (59.1%) fueron ensayos clínicos, existiendo una diferencia estadísticamente significativa entre Fondecyt y Fonis respecto del tipo de estudio utilizado (p=0.000). Los adultos fueron el grupo que en mayor porcentaje participó en los proyectos, tanto de Fondecyt como de Fonis, seguidos por los niños (20.7 y 27.3%) y las mujeres embarazadas (3.4 y 9.1%), respectivamente (Tabla 1).
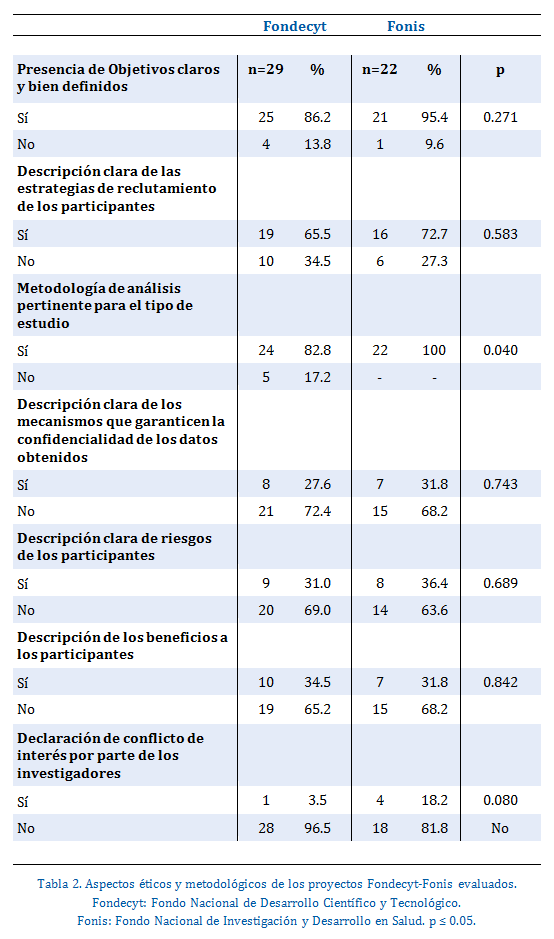
Al evaluar los aspectos metodológicos de los proyectos Fondecyt y Fonis se encontró que ambos contaban con objetivos claros y bien definidos (86.2% y 95.4% respectivamente). El 65.5% de los proyectos de Fondecyt presentaban una descripción clara de la estrategia de reclutamiento de los participantes, contra el 72.7 de los de Fonis. En relación a la metodología de análisis utilizada, en el 82.8% de los proyectos Fondecyt y el 100% de los de Fonis, dicha metodología era pertinente para el tipo de estudio planteado, presentándose una diferencia estadísticamente significativa entre ambos grupos (p=0.040). En cuanto a los aspectos ético normativos de los proyectos, el 72.4% los de Fondecyt y el 68.2% de los de Fonis no presentaban una descripción clara de los mecanismos para garantizar la confidencialidad de los datos obtenidos. Lo mismo sucedía con respecto a la descripción de los posibles riesgos para los participantes ya que en el 69.0 y 63.6% respectivamente, no fueron descritos. Asimismo, la descripción de los beneficios para los participantes se encontraba presente sólo en el 34.5 y 31.8% de los proyectos de Fondecyt y Fonis, respectivamente. En ambos tipos de proyectos, la declaración de conflictos de interés por parte de los investigadores estaba presente en un porcentaje muy reducido de ellos (Tabla 2).
En relación a las características generales del documento de consentimiento informado (CI), sólo en el 13.8% de los CI de Fondecyt se explicaba que la investigación se adhería a las normas éticas nacionales e internacionales contra el 18.2% de los proyectos Fonis. En el 69.0 y 81.8%, respectivamente, de los CI se hacía una descripción general del proyecto (Tabla 3). Asimismo, el lenguaje utilizado en el CI era claro y comprensible en el 58.6% de los proyectos Fondecyt contra el 59.1% de los Fonis.
En cuanto a los aspectos ético normativos del CI, en los proyectos Fondecyt se observa que en el 58.6% de ellos se describen los eventos adversos conocidos hasta el momento y se explica además la gravedad y frecuencia de ocurrencia de los mismos, lo cual ocurre en los Fonis en el 59.1% de los casos. En el 55.2 y 54.5%, respectivamente, se especifican beneficios para el participante. La explicación del no pago por participar y del derecho a reembolsos por gastos aparece en el 37.9% de los CI de los proyectos Fondecyt y en el 36.4% de los de Fonis. La explicación del mantenimiento de la confidencialidad y del uso de la información en congresos y/o publicaciones aparece en el 72.4 y 77.3% respectivamente. En el 79.3% de los CI del Fondecyt y en el 86.4% de los de Fonis, se hace mención de la participación voluntaria y/o del derecho a negarse a participar en el estudio. En el 69.0 y 86.4% respectivamente se hace mención de la posibilidad de retiro de los participantes en cualquier momento y sin perjuicio. Los datos de contacto del investigador principal para solicitar información aparecen en el 62.1% de los CI del Fondecyt y en el 68.2% de los de Fonis.
Discusión
La OMS define a la investigación en seres humanos como cualquier actividad de las ciencias sociales, biomédicas, de comportamiento o epidemiológica, que incluya la recolección sistemática o el análisis de datos con la intención de generar nuevo conocimiento; en que los seres humanos: a) Son expuestos a manipulación, intervención, observación u otra interacción con los investigadores, sea directamente o a través de la alteración de su ambiente; o b) Son identificables individualmente por intermedio de la recolección, preparación o uso de material biológico o médico u otros registros, por los investigadores(2).

La evaluación realizada por los comités de ética de la investigación, tanto al valor social y científico como a los componentes éticos de un proyecto de investigación en el que participan sujetos humanos y su adecuación a las normas éticas locales e internacionales son esenciales para garantizar la protección de dichos sujetos. El valor social de un proyecto se fundamenta en la aportación que realizará a la sociedad en su conjunto al evaluar un tratamiento, una intervención o una teoría que mejorará la salud y el bienestar o el nivel de conocimiento existente alrededor del problema planteado. La validez científica del mismo se puede medir a través de la presencia de objetivos e hipótesis claras y métodos científicos aceptados para producir datos confiables y válidos. Los componentes éticos de los proyectos se valorarán a través de la razón riesgo beneficio, cuidando siempre de minimizar los riesgos y daños potenciales, maximizando los beneficios. Importante también es el cumplimiento de todos los requerimientos necesarios en cuanto a la estructuración de un consentimiento informado y la protección de su privacidad a través de la garantía de confidencialidad(10).
En el presente estudio se ha analizado la aplicación de las normas éticas internacionales y locales a los proyectos de investigación financiados por el Fondecyt y Fonis y las diferencias entre ambos basándonos en los anteriores criterios. Se pudo observar que existen deficiencias en la estructuración del proyecto de investigación, tanto de aquellos pertenecientes a Fondecyt como a Fonis, ya que en ambos, sólo en alrededor del 40% se hace mención explícita de que se adhieren a pautas o normas éticas locales o internacionales. Existieron también diferencias entre ambos respecto a la preparación académica del investigador principal del proyecto, ya que más del 50% de ellos tenían un doctorado en el caso de Fondecyt contra sólo el 18% de los de Fonis, coincidiendo con lo reportado por Conicyt en un informe al respecto(5).
Los aspectos metodológicos de los proyectos de ambas entidades fueron bien calificados y no presentaban diferencias notorias. Sin embargo, en lo relacionado a los aspectos ético normativos de los mismos, se pudo observar que tanto los proyectos de Fondecyt como de Fonis expusieron diversas fallas, entre ellas no hacer explícito en el documento los mecanismos que garanticen la confidencialidad, los riesgos y los beneficios de participar en el estudio, la falta de declaración de conflicto de intereses por parte de los investigadores, deficiencias que ya habían sido previamente reportados por diversos autores en Chile(7,8,11). Es también notoria la deficiencia en la descripción clara de los mecanismos que garanticen la confidencialidad de los datos obtenidos, ya que sólo un tercio de los proyectos financiados por ambas entidades los describen, lo cual reportan también Winkler et al,2011(12). Asimismo, en una evaluación de los proyectos de investigación sometidos al comité de ética de Fondecyt, Santos et al, 2010(11), encontraron discrepancias entre evaluaciones de diferentes Comités de Bioética.
Si bien la elaboración e implementación de un documento de consentimiento informado se ve influido por diversos factores, entre ellos las capacidades comunicativas de los investigadores, el respeto a la autonomía del individuo y el estricto compromiso con la verdad científica(9), y aunque la noción de la voluntariedad de la participación del sujeto en la investigación se considera central en la ética de la investigación(13), las deficiencias en la estructuración de dicho documento y en general en la información que se les entrega a los participantes en una investigación, han sido documentadas previamente por otros autores(14,15).
En este estudio, se encontró que las deficiencias se centraban de manera más importante en la falta de adherencia a las normas éticas internacionales dentro del documento de consentimiento informado, tanto en los proyectos Fondecyt como Fonis. En ambos, el lenguaje utilizado muchas veces no es claro y en más del 50% de los consentimientos no se describen los posibles eventos adversos, ni los beneficios para el individuo, ni se explica el no pago por participar. En más del 20% de los proyectos de Fondecyt no se hace mención explícita de la participación voluntaria de sujetos, además de que en un porcentaje alto de los CI (37.9 y 31.8% de los proyectos de Fondecyt y Fonis, respectivamente), no aparecen los datos de contacto del investigador principal, lo cual fue previamente documentado por otros autores(11,12) .
Las limitaciones del presente trabajo están relacionadas principalmente con el diseño utilizado, ya que al tratarse de un estudio de tipo exploratorio no fue posible realizar un análisis a mayor profundidad, necesario para entender mejor el fenómeno de la correcta aplicación de las pautas éticas en los proyectos de investigación con seres humanos.
Desafortunadamente, tal y como lo refieren Lolas et al 2012(16) en una publicación reciente, en América Latina el cumplimiento de los requisitos éticos en la investigación que se realiza en seres humanos, muchas veces se lleva a cabo más por la presión que ejercen las agencias internacionales que financian la investigación, que por una necesidad sentida de la comunidad científica local. Se hace necesario entonces una reflexión en torno a lo propuesto por Bota et al, 2004, quien plantea que se requiere de un cambio en el paradigma actual, un cambio conceptual y de objetivos, esto es, ir de una cultura de la adherencia a una cultura de conciencia. La primera es manejada por las regulaciones y la segunda representa una cultura de responsabilidad y compromiso profesional.
Conclusiones
Los proyectos Fondecyt-Fonis evaluados presentan deficiencias en algunos aspectos ético-metodológicos, especialmente la falta de adherencia a las normas éticas internacionales y locales en lo que se refiere al documento de consentimiento informado, ya que entre otras cosas el lenguaje utilizado en la elaboración del mismo muchas veces no es claro, ni se describen los posibles eventos adversos, ni los beneficios para el participante y en un porcentaje importante de los mismos los datos de contacto del investigador principal no aparecen en el documento.
Bibliografía
1. Declaración de Helsinki de la AMM - Principios éticos para las investigaciones médicas en seres humanos (2008). Disponible en: http://www.wma.net/es/30publications/10policies/b3/. [ Links ]
2. Council for International Organizations of Medical Sciences (CIOMS). International Ethical Guidelines for Biomedical Research Involving Human Subjects. Disponible en: http://www.cioms.ch/frame_guidelines_nov_2002.htm. [ Links ]
3. Norma General Técnica No 57. Diario Oficial, 14 de Noviembre 2000, pág. 5. Disponible en: Norma (www.ispch.cl/formularios/norma_tec/norm_tec_n_57.pdf-17/02/2011). [ Links ]
4. Ley No 20.120 "Sobre investigación en seres humanos, su genoma y prohibe la clonación humana" Diario Oficial de 22-9-2006. Disponible en: http://recursoslegales.bcn.cl/jspui-rl/bitstream/10221.3/3851/2/HL20380.PDF/2011. [ Links ]
5. CONICYT. Programa Fondecyt. Impacto y Desarrollo 1981-2000. Disponible en: http://www.conicyt.cl/573/articles-4010_memoria_fondecyt.pdf. [ Links ]
6. Comité Asesor de Bioética de FONDECYT / CONICYT 2008. Disponible en: (http://www.fondecyt.cl/578/propertyvalue-57382.html, 2010). [ Links ]
7. Lavados M, Salas S. Problemas éticos en los proyectos de investigación biomédica presentados al Comité de Ética de la Escuela de Medicina de la Pontificia Universidad Católica de Chile. Revista Médica de Chile 1997; 125: 1011-18. [ Links ]
8. Téllez R. Discrepancias entre Comités de Ética en la evaluación de proyectos de investigación. Experiencia del Comité Ético-Científico del Servicio de Salud Metropolitano Sur Oriente (SSMSO). En: Ética de los Comités de Ética y Bioética en Investigación Científica Biomédica y Social. 5to. Taller de Bioética, Comité Asesor de Bioética del Fondecyt-Conicyt. Disponible en: http://www.conicyt.cl/fondecyt/files/2012/09/libro_etica_2011.pdf. [ Links ]
9. Cañete R, Guilhem D, Brito K. Consentimiento informado: algunas consideraciones actuales. Acta Bioethica 2012; 18 (1): 121-127. [ Links ]
10. Emmanuel EJ, Wendler D, Grady C: What makes clinical research ethical? JAMA 2000, 283(20):2701-2710. [ Links ]
11. Santos M, Michaud P. Méndez G, Téllez R, Sotomayor M, Winkler M, Valenzuela F, Núñez S, Silva E, Boisier M. Funcionamiento de Comités de Bioética de Investigación en Seres Humanos: Experiencia nacional en el área Fondecyt de ciencias biomédicas. En: 5to Taller de Bioética, Comité Asesor de Bioética del Fondecyt-Conicyt 2010. Disponible en: http://www.conicyt.cl/fondecyt/files/2012/09/libro_etica_2011.pdf. [ Links ]
12. Winkler M, Sotomayor M, Villarroel R, Méndez G, Téllez R, Salinas R, Valenzuela F, Núñez S, Silva E, Boisier ME, Santos M. Desafíos éticos en la investigación científica en ciencias sociales. En: Ética Clínica y Comités de Ética en Latinoamérica. León Correa F Ed. Disponible en: http://medicina.udd.cl/centro-bioetica/files/2011/09/FELAIBE-Comites-deliberacion.pdf. [ Links ]
13. Pauwels E. Ethics for Researchers. Facilitating Research Excellence in FP7. European Commission. Disponible en: http://ec.europa.eu/research/science-society/home_en.cfm. [ Links ]
14. Palmour M, Affleck W, Bell E, Deslauriers C, Pike B, Doyon J, Racine E. Informed consent for MRI and fMRI research: Analysis of a sample of Canadian consent documents. BMC Medical Ethics 2011, 12:1-8. [ Links ]
15. Martín-Arribas M, Rodríguez-Lozano I, Arias-Díaz J. Revisión ética de proyectos. Experiencia de un comité de ética de la investigación. Rev Esp Cardiol. 2012; 65(6):525-529. [ Links ]
16. Lolas F. Rodriguez E. Ethics in psychosocial and biomedical research - A training experience at the Interdisciplinary Center for Bioethics (CIEB) of the University of Chile. Acta Bioethica 2012; 18 (1): 9-56. [ Links ]
17. Bota A, Estévez A, Fernández L, Hernández M, Hevia A, Lara C, et al. Los comités de evaluación ética y científica de la investigación en seres humanos en los países latinoamericanos y el Caribe: Una propuesta para su desarrollo. Santiago de Chile. Universidad de Chile. 2004. [ Links ]
Fecha de recepción: 12 de diciembre de 2012
Fecha de aceptación: 30 de septiembre de 2013