Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Enfermedades Digestivas
versión impresa ISSN 1130-0108
Rev. esp. enferm. dig. vol.100 no.5 Madrid may. 2008
CARTAS AL DIRECTOR
Manejo diagnóstico preoperatorio del síndrome de Zollinger-Ellison por gastrinoma
Preoperative diagnostic approach for gastrinoma associated to Zollinger-Ellison syndrome
Palabras clave: Síndrome de Zollinger-Ellison. Tumor neuroendocrino pancreático. Gastrinoma pancreático o duodenal. Neoplasia endocrina múltiple tipo 1. Ultrasonografía endoscópica o ecoendoscopia. PAAF. Ultrasonografía intraoperatoria. Octreoscan.
Key words: Zollinger-Ellison syndrome. Neurocrine pancreatic tumor. Pancretic or duodenal gastrinoma. Multiple endocrine neoplasia type 1. Endoscopic ultrasound imaging. PAAF. Intraoperative ultrasound imaging. Octreoscan.
Sr. Director:
Los tumores neuroendocrinos (TNE) del páncreas (1) y del tracto digestivo son de difícil diagnóstico; a pesar de la existencia de las modernas técnicas topográficas de diagnóstico por la imagen, alrededor del 20-30% no pueden ser localizados preoperatoriamente (1,2).
El síndrome de Zollinger-Ellison (SZE) asocia úlceras pépticas y diarrea a una neoformación que segrega gastrina (gastrinoma). El gastrinoma es maligno (metástasis) en alrededor del 50% de los casos, estando localizado en el 90% en el "triángulo del gastrinoma", y por orden de frecuencia en el páncreas (45%), duodeno (15-20%) y en otras localizaciones en el 2%.
El SZE se clasifica en SZE esporádico y no familiar (70%) y SZE genético (30%), familiar o no, pero asociado a neoplasia endocrina múltiple tipo 1 (NEM-1) y múltiples carcinoides gástricos.
El SZE esporádico suele ser debido a un gastrinoma pancreá-tico solitario, grande (mayor de 2 cm) y maligno, o a un gastrinoma extrapancreático benigno, incidiendo en pacientes añosos, mientras que el SZE genético (NEM-1) aparece en jóvenes y suele ser debido a gastrinomas pancreáticos y duodenales, pequeños (menores de 2 cm), múltiples y benignos (3).
Algunos gastrinomas pueden no ser funcionantes (no segregan gastrina).
De una serie de 26 casos de SZE, recogidos personalmente en tres hospitales, Hospital Universitario de Bellvitge, Hospital de la Cruz Roja de L’Hospitalet de Llobregat y Centro Médico Teknon de Barcelona, en 18 casos no se había practicado ultrasonografía endoscópica (USE), mientras que en 8 pacientes (6 mujeres y dos varones, de 30 a 68 años) se había realizado USE preoperatoriamente, al igual que en 5 pacientes en los que se presumía un SZE y que la USE negativa y el seguimiento a largo plazo lo descartaron.
En un enfermo con gastrinoma pancreático se practicó USE-PAAF que resultó negativa. De seis TNE en los que hemos realizado, la PAAF fue positiva en el 67%.
De las múltiples técnicas (ultrasonografía, tomografía computerizada, resonancia magnética, Octreoscan, angiografía, etc.) realizadas en la segunda serie, la USE en los pacientes operados y comprobados quirúrgicamente presentó una precisión y una sensibilidad del 80% (4/5), una especificidad, un valor predictivo positivo (VPP) y un valor predictivo negativo (VPN) también del 80% (4/5) (Tabla I). Sólo en tres pacientes se realizó USE más Octreoscan.
De los trabajos publicados (4-9) y de las revisiones realizadas (2,10-12) se deduce que la USE tiene una sensibilidad del 50 al 100% de los casos con una media del 74-78%, localizando mucho mejor los gastrinomas pancreáticos que los extrapancreáticos-duodenales (29%) (6), incluso en la NEM-1 (13-16).
En los enfermos con NEM-1, la USE localiza en un alto porcentaje de casos gastrinomas funcionantes, un 80-90% (13,14), tumores neuroendocrinos pancreáticos (15) y TNE pancreáticoduodenales no funcionantes (16).
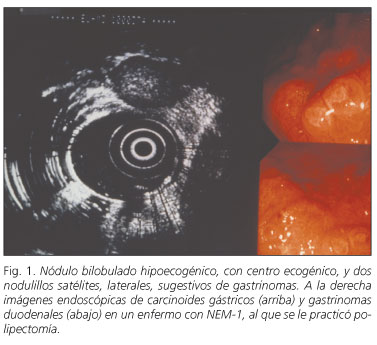
El Octreoscan localiza también en un alto porcentaje de casos (más del 80% en las revisiones), a excepción del insulinoma y los tumores neuroendocrinos (8,12,17); posee un alta sensibilidad del 86% en dos estudios independientes (8,18), pero puede presentar un 12% de falsos positivos (18) y su fiabilidad disminuye en los gastrinomas duodenales al 58% (19), al igual que ocurre con la USE a menos del 50% (8).
En un estudio sobre 122 pacientes (18), los resultados del Octreoscan cambiaron el manejo del 47% de los pacientes. Dada su alta sensibilidad y que evalúa todo el cuerpo, se ha propuesto que la USE y el Octreoscan serían las técnicas más efectivas en la localización de los tumores neuroendocrinos (10), y concretamente en los gastrinomas, dado que la USE más Octreoscan localiza el 90% de los casos (19). El Octreoscan detectaría la enfermedad multifocal y las metástasis, mientras que la USE estudiaría el páncreas y clarificaría los resultados falsos positivos del Octreoscan en el duodeno, páncreas y región peripancreática (1).
Es primordial el intento de localización tumoral preoperatoria, para la táctica y técnicas quirúrgicas que valoraran su resecabilidad completa y consecuente curación. Se debe localizar intraoperatoriamente, si no se ha localizado previamente, y la ultrasonografía intraoperatoria (USI) y la transiluminación duodenal pueden ser de mucha utilidad y buen complemento a la exploración visual y manual rutinaria, realizada por un cirujano experto en TNE.
La exploración quirúrgica rutinaria incrementa la supervivencia, como han demostrado Norton y cols. (20) comparando 160 pacientes en los que se llevó a cabo dicha exploración frente a 35 casos no operados cuya supervivencia a los 15 años fue menor, del 74 frente al 98% en el primer grupo.
El algoritmo diagnóstico preoperatorio sería para los gastrinomas, Octreoscan más USE, para los insulinomas tomografía computerizada (TC) más USE y para el resto de los TNE del páncreas, debido a su mayor tamaño, US/TC más USE.
M. J. Varas Lorenzo
Unidad de Ecografía-Doppler y Ecoendoscopia. Servicio de Aparato Digestivo. Centro Médico Teknon. Barcelona
Bibliografía
1. Fritscher-Ravens A. Endoscopic ultrasound and neuroendocrine tumours of the pancreas. JOP 2004: 5: 273-81. [ Links ]
2. Varas MJ, Miquel JM, Maluenda MD, et al. Preoperative detection of gastrointestinal neuroendocrine tumors using endoscopic ultrasonography. Rev Esp Enferm Dig 2006; 98: 828-36. [ Links ]
3. Varas MJ. Tumores de los islotes pancreáticos. En: Vilardell F, et al. Enfermedades Digestivas. Tomo II. Madrid-Barcelona: Aula Médica; 1998. p. 1516-24. [ Links ]
4. Palazzo L, Roseau G, Chaussade M, et al. Preoperative localization of pancreatic endocrine tumors by endoscopic ultrasonography (EUS). Gastroenterology 1992; 102: A284. [ Links ]
5. Palazzo L, Roseau G, Salmerón M. Endoscopic ultrasonography in the preoperative localization of pancreatic endocrine tumors. Endoscopy 1992; 24 (Supl. 1): 350-3. [ Links ]
6. Ruszniewski P, Amouyal P, Amouyal G, et al. Diagnostic value of endoscopic ultrasonography (EUS) for the localization of gastrinomas. Gastroenterology 1993; 104: A331. [ Links ]
7. Zimmer T, Ziegler K, Bader M, et al. Localisation of neuroendocrine tumours of the upper gastrointestinal tract. Gut 1994; 35: 471-5. [ Links ]
8. Zimmer T, Stolzel U, Bader M, et al. Endoscopic ultrasonography and somatostatin receptor scintigraphy in the preoperative localization of insulinomas and gastrinomas. Gut 1996; 39: 562-8. [ Links ]
9. Anderson MA, Carpenter S, Thompson NW, et al. Endoscopic ultrasound is highly accurate and directs managements in patients with neuroendocrine tumors of the pancreas. Am J Gastroenterol 2000; 95: 2271-7. [ Links ]
10. Zimmer T, Scherübl H, Faiss F, et al. Endoscopic ultrasonography of neuroendocrine tumors. Digestion 2000; 62: 45-50. [ Links ]
11. Pellicano R, De Angelis C, Resegotti A, Rizzetto M. Zollinger-Ellison syndrome in 2006: Concepts from a clinical point of view. Panminerva Med 2006; 48: 33-40. [ Links ]
12. Kahn SA, Guandalini S, Rabedolb K. Zollinger-Ellison syndrome. e-medicine WebMD. Sept. 2006. [ Links ]
13. Palazzo L, Borrotto E, Napoleon B, et al. Is endoscopic ultrasonography accurate for the localization of pancreatic and duodenal tumors in patients with multiple endocrine neoplasia type 1? Gastroenterology 1994; 106: A313. [ Links ]
14. Wamsteker EJ, Gauger PG, Thompson NW, Scheiman JM. EUS detection of pancreatic endocrine tumors in asymptomatic patients with type 1 multiple endocrine neoplasia. Gastrointest Endosc 2003; 58: 531-5. [ Links ]
15. Hellman P, Hennings J, Akerström G, Skogseid B. Endoscopic ultrasonography for evaluation of pancreatic tumours in multiple endocrine neoplasia type 1. Br J Sur 2005; 92: 1508-12. [ Links ]
16. Thomas-Marques L, Murat A, Delemer B, et al. Prospective endoscopic ultrasonographic evaluation of the frequency of nonfunctioning pancreaticoduodenal endocrine tumors in patients with multiple endocrine neoplasia type 1. Am J Gastroenterol 2006; 101: 266-73. [ Links ]
17. Scherülbl H, Riecken E-O, Wiedenmann B. Somatostatin-receptor scintigraphy in endocrine tumors. Gastroenterology 1994; 106: 1723-4. [ Links ]
18. Gibril F, Reynolds JC, Doppman JL, et al. Somatostatin receptor scintigraphy: Its sensitivity compared with that of other imaging methods in detecting primary and metastatic gastrinomas. A prospective study. Ann Intern Med 1996; 125: 26-34. [ Links ]
19. Cadiot G, Lebtahi R, Sarda L, et al. Preoperative detection of duodenal gastrinomas and peripancreatic lymph nodes by somatostatin receptor scintigraphy. Gastroenterology 1996; 111: 845-54. [ Links ]
20. Norton JA, Fraker DL, Alexander HR, et al. Surgery increases survival in patients with gastrinoma. Ann Surgery 2006; 244: 410-9. [ Links ]