¿QUÉ HIZO AL GERIATRA PARTICIPAR EN EL EQUIPO MULTIDISCIPLINAR? ESCENARIO ACTUAL DE ENVEJECIMIENTO Y CÁNCER
Según datos del último informe sobre población mundial de las Naciones Unidas, se estima que para el año 2050 el 16% de la población tendrá más de 65 años (frente al 9% actual); en Europa será aún mayor esta cifra, aproximándose a una de cada cuatro personas mayores de 65 años. El número de octogenarios se triplicará y será cuatro veces mayor el número de mayores que necesitarán ayuda para realizar sus actividades cotidianas 1.
En España, el grupo de mayores de 65 años representa el 19,1% del total de la población (fecha de la consulta: enero de 2018) y, según el modelo de proyección del Instituto Nacional de Estadística (INE), para 2068 alcanzará el 29,4%. Sigue creciendo en mayor proporción la franja de los octogenarios (6,1%) y la generación del baby boom alcanzará la jubilación en torno al año 2024 2.
Nuestra esperanza de vida a los 65 años se sitúa entre las más altas de la Unión Europea y del mundo, siendo de 19,1 años en hombres y 23 años en mujeres, aunque si se habla de esperanza de vida saludable en este tramo etario, el 53,7% del tiempo por vivir en hombres lo es en buenas condiciones, mientras que solo el 44% en el caso de las mujeres.
En cuanto al cáncer, la incidencia estimada de tumores en la población mundial se incrementará un 63,1% y pasará de 18,1 millones en 2018 a 29,5 millones en 2040 3.
El número de nuevos casos diagnosticados en España para 2019 se estima en 277.234, un 12% más que en 2015. Más de la mitad de los pacientes diagnosticados (60,9%) tienen 65 años o más 4. Los tipos de cánceres más frecuentes en nuestro país son los de colon y recto, próstata, mama, pulmón y vejiga urinaria, y les siguen a mucha distancia los linfomas no Hodgkin, los cánceres de cavidad oral y faringe y los de páncreas y de estómago. En 2017 fueron la segunda causa de fallecimiento (26,7%), por detrás de las enfermedades del sistema circulatorio, con el cáncer de pulmón como responsable del mayor número de muertes.
En cuanto a la supervivencia, la de nuestro país es del 53% a los cinco años, similar a la de países de nuestro entorno, y la mayoría de los supervivientes de cáncer son mayores de 65 años.
Si se combina el imparable envejecimiento de la población mundial con el aumento significativo de la incidencia de cáncer en las próximas décadas, el incremento de la tasa de supervivientes y el creciente impacto económico de esta enfermedad, se obtendrá una visión completa de cómo la atención específica al paciente mayor con cáncer es ya un asunto de primer orden para los sistemas sanitarios. Como consecuencia de esta perspectiva multidimensional surgió la denominada "oncogeriatría" hace más de 20 años, que usa la investigación clínica para incorporar conceptos geriátricos a los cuidados oncológicos, teniendo en cuenta la relevancia que adquiere el manejo multidisciplinar de estos procesos.
¿POR QUÉ ES NECESARIA LA VALORACIÓN GERIÁTRICA INTEGRAL Y CUÁL ES SU VALOR AÑADIDO?
Sabemos que la edad cronológica no es el equivalente de la biológica y que el envejecimiento se caracteriza por una gran heterogeneidad entre individuos en lo que respecta al estado de salud.
La valoración geriátrica integral (VGI) (proceso diagnóstico multidimensional e interdisciplinar capaz de identificar necesidades de cuidados y procesos no conocidos, diseñar en base a estos planes de cuidados e intervenciones y mejorar así los resultados de los pacientes mayores frágiles 5)) ha demostrado ser capaz de englobar esta diversidad de los pacientes mayores. Asimismo, los especialistas en cáncer también han comenzado a captar el concepto geriátrico de fragilidad, estado clínico multidimensional de vulnerabilidad ante factores estresantes como el cáncer o el tratamiento para este, condicionado por una limitación en la respuesta de los mecanismos compensadores, dinámico en el tiempo y potencialmente modificable, que sitúa al paciente en una situación de alto riesgo de malos resultados de salud.
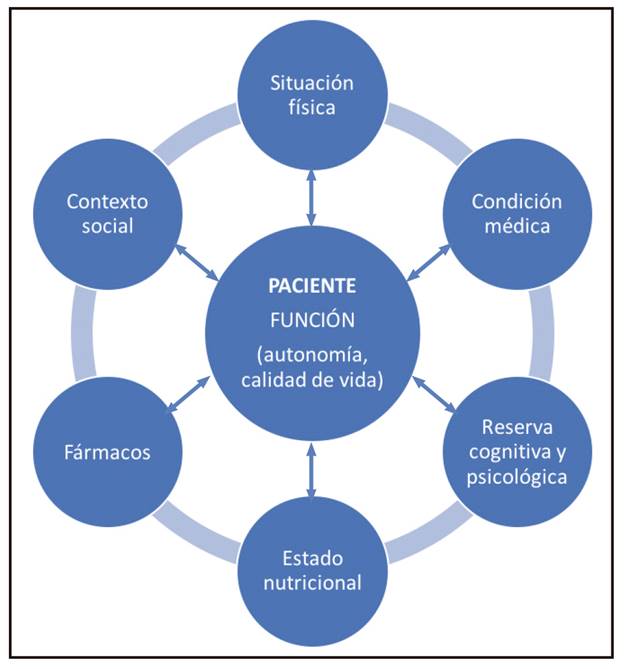
Existe importante evidencia del valor añadido de la VGI en la oncología (Fig. 1). Identifica síndromes geriátricos y problemas en pacientes con una buena situación funcional; predice toxicidad grave por quimioterapia, mortalidad precoz en pacientes mayores que están recibiendo quimioterapia y morbilidad postoperatoria, complicaciones, estancia hospitalaria y supervivencia; identifica áreas de vulnerabilidad no conocidas previamente que afectan directamente a la toma de decisiones del oncólogo; predice supervivencia global (competing causes of mortality); y explora las preferencias del paciente, sus valores y los objetivos de las opciones terapéuticas 6. Teniendo en cuenta todo esto, no resulta extraño que sus hallazgos tengan un impacto relevante en el proceso de toma de decisiones por parte del equipo multidisciplinar que diseña un tratamiento individualizado para cada paciente. Más aún, a partir de los resultados de la VGI, el geriatra planifica una serie de intervenciones sobre las áreas de vulnerabilidad detectadas, con los objetivos de optimizar la situación del paciente antes de que este inicie su tratamiento oncoespecífico, contribuir a que lo tolere con seguimiento durante el mismo y minimizar o tratar las "secuelas" en el superviviente, tanto a nivel médico como a niveles cognitivo y funcional.
En la Tabla 1 se resumen los motivos por los que un paciente mayor con cáncer puede ser remitido al geriatra.
¿QUIÉNES SE BENEFICIAN DE UNA VGI? MÉTODOS DE CRIBADO
Los documentos de posicionamiento, primero de la Sociedad Internacional de Oncogeriatría (SIOG) 6 y más recientemente de la Sociedad Americana de Oncolocía Clínica (ASCO) 7, sitúan a la VGI como la pieza clave de la aproximación al tratamiento del mayor con cáncer. Por su demostrado valor, lo ideal sería aplicarla en todos los pacientes, pero "consume tiempo y recursos", por lo que se han ido desarrollando test de cribado para identificar de forma rápida y sencilla a aquellos pacientes que más se van a beneficiar de una VGI.
Soubeyran y cols. diseñaron una herramienta de cribado llamada G8 8. Es la más utilizada y está específicamente diseñada para pacientes mayores con cáncer. Se compone de ocho ítems: edad cronológica, apetito, pérdida de peso, índice de masa corporal (IMC), movilidad, situación cognitiva y anímica, medicación y percepción subjetiva de salud. Se tarda en pasar aproximadamente cinco minutos, considerándose una puntuación menor o igual a 14 anormal, que, por lo tanto, es criterio para derivar a un geriatra. Tiene una elevada sensibilidad y valor predictivo negativo (VPN), pero una baja especificidad (64,4%). Fue validada con el estudio Oncodage 9 y predice toxicidad y supervivencia en varios tipos de cáncer, pero no en hematológicos.
La Vulnerable Elders Survey (VES-13) 10 es otra herramienta de screening altamente predictiva de alteración del estado funcional que se recomienda como un instrumento de evaluación inicial. La realiza el propio paciente en aproximadamente cinco minutos y se toma como punto de corte un valor mayor o igual a 3 (paciente vulnerable) para identificar la necesidad de realizar una evaluación más profunda. Tiene menor sensibilidad y mayor especificidad que el G8, se ha desarrollado en la comunidad y es predictiva de toxicidad y supervivencia en población general.
¿CÓMO PODEMOS CLASIFICAR A LOS MAYORES CON CÁNCER TRAS UNA VALORACIÓN GERIÁTRICA INTEGRAL? ¿PARA QUÉ ES ÚTIL? CONCEPTO EN EVOLUCIÓN DE FRAGILIDAD
La estratificación y clasificación de fragilidad en los mayores con cáncer se está desarrollando para ayudar a los médicos a seleccionar tratamientos oncoespecíficos e intervenciones geriátricas, puesto que la salud en el mayor, y también en el mayor con cáncer, se mide en términos de función (fragilidad) y la determinación de la edad biológica es un proceso en evolución.
Actualmente, podríamos decir que existen cuatro clasificaciones importantes del paciente mayor con cáncer en relación a su "fragilidad" o capacidad de reserva, evaluada con la VGI.
Hace ya tiempo que Balducci creó un sistema para clasificar al paciente mayor con cáncer basado en los hallazgos de la VGI en el que se identifican tres grupos: robustos, vulnerables y frágiles. Los pacientes robustos (fit) se pueden beneficiar de un tratamiento oncoespecífico estándar; los entonces llamados vulnerables, de un tratamiento adaptado; y los "frágiles", de un tratamiento paliativo 11. Droz y cols. diseñaron otra clasificación, propuesta en las guías clínicas de la SIOG 12 y originalmente desarrollada para la clasificación de los pacientes mayores con cáncer de próstata (llamada SIOG1). Su versión actualizada (llamada SIOG2) solo evalúa a aquellos pacientes ya cribados por un G8 anormal y de nuevo identifica tres grupos: los robustos, los actuales vulnerables y los denominados frágiles (según han ido evolucionando estos conceptos) 13). Finalmente, Ferrat, mediante una aproximación estadística, diferencia cuatro perfiles de salud: relativamente saludables (LC1), malnutridos (LC2), con deterioro cognitivo o trastorno del ánimo (LC3) y globalmente deteriorados (LC4) 14.
Los cuatro índices actuales de clasificación del mayor con cáncer son igualmente válidos en términos de su capacidad para predecir mortalidad al año e ingresos no programados a los seis meses, aunque la concordancia entre ellos es de pobre a moderada 15.
En oncohematología también se utiliza con frecuencia la siguiente clasificación 16:
- Pacientes sin comorbilidad y con buena situación funcional: tratamiento intensivo "go-go".
- Pacientes con datos de vulnerabilidad, no candidatos a esquemas de quimioterapia intensiva pero sí subsidiarios de tratamiento activo: tratamiento de baja intensidad "slow go".
- Pacientes con comorbilidades significativas y con mala situación funcional: tratamiento de soporte/paliativo "no go".
Las líneas de investigación futuras deberían enfocarse en demostrar en estudios de impacto clínico la utilidad de la estratificación de los mayores con cáncer en (Fig. 2):
- Toma de decisiones de tratamiento oncoespecífico.
- Diseño de intervenciones geriátricas.
- Estratificación de mayores con cáncer en los ensayos clínicos.

Figura 2. Modelo de clasificación y recomendaciones de tratamiento desde la perspectiva de geriatría (elaboración propia).
A pesar de que actualmente no existe preferencia en el uso de una herramienta sobre otra para detectar fragilidad, sí se recomienda de forma contundente el empleo de al menos alguna de ellas (como la escala FRAIL o la Short Physical Performance Battery [SPPB]) para ayudar a identificar a aquellos pacientes de alto riesgo que más se podrían beneficiar de una valoración geriátrica completa y exhaustiva. Tras esta, la clasificación del paciente en un subgrupo nos permitiría crear un plan de intervención multidimensional e individualizado con el objetivo de mejorar los resultados del tratamiento específico para su cáncer.
Para expresar todo esto de una forma más práctica y comprensible, podríamos concluir que la clasificación de los pacientes mayores con cáncer según su estado de fragilidad resulta extraordinariamente útil: desempeña un importante papel en la selección del tipo de tratamiento de un paciente, por ejemplo, con linfoma 17) o con cáncer de pulmón 18,19, puede ayudar a decidir la dosis de radioterapia a emplear 20, ayuda a estimar la supervivencia de un mayor con mieloma múltiple 21, predice la mortalidad de las pacientes mayores con cáncer de mama y colon 22,23, predice de forma independiente la aparición de complicaciones postoperatorias tras una cirugía mayor abdominal 24,25,26, así como la fatiga relacionada con la radioterapia en cáncer de mama 27 y la toxicidad y la tolerancia a la quimioterapia 21,28,29,30, etc.
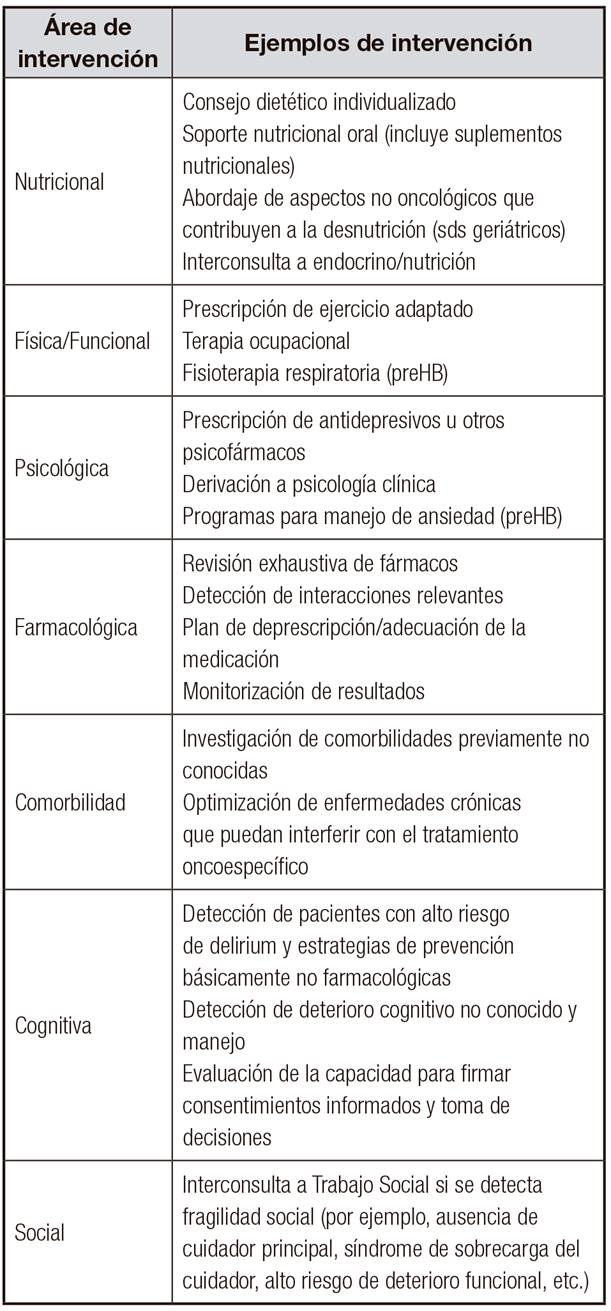
INTERVENCIONES GERIÁTRICAS BASADAS EN LA VALORACIÓN GERIÁTRICA INTEGRAL. ÁREAS DE OPTIMIZACIÓN: LO QUE EL GERIATRA PUEDE APORTAR AL EQUIPO MULTIDISCIPLINAR (Tabla 2)
Según la SIOG, las intervenciones geriátricas pueden ser eficaces para mejorar los parámetros nutricionales (grado de recomendación B), la situación funcional (grado de recomendación A) y la aplicación de un tratamiento adecuado (grado de recomendación A).
En una reciente revisión sistemática (36 publicaciones) 31 se han analizado todos los datos disponibles hasta la actualidad en lo que se refiere al efecto de la VGI en el tratamiento multidisciplinar de los mayores con cáncer, centrándose en la toma de decisiones del tratamiento oncológico, la implementación de intervenciones no oncológicas y el impacto de estas en los resultados del tratamiento.
Tras la VGI se modificó el plan de tratamiento inicialmente propuesto en un 28% de los pacientes (rango 8-54%), sobre todo a una opción menos intensiva.
Se realizaron recomendaciones no oncológicas en la mayoría (72%), fundamentalmente en relación a aspectos sociales (39%), estado nutricional (32%) y polifarmacia (31%).
El efecto sobre los resultados del tratamiento fue variable, con tendencia a un efecto positivo para conseguir completar el tratamiento en un 75% de los estudios y a tener menos complicaciones/toxicidad relacionadas con el tratamiento (55%) 31.
Actualmente, las recomendaciones de tratamiento se hacen a medida de las características del tumor, pero no necesariamente teniendo en cuenta el estado de salud ni las reservas del paciente.
En uno de los estudios revisados, de Corre y cols. 32, el uso de la VGI en la toma de decisiones resultó en un mejor plan a medida, consiguiendo prevenir tanto el infratratamiento como el sobretratamiento. Así, los pacientes que se sometieron a la VGI tuvieron mayores tasas de tratamiento completado y menos toxicidad global con similares resultados oncológicos en el brazo control.
Para mejorar el proceso de toma de decisiones en esta creciente población se van a necesitar más y potentes datos sobre el efecto de la VGI en resultados oncológicos y no oncológicos, tales como supervivencia global, calidad de vida, uso de recursos sanitarios y función física (Fig. 1).
BINOMIO NUTRICIÓN Y EJERCICIO FÍSICO
La relevancia de la desnutrición en el escenario oncológico es de sobra conocida. Del 10 al 20% de las muertes por cáncer pueden atribuirse más a la desnutrición que al cáncer en sí mismo y su presencia afecta a más de la tercera parte de los pacientes en la mayoría de las localizaciones del cáncer.
Si hablamos solo de pacientes mayores, un reciente e importante estudio publicado en 2018 (NutriCancer) 33 confirmaba la elevada prevalencia (44,9%) de desnutrición en este grupo poblacional, a partir de una cohorte de mayores de 70 años con cáncer, tanto hospitalizados como ambulatorios.
En el contexto de carcinogénesis tiene lugar un fracaso en la síntesis de músculo esquelético, por lo que el objetivo principal de la estrategia nutricional de forma global es preservar la masa magra.
La situación nutricional es crucial antes de iniciar el tratamiento oncoespecífico y aún más durante la fase activa del mismo.
Existe una amplia evidencia científica que relaciona la desnutrición con resultados adversos en cáncer. Es un potente predictor de mortalidad y morbilidad 34, reduce el tiempo de exposición a tratamiento quimioterápico, incrementa la toxicidad de las terapias antineoplásicas 35 y se asocia con menores tasas de respuesta, peor calidad de vida 36,37, declinar en la situación funcional 38 y mayor estancia hospitalaria.
Un reciente metaanálisis confirma que la desnutrición está asociada a mayor mortalidad por cualquier causa en mayores con cáncer 39. Futuros estudios de intervención a gran escala podrían determinar si reduciendo la prevalencia de la desnutrición en mayores con cáncer se podría incrementar su supervivencia global.
Se debe realizar una valoración nutricional lo antes posible tras el diagnóstico de cáncer, y también llevar a cabo reevaluaciones posteriores. Actualmente no existe un método ideal de screening ni de diagnóstico para este grupo poblacional. Los dos instrumentos que se recomienda utilizar como cribado en el paciente oncogeriátrico son: el MNA Short Form, con un valor predictivo negativo del 93,2% y una elevada sensibilidad del 98,1% 40, y el Abridged Patient-Generated Subjective Global Assessment (aPGSGA), creado para pacientes oncológicos y útil, además, para clasificar la gravedad de la caquexia y la eficacia de las valoraciones nutricionales 41.
Las estrategias de intervención nutricional desde la perspectiva de un geriatra incluyen los siguientes puntos clave:
Consejo dietético individualizado. Es la más utilizada y debe ser la primera que se lleve a cabo en todos los pacientes desnutridos o en riesgo con tracto gastrointestinal funcionante. Puede ser llevada a cabo por diferentes miembros del equipo multidisciplinar (nutricionista, endocrino, enfermera especializada, geriatra, oncólogo médico o radioterápico, etc.), pero siempre que tengan un entrenamiento y formación adecuados. Tiene como objetivo proporcionar una serie de consejos de forma individualizada para alcanzar los requerimientos específicos de cada paciente. Para que tenga éxito, es importante pactar los objetivos de las recomendaciones y motivar para su cumplimiento.
Incluye la detección e intervención para el control de los síntomas asociados a la enfermedad oncológica que interfieren con la alimentación, como son náuseas y vómitos, disfagia, disgeusia, mucositis, estreñimiento, etc.
Soporte nutricional oral. Consiste en diseñar una dieta enriquecida y/o prescribir suplementos nutricionales orales (SNO). Según las últimas guías de la European Society for Clinical Nutrition and Metabolism (ESPEN) 42 de desnutrición en cáncer, los SNO deberían recomendarse en todos los mayores frágiles con cáncer y en aquellos con desnutrición o riesgo de presentarla (grado de recomendación A). En estudios cada vez mejor diseñados y con mayor potencia estadística, el uso de SNO está demostrando mejorar variables nutricionales como la ganancia de peso y el IMC, pero también otras relevantes como son la autonomía en el autocuidado o la calidad de vida. También han demostrado ser coste-efectivos 43,44.
Farmaconutrientes - Agentes anticatabólicos y antiinflamatorios. Cada vez más estudios demuestran que la toma de SNO que contienen determinados aminoácidos (aa) esenciales como glutamina o leucina puede mejorar la síntesis de proteína muscular incluso en un ambiente de inflamación. Sin embargo, la revisión de Beaudart publicada recientemente concluye que la evidencia disponible de la suplementación con aa esenciales, leucina o su metabolito hidroxi-metilbutirato (HMB) en la masa muscular, fuerza muscular y función física aún no es lo suficientemente potente como para que se puedan hacer recomendaciones generales, de modo que se necesitan ensayos clínicos potentes y bien diseñados para proporcionar evidencia que sustente las recomendaciones clínicas 45.
Está claro que es necesaria una intervención específica para contrarrestar y manejar los efectos deletéreos de la desnutrición. Sin embargo, la eficacia y la elección de las estrategias permanecen controvertidas, y no existe aún evidencia potente para el manejo nutricional específico en mayores con cáncer gastrointestinal según la última guía publicada por la SIOG al respecto 46.
Además de lo anterior, es indispensable abordar los factores (básicamente síndromes geriátricos) que contribuyen a la desnutrición y que no están relacionados con el cáncer, como por ejemplo: deterioro cognitivo, privación sensorial, estado de ánimo, ausencia de soporte social, dependencia funcional, etc. Se debe continuar abordando la desnutrición en todas las fases del contínuum del cáncer, diseñando planes de intervención multimodal e individualizados tanto en el escenario de la prehabilitación como en el del tratamiento activo, el proceso avanzado o "crónico" o el superviviente (para el cual aún no hay recomendaciones basadas en la evidencia).
Cualquier estrategia de intervención nutricional en el mayor con cáncer debe ir acompañada de la prescripción de ejercicio físico. El papel que desempeña el músculo en la recuperación integral del paciente desnutrido con enfermedad asociada se evidencia cada vez más relevante. Así, la baja masa muscular (uno de los elementos que definen la sarcopenia) está emergiendo como un importante factor pronóstico de la tolerancia al tratamiento para el cáncer y la supervivencia global, además de relacionarse por mecanismos aún en investigación con la presencia de fragilidad. Sin embargo, aún no hay un enfoque estandarizado para medirla, ni consenso para determinar el punto de corte.
Tanto el American College of Sports Medicine como las últimas guías de ESPEN incluyen recomendaciones de actividad física, pero es probable que sus objetivos no puedan ser alcanzados por pacientes vulnerables o frágiles con cáncer.
El conocido como proyecto Vivifrail (http://vivifrail.com/es/documentacion) contiene un programa de ejercicios multicomponente para prevenir fragilidad y caídas en mayores de 70 años. La prescripción del ejercicio se realiza en base a la puntuación obtenida en pruebas que evalúan la función física, como la velocidad de la marcha o el Short Performance Physical Battery (SPPB). No fue diseñado para pacientes oncológicos pero proporciona una buena base sobre la que trabajar con leves adaptaciones para cada patología neoplásica y cada escenario clínico, ya que actualmente no existen aún en la literatura programas de prescripción de ejercicio específicos oncogeriátricos 47.
Prehabilitación
La prehabilitación se puede definir como el proceso de capacitar a los pacientes para resistir el estrés que va a suponer iniciar un tratamiento específico para el cáncer (cirugía, radioterapia, quimioterapia, inmunoterapia, etc.) aumentando su capacidad funcional. Hay evidencia de que los pacientes que se someten a ella recuperan antes su capacidad funcional precirugía (por ejemplo, tienen menor estancia hospitalaria, menores complicaciones, etc.), sobre todo en cáncer colorrectal, de pulmón y de mama.
El eje principal es un programa de ejercicios estructurados que debe contener ejercicios aeróbicos y de resistencia y que también incluye la optimización de la reserva nutricional y, en ocasiones, estrategias psicológicas para reducir la ansiedad. El tiempo propuesto es de cuatro a ocho semanas antes de iniciar el tratamiento, pero se han observado beneficios con siete y 14 días 48.
INTERVENCIÓN SOBRE POLIFARMACIA Y ADECUACIÓN DE LA MEDICACIÓN
Otra intervención esencial ligada a las anteriores es la revisión exhaustiva de la medicación y la elaboración de un plan de "deprescripción" si está indicado.
La prevalencia de polifarmacia (toma de cinco o más fármacos) en los mayores con cáncer antes de iniciar el tratamiento oncoespecífico es elevada (48-84%). Un 43% toma diez o más fármacos y hasta un 51% está tomando medicación potencialmente inapropiada (MPI) siguiendo los criterios Beers y Screening Tool of Older Person's Prescription - Screening Tool to Alert to Right Treatment (STOPP-START) 49.
Las MPI más frecuentes en el mayor con cáncer según lo publicado son las benzodiacepinas, los fármacos de la esfera gastrointestinal (inhibidores de bomba de protones, antieméticos, laxantes, etc.), los antiinflamatorios no esteroideos y los antiplaquetarios 49.
Existe evidencia de que la presencia de polifarmacia se asocia con: mayor probabilidad de no recibir tratamiento quirúrgico para el cáncer 50, mayor riesgo de complicaciones posquirúrgicas 51, mayor incidencia de delirium 52, mayor deterioro funcional 53, mayor estancia hospitalaria 54, mayor mortalidad a los 30 días 55, y mayor toxicidad de grado 3-4 relacionada con la quimioterapia 56. También puede influir en el tratamiento oncoespecífico al aumentar el riesgo de interacciones que pueden conducir a efectos adversos. Y no se ha de olvidar un asunto de creciente importancia como es su implicación en la adherencia a los tratamientos oncoespecíficos, cada vez más frecuentemente administrados por vía oral.
Se deben llevar a cabo las estrategias de intervención en el tratamiento farmacológico en los momentos de inicio o modificación del tratamiento oncoespecífico cuando haya cambios en el manejo de la enfermedad o en la condición clínica y durante el crítico momento de la transición de cuidados (como las altas hospitalarias).
En la elaboración de un plan de "deprescripción" o adecuación de medicación se debe determinar la expectativa de vida y establecer los objetivos de cada tratamiento prescrito, revisar toda la medicación, evaluar lo apropiado de cada fármaco, identificar medicaciones que se pueden retirar en este momento, crear el plan de "deprescripción" sobre cómo hacerlo y monitorizar y revisar los resultados en el paciente, estableciendo canales de comunicación adecuados 57.
En este momento adquiere especial importancia la estimación de la expectativa de vida para determinar lo apropiado o no de un fármaco. Muchas medicaciones no oncoespecíficas, sobre todo aquellas prescritas con indicación de prevención, pueden resultar inapropiadas e inútiles en pacientes con una expectativa de vida limitada.
DETECCIÓN Y MANEJO DE LA COMORBILIDAD
La comorbilidad en adultos mayores con cáncer compromete el pronóstico funcional y vital, aumentando la vulnerabilidad al tratamiento oncológico 58, pero no siempre de forma lineal con la suma de enfermedades. Así, aquellos pacientes con comorbilidad tienen menos probabilidad de recibir un tratamiento oncoespecífico 59, si bien algunos bien seleccionados podrían beneficiarse de él, apoyada esta selección en herramientas que valoren el impacto de la comorbilidad sobre la supervivencia.
En la práctica clínica la mejor opción es una VGI exhaustiva, resumida en una lista de comorbilidades y problemas que deben optimizarse antes (prehabilitación) y durante la intervención oncológica 60.
PREVENCIÓN Y MANEJO DEL DELIRIUM. DETECCIÓN DE DETERIORO COGNITIVO
La prevalencia de delirium es elevada en mayores con cáncer, aún más en fases avanzadas de la enfermedad (85-90%), y es un factor independiente de mal pronóstico a corto plazo 61. Es importante detectar a aquellos pacientes que presentan alto riesgo de desarrollar delirium antes de una cirugía, hospitalización o inicio de tratamiento oncoespecífico, informar a sus cuidadores e implementar estrategias de prevención. Lo más efectivo son las intervenciones no farmacológicas, representadas en el programa HELP (www.hospitalelderlifeprogram.org), mundialmente conocido, aunque aún no ha sido probado en oncogeriatría 62.
Asimismo, la valoración del estado cognitivo antes de iniciar el tratamiento oncoespecífico es muy útil para conocer la situación cognitiva basal del paciente, considerar si existe demencia como factor "competidor" de mortalidad, conocer la comprensión de la enfermedad y la capacidad del paciente para tomar decisiones y también para seleccionar y planificar el tratamiento.
INTERVENCIONES PSICOLÓGICAS. ABORDAJE DE TRASTORNOS DEL ÁNIMO, SUEÑO Y ANSIEDAD
La prevalencia de depresión en pacientes con cáncer es del 6-28% y este porcentaje se multiplica por 2-3 veces en mayores. Su presencia se asocia con disminución de la calidad de vida, deterioro funcional, estancias hospitalarias más prolongadas, progresión más rápida de la enfermedad, deterioro cognitivo, toxicidad medicamentosa, menor adherencia al tratamiento y mayor mortalidad 63,64. A pesar de ello, es infradiagnosticada y su presencia se confunde con síntomas propios de la edad. Además, en el adulto mayor predominan las formas subclínicas, con menos síntomas clásicos como tristeza y más síntomas propios del cáncer. Se debe detectar su presencia en todos los pacientes y realizar un abordaje tanto farmacológico como no farmacológico, derivando al psicólogo o a programadas de manejo de la ansiedad en el escenario, por ejemplo, de prehabilitación 63.
El insomnio es aún más prevalente entre los mayores con cáncer (> 50%) y también infradiagnosticado e infratratado. En la práctica clínica se debe hacer un cribado de alteraciones del sueño en todo mayor con cáncer y, como en la depresión, implementar estrategias de intervención cognitivas-conductuales y farmacológicas 65,66.
ASPECTOS SOCIALES
Por último, y sin que resulte menos importante, el geriatra debe detectar qué necesidades o vulnerabilidades presenta el paciente mayor con cáncer desde el punto de vista social, tales como: existencia de red social/familiar, ausencia de cuidador principal o sobrecarga del mismo, alta probabilidad de deterioro funcional significativo durante, por ejemplo, la convalecencia de una cirugía o tratamiento quimioterápico (lo cual puede determinar una estancia temporal en residencia o conseguir mayor asistencia en domicilio), imposibilidad de venir acompañado a las revisiones o días de tratamiento, dificultad para acceder a la asistencia sanitaria por lejanía geográfica, barreras arquitectónicas y otras características de la vivienda, etc.
Todo ello puede afectar a la toma de decisiones con respecto al tratamiento que se proponga al paciente, pero muchos de estos aspectos son modificables y solucionables, de forma que se debe solicitar lo antes posible una valoración e intervención por parte de los compañeros de Trabajo Social que forman parte del equipo multidisciplinar.
CONCLUSIONES
La valoración por un geriatra permite: identificar déficits, clasificar a los mayores, identificar vulnerabilidad e intervenir sobre ella, predecir toxicidad al tratamiento oncoespecífico y predecir mortalidad. Su presencia en el equipo multidisciplinar es útil tanto en el momento de participar en la toma de decisiones como en el de planificar intervenciones en determinados aspectos que influyen en los resultados del tratamiento oncoespecífico, en la supervivencia, en la autonomía y en la calidad de vida de los pacientes. La valoración geriátrica ofrece la posibilidad de aplicar un tratamiento adaptado a las características de cada paciente.
La función física y el estado nutricional son los dos dominios de la valoración geriátrica más frecuentemente asociados con mortalidad y pobres resultados de los tratamientos sistémicos oncoespecíficos, por lo que las intervenciones sobre ellos adquieren especial relevancia.
Es necesario continuar investigando para obtener evidencia científica específica y adaptar los modelos asistenciales para trabajar de forma multidisciplinar, siendo imprescindible la colaboración entre los distintos especialistas implicados en la atención al paciente mayor con cáncer.