INTRODUCCIÓN
El tumor inflamatorio de Pott se define como uno o más abscesos subperiósticos secundarios a una osteomielitis del hueso frontal. Generalmente se deben a la complicación de una sinusitis frontal o después de un traumatismo craneal. Actualmente es una complicación muy rara debido a la terapia con antibióticos [1]. Esta patología la vamos a encontrar predominantemente en el grupo de edad de la adolescencia, y rara vez en adultos. El tumor de Pott es un factor de riesgo de complicaciones intracraneales como empiema subdural o el absceso cerebral [2].
El objetivo de este estudio es proporcionar una revisión actualizada de la cirugía y del tratamiento médico; en el que vamos a valorar las distintas opciones terapéuticas en pacientes con abscesos subperiósticos secundarios a osteomielitis del hueso frontal.
MATERIAL Y MÉTODO
Se realizó una búsqueda en PubMed (“Pott Puffy Tumor/drug therapy”[Mesh] OR “Pott Puffy Tumor/surgery”[Mesh] OR “Pott Puffy Tumor/therapy”[Mesh]), BVS (biblioteca virtual en salud España) y Scopus. Se seleccionaron un total de 20 artículos [3-22]. La revisión se realizó siguiendo los criterios PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-analysis) [23].
Los criterios de inclusión fueron: Casos publicados de pacientes de cualquier edad y sexo con diagnóstico de absceso subperióstico secundario a osteomielitis del hueso frontal en los últimos 5 años. Estudios que incluyen una descripción clínica básica de la edad, sexo, presentación clínica y tratamiento. Descripción del tipo de tratamiento realizado, incluyendo, las diversas técnicas quirúrgicas, clase de antibiótico seleccionado, tiempo de tratamiento y presencia o no de recurrencia. Casos y serie de casos. Estudios escritos en inglés y español.
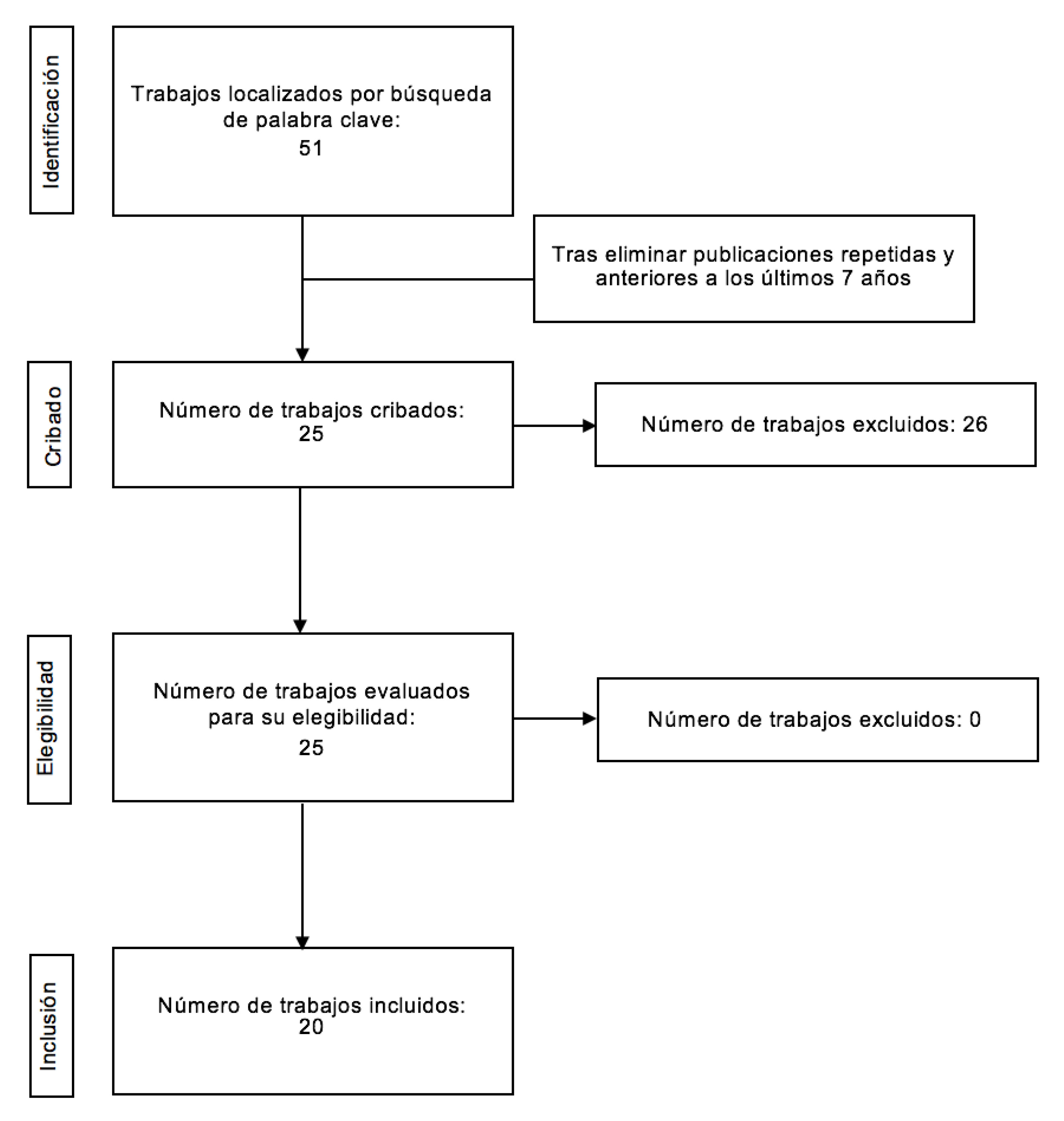
Se excluyeron de la revisión: Revisiones bibliográficas. Publicaciones con material redundante. Estudios realizados en animales. La secuencia de selección de los artículos se resume en la Figura 1.
En lo que respecta a las técnicas endoscópicas descritas se encuentran:
Draf tipo I: drenaje simple en el que se eliminan todas las celdas de etmoidales anteriores y superiores del receso frontal. La finalidad es que el ostium del seno frontal drene directamente a un receso frontal permeable.
Draf 2A: drenaje extendido en el que el suelo del seno frontal se reseca desde la lámina papirácea hasta el cornete medio.
Draf 2B: drenaje extendido en el cual el piso del seno frontal se reseca desde la lámina papirácea hasta el tabique nasal.
Draf 3: drenaje mediano endonasal en el cual el suelo del seno frontal se reseca desde la lámina papirácea derecha hacia la lámina papirácea izquierda con resección adicional del tabique nasal superior y la parte inferior del tabique del seno interfrontal [24]
RESULTADOS
Se seleccionaron 20 artículos en la búsqueda bibliográfica, que cumplen con los criterios de inclusión para la revisión, cuyos datos se resumen en la Tabla 1. Un total de 30 pacientes (24 varones y seis mujeres) fueron revisados; con una media de edad de 27 años. En un 90% la causa fue una rinosinusitis crónica, seguida por traumatismo local y consumo de tóxicos en los dos pacientes restantes. En lo que respecta al germen asilado, el más frecuente, fue el Staphylococcus aureus en un 33.3% del total, seguido por flora mixta en el 16.7%, Streptococcus anginosus en un 10%, Streptococcus intermedius en un 6.7 % y 3.3 % en Staphylococcus epidermidis, Streptococcus constellatus, Streptococcus pneumoniae y Escherichia coli. No especifican especie en el 16.7 % de pacientes.
Tabla 1. Tumor de Pott. Artículos incluidos en la revisión.
| Autor/Año | Edad | Sexo | Etiología | Germen aislado | Cirugía | Antibioticoterapia | Reintervención |
|---|---|---|---|---|---|---|---|
| Van del Poe 2016 | 7 | F | Traumatismo | Streptococcus intermedius | Draf 2A | Penicilina IV 6S | No |
| 10 | F | RSC | Staphylococcus aureus | Draf 2A | Augmentine IV 2S+ Augmentine VO 4S | No | |
| 12 | M | RSC | Staphylococcus aureus | Draf 2A+DE | Augmentine IV 2S+ Augmentine VO 4S | No | |
| 13 | M | RSC | Staphylococcus aureus | No | Augmentine VO 1S | No | |
| 17 | M | RSC | Streptococcus intermedius | Draf 2A | AugmentineVO+ Metronidazol IV 6S | Draf3 (3S) | |
| 23 | M | RSC | Staphylococcus aureus | Draf 2A | Clindamicina IV 6S | No | |
| Ball 2015 | 43 | M | RSC | Streotococcus anginosus | Draf 2A | Metronidazol + Moxicifloxacino VO 3M | No |
| Pérez 2017 | 7 | M | RSC | Flora mixta | Draf A + DE | Cefotaxima + Vancomicina + metronidazol IV 4S | No |
| Corcóstegui 2015 | 32 | M | Traumatismo+ cocaína | Streptococcus pneumoniae | Craneotomía frontal | Vancomicina+ ceftriaxona IV 6S + gentamicina tópica | Craneotomía frontal |
| Koltsidopoulos 2019 | 37 | F | RSC | Staphylococcus aureus | Draf 2A | Vancomicina+ ceftriaxona IV 6S | No |
| Rumi 2019 | 56 | M | RSC | Flora mixta | Draf 3 + craneotomía frontal | Vancomicina+ ceftriaxona IV 6S | No |
| Olmaz 2019 | 12 | M | RSC | Flora mixta | Draf A + DE | Vancomicina+ ceftriaxona IV 6S | No |
| Simonin 2018 | 21 | M | Traumatismo | Staphylococcus aureus | Draf 3 + craneotomía frontal | Vancomicina+ ceftriaxona IV 6S | No |
| Moris 2018 | 55 | F | RSC | Staphylococcus aureus | Sinuplastia con balón | Vancomicina+ ceftriaxona IV 6S | No |
| Cannon 2017 | 5 | M | RSC | Streotococcus anginosus | Draf 2A | Vancomicina+ ceftriaxona IV 6S | No |
| Allfathe 2017 | 7 | F | RSC | Staphylococcus aureus | Draf 1 | Vancomicina+ ceftriaxona IV 6S | No |
| Nastovska 2017 | 15 | M | RSC | Streotococcus anginosus | Draf 1 | Bencympenicilina IV 6S | No |
| Geyton 2017 | 45 | M | RSC | Staphylococcus aureus | Draf 3 | Vancomicina+ ceftriaxona IV 6S | No |
| Simsek 2018 | 65 | M | RSC | Flora mixta | Draf 3 | No especifica | No |
| Pasin 2018 | 81 | M | RSC | Streptococcus constellatus | Draf 2B | Vancomicina+ ceftriaxona IV 6S | No |
| Brown 2017 | 3 | M | RSC | No especifica | Draf 2A | No especifica | No |
| Ganapathy 2017 | 77 | F | RSC | Staphylococcus aureus | Draf 2A | Vancomicina+ ceftriaxona IV 6S | Draf 3 (4S) |
| Apostolakos 2016 | 20 | M | RSC | No especifica | Draf 1 | Metronidazol+ Ceftriaxona IV 6S | No |
| Palabiyik 2016 | 18 | M | RSC | Escherichia coli | Draf 2A | No especifica | No |
| 17 | M | RSC | No especifica | Draf 2A | Vancomicina+ ceftriaxona IV 6S | No | |
| 9 | M | RSC | No especifica | Draf A + DE | Vancomicina+ ceftriaxona IV 6S | No | |
| 11 | F | RSC | No especifica | Draf 2A | Vancomicina+ ceftriaxona IV 6S | No | |
| 7 | M | Traumatismo | Staphylococcus epidermidis | Draf A + DE | Vancomicina+ ceftriaxona IV 6S | No | |
| 17 | M | RSC | No especifica | Draf 2A | Vancomicina+ ceftriaxona IV 6S | No | |
| Miller 2016 | 65 | M | RSC | Flora mixta | Draf 3 | Vancomicina+ ceftriaxona + metronidazolIV 6S | No |
En la mayoría de los casos se realizó un drenaje endoscópico tipo Draf 2A (60%), el 16.7% de los pacientes fueron sometidos a un Draf 3, el 10% a un Draf 1 y el 3.3 % a un Draf 2B. Un paciente fue tratado con sinuplastia con balón y otro con craneotomía externa aislada. Del total de pacientes, en el 23.33 %, se realizó una cirugía endoscópica asociada a un abordaje externo; en éstos, había una complicación intracraneal en el momento del diagnóstico. Todos los pacientes tenían antibióticos orales o intravenosos de duración variable; aunque predomina el esquema terapéutico de vancomicina y ceftriaxona intravenosas durante 6 semanas en el 53.3% de los pacientes. No hubo más complicaciones después de la intervención endoscópica sinusal, con resolución completa del cuadro. Las cirugías de Draf 3 y 2B se realizaron con neuronavegador de forma sistemática. No hubo mortalidad en los pacientes revisados y después del drenaje endonasal, no hubo ninguna indicación adicional que requiriera la conversión a un enfoque externo debido al fracaso del procedimiento primario. Sólo en dos pacientes hubo que realizar un tratamiento endoscópico más agresivo (a las 4 semanas en uno y a las 6 semanas en otro) por la persistencia del absceso subperióstico y re-estenosis del orificio del receso del frontal; y en un paciente, una craneotomía frontal. La presencia de fístulas (presentes en dos de los pacientes), cicatrizaron sin necesidad de desbridamiento quirúrgico o cierre.
DISCUSIÓN
El tumor inflamatorio de Pott es un absceso subperóstico de la pared anterior del seno frontal, asociado a una osteomielitis del hueso frontal subyacente; descrito por Sir Percival Pott en 1768 por primera vez. Por lo general, está relacionado con la sinusitis frontal; sin embargo, también puede ocurrir como resultado de un traumatismo craneal o abuso de cocaína [7]; como ocurre en dos de los pacientes de la revisión.
Puede ser detectado en pacientes de todas las edades, con una mayor incidencia entre los adolescentes; pues es el momento en el que la vascularización de las venas diploicas, que recogen el drenaje venoso del seno frontal, alcanzan su máximo desarrollo; esto explicará las complicaciones intracraneales sin la extensión directa del hueso en los adolescentes [23].
Los organismos más comunes fueron, Stafilococus, Stretococcus y flora mixta (incluyendo bacterias anaerobias); al igual que la descrita en el resto de la literatura [1,2,23]. Debido a la concentración relativamente baja de oxígeno en el seno frontal, los cultivos de los pacientes con tumor inflamatorio de Pott, a menudo revelaron afectación polimicrobiana [1,2,25]. Hasta una cuarta parte de los pacientes revisados no tuvo crecimiento debido, en la mayoría de las ocasiones, al tratamiento antibiótico previo.
El drenaje quirúrgico externo había sido el método histórico de manejo del tumor de Pott; permite el drenaje de la colección purulenta y la eliminación de segmentos osteomielíticos de la cara ósea anterior del seno frontal. Sin embargo, la posibilidad de crear una fístula sinocutánea, junto con la aparición de antibióticos mejorados y las técnicas endoscópicas, tal vez han llevado a la disminución de la utilidad de un procedimiento externo [1].
Leong et al en su revisión sistemática de 29 casos ha demostrado la seguridad y eficacia de la cirugía endonasal en el tratamiento del tumor de Pott, exponiendo que, la sinusotomía frontal o la sinuplastia con balón fueron suficientes, junto a los antibióticos, para restablecer el drenaje del seno frontal durante la fase aguda de la infección [2]. Ninguno de estos casos resultó en la progresión de la enfermedad (infección recurrente o formación de abscesos que requieren drenaje externo [2]; al igual que en la realizada por nosotros. En la mayoría de los casos revisados, la cirugía endoscópica con un procedimiento Draf 2A era suficiente, consiguiendo un buen drenaje seno en la mayoría de los pacientes. Las cirugías de Draf 3 y 2B se realizaron con neuronavegador de forma sistemática en los pacientes revisados y en la mayoría de las ocasiones en el 2A; utilizando instrumentación angulada y fresas comedoras y sistemas visuales de alta definición. En algunas series de caso se recomienda presión externa suave en la zona frontal para facilitar la salida del pus, así como una forma de orientación y al finalizar la cirugía endoscópica realizar abundantes lavados con suero salino fisiológico. Por lo general no se dejan stents o drenajes [3].
La cirugía de revisión se realizó en tres pacientes debido a la re-estenosis del frontal. La tasa de re-estenosis es algo moderada, por lo que es posible que sea aconsejable un tratamiento endoscópico de inicio de lo más conservador posible [3,26].
Los pacientes con extensión intracraneal (meningitis, empiema epidural, absceso del lóbulo frontal y trombosis del seno cavernoso) de la infección, pueden requerir un enfoque combinado endoscópico y neuroquirúrgico; algo que se realiza de forma sistemática en nuestra revisión de pacientes [22].
En lo que respecta al esquema de antibioticoterapia, se recomiendan entre 4 a 6 semanas de antibioticoterpia; preferentemente de manera intravenosa; al menos las primeras semanas; sería con cefotaxima o ceftriaxona 200mg/kg/día; pues las cefalosporinas de tercera generación atraviesan muy bien la barrera hematoencefálica y cubren gran negativos; asociada a vancomicina 60mg/kg/día para cubrir cocos grampositivos tanto aerobios como anaerobios; la vancomicina además cubre el Staphylococcus aureus meticilín resistente [5]. Sin embargo, es importante recordar que la terapia con antibióticos por sí sola es poco probable que sea adecuada para la resolución completa del cuadro; sólo en un paciente de la revisión se utilizó antibioticoterapia de forma exclusiva. Aunque la base de evidencia para esta afirmación es baja, el objetivo del tratamiento sigue siendo drenar y ventilar el seno frontal y tratar la infección (sinusitis, osteomielitis) al mismo tiempo; como prácticamente, en la totalidad de los artículos revisados.
se resuelve después del drenaje endonasal del seno frontal. Algunos autores abogan por la colocación de un stent externo temporal en el tracto de la fístula para permitir la irrigación del seno, otros cirujanos extirpan la fístula con un cierre de múltiples capas con músculo temporal y fascia; en nuestro caso ambas remitieron de forma espontánea tras el tratamiento endoscópico [1,2,4,5]. Encontramos una tasa de recuperación del 100% en todos los pacientes revisados con el esquema de tratamiento propuesto.
CONCLUSIONES
El tumor inflamatorio de Pott sin complicaciones se puede manejar con éxito mediante un enfoque endoscópico, combinado con antibióticos durante varias semanas. La disponibilidad de instrumentos en ángulo motorizados, sistemas visuales de alta definición, así como la neuronavegación, han proporcionado a los otorrinolaringólogos modernos una alternativa que supera a las técnicas abiertas tradicionales. Además, la biodisponibilidad mejorada de los antibióticos puede reducir la necesidad de una craneotomía y drenajes externos.