INTRODUCCIÓN
El riñón pélvico es una variante anatómica producida por un fallo en la migración renal entre la cuarta y octava semana del desarrollo embrionario (1). Se estima que su incidencia es de 1 de cada 2100-3000 nacimientos en la población general (2) y su asociación con aneurismas de aorta abdominal (AAA) es todavía más infrecuente. En un estudio publicado por Faggioli y cols. únicamente el 0,18 % de los pacientes que se sometieron a una cirugía aórtica mayor presentaban dicha variante anatómica (3). Hasta la fecha, han sido reportadas en la literatura 29 reparaciones de AAA asociados a riñón pélvico (2,4). Exponemos un caso exitoso de tratamiento quirúrgico de AAA con riñón pélvico solitario donde se preservó la vascularización renal mediante bypass con vena safena invertida.
CASO CLÍNICO
Varón de 69 años, exfumador, remitido por hallazgo ecográfico casual de AAA. Presentaba antecedentes de cardiopatía isquémica crónica, hipertensión arterial, dislipemia, hiperuricemia e insuficiencia renal estadio 4 (creatinina: 2,75 mg/dl). Se realizó angioTC evidenciando la ausencia de riñones en localización ortotópica, un AAA de 56 mm de diámetro máximo y un riñón único de localización pélvica derecha. La vascularización renal consistía en una arteria única que nacía de la bifurcación aórtica (Fig. 1A).
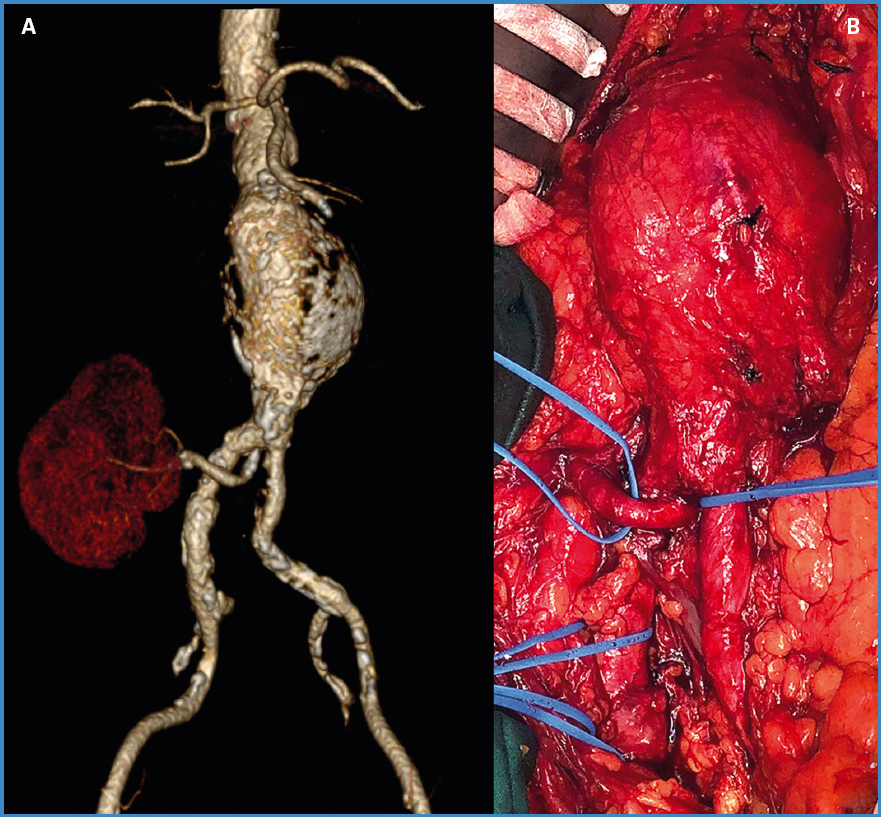
Figura 1. A. Reconstrucción 3D de angio-TAC preoperatoria. B. Imagen intraoperatoria del AAA con riñón pélvico solitario derecho asociado.
A la exploración física destacaba la presencia de una masa abdominal pulsátil y pulsos a todos los niveles en ambos miembros inferiores.
El paciente se sometió a tratamiento quirúrgico de forma programada bajo anestesia general. Se realizó un abordaje aórtico transperitoneal mediante laparotomía media. A continuación, se procedió a la disección del cuello aórtico proximal de ambas iliacas comunes y se controló la arteria del riñón ectópico con vessel loops (Fig. 1B). Tras anticoagulación sistémica con 5000 UI de heparina sódica e infusión de manitol intravenoso, se ligó la arteria renal proximal y se realizó una anastomosis término-terminal de un segmento de vena safena interna (VSI) invertida. A través de ella se infundieron bolos de solución salina fría cada 15-20 minutos. Tras el clampaje aórtico se llevó a cabo una arteriotomía longitudinal sobre el aneurisma, extracción del trombo mural y la anastomosis de un injerto de dacrón de 14 x 7 mm a nivel proximal. Seguidamente, se adecuó la longitud y orientación del segmento de VSI, se anastomosó su extremo proximal a la rama derecha de la prótesis y se clampó distalmente. Esto permitió mantener la perfusión renal durante la realización de las anastomosis de ambas ramas protésicas a las iliacas comunes. El tiempo total de isquemia renal fue de 60 minutos. Se ha de señalar que la rama derecha precisó ser tunelizada por el interior de la arteria iliaca común proximal para así evitar la compresión de la vena renal (Fig. 2A).
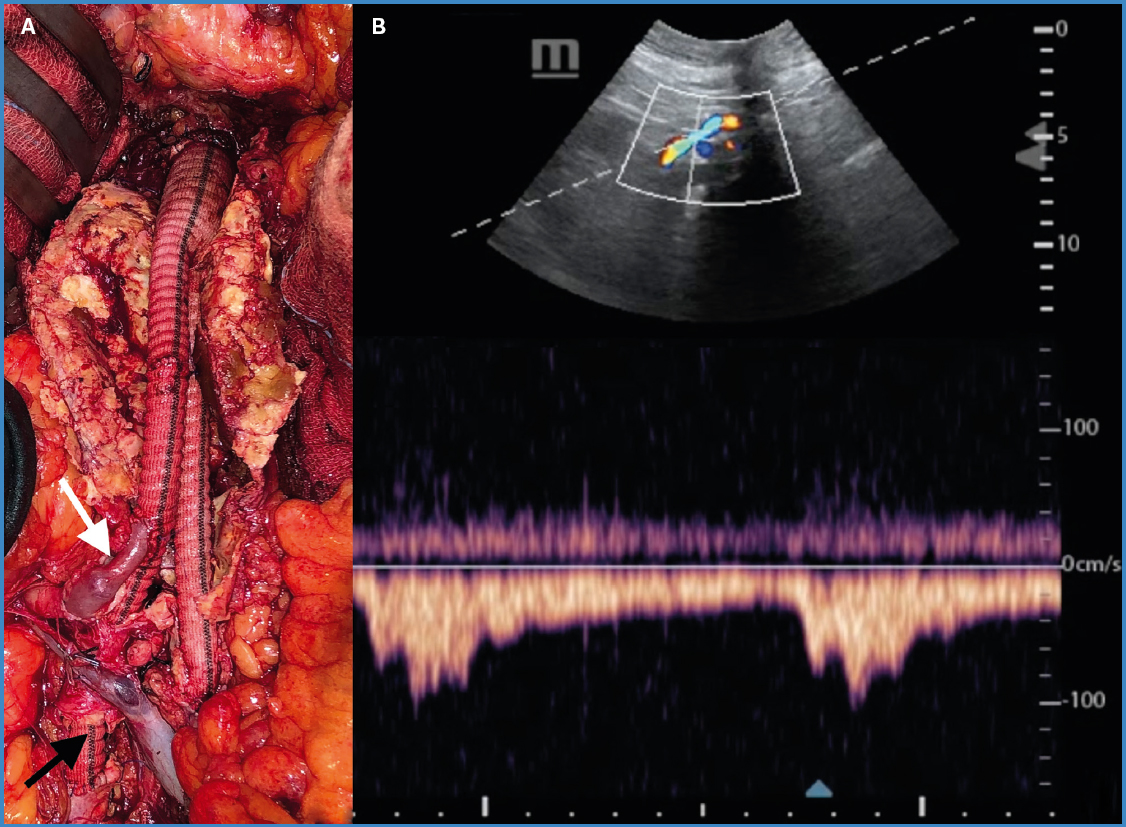
Figura 2. A. Imagen intraoperatoria tras el tratamiento. Flecha blanca: bypass renal. Flecha negra: tunelización de rama protésica por el interior de arteria iliaca común derecha con el objetivo de evitar la compresión de la vena renal. B. Ecografía doppler control del bypass renal un mes tras la cirugía.
El posoperatorio transcurrió sin incidencias relevantes a excepción de un deterioro transitorio de la función renal. Alcanzó los 3,6 mg/dl de creatinina a las 48 h de la cirugía y recuperó niveles basales (2,29 mg/dl) al alta tras seis días de estancia hospitalaria (24 h en unidad de reanimación).
En el control realizado un mes posoperatorio el paciente no presentó complicaciones evidenciando mediante ecodoppler permeabilidad del bypass renal, así como del injerto protésico y sus ramas (Fig. 2B).
DISCUSIÓN
La presencia de un riñón ectópico de localización pélvica supone un reto a la hora de plantear el tratamiento de la patología aneurismática concomitante.
Por un lado supone una limitación a la hora de efectuar tratamientos endovasculares y obliga a la utilización de endoprótesis con ramas o fenestraciones manufacturadas a medida (5,6). La utilización de este tipo de técnicas resulta habitual en el tratamiento de pacientes que presentan arterias polares renales adicionales en riñones ortotópicos. Sin embargo, la presencia de riñones de localización pélvica implica una dificultad en diseño de los dispositivos ya que se precisan de ramas o fenestraciones con orientación y localización atípica. Asimismo, en los casos donde existen arterias renales múltiples, es fundamental considerar el diámetro de las mismas para valorar cual de ellas es susceptible de ser conservada. En pacientes en los cuales la función renal preoperatoria está dentro de la normalidad y se conserva la función de la arteria renal principal, las arterias renales de diámetro inferior a 3 mm pueden ser sacrificadas (6).
Por otro lado, esta variante anatómica también aumenta la complejidad de los casos sometidos a tratamiento quirúrgico, ya que implica someter al riñón ectópico a un periodo de isquemia normotérmica. La necesidad de minimizar el tiempo de isquemia renal durante el clampaje constituye un aspecto fundamental a la hora de llevar a cabo este tipo de abordaje, habiéndose descrito diferentes técnicas para este fin. El método más sencillo es la administración de catecolaminas y diuréticos durante el clampaje simple, aunque debería ser empleado en casos donde se prevé un tiempo de isquemia corto. La técnica de doble clampaje proximal, descrita en el tratamiento de AAA en pacientes trasplantados, permite mantener flujo retrógrado durante la realización de la anastomosis proximal (7). La perfusión renal selectiva con soluciones cristaloides frías de forma continua o mediante bolos, constituye la técnica más frecuentemente utilizada (2). Finalmente, la realización de un bypass aortofemoral o axilofemoral temporal o la utilización de bombas de circulación extracorpórea permiten mantener de forma continua la perfusión renal, aunque conllevan un aumento de la complejidad del procedimiento.
En nuestro caso, dada la edad y las características del paciente se optó por realizar un tratamiento quirúrgico. Como método para minimizar el daño por isquemia renal optamos por la infusión de solución salina fría, ya que se trata de un método simple y eficaz con el que además estamos familiarizados dada nuestra experiencia en el campo del trasplante renal.
Una planificación preoperatoria minuciosa resulta fundamental en el tratamiento de aneurismas aórticos asociados a riñones pélvicos. La elección de la técnica quirúrgica o endovascular a utilizar debe basarse en las características del paciente, la disposición y vascularización del riñón ectópico, la morfología del aneurisma y la experiencia del cirujano. Además, a la hora de realizar un abordaje quirúrgico, se debe considerar el uso de las diferentes técnicas existentes para minimizar lo máximo posible el tiempo de isquemia renal.














