Introducción
La mama tuberosa es una entidad malformativa muy frecuente en mujeres jóvenes que se produce por una alteración en el desarrollo de la mama con hipoplasia en los diferentes cuadrantes de la misma asociada con frecuencia a una marcada asimetría, y que puede generar un impacto psicológico importante en las pacientes que la sufren.
Para entender la fisiopatología de esta malformación es importante entender su origen embriológico. La mama tiene un origen ectodérmico y se desarrolla a partir del desdoblamiento de las capas superficial y profunda de la fascia superficial. La teoría que mejor explica las diferentes entidades clínicas de mamas tuberosas se basa en una alteración en el desdoblamiento de la fascia superficial, con engrosamiento de la misma en la región periareolar.(1) Este anillo constrictivo provoca las características clínicas presentes, en diferente grado, en las mamas tuberosas:(1) herniación de la areola sobre el anillo constrictor; hipoplasia de polo inferior (y en casos severos de polo superior); y surcos submamarios de implantación alta con distancia pezón-surco submamario corta.
En base a estas características clínicas se han desarrollado diferentes clasificaciones de mama tuberosa, de las que las más conocidas son la de Grolleau(2) y la de Von Heinburg.(3) Por su simplicidad, para nuestra toma de datos utilizamos la clasificación de Grolleau que establece 3 grados de mama tuberosa: grado I, hipoplasia del cuadrante inferomedial; grado II, hipoplasia de ambos cuadrantes inferiores; y grado III, hipoplasia de los 4 cuadrantes de la mama.
En cuanto a su tratamiento, la gran cantidad de técnicas quirúrgicas descritas y utilizadas en similar frecuencia por diferentes cirujanos plásticos demuestra el gran reto quirúrgico que supone esta patología. Entre el arsenal quirúrgico disponible destacamos la técnica de Puckett,(4) que a través de una incisión periareolar inferior realiza un colgajo glandular con pedículo transversal que desdobla hacia cuadrantes inferiores para solventar la ausencia de tejido en los mismos. Más tarde, Ribeiro(5) expuso su técnica de colgajos glandulares con el objetivo principal de evitar el material protésico, punto coincidente y fundamental en el desarrollo del presente artículo. Para ello, y mediante una incisión periareolar, libera completamente la glandular mamaria de su envoltura cutánea para realizar posteriormente un colgajo glandular de pedículo inferior que se pliega sobre sí mismo con el objetivo de rellenar el polo inferior y descender el surco submamario. El principal problema de esta técnica viene derivado de la limitación en cuanto al volumen mamario que proporciona.
Derivada de las anteriores, Palacín(6) desarrolla una técnica en la que añade a la técnica de Puckett un abordaje submamario e incisiones transversales para facilitar el descenso de la mama presa en los polos superiores, asociando habitualmente el uso de material protésico.
Por último, destacar el aumento exponencial del uso de injertos grasos para el tratamiento quirúrgico de esta malformación. Se trata de un procedimiento muy útil en la mayoría de las pacientes, seguro y con una tasa de complicaciones muy baja.(7) La técnica de procesamiento del tejido graso a infiltrar, bien descrita por Coleman,(8) permite una tasa de prendimiento alta, con resultados naturales y evitando el uso de material protésico.
A modo de resumen, con colgajos glandulares conseguimos restaurar principalmente las alteraciones de la forma de la mama y se tendrán que asociar al uso de material protésico y/o injerto graso para corregir el defecto o asimetría de volumen.
En este artículo exponemos una serie amplia de pacientes en la que analizamos la transición que hemos llevado a cabo en el manejo de la mama tuberosa en el Hospital General de Alicante, España, pasando del uso de prótesis mamarias en la mayoría de los casos, a la reconstrucción exclusiva con injerto graso en el transcurso de 9 años. Esta transición en la elección de la técnica vino motivada principalmente por el alto número de complicaciones y reintervenciones a las que se exponían las pacientes por el hecho de ser portadoras de implantes mamarios desde edades tempranas.
Este cambio de paradigma que analizamos continúa la línea evolutiva en reconstrucción por cáncer de mama en la que se prioriza cada vez más la reconstrucción con tejido autólogo.(9)
Material y método
Presentamos un estudio descriptivo y retrospectivo en el que recogemos 101 casos de cirugía de mamas tuberosas operados entre noviembre de 2010 hasta junio de 2022 en el Servicio de Cirugía Plástica del Hospital Universitario de Alicante, España, hospital del seguro público de salud español. Hasta 2013 el uso de prótesis mamaria fue el procedimiento habitual, siendo sustituido desde 2014 por el uso exclusivo de tejido autólogo.
En la primera visita, junto con la exploración física, valoramos también las posibles zonas donantes de grasa así como los factores que puedan suponer un riesgo de complicaciones.
Solicitamos una ecografía mamaria previa a la cirugía en pacientes menores de 30 años o una mamografía en aquellas mayores de 30 años. Es importante destacar que, en esta primera consulta, dedicamos un tiempo a advertir a las pacientes de que en nuestro servicio la cirugía se realizará exclusivamente mediante el uso de tejido autólogo sin recurrir a prótesis, y que el objetivo de la intervención será reconstruir el defecto y alcanzar la mayor simetría mamaria posible sin el uso de implantes. También queda reflejada en el consentimiento informado la posibilidad de que puedan necesitar más de un procedimiento quirúrgico.
Los principales criterios de exclusión fueron, en nuestra serie, el tabaquismo severo, un índice de masa corporal (IMC) >32, ecografía mamaria alterada o historia familiar de cáncer de mama consistente. También consideramos como criterio de exclusión las expectativas discordantes por parte de la paciente con respecto a nuestra técnica quirúrgica; es decir, aquellas pacientes que expresan claramente que desean tener un volumen mamario grande o cuadrantes superiores proyectados, resultados que no son alcanzables sin usar implantes.
Intervenimos a pacientes mayores de 18 años a excepción de aquellas que siendo menores de dicha edad y suponiendo un desarrollo mamario completo, presentan un alto impacto psicológico diagnosticado previamente por Psiquiatría.
Recogimos datos en relación a la edad, grado de tuberosidad según la clasificación de Grolleau,(2) número de intervenciones quirúrgicas, procedimiento en mama derecha, procedimiento en mama izquierda y complicaciones.
El tiempo medio de seguimiento de las pacientes de nuestro grupo de estudio fue de 2 años en las pacientes no portadoras de prótesis, y en las que las empleamos la valoración en el servicio se continúa indefinidamente de forma bianual.
Las técnicas quirúrgicas que utilizamos con mayor frecuencia son las siguientes:
- Pexia mamaria: en nuestro servicio realizamos principalmente pexias mamarias de pedículo superior y súperomedial; en cuanto al patrón cutáneo utilizado depende del grado de ptosis, empleando la pexia periareolar en casos de ptosis leve (asociada a técnicas de round-block) o bien pexias con patrón de Wise en aquellos casos donde la ptosis es moderada o severa. En casos seleccionados (mamas de volumen y ptosis moderados) también realizamos la técnica de Lejour.(10) Debido a la elevada frecuencia de asimetría mamaria presente en esta malformación, es muy habitual que empleemos patrones cutáneos diferentes en cada mama. Es importante explicar este punto a las pacientes en la consulta prequirúrgica.
- Injerto graso: utilizamos como zona donante prioritaria la cara interna de los muslos. Realizamos infiltración con solución de ringer actato + 1 ampolla de adrenalina y 1 ampolla de ropivacaína al 7% por cada 1000 ml. Empleamos prendas compresivas en el postoperatorio durante 1 mes como media. La obtención y procesamiento de la grasa la realizamos según la técnica de Coleman(8) y, en los últimos años, hemos utilizado cada vez con mayor frecuencia sistemas cerrados de filtrado y lavado de la grasa que nos permiten optimizar el tiempo quirúrgico.
Para la lipoinyección en la zona receptora, empleamos pequeños puertos ocultos en el surco submamario y/o utilizando las cicatrices previas de la pexia mamaria, evitando incisiones en la línea media mamaria que puedan dar como resultado cicatrices inestéticas. Infiltramos como máximo 250 cc de grasa purificada en cada mama por procedimiento, aunque la cantidad exacta depende del volumen previo de cada mama. Para lograr una mayor tasa de prendimiento del tejido graso infiltrado, es muy importante infiltrar la grasa en diferentes planos (subcutáneo, subglandular y subfascial/intramuscular). Recomendamos realizar un segundo tiempo quirúrgico de injerto graso tras un intervalo mínimo de 3 meses.
- Colgajos glandulares: utilizamos como colgajo principal la técnica de Puckett,(5) y con menor frecuencia hemos realizado colgajos de pedículo lateral según técnica de Grolleau.(11)
- Prótesis mamarias: las empleamos hasta el año 2013, principalmente de gel de silicona, anatómicas y texturizadas. Al asociar habitualmente el uso del colgajo de Puckett, la vía de colocación de los implantes fue principalmente la periareolar y el plano de colocación del implante el submuscular. En aquellos casos que no requirieron pexia periareolar, la vía de abordaje fue la submamaria, realizando la técnica de Palacín.(6)
- Expansores mamarios: en 1 solo caso, con tuberosidad severa e hipoplasia total, empleamos un expansor mamario tipo Becker.
El esquema general sobre el que trabajamos sería el siguiente (Tabla I.):
-
Primera cirugía:
■ Pacientes a partir de 18 años de edad, a excepción de aquellos casos con deformidades mayores que generen impacto en sus actividades básicas de la vida diaria (ABVD).
■ Si hay asimetría, la simetrización se realizará hacia la mama de menor tamaño.
■ Pexia mamaria: periareolar / Wise.
■ Injerto graso uni/bilateral.
■ Corrección de la tuberosidad si precisa (técnica de Puckett).
-
Segunda cirugía:
-
Tercera cirugía:
Tabla I. Algoritmo terapéutico en el manejo de la mama tuberosa.
| OBJETIVO | TÉCNICA QUIRÚRGICA | |
|---|---|---|
| PRIMERA CIRUGÍA | Corregir forma y volumen mamario. Simetrización a la mama de menor tamaño. |
- Remodelado glandular (Puckett). - Lipoinjerto. - Simetrización mama contralateral (pexia mamaria). |
| SEGUNDA CIRUGÍA (Mínimo 3 meses tras la primera cirugía) | Completar la corrección en volumen si precisa. |
- Segundo tiempo lipoinjerto. - Retoque cicatrices si precisa. |
| TERCERA CIRUGÍA (Mínimo 3 meses tras la segunda cirugía) | Corregir volumen si precisa en deformidades muy acentuadas. |
- Tercer tiempo lipoinjerto (poco frecuente). - Retoque cicatrices si precisa. |
Realizamos el procedimiento en todos los casos bajo anestesia general. En cuanto al postoperatorio, el tiempo de ingreso es corto, con alta durante el mismo día en la mayoría de los casos. Pautamos antibioticoterapia, habitualmente con ceftriaxona (1gr preoperatorio) que continuamos con cefalosporinas durante 7 días para evitar complicaciones en relación al injerto graso. Mantenemos un vendaje durante los 3 primeros días, hasta la primera revisión en consulta donde lo sustituimos por un sujetador sin costuras si la evolución ha sido favorable. Realizamos seguimiento a la semana, al mes y al año de la intervención.
Resultados
En el periodo comprendido entre noviembre de 2010 y junio de 2022 intervinimos 101 casos de mujeres diagnosticadas de mamas tuberosas en diferente grado. Hasta el año 2013 priorizamos el uso de prótesis mamarias más colgajo glandular tipo Puckett. A lo largo del 2013 comenzamos a sustituir el uso de material protésico por tejido autólogo. La razón que motivo esta transición es- tuvo en que, al ser la edad media de las pacientes intervenidas baja, el índice de reintervenciones relacionadas con las prótesis mamarias era demasiado alto (por contractura capsular principalmente), lo que suponía nuevas intervenciones quirúrgicas en esas pacientes y un gasto sanitario elevado para un servicio de Cirugía Plástica público.
Desde noviembre de 2010 hasta diciembre de 2013 operamos un total de 26 pacientes, de las que en 21 (80.8%) empleamos material protésico y en las 5 restantes (19.2%) empleamos tejido autólogo.
Desde 2014 hasta junio del 2022 operamos a 75 pacientes, en las que únicamente empleamos prótesis en 9 (12%), mientras que empleamos tejido autólogo en 66 (88%). Esto supuso un claro cambio en el paradigma de indicación de técnica quirúrgica en mamas tuberosas en nuestro servicio.
La edad media de las pacientes de nuestro estudio fue de 23 años (mínima de 17 años y máxima de 36 años). En cuanto a los grados de tuberosidad según la clasificación de Grolleau, 19 casos (18.9%) correspondieron a tuberosidad grado I, 54 casos (53.4%) a grado II y 28 (27.7%) a grado III.
En cuanto a las técnicas quirúrgicas empleadas en el periodo de estudio total (noviembre de 2010 a junio de 2022), realizamos en 15 casos (14.9%) pexias mamarias aisladas con las técnicas descritas previamente; en 31 casos (30.7%) pexias mamarias con injerto graso; en 25 casos (24.8%) asociamos pexia mamaria, colgajo glandular tipo Puckett más injerto graso; y por último, en 30 casos (29.7%) realizamos reconstrucción con técnica Puckett más prótesis mamaria.
La tasa media de intervenciones en el grupo de 101 pacientes fue de 2.1 tiempos quirúrgicos (mínima 1 tiempo quirúrgico, máximo 4 tiempos quirúrgicos), incluyendo en estos datos las intervenciones realizadas con anestesia local para retoques de cicatriz (Tablas II y III).
Tabla II. Técnicas mamarias utilizadas en función del grado de tuberosidad.
| 101 pacientes, noviembre 2010 – junio 2022 | |
|---|---|
| Reconstrucción con prótesis | 30 casos (29.7%) |
| Reconstrucción con tejido autólogo | 71 casos (70.3%) |
| Grados de Grolleau | 19 casos (18.9%) grado I; 54 casos (53.4%) grado II; 28 casos (27.8%) grado III |
| Edad media de las pacientes | 23 años (mínima 17, máxima 36) |
| Media de tiempos quirúrgicos | 2.1 tiempos (mínimo 1, máximo 4) |
| Reconstrucción con pexia mamaria | 15 casos (14.9%) |
| Pexia mamaria + lipoinjerto | 31 casos (30.7%) |
| Pexia mamaria + Puckett + lipoinjerto | 25 casos (24.7%) |
| Puckett + prótesis | 30 casos (29.7%) |
Tabla III. Transición del uso de material protésico a tejido autólogo en nuestro periodo de estudio
| Noviembre 2010 - Diciembre 2013 | Enero 2004 - Junio 2022 | |
|---|---|---|
| Uso de material protésico | 21 pacientes (80.8%) | 9 pacientes (12%) |
| Uso exclusivo de tejido autólogo | 5 pacientes (19.2%) | 66 pacientes (88%) |
En aquellos casos en los que se lleva a cabo pexia mamaria y técnica de Puckett, se pueden realizar de forma simultánea ambos procedimientos sin aumentar la tasa de complicaciones ni disminuir la tasa de prendimiento graso.
En cuanto a las complicaciones en el postoperatorio inmediato de aquellas pacientes intervenidas con uso de tejido autólogo, únicamente 1 paciente necesitó reintervención por hematoma unilateral; se trataba de un caso en el que habíamos realizado técnica de Puckett más lipoinjerto. No encontramos ningún caso de infección mamaria ni de otras complicaciones agudas.
El seguimiento habitual de las pacientes de nuestro grupo de estudio fue de 2 años en aquellos casos tratados con tejido autólogo. Sin embargo, en los casos en los que empleamos prótesis, continuamos el seguimiento de forma indefinida, bianualmente, siendo el seguimiento máximo de las pacientes del grupo de estudio de 8 años y 10 meses.
En cuanto a las complicaciones a largo plazo, la más frecuente fue el ensanchamiento de las cicatrices periareolares que se produjo en 21 casos (20.8%). Corregimos esta complicación habitualmente en el segundo tiempo quirúrgico que suelen precisar las pacientes en las que hemos empleado tejido autólogo. No tuvimos ningún caso de necrosis grasa que precisara intervención. Tampoco hemos detectado ningún caso de cáncer de mama a lo largo del seguimiento de esta cohorte de pacientes. En cuanto a las zonas donantes, no tuvimos tampoco ninguna complicación que precisara reintervención quirúrgica (Fig. 1, 2, 3, 4).
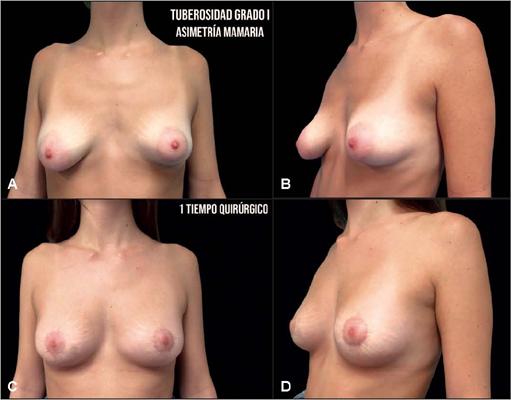
Fig. 1A y B. Mujer de 24 años con tuberosidad grado I de Grolleau. Pexia mamaria periareolar, round-block. Un tiempo quirúrgico. C y D. Imágenes postoperatorias a los 12 meses de seguimiento.
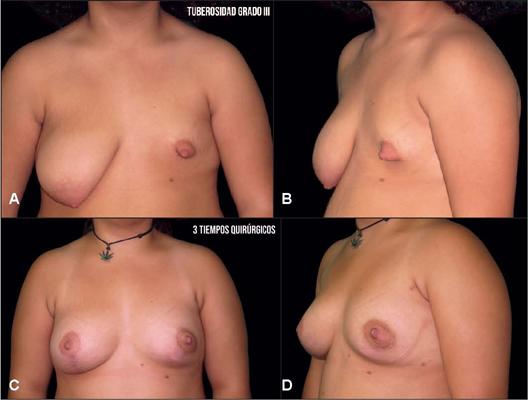
Fig. 2A y B. Mujer de 19 años con tuberosidad grado III de Grolleau y asimetría marcada. Tratamiento en 3 tiempos quirúrgicos. Primer tiempo: pexia mamaria con patrón de Wise en mama derecha y pexia periareolar en mama izquierda más injerto graso de 170 cc. Segundo tiempo: lipoinjerto de 210 cc en mama izquierda y 30 cc en mama derecha. Tercer tiempo: lipoinjerto de 70 cc en mama izquierda. C y D. Imagenes postoperatorias a los 12 meses de seguimiento, tras la última intervención.
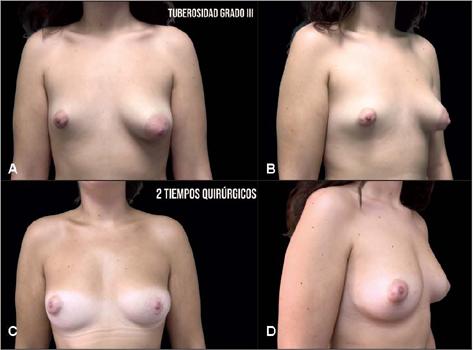
Fig. 3A y B. Mujer de 21 años con tuberosidad grado III de Grolleau. Primer tiempo quirúrgico: pexia periareolar en mama izquierda más lipoinjerto en mama derecha de 250 cc. Segundo tiempo quirúrgico: lipoinjerto de 220 cc en mama derecha y de 40 cc en mama izquierda, más retoque de cicatriz ensanchada. C y D. Imágenes postoperatorias a los 12 meses de la última intervención.
Discusión
Planteamos en este artículo el modo actual de afrontar en nuestro servicio la cirugía en pacientes con mamas tuberosas. El motivo por el que cambiamos nuestro protocolo de actuación en estas pacientes, en su mayoría jóvenes o adolescentes, fue el alto índice de reintervenciones que precisaban en relación al hecho de ser portadoras de prótesis mamarias. Esto suponía, a largo plazo, nuevas intervenciones quirúrgicas de forma casi asegurada y un gasto sanitario elevado para un servicio de Cirugía Plástica de un hospital del sistema público de salud.
En nuestra cohorte de estudio, la tasa media de intervenciones fue de 2.1 tiempos quirúrgicos por paciente, incluyendo en estos datos las intervenciones que fueron necesarias para retoques de cicatrices con anestesia local. Debemos tener en cuenta que el segundo tiempo quirúrgico para injerto graso suele ser, en nuestras manos, una cirugía de 1 hora de duración, en la que la paciente es dada de alta hospitalaria en el mismo día. Limitamos el seguimiento de estas pacientes a un máximo de 2 años tras la última cirugía, mientras que para las pacientes portadoras de prótesis, llevamos a cabo un seguimiento de por vida, de forma bianual.
Teniendo en cuenta, como hemos dicho, que las pacientes con mamas tuberosas suelen ser muy jóvenes cuando se someten a cirugía y que según los datos publicados, las pacientes portadoras de material protésico presentan de media una tasa de reintervención de en torno al 20% a los 20 años,(12) nuestros resultados nos parecen muy favorables para decantarnos por la técnica que emplea solo material autólogo como una alternativa muy atractiva, segura y fácil de reproducir, que consigue un resultado natural y armónico con los cambios morfológicos que ocurren luego a lo largo de los años en el resto del cuerpo de las pacientes.(13)
Al utilizar material autólogo, evitamos aquellas complicaciones asociadas a implantes mamarios, que son elevadas, y entre las cuales destacamos:
- Contractura capsular periprotésica: 10 de cada 100 mujeres desarrollan cierto grado de contractura capsular a los 10 años de la implantación y pueden requerir nuevas intervenciones.(14)
- Mayor riesgo de dehiscencia y problemas de cicatrización, con sufrimiento y necrosis de la piel.
- Rotura de implantes.
- Linfoma anaplásico de células gigantes asociado a prótesis mamarias (LACG-AIM).(15)
- Sindrome ASIA (Sindrome autoinflamatorio inducido por adyuvantes),(16) aunque su evidencia científica está aún en estudio.
- La complicación más frecuente observada en nuestro grupo de estudio de 101 casos fue el ensanchamiento de las cicatrices periareolares (21 casos, 20.8%), si bien se trata de una complicación menor que se puede solventar con anestesia local sin precisar ingreso hospitalario. En nuestra experiencia, la inclusión de técnicas de round-block con material no reabsorbible disminuye en gran medida el índice de ensanchamientos periareolares.
En términos de resultados, hemos de tener en cuenta el filtro al que sometemos la indicación de este tipo de cirugía de mamas tuberosas entre nuestras pacientes, ya que tal y como hemos comentado en el apartado de Material y Método, durante la primera consulta explicamos que la reconstrucción con tejido autólogo va enfocada a restituir la forma alterada de la mama, simetrizando a la de menor tamaño, pero no tiene como objetivo conseguir grandes volúmenes mamarios, ni resultados con mucha proyección en polos superiores, que sí se pueden conseguir con material protésico. Esto nos lleva a descartar a las pacientes que tienen unas expectativas potencialmente incompatibles con la técnica utilizada en nuestro servicio.
En definitiva, y siguiendo el camino de la reconstrucción mamaria tras cáncer de mama en la que, en nuestra práctica, priorizamos siempre que es posible la reconstrucción con tejido autólogo, presentamos nuestra experiencia con esta alternativa de tratamiento quirúrgico de la mama tuberosa sin utilización de material protésico, con resultados consistentes, reproducibles y con una tasa de complicaciones baja.
Su empleo ha supuesto un cambio importante en el enfoque de tratamiento de esta entidad en nuestro hospital y, en base a ello, proponemos nuestro algoritmo terapéutico simplificado en la Tabla I.
Conclusiones
En nuestra experiencia, la cirugía de la mama tuberosa mediante el uso exclusivo de tejido autólogo permite corregir esta malformación en forma y volumen, con resultados reproducibles, sin recurrir al uso de material protésico, y con menores complicaciones y necesidad de reintervenciones a largo plazo.
Es importante para lograr este objetivo que las expectativas de las pacientes, una vez informadas del procedimiento a seguir, acepten que se trata de una técnica enfocada a restituir la forma alterada de la mama, simetrizando a la de menor tamaño, pero que no tiene como objetivo conseguir grandes volúmenes ni una gran proyección en polos superiores, que sí se podrían conseguir con el empleo de material protésico.