Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Clínica de Medicina de Familia
versão On-line ISSN 2386-8201versão impressa ISSN 1699-695X
Rev Clin Med Fam vol.9 no.1 Barcelona Fev. 2016
UN PACIENTE CON...
Enfermedad celíaca y déficit de IgA
Celiac disease and IgA Deficiency
Rafael Ramírez Montesinosa, Lidia Tikhomirovaa y Tomás Sempereb
aServicio de Medicina Interna. Hospital Sant Pau y Santa Tecla. Tarragona (España).
bServicio de Radiología. Hospital Sant Pau y Santa Tecla. Tarragona (España).
Dirección para correspondencia
RESUMEN
La enfermedad celíaca (EC) es una alteración sistémica de carácter autoinmune desencadenada por el consumo de gluten y prolaminas en individuos con predisposición genética. Los autoanticuerpos específicos anti-transglutaminasa 2 de tipo IgA, incluyendo antiendomisio y antigliadina, con alta especificidad, son marcadores de elección para su diagnóstico. Aproximadamente el 1 % de los casos de EC se presentan en asociación con inmunodeficiencia selectiva de IgA. Presentamos un caso de EC asociado a inmunodeficiencia selectiva de IgA que muestra posibles dificultades para su diagnóstico.
Palabras clave: Enfermedad Celíaca. Deficiencia de IgA. Enfermedades Autoinmunes.
ABSTRACT
Celiac disease (CD) is a systemic autoimmune disorder triggered by gluten and prolamine consumption in individuals with genetic predisposition. Specific anti-transglutaminase 2 IgA autoantibodies, including highly specific anti-endomysial and anti-gliadin antibodies, are markers of choice for diagnosis. Approximately 1% of CD cases are associated with selective IgA immunodeficiency. We report a case of CD associated with selective IgA immunodeficiency that shows possible difficulties for diagnosis.
Key words: Celiac Disease. IgA Deficiency. Autoimmune Diseases.
Introducción
La enfermedad celíaca (EC) es una afectación sistémica de carácter autoinmune desencadenada por el consumo de gluten y prolaminas relacionadas en individuos con predisposición genética. Los autoanticuerpos específicos anti-TG2 de tipo IgA, incluyendo antiendomisio y antipéptidos deamidados de gliadina, con una especificidad de entre el 98 y el 100 %, son los marcadores de elección para el diagnóstico1. No obstante, la EC puede presentarse en asociación con inmunodeficiencia selectiva de IgA, lo que puede comportar dificultades diagnósticas. El déficit selectivo de IgA no suele implicar una importante predisposición a infecciones, pero en caso de confirmarse hace recomendable la determinación de autoanticuerpos contra la propia IgA2. La positividad de estos puede comportar un riesgo incrementado de reacción anafiláctica tras la tranfusión de hemoderivados, fundamentalmente de plasma fresco2. El siguiente caso refleja las dificultades clínicas que pueden presentarse en el diagnóstico de EC en presencia de dicho déficit.
Caso clínico
Varón de 36 años remitido desde Atención Primaria para valoración en consultas externas de Medicina Interna, por un cuadro de astenia, febrícula y pérdida ponderal de 8 kg. en los últimos 2 meses. El diagnóstico diferencial planteado por su médico de cabecera consideraba la enfermedad neoplásica, malabsorción intestinal o proceso infeccioso subagudo. Había padecido una meningitis C en la infancia, una fibrilación auricular paroxística y un pólipo adenomatoso resecado años antes en el estudio de una alteración en el hábito deposicional autolimitada.
En el hemograma destacaba una linfocitosis con niveles absolutos de 4,4 x 103/mm3 [1,5-4x103] y VCM 79 [81-99]. La bioquímica objetivó niveles de ferritina de 18 ng/dl [12-300], hierro de 26 µg/dl [50-200], albúmina de 3,4 g/dl [3,5-5,2], proteínas totales de 5,4 g/dl [6,5-8,2] y β2-microglobulina de 3,7 mg/l [1,06-2,22]. Los análisis de hormonas y marcadores tumorales, incluídos TSH, cortisol basal, alfafetoproteina, CEA, CA 19.9, PSA, enolasa neuronal y Cyfra 21.1 fueron normales. En la inmunología, ANAs, Anti LKM, Anti Músculo liso, Anti MPO, ECA y factor reumatoide fueron negativos. También lo fueron el ELISA para VIH y el PPD. La TAC toracoabdominal objetivó una lentificación del tránsito con dilatación y edema de asas de intestino delgado y múltiples adenopatías mesentéricas (figura 1). Los anticuerpos IgA antigliadina y antitransglutaminasa, recomendados en las principales guías de práctica clínica para el diagnóstico de la enfermedad celíaca3, resultaron negativos. La fibrogastroscopia mostró una gastritis moderada con duodenitis crónica y atrofia inespecífica de vellosidades con aumento de linfocitos intraepiteliales. Dada la ausencia de un diagnóstico de certeza de EC, ante el cuadro clínico, la importante manifestación adenopática y la positividad en la β-microglobulina, conocido marcador tumoral de linfomas no Hodgkin4, se planteó la realización de una laparotomía exploradora con biopsias ganglionares para el despistaje de un síndrome linfoproliferativo. No obstante, considerando la elevada prevalencia de la EC y su posible asociación a una inmunodeficiencia selectiva de IgA1, se realizó una electroforesis de proteínas que objetivó una hipogammaglobulinemia con recuento absoluto de gammaglobulinas de 0,76 g/dl [2-3,5]. Los niveles totales de IgA fueron inferiores a 2 mg/dl [71-391], con IgM de 46,2 mg/dl [650-1700].
Discusión
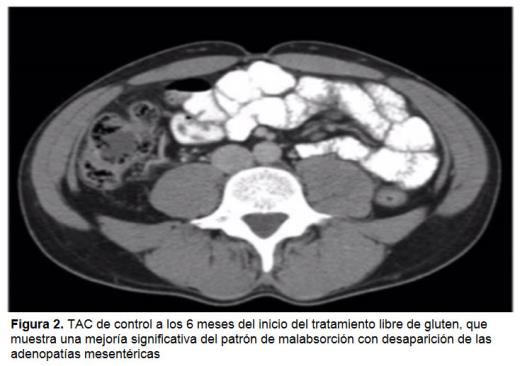
La atrofia vellositaria en la biopsia duodenal se considera un criterio Marsh 3a, compatible con EC del adulto5. No obstante, no es diagnóstica en ausencia de anticuerpos IgA antigliadina o antitransglutaminasa3. Por otra parte, la inmunodeficiencia selectiva de IgA se presenta en 1-2 de cada 100 casos de EC, dificultando así su diagnóstico1,6. En nuestro caso, se confirmó la EC con la determinación de los anticuerpos tipo IgG antigliadina y antitransglutaminasa, recomendados en casos de sospecha de EC asociada a inmunodeficiencia de IgA3, de 23,5U/ml [<10] y 234 U/ml [<7] respectivamente. También fue positiva la determinación del HLA-DQ2, gen asociado a la forma familiar de enfermedad celiaca1,3. Posteriormente se diagnosticó de EC su hijo. Tras 6 meses de dieta libre de gluten se normalizó el peso, la hipogammaglobulinemia, los niveles de IgG antigliadina y antitransglutaminasa y la IgM total, persistiendo el déficit selectivo de IgA. La TAC de control objetivó una mejoría significativa del patrón de malabsorción con desaparición de las adenopatías mesentéricas (figura 2). El presente caso muestra las dificultades que se puede encontrar el médico de familia para el diagnóstico de la EC del adulto cuando esta se presenta con inmunodeficiencia selectiva de IgA. Para evitar los resultados falsos negativos, que en este caso podrían habernos conducido a la realización de una laparotomía exploradora y al retraso en el diagnóstico de EC en el hijo del paciente, es necesario tener en consideración esta asociación, y solicitar que los laboratorios determinen los niveles de IgA total cuando exista elevada sospecha de EC y los autoanticuerpos específicos antitransglutaminasa de tipo Ig A resulten negativos1,7.
Bibliografía
1. Polanco Allué I. Enfermedad celíaca. Rev Lab Clin. 2014; 7 (4): 141-4. [ Links ]
2. Rojas-Torres DS, Bastidas-Yaguana DK, Sierra-Santos L, Aguilar-Shea AL. Importancia del déficit selectivo de inmunoglobulina A. Semergen. 2014; 40 (3): e65-e68. [ Links ]
3. Ludviqsson JS, Bai JC, Biaqi F, Ciacci C, Ciclitira PJ, Green PH, et al.; BSG Coeliac Disease Guidelines Development Group; British Society of Gastroenterology. Diagnosis and management of adult coeliac disease: guidelines from the British Society of Gastroenterology. Gut. 2014; 63 (8): 1210-28. [ Links ]
4. Johnson PW, Whelan J, Longhurst S, Stepniewska K, Matthews J, Amess J, et al. Beta-2 microglobulin: a prognostic factor in diffuse aggressive non-Hodgkin's lymphomas. Br J Cancer. 1993; 67 (4): 792-7. [ Links ]
5. Marsh MN. Gluten, major histocompatibility complex, and the small intestine. A molecular and immunobiological approach to the spectrum of gluten sensitivity ("celiac sprue"). Gastroenterology. 1992; 102 (1): 330-54. [ Links ]
6. Vita Garay LA, Bengoechea Gallastegui L, Abalo Durán C, Fernández Fernández J, Castiella Eguzkiza A. Enfermedad celíaca y déficit selectivo de inmunoglobulina A. Gastroenterol Hepatol. 2005; 28 (6): 361. [ Links ]
7. Bienvenu F, Anghel SI, Besson Duvanel C, Guillemaud J, Garnier L, Renosi F, et al. Early diagnosis of celiac disease in IgA deficient children: contribution of a point-of-care test. BMC Gastroenterol. 2014, 14: 186. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Rafael Ramírez Montesinos.
Rambla Vella, 14.
C.P. 43003. Tarragona (España).
Correo electrónico: rramirez@xarxatecla.cat.
Recibido el 23 de mayo de 2015.
Aceptado para su publicación el 27 de junio de 2015.