INTRODUCCIÓN
La leucemia mieloide crónica (LMC) es una enfermedad rara, con una incidencia de 1-2 casos por cada 100.000 habitantes por año y una mediana de edad al diagnóstico de 65 años1. Supone el 15-20% de los casos de leucemia en adultos2,3. Se trata de una neoplasia mieloproliferativa causada por una translocación entre los brazos largos de los cromosomas 9 y 22 [t(9;22)], que da lugar al cromosoma Philadelphia (Ph+), presente en el 90-95% de los casos1,4. La consecuencia molecular es el gen de fusión BCR-ABL, cuyo transcrito codifica una proteína tirosin kinasa (Bcr-Abl) con actividad constitutiva que afecta a la regulación de la proliferación celular y la apoptosis5.
El curso natural de la enfermedad se divide en 3 fases: crónica (FC), que supone el 90% de los casos al momento del diagnóstico, fase acelerada (FA) y fase blástica (FB)2,5. Aunque el trasplante alogénico de progenitores hematopoyéticos es la única opción curativa, su elevada morbimortalidad y la escasez de donantes, hacen que se consideren candidatos aproximadamente un 25% de los pacientes4,6. El tratamiento con interferón-alfa (IFNα) fue durante un tiempo el tratamiento de elección, ya que logró obtener respuestas citogenéticas completas en 5-20% de los pacientes2 y demostrar ventajas en la supervivencia comparado con busulfan o hidroxiurea7.
Fruto del mayor conocimiento de la patogenia de la enfermedad, fue desarrollado imatinib, el primer inhibidor de tirosin kinasas (ITK), cuya diana terapéutica es el Bcr-Abl1. Su aprobación cambió el paradigma del tratamiento tras superar al IFNα en tasa de respuestas y supervivencia libre de progresión (SLP), convirtiéndose en la terapia estándar en primera línea1,3,8,9,10. Según diferentes estudios, consigue un 49-77% de respuesta citogenética completa y un 18-58% de respuesta molecular mayor el primer año de tratamiento, además de un 83-94% de SLP y 83-97% de supervivencia global (SG) a los 5 años de tratamiento11.
Se han validado como marcadores subrogados de supervivencia la respuesta hematológica completa (RCH), la respuesta completa citogenética (RCyC) y la respuesta molecular mayor (RMM)5. La respuesta precoz a ITK es el factor pronóstico más importante de la enfermedad, ya que alcanzar respuestas óptimas consigue esperanzas de vida comparables con la población general. Esta respuesta óptima consiste en lograr obtener respuestas citogenéticas y moleculares de forma temprana y sostenida, para lo cual se ha definido el umbral de respuesta que debe alcanzarse en determinados tiempos tras el inicio de tratamiento con ITK11.
La falta de adherencia en los tratamientos crónicos es un problema. Diversos estudios han comunicado la falta de adherencia al tratamiento con imatinib, poniendo de manifiesto que este factor supone un nuevo reto en el manejo de esta patología, ya que está directamente relacionado con la efectividad12,13.
Por todo lo anteriormente expuesto se ha planteado un estudio observacional longitudinal retrospectivo, con el objetivo de evaluar la efectividad, seguridad y adherencia a imatinib en LMC en la práctica clínica habitual.
MÉTODOS
Diseño, pacientes y tratamiento
Estudio observacional, longitudinal, retrospectivo de utilización de imatinib en LMC en cualquier línea de tratamiento, en práctica clínica habitual llevado a cabo en el Área Sanitaria de Pontevedra-Salnés entre noviembre de 2001 y diciembre de 2015. Los criterios de inclusión del estudio fueron los siguientes: pacientes adultos (≥18 años) diagnosticados de LMC Ph+ en FC14, con un adecuado estatus funcional (ECOG <2) según la escala diseñada por el Eastern Cooperative Oncology Group. Los pacientes fueron estratificados en cuanto a riesgo según el índice de Sokal15.
Los datos se obtuvieron de la revisión de las historias clínicas en papel y en formato electrónico (IANUS®) y de las aplicaciones informáticas de gestión farmacéutica para pacientes externos: Dippex® y Silicon®.
La adherencia (ADH) se definió como el grado de concordancia entre la conducta del paciente y las recomendaciones realizadas por el profesional sanitario en relación con la toma de medicación12. Utilizando la información del registro de dispensaciones, se calculó la adherencia de cada paciente según la fórmula: (dosis totales dispensadas x 100)/dosis totales prescritas16. Se categorizó a los pacientes como "no adherentes" (si ADH <85%) o "adherentes" (si ADH ≥85%), ya que este punto de corte se ha relacionado con la probabilidad de pérdida de respuesta al tratamiento17. También se calculó la adherencia media al tratamiento, considerando las adherencias superiores al 100% como 100%.
Efectividad y seguridad
La variable principal de efectividad fue la tasa de respuesta al tratamiento en sus tres vertientes (hematológica, citogenética y molecular), definidas según criterios de The European LeukemiaNet (ELN) acorde al periodo de estudio y que se detallan a continuación11,14,18:
La respuesta completa hematológica (RCH) se definió como la normalización en sangre periférica de los recuentos celulares, en ausencia de formas inmaduras y sin presencia de bazo palpable. La pérdida de RCH se definió como la aparición de alguno de los siguientes: leucocitos >20 x109/L, plaquetas > 600 x109/L o la presencia de formas inmaduras en al menos dos determinaciones analíticas consecutivas.
La respuesta citogenética se graduó como: completa (RCyC) si había 0% de cromosomas Ph+ o parcial (RCyP) si había entre 1-35% Ph+, en al menos 20 metafases, medidos mediante análisis convencional del cariotipo. La pérdida de RCyC se definió como la aparición de cromosomas Ph+ en al menos dos determinaciones consecutivas.
La respuesta molecular se determinó mediante reacción en cadena de la polimerasa con transcriptasa inversa, cuantificando el nivel de transcritos BCR-ABL en sangre periférica medido en la escala internacional (IS). Se catalogó como: respuesta molecular mayor (RMM) si BCR-ABL ≤0.1% IS o respuesta molecular completa (RMC) si los BCR-ABL indetectables. Actualmente se correspondería con RM4.0 si ≤0.01%, RM4.5 si ≤0.0032% o RM5.0 si ≤0.001% en la escala internacional. La pérdida de RMM se definió como la detección de transcritos BCR-ABL >0.1% en sangre periférica en al menos dos test consecutivos.
Como variables secundarias se determinaron la SLP y SG, entendiéndose como progresión la muerte durante el tratamiento con imatinib o la transformación a FA ó FB según los criterios especificados por ELN14.
La seguridad fue evaluada mediante la aparición de efectos adversos (EA), siendo graduados los de tipo hematológico y bioquímico de acuerdo a la terminología Common Toxicity Criteria Adverse Events (CTCAE) v4.0. El porcentaje de pacientes que experimentó EA se calculó contando la primera aparición de un determinado EA en cada paciente.
Análisis estadístico
El análisis estadístico de los datos se realizó mediante el programa SPSS v19. Para la valoración de las variables continuas de distribución normal se utilizaron medias y desviación estándar (medianas y rangos para aquellas que no presentaban distribución normal), mientras que para las variables categóricas se utilizaron frecuencias y porcentajes. Las tasas de respuesta fueron estimadas como porcentajes de la mejor respuesta obtenida por los pacientes durante el seguimiento. Aquellos pacientes en los que no se realizaron análisis citogenéticos o moleculares fueron considerados como no respondedores. Las variables SLP y SG fueron analizadas según el método Kaplan-Meier.
RESULTADOS
Pacientes y tratamiento
Se incluyeron en el estudio un total de 39 pacientes, cuyas características basales se describen en la tabla 1. La mediana de tiempo desde el diagnóstico hasta el inicio de tratamiento con imatinib fue de 0,7 (0-56,9) meses. El 25,6% de los pacientes habían recibido tratamiento con IFNα en primera línea. La dosis media administrada de imatinib fue de 436,6 (358-707) mg/día y la mediana de duración del tratamiento fue de 50,6 (1,3-171,4) meses. En el momento del análisis continuaban recibiendo tratamiento 17 (43,6%) pacientes, mientras que en 18 (46,1%) pacientes se había suspendido el tratamiento por los siguientes motivos: 11 (28,2%) falta ó pérdida de efectividad, 5 (12,8%) efectos adversos y 2 (5,1%) por otras causas. Además, 3 (7,7%) pacientes fallecieron durante el tratamiento y se produjo 1 (2,6%) pérdida de seguimiento. Se detectaron mutaciones en 4 de los pacientes a los que se suspendió el tratamiento por falta o pérdida de efectividad: His361Ser, Met244Val, Met318Val y Met370Thr. La progresión a FA ocurrió en 2 (5,1%) pacientes y no hubo ninguna progresión a FB.
Tabla 1. Características basales de los pacientes.
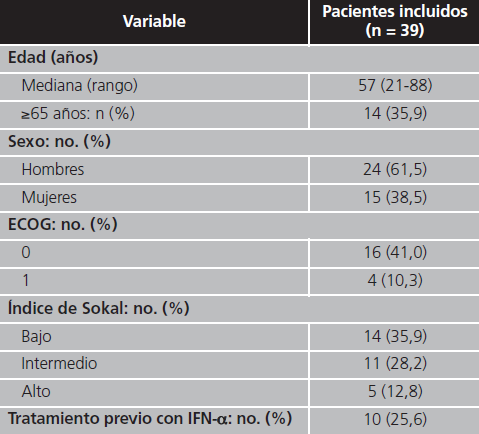
ECOG: Eastern Cooperative Oncology Group; IFN-α: interferón alfa.
La adherencia media al tratamiento fue de 94,9% (59,0-100,0%). Se identificaron como adherentes un 92,3% de pacientes.
Efectividad
La tabla 2 muestra la tasa acumulada de respuesta al tratamiento. Las tasas de respuesta alcanzadas con imatinib fueron: 100% RCH, 84,6% RCyC y 66,7% RMM. De estos pacientes, 1 (2,6%) perdió la RCH, 7 (21,1%) perdieron la RCyC y 14 (53,8%) perdieron la RMM.
Tabla 2. Tasa acumulada de mejor respuesta al tratamiento con imatinib.
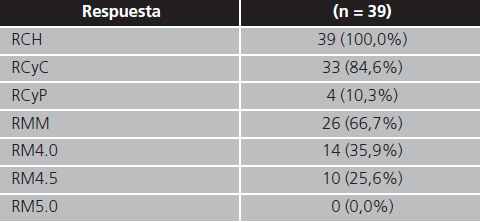
RCH: respuesta completa hematológica; RCyC: respuesta completa citogenética; RCyP: respuesta citogenética parcial; RMM: respuesta molecular mayor; RM4.0: respuesta molecular 4.0; RM4.5: respuesta molecular 4.5; RM5.0: respuesta molecular 5.0.
La mediana de tiempo necesario para alcanzar las respuestas fue: 0,7 (0,1-6,9) meses para RCH, 8,1 (2,8-34,2) meses para RCyC y 15,8 (3,2-124,8) meses para RMM. La mediana de duración de RCyC y RMM fue de 31,3 (0,3-153,1) y 40,6 (4,5-153,1) meses respectivamente. La figura 1 muestra las curvas de SLP y SG de los pacientes tratados con imatinib. Las tasas de SLP y SG a los 8 años fueron de 94,4% (IC95%: 86,9-100,0) y 94,4% (IC95%: 87,3-100,0) respectivamente.
Un total de 11 (28,2%) pacientes precisaron escalada de dosis por falta/pérdida de efectividad citogenética (27,3%), molecular (45,5%) o ambas (27,3%).
Seguridad
Todos los pacientes experimentaron algún tipo de EA (Tabla 3), que generalmente fueron reversibles cuando se manejaron con tratamiento de soporte adecuado. Los EA fueron más frecuentes los primeros años de tratamiento, produciéndose un 74,2% durante los dos primeros años de tratamiento. Se produjo un pequeño porcentaje de EA hematológicos grado 3-4: 4 pacientes (10,3% del total) experimentaron neutropenia grado 3-4 y 2 (5,1%) trombopenia grado 3. Los EA de tipo no hematológico más frecuentes fueron: edemas (53,8%), dolor músculo-esquelético (43,6%) y calambres (38,5%).
Tabla 3. Efectos adversos relacionados con el tratamiento con imatinib.
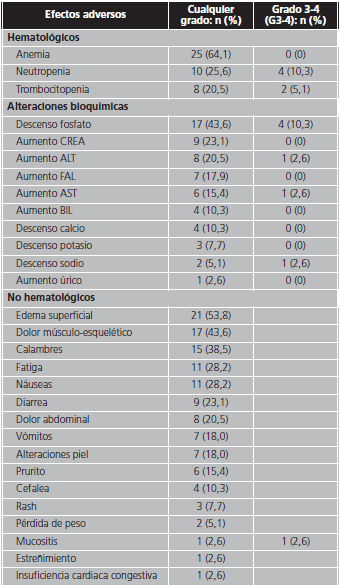
ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; CREA: creatinina; BIL: bilirrubina; FAL: fosfatasa alcalina.
Motivado por los EA se realizaron 8 interrupciones temporales del tratamiento (37,5% por toxicidad hematológica y 62,5% no hematológica) en 6 pacientes y se llevaron a cabo reducciones de dosis (50% de causa hematológica, 50% no hematológica) en 4 pacientes.
Hubo 3 fallecimientos (7,7%) durante el tratamiento con imatinib no relacionados con el fármaco: uno por infección respiratoria, otro por fibrosis pulmonar y otro por adenocarcinoma de próstata metastásico.
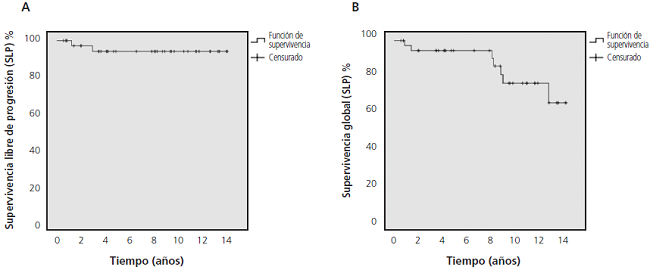
Figura 1. Supervivencia libre de progresión (SLP) y supervivencia global (SG) estimadas por Kaplan Meier.
La tasa estimada de SLP a 8 años fue de 94,4% (IC95%: 86,9-100,0), considerándose como progresión la muerte por cualquier causa, la transformación a fase acelerada o blástica. La tasa estimada de SG a 8 años fue de 94,4% (IC95%: 87,3-100,0), que disminuyó a 65,4% (IC95%: 44,9-95,3) a los 14 años.
DISCUSIÓN
Diferentes estudios llevados a cabo con imatinib en LMC han demostrado su capacidad para alterar el curso natural de la enfermedad logrando altas tasas de respuesta con un aceptable perfil de seguridad4,8,9,10. En el presente estudio se ha evaluado el comportamiento de imatinib en condiciones reales de utilización. Nuestros pacientes fueron ligeramente mayores respecto al estudio IRIS de imatinib, con una mediana de edad 57 vs 50 años y un 35,9% de pacientes ≥65 años vs 20,6% de pacientes ≥60 años4. La mayoría de los pacientes fueron tratados con la dosis estándar de 400 mg (dosis media del estudio 436,6 mg/día) durante una mediana de 50,6 (1,3-171,4) meses.
En cuanto a las variables de efectividad, las tasas de respuestas observadas en nuestro estudio coinciden con los datos reportados en el seguimiento a 5 años del estudio IRIS (SG 94,4% vs 89,0%, SLP 94,4% vs 93,0%, RCH 100,0% vs 98,0%, RCyC 84,6% vs 87,0% y RMM 66,7% vs 65,0%)8. La respuesta molecular de nuestros pacientes fue profunda (35,9% RM4.0 y 25,6% RM4.5) y ligeramente inferior a la encontrada en los datos actualizados de los estudios DASISION a 4 años (42,0% RM4.0 y 30,0% RM4.5) y ENESTnd a 5 años (31,0% RM4.5)19,20. El porcentaje hallado de pacientes que continúan tratamiento con imatinib a los 4 años en nuestro estudio (43,6%), se diferencia del de otros trabajos que apuntan que esta cifra es del 69% a los 5 años8.
Entre las posibles causas de pérdida de efectividad se encuentran, por una parte la aparición de resistencias y por otro lado la falta de adherencia.
El desarrollo de mutaciones de resistencia a ITK en el dominio kinasa de BCR-ABL es, en general minoritario, pero puede suponer el 50% de los casos cuando nos referimos a pacientes con fracaso terapéutico y progresión de la enfermedad3,11. El análisis mutacional de nuestra muestra reveló que el 10,3% de los pacientes presentaban mutaciones, de las que solo una (Met244Val) se había reportado anteriormente como positiva para sensibilidad intermedia a imatinib21. Se desconoce la implicación clínica del resto de mutaciones identificadas.
La falta de adherencia al tratamiento es otra de las posibles causas de falta de respuesta22. Comparar estudios de adherencia resulta complicado debido a los diferentes métodos de medida empleados para estimarla23,24. Para nuestra población se estimó mediante el registro de dispensaciones una ADH media de 94,9%, mejor que el 90,9% obtenido por el estudio ADAGIO a través de la escala Basel Assessment of Adherence Scale (BAAS)12. Sin embargo, fue ligeramente inferior a la experiencia de Marin (98,0%) o Ibrahim (97,6%), donde la medida se efectuó a través de dispositivos microelectrónicos que registraban la apertura de los frascos de medicación, sistema que puede reflejar mejor el verdadero comportamiento de los pacientes13,17.
A pesar del elevado porcentaje de EA registrado, el tratamiento fue aceptablemente tolerado en la mayoría de los casos, ya que solo ocasionó la suspensión del tratamiento en un 12,8% de los pacientes. Aunque este porcentaje resultó muy superior al 3% notificado por el estudio pivotal, probablemente se pueda atribuir a la falta de alternativas terapéuticas que había en aquella época para el tratamiento de la LMC25. La mayoría de los EA fueron manejables con tratamiento de soporte adecuado, interrupciones ó reducciones temporales de dosis. El perfil de toxicidad del fármaco se corresponde con experiencias previamente publicadas. En cuanto a los EA de tipo no hematológico más frecuentes, comparado con los pacientes del estudio IRIS, edema y calambres tuvieron una incidencia similar, pero las náuseas fueron menos frecuentes, posiblemente por no quedar documentados en la historias clínicas. Por contra, identificamos un mayor impacto de dolor músculo-esquelético, probablemente debido a que se cuantificó conjuntamente con artralgias y mialgias, mientras que en el mencionado estudio se reportaron desglosados. Coincidiendo con otros estudios, los EA de grado 3-4 de tipo hematológico fueron los más frecuentes, siendo la neutropenia el más común de este tipo. En nuestro estudio se produjo 1 caso (2,6%) de insuficiencia cardiaca congestiva, un EA raro pero potencialmente grave6 que provocó la hospitalización del paciente y la suspensión definitiva del tratamiento.
Este estudio está sujeto a las limitaciones inherentes a las revisiones retrospectivas, ya que las bases de datos pueden carecer de los datos precisos. Se utilizó únicamente la información de los registros de dispensación, el cual puede sobreestimar la adherencia, ya que recoger la medicación en la farmacia no implica necesariamente tomarla. Sin embargo, identifica de manera inequívoca a aquellos pacientes no adherentes, ya que si no acuden a recoger la medicación es imposible que puedan tomarla. No se pudieron demostrar diferencias estadísticamente significativas en la respuesta al tratamiento entre pacientes adherentes y no adherentes, debido al reducido tamaño de la muestra y a la falta de proporcionalidad entre el número de pacientes adherentes (33) y no adherentes (3). Existe amplio debate en cuanto a la posibilidad de interrumpir el tratamiento con imatinib en un futuro, tal y como se han planteado algunos autores, en pacientes altamente seleccionados con respuesta molecular profunda11,26. Sin embargo, parece existir cierto consenso en cuanto a la necesidad de alcanzar RM4.5 durante al menos 2 años consecutivos y a que no se recomienda al margen de ensayos clínicos27. En nuestra cohorte, uno de los pacientes, que acababa de alcanzar RM4.5, tuvo que abandonar el tratamiento con imatinib en junio de 2012 por anemia persistente. Permaneció sin tratamiento desde entonces y continúa en RM4.5.
En conclusión, imatinib ha demostrado una notable efectividad, con una elevada tasa de respuestas, que además fueron duraderas. Se constata así el beneficio del tratamiento en práctica clínica habitual, ya que los resultados obtenidos en nuestro estudio sugieren perfiles de efectividad, seguridad y adherencia similares a aquellos encontrados en la literatura científica.














