INTRODUCCIÓN
Un biosensor es un dispositivo analítico que transforma procesos biológicos en señales eléctricas u ópticas cuantificables. El biosensor está en contacto directo con la muestra a través del biorreceptor, uniéndose a él específicamente a través de un sitio selectivo. Esta unión específica es capaz de generar una señal, que es captada y transformada por el transductor en una señal inteligible y cuantificable por el detector. En base al fundamento del transductor, los biosensores se pueden clasificar en electroquímicos, ópticos, térmicos y de masa. En función de la naturaleza del proceso biológico, los biosensores pueden ser catalíticos, cuyos receptores son enzimas, tejidos o microorganismos, o de afinidad, basados en inmunosensores y quimiorreceptores1. En la actualidad existe una gran demanda de dispositivos de sensado de agentes biológicos que permiten una detección “on site”, simples de usar, con bajo coste y gran estabilidad2. Todos los esfuerzos en este campo van encaminados a desarrollar técnicas de biodetección que puedan combinar una excelente sensibilidad y especificidad con corto tiempo de análisis, y que, a su vez, sea posible miniaturizar3.
Un gran número de los biosensores desarrollados utilizan la unión antígeno-anticuerpo como herramienta diagnóstica, dada su gran especificidad. Estos inmunosensores son utilizados en campos muy diversos, como control ambiental, diagnóstico clínico, industria alimentaria, seguridad y defensa4. En particular, equipos de identificación de agentes de guerra biológicos, como toxinas proteicas (ricina, toxina botulínica, etc.) se basan en técnicas inmunológicas5,6,7.
El sistema de detección acoplado en cada biosensor determina el umbral de detección. Sin embargo, el éxito de la capacidad diagnóstica de los inmunobiosensores depende en gran medida de la inmovilización de los anticuerpos8,9.
En nuestro trabajo, queremos estudiar y comparar diversos procesos de inmovilización de anticuerpos en superficies planares para su aplicación en biosensores “on site” de detección de agentes de guerra biológicos. Así, esta inmovilización, por una parte, ha de ser estable y duradera y, por otra parte, ha de afectar lo menos posible a la región de unión del anticuerpo al antígeno; incluso, una buena orientación de dicha región, una vez el anticuerpo se fije a la superficie, podría facilitar la interacción del agente biológico con la región de reconocimiento del anticuerpo10.
En correspondencia con la bibliografía existente8,9 y atendiendo a la extensión de su uso, se han elegido los siguientes métodos de inmovilización de anticuerpos: adsorción pasiva, inmovilización covalente a través de un crosslinker, inmovilización orientada por afinidad utilizando proteínas mediadoras.
MATERIAL Y MÉTODOS
Materiales
La superficie planar elegida fue una membrana de nylon Zprobe (Biorad).
Se eligió como simulante de toxinas proteicas albúmina de suero bovino (BSA) (Sigma-Aldrich). La BSA fue preparada a una concentración de 1 mg/mL en tampón fisiológico fosfato salino pH 7,4 (PBS) marcada con ficoeritrina (RPE) con el kit de conjugación (AbDSerotec). Posteriormente, fue ensayada a una concentración de 5 µg/mL.
El anticuerpo de elección fue un anticuerpo policlonal de oveja anti-BSA marcado con fluoresceína (FITC) (ThermoFisher) para el seguimiento de la inmovilización del anticuerpo y su cuantificación, diluido en tampón fisiológico fosfato salino pH 7,4 (PBS) a una concentración de 50 µg/mL.
Se utilizaron como reactivos de inmovilización glutaraldehído (Scharlau), preparado al 0,5% en agua destilada, y la proteína quimérica A/G (ThermoPierce), preparada a 50 y 100 µg/mL en PBS1x.
El tampón de bloqueo utilizado fue PBS-caseína a pH 7,4.
Métodos de biofuncionalización estudiados
La membrana fue recortada en trozos de 4x4 mm y éstos se depositaron en el interior de una placa negra multipocillo (Nunc), previamente bloqueada con PBS-caseína. Se utilizaron tres trozos de membrana previamente dimensionados como se indica arriba para cada uno de los métodos de inmovilización ensayados. Cada ensayo se realizó por duplicado.
Adsorción pasiva
Sobre la membrana se depositaron 500 ng de anticuerpo en tampón fosfato salino (PBS) en un volumen de 10 µL, y se incubó a 4 °C toda la noche (o/n). Después de ser lavada la membrana en los pocillos con PBS1x (200 µL/pocillo, 5 minutos, tres lavados) y bloqueada con PBS-caseína, se incubó con el antígeno a detectar (50 ng de BSA-RPE en 10 µL PBS caseína) 1 hora a temperatura ambiente.
Unión covalente
La membrana fue tratada con glutaraldehído al 0,5% (200 µL/pocillo) en PBS durante 15 minutos y lavada posteriormente en PBS (200 µL/pocillo 5 minutos, tres lavados). Después 500 ng de anticuerpo, en 10 µL PBS, se depositaron sobre la membrana, que se incubó a 4 °C toda la noche (o/n). La membrana, después de ser lavada con PBS y bloqueada con PBS-caseína, se incubó con el antígeno a detectar, 50 ng de BSA-RPE, en 10 µL de PBS caseína durante 1 hora a temperatura ambiente.
Unión orientada a través de proteína mediadora
Se ensayaron dos cantidades de proteína quimérica A/G, 500 ng y 1 µg, en 10 µL de PBS, que se depositaron sobre la membrana y se incubaron a 4 °C toda la noche (o/n). La membrana, después de ser lavada y bloqueada con PBS-caseína, se incubó con el anticuerpo durante 1 hora a temperatura ambiente y, tras un nuevo lavado para eliminar el excedente, se incubó con 50 ng de BSA-RPE, 1 hora a temperatura ambiente.
Obtención de datos para cada método de inmovilización
Se realizaron tres medidas de fluorescencia:
Medida inicial del anticuerpo inmovilizado
Después de la incubación del anticuerpo con la membrana y tras su correspondiente proceso de lavado, se midió la fluorescencia de FITC (ʎ excitación=490 nm; ʎ emisión= 521 nm; ʎcutoff=515 nm) mediante un lector de fluorescencia multipocillo (SpectraMaxGemini XPS, Molecular Devices).
Medida final del anticuerpo inmovilizado (después de la inmunocaptura)
Al finalizar el proceso de unión del anticuerpo con BSA-RPE y su posterior proceso de lavado, se midió la fluorescencia de FITC (ʎ excitación=490 nm; ʎ emisión= 521 nm; ʎcutoff=515 nm) mediante un lector de fluorescencia multipocillo (SpectraMaxGemini XPS, Molecular Devices).
Medida de la BSA-RPE unida al anticuerpo inmovilizado (medida de inmunocaptura)
Tras la incubación con BSA-RPE y posterior proceso de lavado, se midió la fluorescencia de RPE (ʎ excitación=495 nm; ʎ emisión= 576 nm; ʎcutoff=570 nm) mediante un lector de fluorescencia multipocillo (SpectraMaxGemini XPS, Molecular Devices).
Análisis de resultados
Valoración de la inmovilización del anticuerpo
Lectura de la fluorescencia de FITC inicial y final del anticuerpo inmovilizado.
Cálculo de porcentaje de retención del anticuerpo: Comparación del valor final de fluorescencia de FITC asociada al anticuerpo anti-BSA respecto al valor inicial tras la incubación del anticuerpo y primer lavado.
Densidad del anticuerpo unido a la membrana. Se determinó el anticuerpo inmovilizado en términos de porcentaje, tomando como control el método clásico de adsorción pasiva.
Análisis estadístico de los resultados: One Way ANOVA y posterior test de Comparación Múltiple Tukey.
Valoración del sistema de inmunocaptura de BSA
Lectura de la fluorescencia de RPE.
Cálculo de la eficiencia del sistema de inmunocaptura: comparación del valor de fluorescencia de BSA obtenido respecto al valor de fluorescencia del anticuerpo inmovilizado.
Análisis estadístico de los resultados
El tamaño muestral fue de 12-6 (12 en el caso de la valoración del anticuerpo inmovilizado, 6 en la determinación de la eficacia del sistema de inmunocaptura).
La normalidad fue previamente estudiada aplicando el test de normalidad D’Agostino-Pearson o el test de Kolmogorov-Smirnov (con el valor P Dallal Wikinson-Liliefor) (GraphPad Prism).
Después se realizó un test One Way ANOVA y posterior test de Comparación Múltiple Tukey.
RESULTADOS
Valoración de la inmovilización del anticuerpo
Porcentaje de retención del anticuerpo
El test de normalidad ensayado indica que la población presenta una distribución normal.
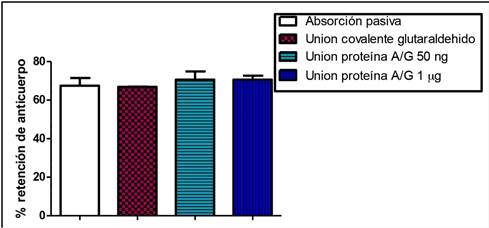
El test One-Way ANOVA y el post-test Tukey realizado no muestra ninguna diferencia significativa entre los grupos, indicando que el porcentaje de retención del anticuerpo es similar en todos los métodos de biofuncionalización ensayados (Figura 1, Tabla 1).
Tabla 1 Porcentaje de retención del anticuerpo inmovilizado. Valores medios, erros estándar de la media (SEM), tamaño muestral (N).
| TRATAMIENTO | MEDIA | SEM | N |
|---|---|---|---|
| Absorción pasiva | 67,46899 | 4,015005 | 13 |
| Unión covalente glutaraldehido | 66,8725 | 0,1666765 | 8 |
| Unión proteína A/G 500 ng | 70,63025 | 4,272686 | 12 |
| Unión proteína A/G 1 ng | 70,62134 | 2,086897 | 12 |
Densidad del anticuerpo unido a la membrana
El test de normalidad ensayado indica que la población presenta una distribución normal.
El test One-Way ANOVA y el post-test Tukey realizado pone en evidencia que cuando se utiliza glutaraldehído se retiene más densidad de anticuerpo que mediante adsorción pasiva, mientras que cuando se utiliza proteína A/G se retiene una menor densidad de anticuerpo (Figura 2, Tabla 2).

Figura 2 Densidad del anticuerpo inmovilizad. Porcentaje respecto a adsorción pasiva. *** p < 0,001; * p < 0,05. Diferencias frente a Adsorción pasiva. One-way ANOVA, test de Comparación Múltiple Tukey).
Tabla 2 Densidad del anticuerpo inmovilizado, porcentaje respecto a adsorción pasiva. Valores medios, error estándar de la media (SEM), tamaño muestral (N).
| TRATAMIENTO | MEDIA | SEM | N |
|---|---|---|---|
| Absorción pasiva | 99,99923 | 5,717187 | 13 |
| Unión covalente glutaraldehido | 130,0225 | 5,874725 | 8 |
| Unión proteína A/G 500 ng | 47,024 | 6,538109 | 5 |
| Unión proteína A/G 1 ng | 63,075 | 6,115917 | 6 |
Eficiencia del sistema de inmunocaptura del antígeno
El test de normalidad ensayado indica que la población presenta una distribución normal.
El test One-Way ANOVA y el post-test Tukey realizados muestran que existen diferencias significativas en la eficacia del sistema de inmunocaptura resultante en función del método de inmovilización del anticuerpo (Figura 3, Tabla 3). Así, la eficiencia del sistema de inmunocaptura mediante unión covalente con glutaraldehído, es estadísticamente inferior a la de la adsorción pasiva, a pesar de mostrar un incremento en la densidad del anticuerpo fijado. La inmovilización del anticuerpo a través de proteínas mediadoras A/G incrementa la eficiencia de unión de la BSA en el sistema, siendo estadísticamente superior a todos los demás modelos de biofuncionalización ensayados, a pesar de mostrar una menor densidad de anticuerpo inmovilizado.
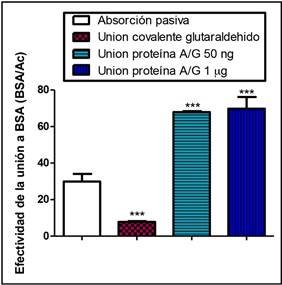
Figura 3 Efectividad de la unión a la BSA en los distintos modelos de biofuncionalización.* p< 0,05, ** p <0,01, *** p<0,001. Diferencias respecto al grupo “Absorción pasiva”. (One Way ANOVA seguido del test de Comparación Múltiple Tukey).
Tabla 3 Efectividad de la unión a la BSA en los distintos modelos de biofuncionalización. Valores medios, erros estándar de la media (SEM), tamaño muestral (N).
| TRATAMIENTO | MEDIA | SEM | N |
|---|---|---|---|
| Absorción pasiva | 29,9026 | 4,166912 | 5 |
| Unión covalente glutaraldehido | 7,86 | 0,362243 | 6 |
| Unión proteína A/G 500 ng | 67,889 | 0,536948 | 6 |
| Unión proteína A/G 1 mg | 69,79267 | 6,394182 | 6 |
DISCUSIÓN
La inmovilización de los anticuerpos determina en gran medida la capacidad diagnóstica de los inmuno-biosensores por lo que es de crucial importancia el desarrollo de procesos de inmovilización que permitan una unión antígeno-anticuerpo lo más eficiente posible. Además, esta unión ha de ser también estable y duradera dado que su aplicación final es el desarrollo de biosensores para la detección de agentes de guerra biológica “on site”, por lo que tendrían que soportar duras condiciones ambientales y largos periodos de almacenamiento.
Este trabajo, en consonancia con trabajos previos como aquellos publicados por Sharma y col, (2016) 8 y Shen y col. (2017) 9, señala la importancia de una buena inmovilización del anticuerpo. Hemos comparado las tres formas de inmovilización más frecuentes en superficies planares de amplio uso: la inmovilización por adsorción pasiva, la inmovilización covalente y la inmovilización orientada mediante proteínas mediadoras.
La inmovilización del anticuerpo por adsorción pasiva es la comúnmente utilizada en los inmunoensayos de uso más extendido como los ELISAs. Por este motivo, se ensayó la biofuncionalización por adsorción pasiva y se comparó con un tipo de inmovilización que fuera más estable y duradera (inmovilización covalente) y con otro tipo de inmovilización que asegurara la orientación del anticuerpo y que fuera de elevada afinidad, aunque no fuese completamente irreversible (biofuncionalización mediante proteínas mediadoras).
La unión más fuerte que existe en la naturaleza es el enlace covalente, proporcionando uniones estables y duraderas. La inmovilización covalente del anticuerpo utilizando soportes activados con grupos aldehído, para inmovilizar las proteínas mediante una reacción con los grupos amino primario de su superficie11, está descrita en la literatura. El trabajo de Karey y Sirbasku12 muestra que el glutaraldehído sobre superficies de nylon, como las membranas Zprobe, incrementa la inmovilización de distintas proteínas en este tipo de membranas. Trabajos más recientes, como aquellos llevados a cabo por Peng y colaboradores (2016) 13 demostraron que el glutaraldehído resultaba ser un método de fijación covalente de anticuerpos en discos de celulosa.
Por esto se decidió estudiar el método de inmovilización covalente con glutaraldehído en nuestro modelo de inmunocaptura. Nuestros resultados muestran que el glutaraldehído, sí que incrementa la densidad del anticuerpo unido, pero no así el porcentaje de retención del mismo durante el proceso. Además, disminuye la eficacia de la unión antígeno-anticuerpo. Esto podría explicarse porque la reacción suele requerir pHs ligeramente ácidos y superficies hidrofóbicas. A pH superior a 6, como es nuestro caso, el glutaraldehído es altamente reactivo14 pudiendo provocar cambios que afecten al reconocimiento antigénico del anticuerpo. Por lo tanto, la inmovilización covalente con glutaraldehído no ofrece ninguna ventaja sobre la inmovilización clásica del anticuerpo por adsorción pasiva sino, al contrario, supone una pérdida de eficacia en cuanto a la inmunocaptura del antígeno.
Otro método de inmovilización ensayado es el que emplea proteínas mediadoras como puente de unión entre el soporte y el anticuerpo. Esta es una unión muy fuerte, con una alta constante de disociación, aunque no es una unión covalente, con lo que podría revertirse con la desnaturalización de la proteína. El uso de estas proteínas mediadoras permite una unión orientada del anticuerpo al unirse específicamente a la región constante (Fc) del mismo, de forma que la región variable de unión al antígeno (Fab) queda accesible para la unión antígeno-anticuerpo. El uso de estas proteínas para la inmovilización de anticuerpos es muy extendido, no sólo en columnas de afinidad sino también en sensores. Trabajos recientes como los llevados a cabo por Shen y colaboradores (2017) 9 ponen de manifiesto que la inmovilización orientada a través de estas proteínas mediadoras es una técnica preferente en la fijación de anticuerpos a distintos soportes. Así, Anderson y colaboradores15 utilizaron la inmovilización de los anticuerpos a través de proteína A en un biosensor de fibra óptica.
Dentro de estas proteínas mediadoras, destacan la proteína A, que pertenece a la pared celular de Staphylococcus aureus, y la proteína G, que es una proteína de superficie de los grupos C y G del género Streptococcus.
Sin embrago, la reactividad que presentan ambas proteínas mediadoras por las distintas inmunoglobulinas es diferente. Por eso, en este trabajo se eligió una proteína quimérica A/G frente a la proteína A o a la proteína G, consiguiendo así un amplio espectro de unión y siendo menos dependiente de variaciones de pH. Además, en esta proteína quimérica se ha eliminado el sitio de unión de la proteína G a la albúmina sérica, con lo que se evitan uniones inespecíficas con la BSA, que es el antígeno utilizado en este modelo de inmunocaptura. Esta proteína quimérica ha sido usada en el desarrollo de biosensores como el SpectroSens para la monitorización de diversas biomoléculas16.
Nuestros resultados muestran que, aunque la densidad del anticuerpo unido es menor que el observado en cualquiera de los otros dos métodos comparados (adsorción pasiva y unión covalente con glutaraldehído), el sistema es mucho más eficiente en cuanto a la inmunocaptura del antígeno. Resultados similares fueron obtenidos por Anderson y colaboradores 15 que obtuvieron una inmunocaptura más eficiente con el anticuerpo inmovilizado con proteína A que cuando el anticuerpo estaba inmovilizado covalentemente.
Puesto que en esta inmovilización la densidad del anticuerpo inmovilizado es menor, y el porcentaje de retención del anticuerpo no varía, el aumento en la eficacia de la inmunodetección será debido, posiblemente a la inmovilización orientada del mismo.
Por lo tanto, el empleo de las proteínas A/G mejoran la efectividad del sistema de inmunocaptura, siendo necesaria una menor cantidad de anticuerpo para obtener resultados mucho mejores, lo que abarataría la producción del dispositivo de inmunodetección “on site”. El coste de la producción de anticuerpos específicos y sensibles frente a agentes de guerra biológicos son elevados, dada la infraestructura y permisos que requieren, siendo además necesario en la mayoría de los casos la obtención in house de los mismos por su ausencia en el mercado.
Todo esto hace que la proteína recombinante A/G sea un método de elección en la inmovilización de anticuerpos en superficies de uso extendido como el nylon, para su aplicación en el desarrollo de biosensores de campo, de gran utilidad para las Fuerzas y Cuerpos de Seguridad del Estado ante una posible amenaza bioterrorista.