INTRODUCCIÓN
La dihidropirimidina deshidrogenasa (DPD) es la principal enzima responsable del metabolismo del 5-fluorouracilo (5-FU)1, un análogo de pirimidina frecuentemente empleado en el tratamiento de diferentes tumores sólidos. La deficiencia completa o parcial de DPD aumenta el riesgo de sufrir reacciones adversas tras la exposición a 5-FU y otros tratamientos que resulten biotransformados en este, como capecitabina, tegafur y flucitosina2.
La caracterización del genotipo es la técnica más ampliamente empleada en nuestro entorno para identificar la deficiencia de DPD, si bien es cierto que el método de referencia es la determinación de la actividad de esta enzima en células mononucleares de sangre periférica. Además de estas estrategias, se han propuesto otras opciones analíticas dirigidas a prevenir la toxicidad asociada al tratamiento con fluoropirimidinas (FP)3. Entre las más aceptadas se encuentra la prueba fenotípica que consiste en la determinación de las concentraciones séricas o plasmáticas de uracilo (U), substrato endógeno de la DPD. En mayo de 2020, la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) emitió una alerta en la que estableció el rango de concentraciones plasmáticas de U endógeno [16-150 ng/ml] compatible con un déficit parcial de esta enzima4.
La idoneidad de la determinación de las concentraciones de U para prevenir el riesgo de toxicidad severa ha sido puesta en duda recientemente alegando la influencia de diferentes factores, fundamentalmente asociados a la etapa preanalítica5.
El Instituto de Toxicología de la Defensa (ITOXDEF) es el órgano técnico superior en el ámbito toxicológico de las Fuerzas Armadas. Entre sus misiones principales se encuentra la investigación, que se sustenta en su personal especializado, un avanzado equipamiento tecnológico y la competencia técnica para realizar las determinaciones de alrededor de 200 parámetros acreditados por la Entidad Nacional de Acreditación (ENAC). Estas capacidades permiten al ITOXDEF involucrarse en diferentes proyectos de investigación relacionados con la toxicología.
El objetivo de nuestro estudio fue determinar la concentración sérica de U endógeno en una población candidata a recibir tratamiento con FP y comprobar si su distribución es compatible con la prevalencia del déficit parcial de DPD estimada en población caucásica (3-8%). En caso de no resultar compatible se pretende realizar una revisión de la evidencia relativa a los posibles factores que pueden influir en la determinación de este analito.
MÉTODOS
Estudio observacional prospectivo en el que se incluyeron pacientes oncológicos candidatos a tratamiento con FP. El estudio se llevó a cabo en un único centro hospitalario de tercer nivel entre los meses de octubre de 2021 y mayo de 2022. Las variables recogidas fueron sexo, edad, tipo de cáncer y concentraciones séricas de U en dicha población.
Para esta determinación, previamente al inicio del tratamiento con FP, se tomó sangre en tubos de extracción con gel separador. Tras la centrifugación las muestras fueron congeladas a una temperatura de -80 ºC.
Para la determinación de U se empleó un sistema Dionex Ultimate 3000 UHPLC acoplado a un espectrómetro de masas cuadrupolo-orbitrap híbrido Q-exactive, mediante una fuente de ionización electrospray (ESI) (ThermoFisher Scientific, Waltham, MA). El método analítico desarrollado en el ITOXDEF se recoge en la tabla 2.
Tabla 2. Resultados y condiciones de ensayo en estudios publicados que emplearon como método analítico LC-MS/MS.
| ETAPA PREANALÍTICA | ETAPA ANALÍTICA | C. uracilo [ng/ml] | Ref. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Matriz | Población | Anticoagulante | Ayuno | Hora de extracción | T. máx. hasta centrifugación | Centrifugación | Congelación | Preparación muestras | Equipo | Columna | Ion [m/z] | Patrón interno | ||
| P | 123 vol. sanos asiáticos | Heparina | SI | 8am-9am | N.E. | N.E. | Tª-30 ºC t: N.E. | PP: Sulfato de amonio EX: Isopropanol-acetato de etilo (15/85 v/v) EV: 45 ºC 15´, N2 R: metanol 10% | API 3000 TQ | Amide C16 (150 x 4.6 mm) | [M+H]+: 110,8 42,1 | 5-BU 5-FU | Media: 20,1±9,2 Mediana: 18,7 Rango: 7,6-60,5 | Jiang et al. 20026 |
| P | 10 pac. en tto. con 5-FU | Heparina de litio | N.E. | N.E. | 5 min. mantenida en hielo t: N.E. | Tª N.E. t: 10 min. F: 3.000 g | Tª-20 ºC t: N.E. | PP: Sulfato de amonio EX1: Acetato de etilo-2-propanol (10:1 v/v) EV: N2 (40 ºC) EX2: fase orgánica R: Ac. Fórmico 0,1% +sonicación Centrifugación | 4000 QTRAP | Atlantis dC18 (2,1 x 150 mm, 3 μm) conectado a Atlantis dC18 (2.1x10 mm, 3μm) | [M+H]+: 113 70.00 | U-2-13C UH2-13C415N2 5-FU-15N2 | Rango: 7,8-29,1* *antes de la infusión | Büchel et al. 20127 |
| P | 26 pac. | EDTA | SI | 8am-10am | <30min. | Tª 4 ºC t: 10 min F: 3.200 g | Tª -20 ºC t: N.E. | PP: Sulfato de amonio EX: Isopropanol-acetato de etilo (15/85 v/v) EV: sistema de vacío R: Ac. acético 0,5% +vortex Centrifugación | Acquity TQD | Acquity BEH C18 (100 x 2.1 mm, 1,7 μm | [M+H]+: 112.82 70.05*/95.90† | UBr | Media: 9,7±7,7 Mediana:8,4 Rango:0,6-43,3 | Coudoré et al. 20128 |
| P | 320 vol. y 28 pac. | Heparina de litio | N.E. | 7am- 9am 11am-1.30pm | Mantenida en hielo t: <1h | Tª N.E. t: 10 min. F: 3.300 g | Tª -20 ºC t: N.E. | PP: Sulfato de amonio EX1: Acetato de etilo-2-propanol (10:1 v/v) EV: N2 (40 ºC) EX2: fase orgánica R: Ac. Fórmico 0,1% +sonicación Centrifugación | 4000 QTRAP | Atlantis dC18 (2,1 x 150 mm, 3 μm) conectado a Atlantis dC18 (2.1x10 mm, 3 μm) | [M+H]+: 113 70.00 | U-2-13C | Voluntarios sanos: Media: 14,6 Rango: 3,4- 62,8 Pacientes: Media: 15,7 Rango: 7,8- 34,7 | Sistonen et al. 20149 |
| P | 60 pac. | EDTA | SI (8h) | 8am-9am | Inmediata | N.E. | Tª -70 ºC t: N.E. | PP: Sulfato de amonio EX: Isopropanol-acetato de etilo (15/85 v/v) EV: tubo de vacío 60 ºC R: Agua ultrapura Centrifugación | TSQ Quantum Access | Acquity C18 (150 × 2,6 mm, 1,7 μm) | [M+H]+: 113 70.00*/40†/96† | 5-FU | Media: 15,2style="white-space:pre-line" Rango: 4,5-1093,0style="white-space:pre-line" | Galarza et al. 201610 |
| S | 550 pac. | - | N.E. | N.E. | N.E. | N.E. | N.E. | PP: metanol/acetonitrilo (50:50) Centrifugación 10´,14.000 g EV: corriente de N2 (40ºC) R: Ac. Fórmico 0,1%+vortex Centrifugación | QTRAP 5500 TQ | Acquity HSS T3 (150 × 2.1 mm, 1,8 μm) | [M+H]+: 110,9 42,0 | U-15N2 UH2-13C4 15N2 | Media: NE Rango: 3,2-38,3 P1-91 [<13,0] n=500/550 P92-94 [13,0-13,8] n=16/550 P95-97 [13,9-16,0] n=17/550 P98-100 [>16,0] n=17/550 | Meulendijks et al. 201711 |
| P | 40 pac. | EDTA | N.E. | 8am-11.30am | Inmediata | N.E. | Tª -70 ºC t: N.E. | PP: Sulfato de amonio EX: Isopropanol-acetato de etilo (15/85 v/v) EV: tubo de vacío 60 ºC R: Agua ultrapura | TSQ Quantum Access | Hypercarb (150 × 3 mm, 5 μm) | [M+H]+: 113 70.00*/40†/96† | 5-FU | Media: 11,7 Rango: 5,3-26,2 | Neto et al. 201812 |
| P | 64 pac. | Heparina | N.E. | N.E. | <1,5h | Tª 4 ºC t: N.E. F: N.E. | Tª-20ºC t: N.E. | Tubo con filtro 0,45µm + plasma + isopropanol + acetonitrilo/ác. fórmico (1%) Mezclado Filtración a vacío Extracto diluido en agua | LCMS-8060 TQ | Hypercarb, (150 x 2,1 mm, 3 µm) | [M+H]+: 113,1 70.1* | U-15N2 UH2-13C4-15N2 | Rango: 4,9-36,6 (n=63) | Robin et al. 202013 |
| P | 526 pac. | Heparina, sin gel separador | N.E. | N.E. | < 1,5h a Tª ambiente o < 4h a 4 ºC | Tª 4ºC t: 10 min. F: 3.200 g | Tª -20ºC t: N.E. | PP: Sulfato de amonio EX1: Acetato de etilo-2-propanol (85/15, v/v) EV: N2 (40 ºC) R: Ac. acético 0,5% Centrifugación | 4500QTRAPMD | Cortecs T3 (C18) 2.5 mm (100 x 2.1 mm, 2,5 μm) | [M+H]+: 112.95 70.00*/95.90† | U-13C15N2 UH2-13C15N2 | Mediana: 10,6 Q1-Q3: 8,4-13,8 Rango:3,9-81,6 | Tafzi et al. 202014 |
| P | 37 pac. | Heparina sódica | N.E. | N.E. | t: N.E. Tª 4ºC | Tª N.E. t: 10 min. F: 2.000 g | Tª -80 ºC t: N.E. | PP: ZnSO4 + acetonitrilo/metanol (95/5, v/v) EX1: Ac acético y acetato de etilo/alcohol isopropílico EV: concentrador de vacío 50 ºC R: ác. acético/ác. fórmico/agua (0,25/0,05/99,7, v/v/v) | 6460 TQ (Agilent) | Luna PFP (2) (150 × 2 mm, 3 μm) conectado a PFP (2) (4 × 2.0 mm, 3 μm) | [M+H]+: 113,1 53,1/68,1 | U marcado con isótopos estables (N.E.) | Media: 10,7 Q1-Q3: 9,1-11,9 Rango: 7,2-20,7 | Burns et al. 202115 |
| S | 77 pac | - (con gel separador) | N.E. | N.E. | N.E. | Tª ambiente. t: 5 min. F: 3.500 g | Tª -80 ºC t: N.E. | PP: metanol + agitación + ultrasonidos 5´. Centrifugación 14.100 g, 10´. Eliminación de fosfolípidos en cartucho Phree (Phenomenex) Sequedad: N2 (40 ºC) R: agua tipo I | Cuadrupolo-orbitrap híbrido Q-exactive | Hypercarb (50 × 4,6 mm, 6 μm) conectado a columna Pinacle DB AQ C18 (30 x 2,1 mm, 3 μm) | [M+H]+: 113.03455 70.02935/96,00832* | U-2-13C | Media: 30,4 Mediana: 24,0 Q1-Q3: 17,0-34,5 Rango: 7,1-139,7 | ITOXDEF 2022 |
P: plasma; S: suero; Pac.: pacientes; Vol.: voluntarios; N.E.: no especificado; Tª: temperatura; t: tiempo; F: fuerza g; PP: precipitación proteica; EX: extracción; EV: evaporación; R: reconstitución; TQ: triple cuadrupolo;
*:Ion de cuantificación;
†:Ion de confirmación.
La proporción de pacientes de la muestra con una concentración sérica de U comprendida entre 16 ng/ml y 150 ng/ml se comparó con la proporción poblacional preespecificada de pacientes con deficiencia parcial de DPD, tomando como valor de hipótesis una prevalencia del 8% por ser el límite superior del intervalo referenciado en la alerta emitida por la AEMPS para población caucásica (3-8%).
Para la realización de este test de hipótesis se aplicó una prueba-z empleando la herramienta online MedCalc Software Ltd. Test for one proportion calculator [disponible en https://www.medcalc.org/calc/test_one_proportion.php].
El análisis estadístico se realizó con el software IBM SPSS Statistics v25.0.
RESULTADOS
Se incluyeron 77 pacientes. La mediana de edad fue 71 años (IQR 58,2-79,3) y 44 eran hombres (57,1%). Los tipos de cáncer más frecuentes fueron: colon (23; 29,9%), recto (16; 20,8%) y colorrectal (11; 11,7%). La concentración media de U fue de 30,4 ng/ml (IC 95% 25,0-35,0) (véase tabla 1). La distribución de la serie completa se muestra en la figura 1.
Tabla 1. Distribución de las concentraciones séricas de uracilo.
| Número de pacientes = 77 | Concentración sérica de uracilo (ng/mL) |
|---|---|
| Media | 30,4 |
| Mediana | 24,0 |
| Q1-Q3 | 17,0-34,5 |
| Valor mínimo | 7,1 |
| Valor máximo | 139,7 |
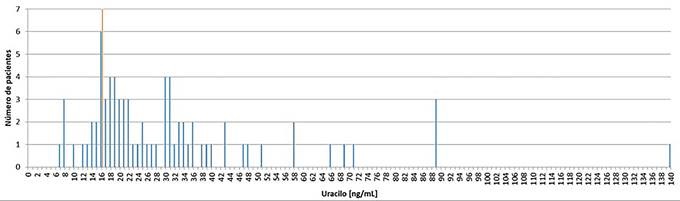
Figura 1. Histograma de frecuencias de los niveles séricos de uracilo en la población estudiada. La línea roja vertical indica el valor establecido como punto de corte para la detección del déficit enzimático de dihidropirimidina deshidrogenasa (16 ng/ml).
Un total de 61 pacientes (79.2% [IC 95% 68,4-87, 6%]) presentaron una concentración de U en el intervalo 16-150 ng/ml y solo 16 (20.8% [IC 95% 12,4-31, 6%]) presentaron un valor de U por debajo de 16 ng/ml. En nuestra muestra (n = 77), al comparar la proporción de pacientes con una concentración de U compatible con deficiencia parcial de DPD (79,2%) con la proporción preespecificada (8%), el estadístico z fue 23,030 y el p-valor <0,0001, rechazando así la hipótesis de que la prevalencia observada en nuestra muestra sería igual a la descrita en población caucásica.
En lo que respecta al método analítico, el coeficiente de correlación R2 fue mayor de 0,99 y el límite de detección inferior a 0,2 ng/ml.
DISCUSIÓN
En nuestro estudio encontramos unas concentraciones séricas de U notablemente superiores a otras publicadas por grupos que emplearon LC-MS/MS con diferentes equipos, condiciones de ensayo y métodos de preparación de las muestras5,8,16 (véase tabla 2). El método analítico desarrollado por el ITOXDEF es rápido, sensible y muestra una buena linealidad, precisión y exactitud en el rango de concentración validado.
De acuerdo con los resultados presentados, existe una diferencia estadísticamente significativa entre la proporción de pacientes con niveles de U compatibles con una deficiencia parcial de DPD observada en nuestra muestra y la prevalencia de esta alteración descrita para población caucásica. Teniendo en cuenta la validez de los resultados arrojados por la técnica empleada en nuestro estudio, parece que esta diferencia puede deberse a la posible influencia de factores relativos al tratamiento preanalítico que no fueron controlados en nuestro estudio (matriz empleada, tiempo hasta centrifugación, temperatura de conservación, hora de extracción, condición de ayuno). Si bien es cierto que no se puede descartar que las condiciones del método analítico (equipo, columna, iones y patrón interno, entre otras), también puedan influir en la determinación.
Matriz y anticoagulante
Cabe destacar que la determinación del U endógeno se realizó en muestras de suero y no de plasma. Se escogió esta matriz por ser el tipo de muestra empleado en el estudio de Meulendijks et al. que resultó fundamental para establecer el punto de corte de U endógeno en 16 ng/ml11. Sin embargo, la Haute Autorité de santé (HAS) francesa recomendó en 2018 que la determinación se llevara a cabo partiendo de sangre venosa extraída en tubos con anticoagulante sin gel separador, es decir, en plasma. Entre los anticoagulantes más frecuentemente empleados se encuentra la heparina de litio y el EDTA. Un estudio reciente observó que los niveles plasmáticos de U tendían a ser superiores en las muestras anticoaguladas con EDTA y lo atribuyó a la posible influencia del pH en la estabilidad del analito17.
La determinación de los niveles séricos estaría libre de la influencia de este condicionante. Además, el hecho de que otros estudios llevados a cabo con muestras de plasma (véase tabla 2) obtuvieran resultados similares a los del trabajo de Meulendijks et al. sugiere que el tipo de muestra probablemente influya en el resultado, pero no justifica por sí solo la divergencia observada en nuestra población de estudio. Por otro lado, se desconoce si el gel separador del tubo de extracción puede influir en la determinación.
Temperatura y tiempo hasta la centrifugación
En lo que respecta a la posible influencia del tiempo transcurrido desde la toma de la muestra hasta su centrifugación, Remaud et al.18 ya publicaron en el 2005 que los niveles de U endógeno de voluntarios sanos se incrementaban conforme aumentaba el tiempo transcurrido desde la extracción de la sangre hasta su centrifugación. Publicaciones posteriores incluyeron en su metodología la necesidad de centrifugar inmediatamente las muestras a fin de minimizar este efecto19. Coudoré et al.8 cifraron en 27,2 ± 15,1%, 163,0 ± 26,8% y 169,0 ± 9,1% las variaciones medias en los niveles de U, cuando el tiempo transcurrido a temperatura ambiente, desde la extracción hasta el centrifugado de las muestras, era de 2 h, 5 h y 24 h, respectivamente. Otros autores estimaron que el incremento a las 6 h era de 21,2 ± 2,1%16. Esta tendencia, aunque en menor medida, también se observó cuando la conservación de las muestras se realizaba a una temperatura de entre 2 y 8 ºC. Jacobs et al. concluyeron que, a esta temperatura, el tiempo máximo de conservación no debía superar las 4 h, debiendo evitar en todo caso la conservación a temperatura ambiente. En base a este y otros estudios la HAS recomendó llevar a cabo la centrifugación de la sangre en los 90 primeros minutos para muestras procesadas a temperatura ambiente y 4 h para aquellas refrigeradas20. Más recientemente se ha concluido que el tiempo transcurrido hasta la centrifugación no debería ser superior a 1 h y el envío de muestras y su conservación debería hacerse en condiciones de refrigeración con la finalidad de asegurar la fiabilidad en la determinación17.
Las muestras analizadas en nuestro centro no se enviaban refrigeradas ni tampoco se estableció con anterioridad un tiempo máximo hasta la centrifugación. Este hecho contribuiría a explicar, en parte, el incremento en las concentraciones de U. Coudoré et al. atribuyen este hecho a la liberación de U desde el DNA y la albúmina y a la degradación de las pirimidinas8. Otra posible explicación sería la conversión de uridina en U, reacción catalizada por la uridina fosforilasa21. Los niveles de uridina han sido relacionados con la actividad de la DPD22. Por otro lado, la uridina fosforilasa se encuentra elevada en pacientes con tumores sólidos23,24 lo que podría hacer que la variación en los niveles de U debido a la actividad enzimática de la uridina fosforilasa fuera mayor en este tipo de pacientes. En este sentido sería interesante comprobar la evolución de uridina y U en diferentes condiciones de conservación. Otro punto interesante es evaluar si estrategias como la implementada por Büchel et al.7 y Sistonen et al.9, consistentes en mantener en hielo durante un tiempo la sangre recién extraída, tiene un efecto beneficioso en el mantenimiento de los valores del analito.
Condición de ayuno y ritmo circadiano
La influencia de la ingesta de alimentos en los niveles de U ha sido testada en 16 voluntarios sanos, observando que tras el consumo de alimentos se produce una disminución del U plasmático en comparación con las determinaciones en un estado de ayuno25. Además, parece que, independientemente del estado alimentado o ayunado, se produce una reducción paulatina entre las 08:00h y las 13:00h. Esta observación es coherente con los resultados del trabajo de Jacobs et al.26, quienes analizaron el ritmo circadiano del U observando un pico de 12,21 ± 0,75 ng/ml a las 05:00 h mientras que el valle se situaría a las 17:00 h con un valor medio de 8,78 ± 0,49 ng/ml.
La condición de ayuno y la hora de extracción han sido definidas con anterioridad en diferentes investigaciones (véase tabla 2), pero no en nuestro estudio. No obstante, las variaciones producidas por estos factores no parecen influir de una forma tan significativa como para poder explicar, por sí solos, los elevados valores de U determinados en nuestra población de estudio.
Congelación
En relación a la congelación del plasma, parece existir una evidencia sólida que avala el empleo de esta técnica de conservación hasta el momento de realizar la determinación6,7,16,17,26,27. En este sentido, una recomendación de la HAS fue la de congelar inmediatamente el plasma obtenido y conservar la cadena de frío hasta el momento del ensayo. Teniendo en cuenta la duración de nuestro estudio y la temperatura de conservación (-80 ºC), no parece razonable que la congelación de las muestras haya podido afectar de forma notoria a los valores de U.
No se ha encontrado en la bibliografía un documento en el que se concreten las condiciones en las que debe realizarse esta prueba de fenotipo antes de iniciar un tratamiento con FP. En este sentido, es importante advertir sobre las consecuencias para el paciente derivadas de la emisión de un resultado con un valor de U distorsionado. Teniendo en cuenta las recomendaciones recogidas en la alerta sanitaria emitida por la AEMPS, en caso de superar los 16 ng/ml se iniciaría un tratamiento con dosis reducidas y en caso de superar los 150 ng/ml no se iniciaría el tratamiento con estos principios activos lo que, en ambos casos, tendría una repercusión negativa en los resultados clínicos de la quimioterapia.
CONCLUSIONES
Nuestro trabajo sugiere que es necesario llevar a cabo más estudios con un diseño dirigido a establecer las condiciones óptimas relativas al pretratamiento de las muestras a fin de evitar o minimizar la influencia de estos factores sobre los valores del analito. Solo cuando se tenga la certeza de que las condiciones fijadas aseguran la fiabilidad y exactitud de la determinación se podrá establecer el umbral de U que permita identificar correctamente a los pacientes que presenten una deficiencia de DPD y que, por tanto, sean susceptibles de sufrir toxicidad asociada al tratamiento con FP.














