Introducción
El uso de los inhibidores de la aromatasa (IA) como terapia coadyuvante después de la cirugía, y/o la radioterapia, y/o la quimioterapia, ha logrado un aumento significativo de la supervivencia en mujeres postmenopáusicas diagnosticadas de cáncer de mama con receptores hormonales (estrógenos y/o progesterona) positivos (RH), en estadios iniciales [1,2].
La acción de la aromatasa sobre la testosterona y la androstendiona produce estradiol y estrona [3]. Estos dos componentes constituyen la principal fuente de estrógenos en la mujer postmenopáusica. Este proceso de aromatización se realiza en los tejidos periféricos, como el tejido adiposo y el músculo. Aproximadamente dos terceras partes de los tumores mamarios han demostrado tener actividad aromatasa, produciendo localmente estrógenos en el propio tumor que estimulan el crecimiento de las células mamarias tumorales [4]. Los IA bloquean directamente la producción de estrógenos en el tumor y además provocan una drástica reducción de los niveles de estrógenos circulantes [5].
La sostenida privación estrogénica derivada de la terapia con IA provoca una pérdida acelerada de la masa ósea, aumentando el riesgo de sufrir una fractura osteoporótica [6]. Asimismo, los IA también pueden producir otros efectos adversos musculoesqueléticos como artralgias y dolores musculares, que pueden afectar al cumplimiento de la terapia durante los años de tratamiento prescrito [7,8].
Por otro lado se ha observado que las pacientes tratadas con IA muestran una gran variabilidad interindividual en la aparición e intensidad de los síntomas musculoesqueléticos, sugiriendo que existen factores que pueden aumentar su aparición. En este sentido, los niveles de vitamina D (Vit D) se han relacionado con la aparición de artralgias [9]. Asimismo, probablemente también existe una base genética que modularía, en parte, el efecto de los IA. Diversos estudios han relacionado variantes genéticas asociadas al aumento de dolor y la pérdida de masa ósea en mujeres tratadas con IA de la cohorte B-ABLE [10,11].
Concretamente, polimorfismos de cambio de un nucleótido (SNPs) en el gen CYP11A1: rs4077581, rs11632698 y rs900798 se asociaron con la pérdida de densidad mineral ósea (DMO) en cuello femoral (CF) a los 2 años de tratamiento con IA [11]. El gen CYP11A1 codifica la enzima de escisión de la cadena lateral del colesterol (nombre alternativo: P450scc) que cataliza el paso primero y limitante de la esteroidogénesis, convirtiendo el colesterol en pregnenolona. Además, la P450scc también puede hidroxilar la vitamina D2, D3 y sus precursores [12,13], sugiriendo un amplio espectro de funciones en el metabolismo celular.
Por otro lado, siete SNPs del gen CYP17A1 (rs4919686, rs4919683, rs4919687, rs3781287, rs10786712, rs6163, rs743572) se asociaron con el aumento de dolor al año de tratamiento con IA [10]. El CYP17A1 (17α-hidroxilasa/17,20 liasa) es una enzima clave en la vía esteroidogénica que produce progestinas, mineralocorticoides, glucocorticoides, andrógenos, y estrógenos.
Ninguno de los SNPs de los genes CYP11A1 y CYP17A1, previamente genotipados, provocan cambios no sinónimos en la proteína, ni se conoce que tengan ninguna función reguladora de la expresión génica.
Es posible que variantes funcionales de los genes implicados, tanto en la región codificante, que modificarían la actividad del enzima, como en regiones reguladoras, que regularían los niveles de expresión génica, pudieran estar implicadas en los efectos secundarios de los IA. Por ello, el objetivo del estudio es la identificación de variantes putativamente funcionales en los genes CYP11A1 y CYP17A1.
Material y métodos
Población de estudio
La cohorte B-ABLE (Barcelona – Aromatase induced Bone Loss in Early breast cancer) es la población de un estudio prospectivo donde se incluyen pacientes postmenopáusicas con cáncer de mama RH positivo, y tratadas en el Hospital del Mar de Barcelona. Las participantes reciben IA (letrozol, exemestano o anastrozol) durante 5 años, o de manera alternativa después de 2 ó 3 años de tratamiento con tamoxifeno (3 y 2 años de IA, respectivamente), de acuerdo a las recomendaciones de la American Society of Clinical Oncology, empezando dentro de las 6 semanas después de la cirugía ó 1 mes después del último ciclo de quimioterapia [14].
Los criterios de exclusión fueron: alcoholismo, insuficiencia renal de grado superior al 3b, artritis reumatoide, enfermedades metabólicas óseas diferentes a la osteoporosis, enfermedad de Paget, osteomalacia, hiperparatiroidismo primario, hipertiroidismo, diabetes mellitus insulinodependiente, tratamiento previo o en curso con antirresortivos, corticosteroides orales o cualquier otro fármaco que pudiera afectar el metabolismo óseo, excepto tamoxifeno.
Mediciones
Densidad mineral ósea
Al inicio y cada 12 meses hasta la finalización del tratamiento se midió la DMO a nivel lumbar (CL L1–L4), cuello femoral (CF) y cadera total (CT) utilizando el densitómetro de energía dual de rayos X (DXA) QDR 4500 SL® (Hologic, Waltham, Massachusetts, EE.UU.). El coeficiente de variación para esta técnica en nuestro centro es del 1% en CL y del 1,65% en CF. Se excluyeron en el seguimiento aquellas densitometrías cuyas imágenes presentaban artefactos, enfermedad degenerativa del disco con osteofitos, artrosis con hiperostosis de las articulaciones facetarias, fracturas vertebrales y/o calcificaciones aórticas, y todas aquellas que pudieran causar un falso aumento de la DMO, de acuerdo a la descripción de Blake et al. [15] Posteriormente se analizó mediante el valor de pérdida relativa de masa ósea.
Escala visual analógica
El dolor articular se midió utilizando la escala visual analógica (EVA), medido al inicio, a los 3 meses y cada 12 meses hasta el final del estudio. Se valoró el dolor de las articulaciones: manos, hombros, rodillas, caderas, tobillos y pies, en una escala del 1 al 10 con decimales. Posteriormente se analizó mediante el cambio absoluto de EVA.
Variables demográficas
Se recogió información de un gran número de variables clínicas en el momento del reclutamiento, incluyendo la edad, las edades de menarquia y menopausia, el tiempo de lactancia, el número de partos, la quimioterapia y radioterapia previa, tratamientos adyuvantes, el peso, la talla, el tabaquismo y la ingesta de calcio mediante la encuesta INDICAD [16].
Construcción de haplotipos
En estudios previos en la cohorte B-ABLE se genotiparon SNPs localizados en los genes CYP11A1 y CYP17A1 [10,11]. Los SNPs que mostraron una asociación estadísticamente significativa con los fenotipos evaluados se escogieron para la construcción de los haplotipos (Figura 1).
Para establecer la relación de los haplotipos del gen CYP11A1 con los SNPs rs4077581, rs11632698 y rs900798 en la cohorte B-ABLE, se calcularon las frecuencias haplotípicas con el análisis haplo.em y se escogieron los haplotipos más comunes (frecuencia >0,01).
Los haplotipos del gen CYP17A1 se construyeron de la misma manera con los SNPs rs743572, rs6163, rs10786712, rs3781287, rs4919687, rs4919686 y rs4919683.
A cada haplotipo se le asignó un código para facilitar su nomenclatura durante el estudio.
Extracción de ADN y secuenciación Sanger
La extracción de ADN se realizó a partir de sangre periférica empleando el kit de purificación de ADN Wizard® Genomic DNA Purification Kit (PROMEGA). Se amplificaron las regiones codificantes, 5’UTR, 3’UTR y promotor proximal (hasta el -601 pb para el CYP11A1 y -589 pb para el CYP17A1) con los primers descritos en la tabla 1.
La secuenciación se efectuó mediante el método de Sanger. Las secuencias fueron analizadas con el programa Sequence Scanner (v1.0) y el alineamiento con la secuencia de referencia (NCBI Reference Sequence: CYP11A1 NG_007973.1 y CYP17A1 NG_007955.1) se llevó a cabo a través del Multiple Sequence Alignment (EMBL-EBI).
Análisis estadísticos
La frecuencia de los SNPs del CYP11A1 y CYP17A1 fue estimada con el algoritmo esperanza-maximización. La asociación entre los haplotipos y los fenotipos (cambio de DMO en CF y aumento de dolor) se analizó con el haplo.glm, basado en análisis de regresión glm, ajustando por edad, índice de masa corporal (IMC), terapia previa con tamoxifeno y quimioterapia. El haplotipo más común fue utilizado como haplotipo de referencia y se asumió el modelo aditivo obteniendo un valor p y el β-coeficiente respecto el haplotipo de referencia.
Las potenciales diferencias entre las características de las pacientes seleccionadas según su haplotipo y con fenotipos extremos fueron evaluadas con la prueba t de Student para muestras independientes.
La asociación entre las variantes genéticas encontradas en la secuenciación y los fenotipos extremos se analizaron mediante regresión lineal múltiple, contemplando los modelos de herencia genética dominante, recesivo y aditivo.
Todos los análisis estadísticos fueron definidos como significativos con P<0,05. Estos se realizaron mediante programa estadístico SPSS (versión 22) y R para Windows (versión 2.15.2) usando los packages, foreign, rms, multtest, plyr, boot, haplo.stats y SNPassoc.
Declaración de ética
Los protocolos del estudio han sido aprobados por el Comité Ético de Investigación Clínica del Parque de Salud Mar (2013/5283/I). Los protocolos aprobados para la obtención de ADN de muestras de sangre se explicaron a las potenciales participantes, que firmaron un consentimiento informado antes de ser incluidas en el estudio.
Resultados
Características basales de las pacientes de la cohorte B-ABLE
En la tabla 2 se muestran las características demográficas, los valores de DMO y la evolución de la sintomatología musculoesquelética mediante EVA, para los genes CYP11A1 y CYP17A1, en las que se procedió a la construcción de los haplotipos.
Tab2 Características basales de las pacientes genotipadas para los genes CYP11A1 y CYP17A1
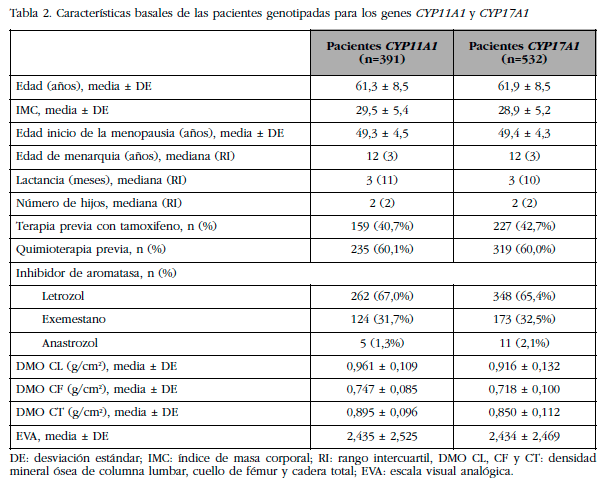
nota1Tab2DE: desviación estándar; IMC: índice de masa corporal; RI: rango intercuartil, DMO CL, CF y CT: densidad mineral ósea de columna lumbar, cuello de fémur y cadera total; EVA: escala visual analógica.
El esquema del procedimiento para llegar al análisis final de asociación genética con los fenotipos extremos de DMO y sintomatología musculoesquelética mediante EVA se muestra en la figura 2.
Construcción de los haplotipos del gen CYP11A1 y del gen CYP17A1
En la tabla 3 se muestran los haplotipos construidos y el análisis de asociación de los genes CYP11A1 y CYP17A1 con el cambio de DMO en CF a los 2 años y el aumento de dolor a los 12 meses de tratamiento con IA, respectivamente.
Tab3 Asociación entre haplotipos de los genes CYP11A1 y CYP17A1, con pérdida de DMO en CF a 2 años y cambios del dolor a los 12 meses de tratamiento con IA, respectivamente

Nota1Tab3*Haplotipo de referencia; a Haplotipos construidos por: rs4077581, rs11632698 y rs900798; b Haplotipos construidos por: rs743572, rs6163, rs10786712, rs3781287, rs4919687, rs4919686 y rs4919683; c Ajustado por: edad, índice de masa corporal, quimioterapia y tamoxifeno previo. DMO: densidad mineral ósea; CF: cuello de fémur; IC: intervalo de confianza.
En el gen CYP11A1, el haplotipo que mostró una mayor diferencia fenotípica respecto el haplotipo de referencia (11.1) fue el 11.2, donde las pacientes portadoras del haplotipo 11.1 en homocigosis tenían una pérdida de DMO de 4,41 veces mayor que las portadoras del haplotipo 11.2 en homocigosis (Tabla 4).
Tab4 Media de los fenotipos (pérdida de DMO en CF en CYP11A1 y aumento del dolor en CYP17A1) de las pacientes de la cohorte B-ABLE portadoras de los haplotipos en homocigosis
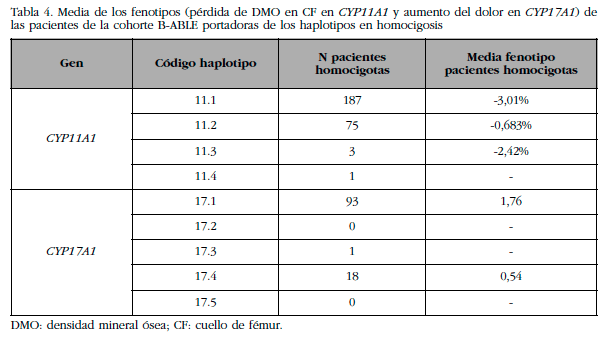
Nota1Tab4DMO: densidad mineral ósea; CF: cuello de fémur.
En el caso del gen CYP17A1, los haplotipos 17.3 y 17.4 mostraron diferencias estadísticamente significativas respecto el haplotipo de referencia (17.1). Las pacientes homocigotas para el haplotipo 17.1 mostraron un aumento del dolor 3,26 veces más que las pacientes homocigotas para el haplotipo 17.4 (Tabla 4).
Selección de pacientes para el estudio genético por secuenciación Sanger
A partir de los resultados del análisis de asociación con haplotipos, se seleccionaron las pacientes de la cohorte B-ABLE portadoras de los haplotipos (con un 99% de probabilidad) que mostraban mayores diferencias fenotípicas: para el gen CYP11A1 se seleccionaron las pacientes portadoras de los haplotipos 11.1 y 11.2 en homocigosis. Para el gen CYP17A1, se seleccionaron aquellas pacientes portadoras de los haplotipos 17.3 y 17.4, tanto en homocigosis como en heterocigosis. Además se seleccionaron las pacientes portadoras del haplotipo 17.1 y cualquier otro haplotipo (a excepción de los 17.3 y 17.4) (Figura 2 y Tabla 3).
Posteriormente, dentro de cada grupo haplotípico del gen CYP11A1 se escogieron a las pacientes que mostraban un fenotipo extremo en la DMO de CF (mayor o menor pérdida de DMO a los 24 meses de tratamiento) (n=40). El mismo proceso se llevó a cabo para los grupos haplotípicos del gen CYP17A1 en que se seleccionaron aquellas pacientes con el fenotipo extremo para artralgia (mayor o menor aumento del dolor los 12 meses de tratamiento) (n=39) (Tabla 5).
Identificación de variantes genéticas y análisis de asociación con los fenotipos extremos
Tras la secuenciación de los genes CYP11A1 y CYP17A1, se encontraron diversos SNPs en ambos genes. Ninguno de ellos correspondía a un cambio no sinónimo, ni en sitios de splicing y, por lo tanto, se descartó un cambio en la secuencia proteica.
Sin embargo, en la región del promotor basal del gen CYP11A1 se encontró una variante genética (D15S520) asociada a la variación de DMO en CF a 24 meses (Coeficiente β=-6,32; Intervalo de confianza (IC) del 95%: [-8,55 ; -4,09]; p=3,71e-06).
El polimorfismo D15S520 es un microsatélite en la posición -373 pb que se utiliza como marcador genético (Sequence Tagged Sites, STS) y que consiste en la repetición en tándem del pentanucleótido (TAAAA)n. En nuestras pacientes, el número de repeticiones observadas fue 4, 6, 8 y 9.
Se encontró que el haplotipo 11.1 correlacionaba con el alelo de 4 repeticiones del pentanucleótido. En cambio, las pacientes portadoras del haplotipo 11.2 presentaban diferentes alelos del microsatélite que podían estar en homocigosis o heterocigosis, pero nunca el alelo con 4 repeticiones.
Discusión
Los IA tienen una serie de efectos secundarios entre los cuales destacan la aparición o el aumento de artralgias y la pérdida de masa ósea, aumentando así el riesgo de fracturas. Todo ello puede afectar el cumplimiento de la terapia, disminuir la calidad de vida de las pacientes y aumentar el riesgo de recidiva del tumor mamario.
En estudios previos, se asociaron variantes genéticas del gen CYP11A1 y del CYP17A1 a la pérdida de DMO en CF [11] y al aumento de dolor articular [10], respectivamente. Ninguno de los SNPs asociados a dichos eventos producía un cambio en la estructura de la proteína y, por lo tanto, se descartó una posible funcionalidad de estos SNPs en la determinación del evento.
Con el objetivo de identificar putativas variantes genéticas funcionales que expliquen la asociación de estos genes con los efectos musculoesqueléticos, se secuenciaron las regiones codificantes y reguladoras de los genes CYP11A1 y CYP17A1.
No se halló ninguna variante en la región codificante que causara un cambio en la secuencia de aminoácidos de la proteína y, por lo tanto, que pudiera implicar un cambio estructural de la enzima. Sin embargo, se halló una variante genética, D15S520, situada en la región reguladora del CYP11A1, que se relacionó con la pérdida de masa ósea.
El D15S520 es un microsatélite basado en la repetición del pentanucleótido (TAAAA)n situado en el promotor del CYP11A1, a 528 pb upstream del inicio de traducción del gen. En nuestro estudio, este polimorfismo se ha encontrado significativamente asociado a la pérdida de masa ósea a los 24 meses de tratamiento con IA. Se ha observado que todas las pacientes portadoras del haplotipo 11.1/11.1 eran también portadoras del genotipo 4/4. En la cohorte B-ABLE, estas pacientes tenían una predisposición mayor a perder masa ósea (-3,014%) que las portadoras de los haplotipos 11.2/11.2 (-0,683%).
Este microsatélite fue previamente asociado al riesgo de padecer cáncer de mama [17,18], aunque existe cierta controversia con los resultados [19,20]. El estudio de Sakoda et al. [18] sugirió que las mujeres portadoras de 4 repeticiones en homocigosis tendrían menor riesgo de sufrir cáncer de mama. Una hipótesis sería que el alelo de 4 repeticiones afectaría la expresión del gen CYP11A1 disminuyendo la producción de estrógenos. Como consecuencia, la menor exposición a estrógenos reduciría el riesgo de padecer cáncer de mama [21], pero durante el tratamiento con IA, los niveles de estrógenos remanentes podrían ser inferiores a los de las pacientes portadoras de los otros alelos, incrementando así la pérdida de masa ósea.
La detección de variantes genéticas que expliquen en parte la acción de los IA sobre el sistema musculoesqulético permitiría llevar a cabo terapias personalizadas con el fin de evitar, o al menos prever con antelación, los efectos secundarios de los IA. Con ello se podría mejorar la adherencia al tratamiento de estas pacientes, que actualmente se sitúa entre el 75,5-78,5%, y así evitar recaídas y un nuevo cáncer de mama contralateral [22].
La principal limitación de este estudio es que no prueba que este microsatélite sea realmente una variante funcional, ya que no existen estudios funcionales del promotor del CYP11A1 que validen esta hipótesis. Sin embargo, el hecho de no haber encontrado ninguna variable funcional en las regiones codificantes de ninguno de los genes estudiados parece indicarnos que la asociación observada entre estos genes y los fenotipos tiene que ser causada por variantes genéticas localizadas en regiones reguladoras. Otra limitación del estudio es la utilización del parámetro EVA para la valoración de la sintomatología musculoesquelética. El EVA asume que el dolor es una experiencia unidimensional que puede medirse en una escala de intensidad de un solo punto. No obstante, la toxicidad reportada por la paciente capta de forma más exhaustiva los efectos secundarios de las terapias (es decir, el dolor) en la experiencia diaria y tiene mayor concordancia con la calidad de vida de la paciente que la toxicidad comprobada por el clínico, siendo así apropiado para la investigación de la sintomatología musculoesquelética. Asimismo, la proporción de la escala de EVA permite detectar las diferencias porcentuales entre las mediciones de EVA obtenidas en múltiples puntos en el tiempo. Otras ventajas del EVA son su facilidad y brevedad de puntuación, mínima intrusividad y simplicidad conceptual.
En conclusión, la variante D15S520 del promotor del gen CYP11A1 podría modular la expresión de este gen, explicando así parte de la variabilidad fenotípica encontrada en la pérdida de masa ósea de las pacientes en tratamiento con IA. Por otro lado, no se ha encontrado ninguna variante en el CYP17A1 que pueda explicar el aumento o disminución del dolor articular observado en las pacientes en tratamiento con IA. Se deberían estudiar más profundamente las regiones promotoras de estos genes para detectar posibles variantes genéticas que podrían estar implicadas en la regulación de su expresión.











 texto em
texto em 






