INTRODUCCIÓN
Los equipos modernos, con sus ajustes predeterminados, optimización automática, etc., requieren unos conocimientos mínimos de los principios físicos y tecnológicos. Sin embargo, ahondar en ellos y entrenarse en cómo y en cuándo realizar los ajustes técnicos mediante los botones y los controles del equipo para obtener la mejor imagen puede ser de gran ayuda en situaciones especiales. Un adecuado manejo de las aplicaciones permite sacar todo el partido a nuestro equipo, guardar las mejores imágenes y evitar errores diagnósticos y terapéuticos (1).
Se conoce como knobology (o botonología) la “ciencia” de la manipulación de los botones, controles, teclas, ajustes técnicos, aplicaciones o herramientas del equipo o del dispositivo. Exige un mínimo conocimiento de los principios físicos y un entrenamiento supervisado (2-4).
Tanto la consola como la pantalla tienen una distribución de los datos y de los botones diferente en cada equipo. Incluso pueden cambiar los nombres de las aplicaciones para la misma función. No todos los equipos tienen todas las aplicaciones, aunque comparten las funciones básicas. Probablemente, si miramos un ecógrafo en uso encontremos algunas teclas más gastadas, identificando así los botones más útiles. Por desgracia, hay muchos botones superútiles apenas desgastados por desconocimiento.
En la pantalla, rodeando el área de imagen o exploración en la que nos centramos para interpretar la exploración, encontramos información muy útil que nos habla del sentido del flujo (código de color o signo de la velocidad en la gráfica), de la profundidad, de la localización del foco, de las escalas de velocidad, de la ganancia, del rango, de la frecuencia, etc. Allí se encuentran los datos técnicos de cómo se ha hecho el estudio y ahí se reflejarán los cambios al realizar ajustes (Fig. 1).
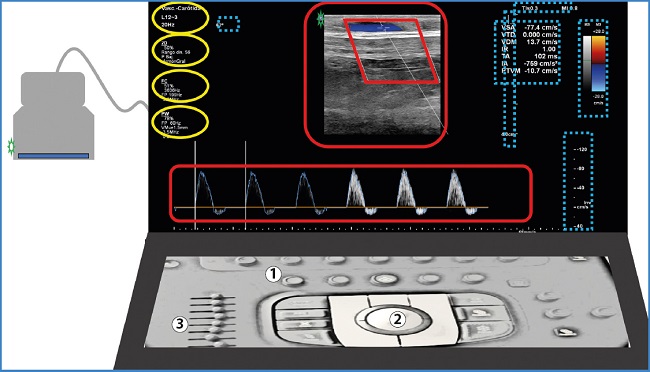
Figura 1. Pantalla con área de imagen o exploración (cuadro rojo con línea continua), y paneles laterales con información técnica. Vemos los datos de sonda y preset, ajustes del modo B, color, Doppler pulsado a la izquierda (círculos amarillos) e información de índice térmico, índice mecánico, profundidad, escala de Doppler color, escala de Doppler pulsado, valores de automedición de la gráfica y ángulo Doppler (cuadros azules con línea discontinua). El marcador de la sonda (surco y prominencia; color en un lateral de la sonda) debe correlacionarse con el indicador en la pantalla (ambos con estrella verde). Podemos tocar un borde de la sonda con el dedo y ver movimiento en la imagen para orientarnos. Es conveniente observar el código universal (craneal a la izquierda) para una adecuada orientación durante el estudio y para su revisión posterior. 1. Consola con botones. 2. Trackball. 3. Deslizadores.
Proponemos el siguiente esquema de exploración y ajustes paso a paso de forma ordenada y sistemática para no olvidar ninguno de ellos (Tabla I).
ON-OFF. ENCIENDE LA MÁQUINA Y REVISA LOS DATOS
Aunque lo diremos de todos los botones, resulta bastante obvio que este es el más importante.
- Al comienzo de cada exploración debemos asegurarnos de que el nombre del paciente coincide con el de la petición. Revisar la historia y los posibles informes previos puede ser útil, aunque nunca puede servir de excusa para una exploración mínima. Antes de comenzar el estudio introduciremos los datos del paciente mediante el teclado. No despreciemos algunas funciones que tienen algunos equipos, como el volcado de datos de la lista de trabajo, ya que facilita esa tarea, lo que evita errores. Podemos obviar este paso en algunos estudios en los que se no precise la grabación de los datos.
- También es el momento de asegurar qué tipo de exploración consta en la petición (en el caso de que no sea un estudio propio) y el motivo. En relación al posible daño o bioefecto de los ultrasonidos, a pesar de su relativa inocuidad, debemos aplicar el principio ALARA (As Low As Reasonably Achievable), especialmente en exploraciones de gestantes o de niños (5,6).
- Optimizar las condiciones de la habitación donde se realiza el examen en cuanto a luz, posición del paciente, explorador y equipo. Aunque la oscuridad completa de un cuarto de exploración de rayos sería lo deseable para evitar la pérdida de contraste que produce la incidencia de la luz, nuestros equipos suelen estar en salas multiusos. Por ello, el brillo de nuestro monitor está regulado de forma diferente a los de radiología. Oscurecer la habitación o entrar en una habitación oscura desde un entorno luminoso tampoco es útil, ya que el ojo humano tarda en adaptarse 20-30 minutos a la oscuridad. La posición del monitor debe ser lo más perpendicular posible al examinador. La posición del paciente debe estar adaptada al tipo de exploración (7,8).
ELIGE LA SONDA O EL TRANSDUCTOR
Una vez todo y todos colocados, nos enfrentamos a la elección más importante (3). En ocasiones el desconocimiento o la prisa pueden empujarnos a usar la sonda ya activa, lo que finalmente nos hará perder más tiempo, cuando no precisión (Fig. 2).
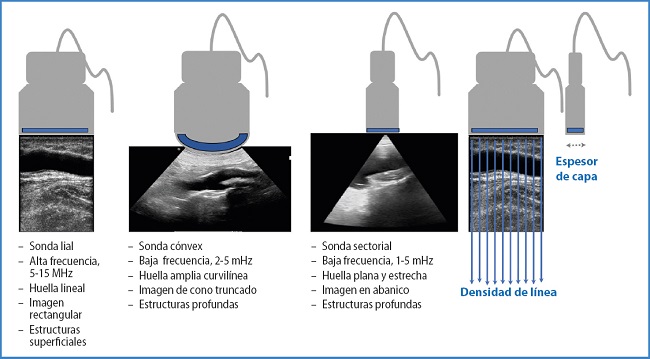
Figura 2. Tipos de sonda. Se clasifican por la forma de la superficie, huella o footprint (área de la sonda que se pone en contacto con la superficie del paciente), colocación de los cristales, por el funcionamiento (linear o phased array), por la imagen que originan, etc. Sonda lineal: puede mostrar una imagen trapezoide aumentando el campo o disminuyendo la resolución lateral. Sonda cónvex o curvilínea: campos amplios con mejor resolución lateral comparada con la sonda sectorial y estudios a mayor profundidad respecto a la sonda lineal. Sonda sectorial: phased array: la imagen se genera por la activación de los cristales de la sonda con retraso de tiempo y fase, generando campos de ultrasonido esféricos. Similar a una sonda cónvex, pero con pérdida de información en zona superficial y con menos resolución lateral. Puede asociarse al uso de Doppler continuo. Densidad de línea y espesor de capa.
Hay un compromiso entre la frecuencia de la sonda, la profundidad y la resolución axial (9-12) o capacidad de distinguir dos objetos situados a lo largo del haz de ultrasonidos (Fig. 3), de forma que, a mayor frecuencia, mayor resolución axial, pero también mayor atenuación, lo que impide hacer estudios profundos. La atenuación es la pérdida de energía de los ultrasonidos a medida que atraviesan las estructuras del cuerpo humano (1,9,10,11,13) (Fig. 4).
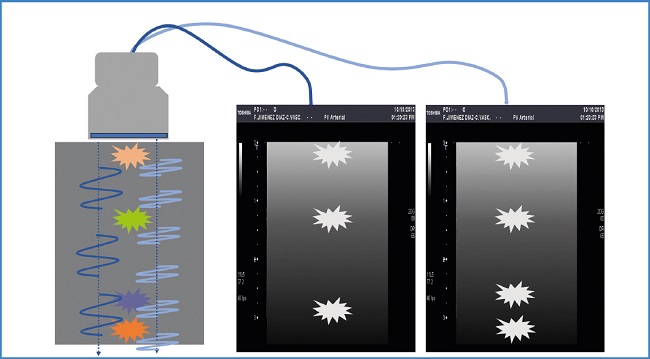
Figura 3. Resolución axial y frecuencia. Existe una relación y un compromiso de los parámetros: si la frecuencia aumenta, la longitud de onda disminuye y mejora la resolución axial de las imágenes, pero aumenta la absorción y por ello no podemos hacer estudios profundos. Debemos ajustar siempre la profundidad de la exploración para trabajar con la mayor frecuencia posible.
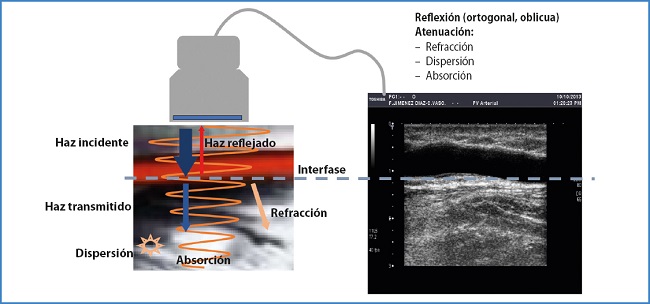
Figura 4. Los ultrasonidos van perdiendo energía a medida que atraviesan los tejidos, lo que se conoce como atenuación. Generan ecos de retorno (reflexión) en las interfases, que son útiles para formar una señal (imagen, gráfica, etc.), por lo que no se consideran atenuación. También sufren dispersión, refracción y absorción. La absorción depende del tejido (hueso > aire > músculos > … > agua), de la profundidad, de la frecuencia, etc.
Luego, por lo tanto, la primera razón para elegir una sonda u otra es la profundidad requerida para el estudio, de forma que, para un estudio superficial, seleccionaremos una sonda lineal de alta frecuencia, y para estudios más profundos usaremos una sonda curvilínea de baja frecuencia. Podríamos hacer todos los estudios con la sonda convex para no tener que cambiar, pero perderíamos resolución axial. La regla para una mejor resolución axial sería trabajar con la frecuencia más alta que permita la profundidad de campo que debemos explorar.
Otra razón al elegir la sonda es la amplitud o anchura de campo (3), mayor en la sonda convex que en las lineales. Algunas sondas lineales pueden ampliar el campo con una disposición trapezoide, pero perdiendo resolución lateral (Fig. 2).
ELIGE EL PRESET (O PRECONFIGURACION)
Los preset son ajustes preseleccionados por el fabricante para un tipo específico de examen. Cada uno de ellos configura condiciones para cada examen en cuanto a energía, frecuencia, ganancia, rango dinámico, etc. También prepara un paquete de medidas, de cálculos y de etiquetas útiles para ese estudio. Por lo tanto, este software automatiza el comienzo de nuestra exploración adaptada a ella de forma fácil, segura y con un ahorro de tiempo notable. Cada transductor tiene un listado de preconfiguraciones.
Elegir un buen preset es importante. No hace falta más que empezar un estudio venoso con el preset de carótida para darnos cuenta de nuestro error. Realizar un estudio obstétrico con preset abdominal puede no respetar la potencia máxima permitida para estudios fetales. Hacer ajustes una vez iniciado un estudio con un preset erróneo nos hace perder tiempo y claramente afecta al principio ALARA.
Si la preconfiguración de fábrica no termina de acomodarse a nuestros gustos o necesidades, podemos crear nuestro propio preset. Por ejemplo, dejar señalado un tiempo de grabación más largo en exploraciones que queramos guardar o publicar, diferenciar estudio venoso profundo o superficial en cuanto a profundidad y foco al comienzo de exploración, etc.
Debemos considerar el preset como un excelente punto de partida para después ajustar aún más el resultado con los botones y adaptarlo a nuestro paciente concreto.
Ponemos gel (el aire es el enemigo de la exploración con ultrasonidos) (3), colocamos la sonda correlacionando el marcador de la sonda y el marcador de la imagen ajustado a convenio (2) (Fig. 1) y…
EMPEZAMOS CON EL MODO B
El equipo se inicia siempre en modo B o en modo 2D, con una imagen bidimensional en escala de grises en tiempo real en la pantalla. Cuando vamos “tocando” los distintos botones vemos que hay valores que van cambiando en el monitor. Pueden hacerlo de forma directa, como cuando se sube la ganancia, o de forma indirecta, ya que hay valores relacionados entre sí y que se modifican al cambiar otro; por ejemplo, al subir la profundidad baja la frecuencia de exploración.
Para mejorar nuestra exploración en modo B, debemos manejar los siguientes parámetros (2-4,14,15) (Fig. 5):
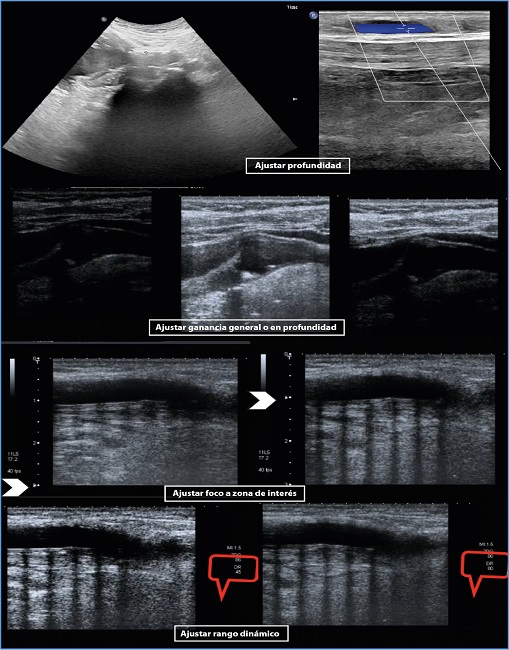
Figura 5. Ajustes del modo B: Profundidad. Ganancia general: TGC. Debemos configurar la señal de forma que las estructuras líquidas se muestren en negro y las altamente ecogénicas, como los huesos, se muestren en blanco. Para ello, en la primera imagen deberemos subir la ganancia general; en la segunda, disminuirla ligeramente. En la tercera debemos aumentar la ganancia en campo medio y profundo. Foco. Rango dinámico.
Profundidad
Con el preset óptimo seleccionado, puede que este sea al ajuste fino más importante que debemos hacer. En la pantalla, a un lado de la imagen en blanco y negro, vemos una línea de puntos o rayas que se relacionan con la profundidad en cm (Fig. 1). Ajustaremos la profundidad para ver la estructura en estudio sin recortar, evitando zonas más profundas que carezcan de interés (cuanto más tejidos y más variados, más ecos de retorno, que deterioran la resolución, y mayor tiempo de trabajo, que disminuye la resolución temporal) (2,14) (Fig. 5).
Zoom o magnificación de la imagen
Puede ser útil para medir estructuras de pequeño tamaño. Debemos diferenciar entre el zoom sobre una imagen congelada (o read zoom) o el zoom que se aplica a un estudio en vivo (o write zoom). En el primer caso, magnificamos la imagen sin mejorarla. El segundo intenta mantener la densidad de pixelado (aumenta la densidad de línea) y mejora la resolución temporal, ya que no se evalúan los ecos fuera de la zona del examen. El zoom no afecta a la profundidad, que sigue dependiendo de la frecuencia de exploración (3).
Ganancia general o ganancia de grises
Amplificador de señal, similar al volumen de un altavoz, que ajusta cómo de oscura o de clara es la imagen que aparece en la pantalla, aumentando o disminuyendo la fuerza de los ecos de retorno. Aparece en pantalla como G (Gain): G 2D (2,14,15) (Fig. 4).
Su manejo puede mejorar la resolución de contraste o la habilidad de distinguir estructuras adyacentes de pequeño tamaño y características tisulares similares. El equipo puede hacerlo de forma automática seleccionando autoajuste (o autogain), lo que evita movimientos de sonda o del paciente.
Output power, potencia, salida
Describe la energía por unidad de tiempo. Guarda relación con la calidad de la imagen, ya que al aumentar la potencia aumenta la amplitud de los ecos reflejados. Los ultrasonidos pueden producir cavitación por efecto mecánico (MI: índice mecánico) y también subir la temperatura de las estructuras que atraviesan por efecto térmico (TI: índice térmico; TIs: en tejidos; TIb: en huesos; Tic: en cráneo) (Fig. 1), por lo que debemos limitar los estudios de alta energía (mayor en Doppler que en modo B) y el tiempo de exploración, especialmente en estudios fetales y oftalmológicos (5,6). Reducir la energía a la mitad puede compensarse aumentando la ganancia (14).
El botón de ganancia puede estar compartido para todos los modos (modo B, Doppler color, Doppler pulsado, etc.) y su manejo afecta solo al modo activo.
TGC o DGC (Time or Depth Gain Compensation): ganancia en profundidad
Es la ganancia, o volumen de brillo amplificado, ajustada a la profundidad. Todos los equipos compensan la pérdida de señal debida a la atenuación, pero en algunos casos debemos hacer un ajuste suplementario, sobre todo en campos profundos (15).
Identificamos unos deslizadores en la consola (Fig. 1) que corresponden a las distintas profundidades o botones de ajuste de ganancia por campos superficial, medio y profundo.
Tanto la ganancia como el TGC pueden aumentar el ruido y los artefactos al amplificar la señal eléctrica de los ecos de retorno. Debemos configurar la señal de forma que las estructuras líquidas se muestren en negro, y las altamente ecogénicas, como los huesos, se muestren en blanco. Si no fuera así, se perderá el detalle debido a las escalas de grises no utilizadas.
Foco
Los ultrasonidos recorren una distancia desde la superficie de la sonda atravesando las estructuras en un haz que va estrechándose (zona de Fresnel) hasta un punto de anchura mínima a partir del cual comienza a ensancharse (zona de Fraunhofer). Con el foco ajustamos en el punto de interés esa zona reducida del haz, con lo que así mejora la resolución lateral o la capacidad de distinguir entre dos puntos situados en plano perpendicular al axial (14,15) (Fig. 6).

Figura 6. Los ultrasonidos recorren una distancia desde la superficie de la sonda atravesando las estructuras en un haz que va estrechándose (zona de Fresnel) hasta un punto de anchura mínima (zona focal) a partir del cual comienza a ensancharse (zona de Fraunhofer). Debemos ajustar el foco en la zona de interés para mejorar la resolución lateral.
Aparece en la pantalla como un punto, un triángulo o un reloj de arena en la zona de marcadores de profundidad. Debemos colocarlo un poco por debajo de la zona de interés (Fig. 5). Ajustaremos varios focos o un foco continuo para una zona amplia, pero disminuyendo la resolución temporal, ya que precisa que se emitan distintas “ráfagas” de ultrasonidos para cada punto focal en cada imagen.
Aunque se represente una imagen en dos dimensiones (2D), en realidad es la proyección de tres dimensiones al incluir la anchura del transductor o grosor o espesor de capa (3), lo que puede sumar artefactos. Es mayor cuando exploramos con baja frecuencia o con modo Doppler. Depende del foco (Fig. 2).
La sonda emite ultrasonidos a lo largo de la superficie con un determinado número de líneas de trabajo o densidad de líneas. Este valor puede ajustarse. El valor máximo está limitado por el equipo. Bajar la densidad disminuye la resolución lateral, genera una imagen suave y delinea mejor las estructuras irregulares o curvas. Aumentar la densidad de líneas mejora la resolución lateral, pero, al aumentar las tareas, disminuye la resolución temporal (Fig. 2).
La resolución temporal está relacionada con la cadencia de imagen, frame rate (FR): el número de imágenes por segundo o la velocidad con la que se actualizan las imágenes en la pantalla (14). Está limitada por la frecuencia y la profundidad del campo explorado (en campos profundos hay un retraso en la recogida de datos) y por la cantidad de información que manejemos a la vez. Para un estudio 2D no móvil (estudio abdominal) necesitamos FR de 15, pero en estudios de estructuras móviles (cardiológico o vascular) o niños necesitamos FR de 40. El ojo humano no detecta FR por encima de 40. En estudios complejos deberemos sacrificar alguna función (peor calidad de imagen, congelar imagen y color y actualizar alternativamente el Doppler pulsado y la imagen, disminuir el cajetín de color, trabajar con PRF bajos, etc.). En resumen, disminuir el “trabajo multitarea” (Tabla II).
Tabla II. Definiciones y manejo de la resolución espacial (axial y lateral), temporal y de contraste (1,3,14).
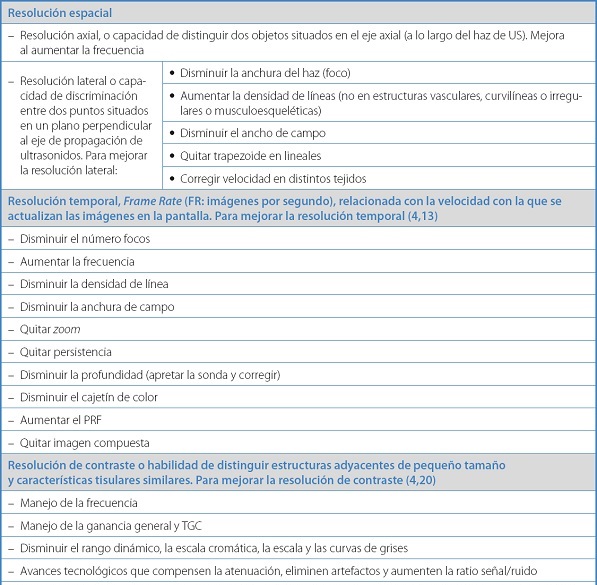
Según el estudio que realicemos debemos ajustar el compromiso entre todo lo anterior. En estudios de estructuras en movimiento (cardiológicos, etc.) tendremos que aumentar la FR, usar un solo foco, etc. En estudios de punciones vasculares, necesitamos una alta resolución espacial lateral y axial y una alta FR. En estudios de punciones para biopsia necesitamos todo: alta resolución espacial lateral y axial, alta resolución de contraste y alta FR.
La persistencia o superposición de imágenes, o frame average, es un allanado temporal (14) que disminuye las variaciones entre las sucesivas imágenes, promediando los fotogramas del modo B y Doppler color a medida que se muestran y ofreciendo una imagen más suave y con mejor definición del contorno. Mejora la resolución espacial (suprime el ruido, el moteado y los artefactos que pueden ser útiles en un diagnóstico), pero puede disminuir la resolución temporal. Si es necesario que un ecógrafo detecte un movimiento rápido (por ejemplo, el corazón o una aguja), es preciso disminuir la persistencia, aunque tengamos imágenes más moteadas.
Otros
- Ángulo de exploración, inclinación o steer (reflexión ortogonal). El principio básico de las técnicas ecográficas es: “Un transductor emite unos breves impulsos de ultrasonidos que se propagan por el cuerpo humano, lo que produce ecos que se reflejan hacia el transductor y se convierten en señal eléctrica y posteriormente en imagen, que aparece en un monitor”. Con el steer del modo B buscamos orientar el haz de ultrasonidos para que la estructura a estudio provoque una reflexión perpendicular y así genere una mejor imagen (8) (Fig. 4).
- Rango dinámico. A cada eco recibido se le asigna un valor de grises, que se muestra en el monitor con 256 gradaciones. Técnicamente podrían usarse valores mayores, pero el ojo humano solo distingue 50-60 gradaciones. El rango dinámico del modo B es el grado de compresión de la escala de grises o el número de tonos entre los valores máximos y mínimos. Si optamos por rangos altos tendremos más valores entre el negro y el blanco, lo que da lugar a una imagen suave. Si disminuimos el rango dinámico tendremos una imagen dura y muy contrastada, con mayor resolución de contraste. Por lo general se usan RD amplios en abdomen para estudios de partes blandas, medios en estructuras vasculares y bajos en cardíacos. Puede manejarse en vivo o en imagen congelada (14) (Fig. 5).
- Escala o mapa de grises. Similar pero no igual al rango dinámico. Mientras el rango dinámico define el número total de grises, el mapa de grises determina la intensidad o cómo de oscuro o claro es cada uno. Aumenta el contraste de las imágenes. Pueden ajustarse en vivo o con imagen congelada (15,16).
- Escala cromática. El ojo humano tiene mayor resolución con una visión en colores que en escala de grises, por eso podemos representar las imágenes en color según una escala policromática o monocromática. Esta función es altamente dependiente del explorador (15,16).
- Imagen panorámica. Para representar estructuras que superan la amplitud del campo, se fusionan imágenes que se obtienen moviendo la sonda a lo largo de la estructura (3).
No todos los ecos de retorno son útiles. Las imágenes se degradan por interferencias y artefactos que dan un aspecto moteado, lo que disminuye la resolución espacial y de contraste. Tres tecnologías han mejorado notablemente la calidad de la imagen de ultrasonidos (2):
Armónicos (THI: Tissue harmonic imaging, DTHI o Differential o inverted Tissue harmonic imaging) (17-19). Se basa en el fenómeno de la propagación no lineal de los ultrasonidos. Se generan endógenamente ecos de retorno con frecuencias múltiplos de la frecuencia fundamental. El equipo elimina la frecuencia fundamental del análisis con distintas técnicas. Frente al ultrasonido convencional que transmite y recibe ultrasonidos con igual ancho de frecuencia, el THI emite una frecuencia y recibe ecos que doblan la frecuencia de transmisión (segundo armónico), pero con menor intensidad. De esta manera identifica la señal de los tejidos y elimina artefactos, ecos débiles, etc., mejorando la resolución de contraste. Mejora la resolución lateral (al estrechar el haz y el grosor) y la penetrancia, lo que es especialmente útil en pacientes obesos, en quistes, estructuras hiperecoicas (calcio), con aire o con grasa. No ayuda en estudios muy superficiales. Puede disminuir la resolución axial, como la visualización de punta de aguja o calcificaciones, para lo que podemos volver al modo convencional.
Algoritmos, filtros y parámetros de suavizado, que en cada equipo se denominan de una manera: SRI (Speckle Reduction Imaging), uScan, XRES, etc. (2,20). Usan distintos filtros de manejo de la imagen para reducir el moteado o “grano” de la imagen. Identifican la señal fuerte y débil de cada pixel, separando la señal del tejido del ruido. Cualquier eco que parece erróneo se elimina a la vez que aumenta el brillo de la señal fuerte y se muestra una imagen más suave, limpia y real, pero perdiendo detalles de 1-2 mm y nitidez en los bordes. Es un posproceso que podemos ajustar en distintos niveles para mejorar la resolución de contraste. Disminuye la resolución temporal.
-
Imagen compuesta (2,21-23). Herramienta que combina el resultado de emitir haces de ultrasonidos, bien con distinta frecuencia (21) o con distintos ángulos de incidencia (entre ± 20° del perpendicular) (23), de forma simultánea. Las distintas imágenes o proyecciones (3-9) capturadas del mismo campo se combinan electrónicamente, dando una sola. En la segunda modalidad, o imagen compuesta espacial, solo se suman las regiones centrales, sobre todo en planos profundos.
Mejora la resolución de contraste (al ver el mismo tejido desde distintos “ángulos” eliminamos artefactos, sombras, etc.), con mejor caracterización de bordes, de estructura interna y microcalcificaciones (placa, úlcera y correlación histológica). Disminuye la sombra acústica y otros artefactos “útiles”, por lo que podemos pasar al modo convencional (24-29). Disminuye la resolución temporal (al aplicar frame average) En exploraciones con movimiento podemos elegir menos imágenes compuestas (cambiar de 7 a 3 imágenes) o cambiar a modo convencional. Aumenta la resolución espacial en vasos no perpendiculares (bifurcación carotidea), ya que tiene menor dependencia del ángulo ortogonal. Tiene mejor reproductibilidad.
CONCLUSIONES
Los botones del equipo de ecografía Doppler no dan calambre. Siempre hay un botón del pánico (suele ser el del modo B) para volver a los ajustes iniciales o la exploración puede reiniciarse si se desconfigura todo.
No desaprovechemos la información que se “oculta” a los lados de la pantalla. El código de color, las escalas, la ganancia, el rango, la frecuencia, etc.; todo está allí esperando nuestra interpretación.
Hay que recordar la importancia de la lista de verificación (checklist), del orden de la exploración y del guardado de los datos.
Debemos aplicar el principio ALARA valorando el riesgo-beneficio en todas las exploraciones. El uso prudente y justificado de cada exploración, el correcto entrenamiento técnico, etc., contribuyen a ahorrar tiempo de exploración y, por tanto, a disminuir los posibles efectos adversos.
Tras encender el equipo y añadir, si fuera preciso, los datos del paciente, empezaremos seleccionando la sonda y el preset en función del tipo de patología, del motivo del estudio y de las características del paciente. De forma automática, todos los equipos comienzan con el modo B o 2D. Los ajustes predeterminados y la preconfiguración (o preset) son un adecuado punto de partida, pero podemos mejorar la imagen afinando la profundidad, la ganancia general, la ganancia ajustada a la profundidad (TGC) y el foco. Para ajustes avanzados, se modificará el ángulo del modo B, el rango dinámico y los armónicos.
Aunque los equipos actuales son muy completos y potentes, la propia tecnología y el inmenso caudal de datos hacen que los recursos sean limitados. Por lo general, el principal pagador del uso abusivo de recursos es la resolución temporal, que se manifiesta en una imagen ralentizada o a saltos. Por ello debemos aplicar sistemas o trucos de ahorro.
Por último, no debemos olvidar que el fin último de la exploración es su utilidad en diagnóstico. Con las funciones del equipo haremos mediciones y cálculos, que archivaremos junto con las imágenes del estudio. Todo debe quedar reflejado en un correcto informe.
Entender la influencia de los ajustes del equipo para obtener una mejor exploración, conocer los fundamentos físicos de la técnica que evite errores y explique artefactos supone hacer un mejor diagnóstico y un mejor tratamiento con la ecografía Doppler.















