INTRODUCCIÓN
A pesar de la disminución de la mortalidad por ictus durante la última década, este sigue siendo la segunda causa principal de muerte en el mundo1-4. Aproximadamente, el 85% de los ictus son de origen isquémico y ocurren como consecuencia de una isquemia cerebral focal que resulta en un daño cerebral irreversible y los consiguientes déficits neurológicos5,6. Las causas más habituales son oclusión aterotrombótica de grandes arterias (la más frecuentemente afectada es la cerebral media y sus ramas, seguida por la basilar), embolia (el émbolo puede alojarse en cualquier zona del árbol vascular), oclusión no trombótica de pequeñas arterias (lo que se conoce como ictus lacunar, en algunas casos la causa podría ser embólica) y estenosis de arteria proximal. Además de estos grandes grupos, hay otras muchas causas de ictus como meningitis, vasculitis, trastornos de la coagulación, displasia fibromuscular y otros trastornos pocos comunes como moyamoya…
La restauración rápida del flujo sanguíneo es esencial para limitar la discapacidad en pacientes con ictus1,6.
El flujo sanguíneo insuficiente en una arteria cerebral puede compensarse en algunos casos con el sistema de colaterales. Esto depende de la localización de la lesión, daño previo en los vasos (ateroesclerosis), el calibre de los vasos, las variantes anatómicas, el tamaño de la lesión aguda, etc. Por ello existe variabilidad de sintomatología entre diferentes pacientes.
Algunas neuronas pueden morir cuando su perfusión habitual disminuye un 5% durante más de 5 minutos, aunque, como hemos comentado, el daño puede ser diverso, no debemos perder la perspectiva que el ictus es una patología tiempo dependiente. Otras áreas pueden persistir funcionales hasta 6 horas si el daño es leve y se mantiene un 40% de la perfusión. Son estas áreas, moderadamente isquémicas pero sin lesión irreversible, el objetivo de la intervención en un ictus. Estas zonas de penumbra se pueden recuperar si logramos restablecer el flujo.
Algunos mecanismos de daño isquémico importantes son el edema, la trombosis microvascular y la apoptosis inducida en dicho ambiente isquémico.
El único tratamiento farmacológico aprobado para restaurar el flujo sanguíneo es el activador del plasminógeno tisular (t-PA) intravenoso, que debe administrarse dentro de las 4 horas y media posteriores al inicio de los síntomas7-9. Desafortunadamente, el lapso de tiempo tan estrecho impide que un número considerable de pacientes con ictus isquémico agudo no logran recibir dicho tratamiento. Además, incluso con la administración de t-PA, solo el 15% de los pacientes tienen una recuperación completa y aproximadamente el 3% tienen hemorragia intracraneal fatal3,7,9.
La trombectomía endovascular es el estándar de atención para pacientes con ictus isquémico agudo secundario a la obstrucción de grandes vasos que se presentan dentro de las 24 horas posteriores al inicio de los síntomas10-12. Sin embargo, solo alrededor del 20% de los pacientes con ictus tienen oclusión de dichos vasos y brindarles tratamiento de manera oportuna es difícil, ya que el procedimiento solo se puede hacer en centros altamente especializados. Aunque los pacientes pueden recibir t-PA y luego ser transferidos a un centro de atención terciaria, identificar a los aptos para el traslado es un reto en hospitales sin acceso a técnicas terapéuticas, sin angio-TC o resonancia magnética (RM) previas a la trombectomía4,6. Gran parte de la bibliografía se centra en el manejo del código ictus en centros que disponen de la capacidad diagnóstica y terapéutica para discernir si el paciente es subsidiario de fibrinólisis o trombectomía, por ello nos parece interesante profundizar en el reto que supone para hospitales como el nuestro el manejo de esta patología.
Los ensayos de reperfusión endovascular crean oportunidades y desafíos para el tratamiento de pacientes con ictus de arterias proximales8,11. Los pacientes con el llamado ictus al despertar, que generalmente no se consideran aptos para la fibrinólisis debido al tiempo, pueden ser candidatos para este tratamiento si se identifica una oclusión proximal2,5,9.
Las imágenes multimodales pueden identificar a los pacientes que se beneficiarían de la reperfusión, a pesar de desconocer el inicio del cuadro. Dichas imágenes pueden eliminar ventanas de tiempo estrictas para la administración del tratamiento, pero el papel de las garantías en la selección de pacientes y su impacto en el resultado aún no se ha determinado.
Existe alguna evidencia de que la administración de t-PA junto con la trombectomía es más eficaz que solo trombectomía1,2,4,7,8,12. Por ello, la fibrinólisis sigue siendo un pilar del tratamiento del accidente cerebrovascular.
El objetivo principal de nuestro estudio es valorar si la realización de la trombectomía en un territorio tan disperso como el de la muestra reduce la mortalidad de forma significativa.
MATERIALES Y MÉTODOS
Diseño del estudio
Se trata de un estudio longitudinal, observacional y descriptivo. Este artículo se enfoca en el estudio de la trombectomía y la relación con los tiempos: hora de tomografía computarizada (TC), hora de llegada a urgencias, mortalidad a los 30 días estratificada por hospitales de la región y el cambio de NIHSS antes y después de la trombectomía. Se ha incluido también el estudio de la relación entre la puntuación del ASPECT (escala topográfica cuantitativa para valorar los cambios isquémicos en los estudios iniciales de TC craneal en pacientes con ictus isquémico agudo del territorio de la arteria cerebral media. Su puntuación va de 0 a 10) registrada y su relación con la mortalidad a 30 días.
Lugar de aplicación
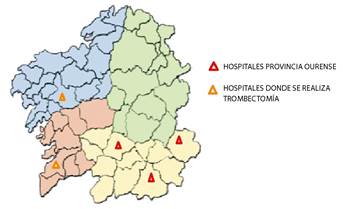
Hospitales pertenecientes a la provincia de Ourense incluidos dentro de la Consellería de Sanidade de la Xunta de Galicia, donde se reclutaron a los pacientes, así como los hospitales de referencia de la comunidad autónoma donde se realizaron las trombectomías (figura 1).
Muestra
De acuerdo con la literatura disponible, el perfil de incidencia del accidente cerebrovascular isquémico en España se encuentra entre 35 y 60 pacientes al año por cada 100.000 habitantes. Extrapolando esta estadística a la provincia de Ourense, podemos estimar un total de 185 pacientes que sufren ictus al año. Por consiguiente, podríamos estimar que, desde la implantación del protocolo de código ictus hasta la fecha de aplicación del análisis, unos 370 pacientes habrían sufrido un accidente cerebrovascular en la provincia de Ourense.
Para efectos del presente estudio se reclutaron pacientes que habían sufrido un ictus entre octubre de 2018 y marzo de 2020 -es decir, desde el mes de implantación del código ictus en la provincia hasta el inicio de la pandemia de la COVID-19- y que estuvieran registrados en el Área Sanitaria de la provincia de Ourense.
Los criterios de inclusión en el estudio son pacientes que presenten focalidad neurológica a su llegada a urgencias (tabla 1. Escala NIHSS. Escala que mide de forma numérica la gravedad del ictus. Puntuación de 0 a 42. Leve <4; moderado <16; grave <25; muy grave ≥25) y que cumplan criterios de inclusión en el código ictus:
Menos de 4 horas y media de evolución.
Personas mayores de edad (≥18 años).
Rankin previo ≤2 (tabla 2. Escala Rankin. Usada para medir el grado de dependencia para las actividades de la vida diaria de las personas que han sufrido un accidente cerebrovascular. Puntuación de 0 a 6).
Atención inicial en cualquier hospital de la provincia de Ourense.
NIHSS >4 y <25.
Tabla 1. Escala de ictus del National Institutes of Health (NIHSS).
| 1.a. Nivel de conciencia | Alerta | 0 |
| No alerta (mínimos estímulos verbales) | 1 | |
| No alerta (estímulos repetidos o dolorosos) | 2 | |
| Respuestas reflejas | 3 | |
| 1.b. Preguntas:
«¿En qué mes estamos?» «¿Qué edad tiene?» |
Ambas respuestas correctas | 0 |
| Una respuesta correcta (o disartria) | 1 | |
| Ninguna respuesta correcta (o afasia) | 2 | |
| 1.b. Órdenes motoras:
«Cierre los ojos» «Abra y cierre la mano» |
Ambas órdenes correctas | 0 |
| Una orden correcta | 1 | |
| Ninguna orden correcta | 2 | |
| 2. Mirada conjugada (horizontal) | Normal | 0 |
| Parálisis parcial de la mirada | 1 | |
| Desviación forzada de la mirada | 2 | |
| 3. Campo visual | Normal | 0 |
| Hemianopsia parcial | 1 | |
| Hemianopsia completa | 2 | |
| Ceguera | 3 | |
| 4. Paresia facial | Movilidad normal | 0 |
| Paresia menor | 1 | |
| Paresia parcial | 2 | |
| Parálisis completa de la hemicara | 3 | |
| 5. Miembro superior derecho / izquierdo | No caída del miembro | 0/0 |
| Caída en menos de 10 segundos | 1/1 | |
| Esfuerzo contra la gravedad | 2/2 | |
| Movimiento en el plano horizontal | 3/3 | |
| No movimiento | 4/4 | |
| 6. Miembro inferior derecho / izquierdo | No caída del miembro | 0/0 |
| Caída en menos de 5 segundos | 1/1 | |
| Esfuerzo contra la gravedad | 2/2 | |
| Movimiento en el plano horizontal | 3/3 | |
| No movimiento | 4/4 | |
| 7. Ataxia de miembros | Ausente | 0 |
| Presente en una extremidad | 1 | |
| Presente en 2 o más extremidades | 2 | |
| 8. Exploración sensitiva | Normal | 0 |
| Perdida de ligera a moderada | 1 | |
| Perdida de grave a total | 2 | |
| 9. Lenguaje | Normal | 0 |
| Afasia de ligera a moderada | 1 | |
| Afasia grave | 2 | |
| Afasia global | 3 | |
| 10. Disartria | Normal | 0 |
| Ligera a moderada | 1 | |
| De grave a anartria | 2 | |
| 11. Extinción a inatención (negligencia) | Normal | 0 |
| Extinción parcial | 1 | |
| Extinción completa | 2 | |
| Total (máximo 42) |
Tabla 2. Escala Rankin.
| NIVEL | GRADO DE INCAPACIDAD | |
|---|---|---|
| 0 | Asintomático | |
| 1 | Muy leve | Pueden realizar tareas y actividades habituales sin limitaciones |
| 2 | Leve | Incapacidad para realizar algunas actividades previas, pero pueden valerse por sí mismos sin necesidad de ayuda |
| 3 | Moderada | Requieren algo de ayuda, pero pueden caminar solos |
| 4 | Moderadamente grave | Dependientes para las actividades básicas de la vida diaria, pero sin necesidad de supervisión continuada (necesidades personales sin ayuda) |
| 5 | Grave | Totalmente dependientes. Requieren asistencia continuada |
| 6 | Muerte | |
ANÁLISIS ESTADÍSTICO
Variables
Las variables independientes incluidas en este estudio son: hospital al que acude el paciente inicialmente (Ourense, Verín, O Barco); hora de llegada al servicio de urgencias; hora de realización de la TC cerebral; NIHSS a su llegada a urgencias; NIHSS tras primera intervención; si se ha realizado o no la angio-TC cerebral posterior a la TC; escala ASPECT; arteria afectada (arteria cerebral media proximal [M1] y arterial cerebral media distal [M2], arteria comunicante interna [CI], tándem CI-M1). Las variables dependientes que se analizaron fueron la mortalidad a 30 días y el cambio de NIHSS (tablas 3 y 4).
Tabla 3. Mortalidad a los 30 días.
| INTERVENCIÓN REALIZADA | VIVO | EXITUS | TOTAL |
|---|---|---|---|
| Fibrinólisis | 64 (86,5%) | 10 (13,5%) | 74 |
| Trombectomía | 18 (81,8%) | 4 (18,2%) | 22 |
| Fibrinólisis + trombectomía | 34 (89,5%) | 4 (10,5%) | 38 |
| Total | 116 (86,6%) | 18 (13,4%) | 134 |
Tabla 4. Descripción de las variables edad, NISHH y ASPECT (media aritmética), así como de sexo, arteria afectada y tipo de ictus en porcentaje.
| VARIABLES | MEDIA ARITMÉTICA | PORCENTAJES (%) |
|---|---|---|
| Sexo | ||
| Mujeres | 26 | 65,00 |
| Hombres | 14 | 35,00 |
| ANGIO-TAC | ||
| Realizado | 37 | 92,50 |
| No realizado | 3 | 7,50 |
| Edad | 78,325 | |
| NIHSS | 15,65 | |
| ASPECT | 8,75 | |
| Arteria | ||
| M1 | 26 | 65,00 |
| M2 | 10 | 25,00 |
| CI | 2 | 5,00 |
| Tándem C1M1 | 0 | |
| ACM distal | 0 | |
| Fosa post | 1 | 2,50 |
| Otros | 1 | 2,50 |
| Tipo de ictus | ||
| Cardioembólico | 16 | 40,00 |
| Aterotrombótico | 7 | 17,50 |
| Indeterminado | 14 | 35,00 |
| Criptogénico | 2 | 5,00 |
| Lacunar | 1 | 2,50 |
ACM: arteria cerebral media; NIHSS: National Institutes of Health Stroke Scale; M1: arteria cerebral media proximal; M2: arteria cerebral media distal.
Se ha realizado estratificación por hospitales de la provincia: Ourense, Verín y O Barco.
Para el análisis descriptivo de las variables independientes, se calculó el rango intercuartílico y la mediana por sexo, edad y hospital. Para determinar el nivel de asociación entre las variables de trombectomía y mortalidad con las variables dependientes, se aplicó la prueba de hipótesis de chi-cuadrado de Pearson, regresión logística y estadística de Mann-Whitney (M-W), según el caso.
Partimos de un índice de confianza (IC) del 95% y de una distribución no normal de la muestra. El análisis estadístico fue llevado a cabo en programas informáticos especializados como IBM SPSS v 22 para Windows y R en su versión 4.0.1 para la realización del análisis de regresión logística.
Consideraciones éticas
El presente estudio se hizo siguiendo los principios de respeto hacia el paciente que se recogen en la Declaración de Helsinki, en el marco de la legislación vigente, como son la Ley 41/2002 Básica Reguladora de la Autonomía del Paciente y de Derechos y Obligaciones en Materia de Información y Documentación Clínica; Ley 3/2005 que modifica la Ley 3/2001 que regula el consentimiento informado y la historia clínica de los pacientes; los decretos 29/2009 y 164/2013, por los cuales se regula el uso y acceso a la historia clínica electrónica; el Convenio de Oviedo y la Ley 14/2007, de 3 de julio, relativa a la investigación biomédica.
También el Reglamento Europeo UE 2016-679, junto con la Ley Orgánica 3/2018, de 5 de diciembre, de Protección de Datos Personal y Garantía de Derechos Digitales, que incluye la obtención, tratamiento, conservación, comunicación y cesión de los datos. Este estudio ha sido aprobado por el Comité de Ética de Investigación Médica y Clínica de Pontevedra-Vigo-Ourense con el código 2019/635.
RESULTADOS
Se encontró que el tiempo entre la llegada al hospital y la realización de alguna intervención (trombectomía/fibrinólisis) fue de 218 minutos de media, con una desviación estándar (DE) de 124,65 minutos. En el estudio también se observó que, de los 153 pacientes totales, 20 (12,9%) fallecieron al cabo de 30 días del evento. En cuanto a la intervención, el 54,2% de los pacientes (84) fueron tratados con fibrinólisis, un 19,4% fueron sometidos a trombectomía y 38 pacientes (26,0%) recibieron terapia combinada (fibrinólisis + trombectomía). Cabe destacar además que 11 (13,1%) de los pacientes bajo fibrinólisis fueron exitus al cabo de 30 días; resultado no muy diferente si contamos la proporción de pacientes fallecidos en ese mismo período con trombectomía (13,3%). La proporción de fallecidos disminuía ligeramente (12,5%) en el caso de la intervención combinada.
Se descubrió que el 18,2% de los pacientes intervenidos con trombectomía en el caso del hospital de Ourense habían fallecido al cabo de 30 días. En el caso de Verín y O Barco, no se registraron fallecimientos con trombectomía.
Se registró una media de 4,97 puntos de variación de NIHSS antes y después de la intervención en toda la muestra. Con un máximo de 24 puntos y una desviación de 6,41 puntos. Se encontraron mejoras en la puntuación (NIHSS final < NIHSS inicial) en el 78,8% de los pacientes, seguido del 12,4% que había empeorado (NIHSS final < NIHSS inicial), y solo el 8,8% no reportó cambios en dicha puntuación (NIHSS final = NIHSS inicial).
Al analizar el cambio de NIHSS por paciente intervenido con trombectomía, se halló que solo el 5,9% de los pacientes que reportaron una mejoría (NIHSS final < NIHSS inicial) falleció al cabo de 30 días. En contraste con los 11 pacientes que habían reportado un empeoramiento en el NIHSS, 3 fallecieron a los 30 días (27,3%). También se descubrió que el 13,0% de los 131 pacientes que fueron sometidos a angio-TC fallecieron en los 30 días posteriores.
Al analizar los resultados relativos a arteria afectada, se encontró que la artería M1 se vio afectada en 71,6% de los pacientes sometidos a trombectomía. En el caso del tándem CI-M1, se obtuvo un 50% entre pacientes sometidos a trombectomía y fibrinólisis. El porcentaje más bajo se reportó en la arteria cerebral media distal (M2), con un 4,3% de pacientes sometidos a trombectomía.
La prueba de chi-cuadrado aplicada entre la mortalidad y el tipo de intervención (fibrinólisis/trombectomía) arrojó un valor p >0,05. Este resultado denota que la evidencia actual no es suficiente para determinar una relación entre la mortalidad del paciente a 30 días y el tipo de intervención al que se ha sometido.
Tomando en cuenta solo la trombectomía, tampoco encontramos relación con la mortalidad.
Los resultados sobre la relación entre tipo de intervención y la mortalidad a los 30 días estratificados por hospitales mostraron un resultado análogo a de la población total. En ninguno de los tres hospitales se observó una asociación importante entre la intervención y la mortalidad. Situación análoga se encontró al analizar la trombectomía por sí sola y la mortalidad en los hospitales más alejados. En contrapartida, el hospital de Ourense arrojó un p <0,05, evidenciando una relación importante en ese centro sanitario. No se encontró suficiente evidencia para el cambio de los valores de NIHSS y el tratamiento de trombectomía en todos los pacientes, ni tampoco con la mortalidad a 30 días (p >0,005).
La correlación entre la trombectomía y la mortalidad se analizó a través de una regresión logística. Este análisis arrojó un odd ratio de 0,979 con un IC del 95% oscilando entre 0,381 y 2,517. Se determinó que realizar una trombectomía disminuye la probabilidad de exitus, pero no presenta asociación estadística.
Hemos intentado en el estudio contrastar la relación entre la angio-TC, la intervención bajo trombectomía y la mortalidad al cabo de 30 días queda patente mediante un segundo análisis de regresión logística aplicada para ambas variables. Con un logaritmo de verosimilitud 118,921 y un odd ratio de 0,970 para trombectomía y 1,062 para angio-TC, se obtuvo un valor p >0,05 en ambos coeficientes.
DISCUSIÓN
En el metanálisis publicado por Katsanos y sus colaboradores4 en 2019 se encontró sobrada evidencia de que la trombectomía mecánica junto con el seguimiento médico reduce el riesgo de mortalidad a los 3 meses; no obstante, poco o casi nada se ha observado para la mortalidad a 30 días. La asociación señalada por Katsanos y sus colaboradores no parece estar gobernada por las características o los procedimientos de cada paciente, ni por su situación demográfica. Una afirmación análoga a la encontrada en el presente estudio, donde no se ha logrado evidencia significativa entre fibrinólisis, trombectomía y angio-TC con la mortalidad de los pacientes a los 30 días.
Para la reducción del riesgo y las tasas de mortalidad combinadas a 30 días, se señala que la trombectomía debería hacerse a los pacientes combinándola con otros tratamientos como la fibrinólisis, en aras de buscar reducir la mortalidad a los 3 meses. Se ha observado, además, que la trombectomía por sí sola suele asociarse con mejores resultados funcionales de la escala de Rankin, y, por lo tanto, la reducción de la mortalidad no parece estar asociada con una mayor probabilidad de discapacidad funcional a largo plazo13-17.
Nuestros resultados parecen estar en consonancia con el estudio a escala nacional estadounidense llevado a cabo por Villwock y sus colaboradores18 en 2016, donde se sugiere una disminución constante del riesgo de mortalidad en pacientes con ictus isquémico después de la introducción del tratamiento de trombectomía. Aunque en dicho estudio se informó acerca de numerosos parámetros clínicos y de procedimiento como posibles predictores del riesgo de mortalidad después de la intervención, en nuestro caso no se encontraron efectos moderadores en ninguno de los modelos de regresión logística aplicados. La oclusión de los vasos proximales, las puntuaciones altas en la escala NIHSS y la necesidad de terapia parecen ser los únicos predictores independientes de mortalidad, aumentando así el riesgo de reperfusión.
Debemos reconocer varias limitaciones en nuestro estudio. Primero, debe enfatizarse que solo hemos analizado la mortalidad a 30 días, lo que dificulta proporcionar una estimación del impacto acumulativo de alguna intervención (fibrinólisis/trombectomía) en la mortalidad por todas las causas en diferentes contextos. En segundo lugar, debe reconocerse que no se incluyeron más variables predictoras en las ecuaciones de regresión logística. De tal manera que, haciendo una comparativa con los logaritmos de verosimilitud, se podría observar cuál sería un modelo explicativo que mejor se ajustara a la probabilidad de exitus en los pacientes al cabo de 30 días.
El hospital de Ourense arrojó un p <0,05 en mortalidad, evidenciando una relación importante en ese centro sanitario con respecto a la mortalidad, estando este centro más cerca de los hospitales de referencia para trombectomía.
Numerosos ensayos y metanálisis han demostrado el impacto en las tasas de resultado funcional después de un ictus en pacientes tratados con trombectomía; sin embargo, ninguno ha demostrado una reducción de la mortalidad después de esta. Estos datos demuestran que hay una reducción significativa de la mortalidad. Estos hallazgos tienen implicaciones para los médicos, los pagadores de servicios de salud y los reguladores que determinan la rentabilidad de los procedimientos.
En sucesivos estudios, debería analizarse la necesidad de trombectomía en pacientes sometidos a fibrinólisis con respecto a la mortalidad para reducir los costes de traslado a hospitales de referencia y mejorar los tiempos de atención.