Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Nutrición Hospitalaria
versión On-line ISSN 1699-5198versión impresa ISSN 0212-1611
Nutr. Hosp. vol.29 no.4 Madrid abr. 2014
https://dx.doi.org/10.3305/nh.2014.29.4.7196
Hiperuricemia y gota: el papel de la dieta
Hyperuricemia ang gout: the role of diet
Bonifacio Álvarez-Lario y J. L. Alonso-Valdivielso
Sección de Reumatología. Hospital Universitario de Burgos. España.
Dirección para correspondencia
RESUMEN
Desde la antigüedad se ha relacionado a la gota con los excesos en el comer y en el beber; sin embargo, ha sido en la última década cuando se ha llegado a un mayor conocimiento sobre los factores dietéticos asociados con el desarrollo de hiperuricemia y gota. La obesidad, el abuso en la ingesta de carnes y las bebidas alcohólicas ya eran vistos como culpables desde la antigüedad. Las legumbres y las verduras ricas en purinas han sido exculpadas tras los estudios. Se han descrito nuevos factores de riesgo, no reconocidos anteriormente, como la fructosa y las bebidas edulcoradas. Finalmente, también se han descrito factores protectores, como los lácteos desnatados. La gota se caracteriza no sólo por el aumento del ácido úrico, eventuales episodios de artritis y el daño crónico articular, sino también por su asociación con diversas comorbilidades y con el aumento del riesgo cardiovascular. La adopción de hábitos dietéticos más sanos puede contribuir a un mejor control de la uricemia y también a una reducción de las enfermedades asociadas. Se recogen las recomendaciones prácticas más habituales según los conocimientos actuales y siguiendo los consejos de las principales guías de tratamiento. Son necesarios más estudios sobre la eficacia real en la práctica clínica de la adopción de unas y otras medidas dietéticas en el tratamiento y evolución de los pacientes con hiperuricemia y gota.
Palabras clave: Dieta. Ácido úrico. Hiperuricemia. Gota. Comorbilidades.
ABSTRACT
From ancient times, gout has been related with excessive eating and drinking; however, it has not been until the last decade that a broader knowledge on dietary factors associated with hyperuricemia and gout has been achieved. Obesity, excessive intake of red meats and alcoholic beverages were already recognized as causal factors from Antiquity. Legumes and purine rich vegetables have been exculpated after the studies. New risk factors, not previously recognized, have been described such as fructose and sweetened beverages. Finally, protective factors have also been described, such as skimmed dairy products. Gout is characterized not only by an increase in uric acid, eventual episodes of arthritis, and chronic joint damage, but also by association with several comorbidities and increased cardiovascular risk. The adoption of more healthier dietary habits may contribute to better management of uricemia and also to a reduction of associated diseases. The most common practice recommendations according to current knowledge and the main treatment guidelines are reviewed. Additional studies are needed on the actual efficacy in clinical practice of the adoption of specific dietary measures on the management and clinical course of patients with hyperuricemia and gout.
Key words: Diet. Uric acid. Hyperuricemia. Gout. Comorbidities.
Introducción
La gota es una enfermedad articular conocida desde la antigüedad y, ya desde entonces, relacionada con los excesos con la comida y con las bebidas alcohólicas1. Sin embargo, la asociación entre el ácido úrico (AU) y la gota no se comprobó hasta 1848, cuando Alfred B Garrod demostró la existencia de una mayor concentración de AU en la sangre de los pacientes gotosos. Por sencillez y uniformidad, el término "ácido úrico" es usado en este artículo como sinónimo de "urato", ya que a un pH fisiológico el 99% de las moléculas están en forma de urato (sólo en algunas zonas del sistema urinario donde el pH es menor de 5.7 la mayor parte de las moléculas están como AU). Los niveles séricos de AU vienen determinados por el balance entre sus tasas de producción y eliminación. Aproximadamente, dos terceras partes de la carga diaria de purinas es generada endógenamente, a partir de la degradación celular; el tercio restante deriva de la dieta2. La mayoría (70 %) del AU producido diariamente es excretada por el riñón; el resto es eliminado en el tracto biliar y después convertido en alantoína por la uricasa de las bacterias del colon. Así, una disminución de la eliminación de AU y/o un aumento en su producción pueden causar hiperuricemia. En la práctica clínica, la causa del 90 % de los casos de hiperuricemia es un defecto en la eliminación renal3. La hiperuricemia es un paso clave inicial en la etiopatogenia de la gota, aumentando drásticamente el riesgo de padecer gota a medida que lo hace la uricemia4,5. Pese a los notables avances de las últimas décadas en el conocimiento de la gota, a la mejora en su diagnóstico y a la existencia de fármacos hipouricemiantes muy eficaces6, los estudios indican que las prevalencias de la hiperuricemia y de la gota están aumentando en la sociedades desarrolladas7-12.
Algunos procesos evolutivos, como la pérdida de actividad de la uricasa y la gran reabsorción tubular renal de urato en los humanos, hacen que los niveles de AU sean mucho mayores en los humanos, y otros primates superiores, que en los demás mamíferos13 y que, además, los humanos seamos muy sensibles a otros factores que pueden incrementar los niveles de urato, como los cambios en la dieta1. A los procesos evolutivos referidos sólo se les puede atribuir un incremento del AU desde menos de 1 mg/dl hasta 2-3 mg/dl14, que son las cifras de uricemia que presentan otros primates superiores o humanos de pueblos indígenas cuya dieta se compone fundamentalmente de frutas y verduras1,15. El notable incremento de los niveles séricos de AU en los humanos de los países desarrollados se atribuye a los cambios en el estilo de vida y, fundamentalmente, en la dieta, más acusados en el último siglo1,14,16. Aunque la dieta sólo representa un tercio de la carga diaria de purinas y la mayoría de hiperuri-cemias son debidas a un defecto en la excreción renal de AU, algunos alimentos favorecen el incremento de AU por el propio aporte exógeno de purinas, otros aumentando la síntesis endógena de purinas y otros alterando la excreción renal de AU, como se verá posteriormente.
Además de los factores dietéticos, otros factores influyen en el aumento del AU en los individuos de las sociedades desarrolladas: la mayor longevidad, el uso de algunas medicaciones -en especial, diuréticos y bajas dosis de aspirina- y el incremento de ciertas condiciones relacionadas con un aumento del AU y del riesgo de gota, como la enfermedad renal crónica o el síndrome metabólico7,17,18. Finalmente, ciertas alteraciones genéticas de la regulación de la síntesis y/o la excreción renal de AU son también importantes en el desarrollo de hiperuricemia y gota; estos factores podrían explicar algunas asociaciones familiares o raciales con el riesgo de padecer gota1,19.
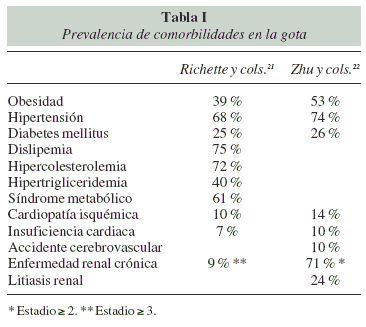
Por otra parte, la hiperuricemia y la gota se asocian con otras enfermedades, como litiasis renal, hipertensión, enfermedad renal crónica, diabetes mellitus, hiperlipidemia, obesidad, síndrome metabólico y aumento del riesgo cardiovascular13,20,22 (tabla I), enfermedades todas ellas susceptibles de mejora con medidas higiénico-dietéticas, lo que ha llevado a la realización de algunos cambios en los consejos dietéticos, no sólo dirigidos a disminuir la uricemia, sino también a mejorar el riesgo cardiovascular y la salud general del paciente23. En este trabajo se revisan los conocimientos actuales sobre la relación de los hábitos dietéticos con la hiperuricemia y la gota.
Factores dietéticos relacionados con la hiperuricemia y gota
Aunque desde la antigüedad se ha asociado la gota con los excesos en el comer y en el beber, sólo recientemente se han puesto de manifiesto los factores dietéticos que se asocian con hiperuricemia y gota.
Alimentos ricos en purinas. Carnes, pescados y legumbres
Entre los alimentos ricos en purinas se encuentran todas las carnes -incluyendo visceras y extractos cárnicos-, todos los pescados -incluyendo los mariscos- y algunos vegetales, como legumbres, espinacas, espárragos, setas y extractos de levadura. Por el contrario, son bajos en purinas los productos lácteos (leche, queso, yogur, helados), huevos, cereales y sus productos (pan, pasta, cereales), verduras (lechuga, tomates y otras verduras, salvo las referidas previamente), frutas, nueces, azúcar y dulces24.
La sospecha de la existencia de una asociación entre dietas ricas en purinas y gota se ha basado en experimentos animales y humanos que examinaron el efecto sobre los niveles de AU de sobrecargas artificiales a corto plazo de purinas purificadas25,26. En estudios con dietas de la vida real, Choi y cols, demostraron que los consumos mayores de carnes y pescados se asociaban con niveles más altos de AU27. y un mayor riesgo de gota28. Entre las carnes, sólo la ingesta de vacuno, cerdo o cordero se asociaba con un mayor riesgo de gota, no asi el consumo de aves de corral27. Cada ración diaria adicional de carne se asociaba con un incremento del 21% del riesgo de gota, mientras que cada ración semanal de pescado se asociaba con un aumento del 7% del riesgo28.
La causa del aumento del riesgo relacionado con las carnes y pescados es multifactorial (tabla II). Por un lado, se ha demostrado el efecto de una sobrecarga de purinas exógenas de origen animal sobre el aumento del AU29; por otra parte, las carnes rojas son la principal fuente de grasas saturadas, que se asocian con una reducción de la excreción renal de urato29.
Algunas verduras crudas, como las espinacas, tienen mayor concentración de purinas que un filete de carne cruda (70 mg/100 g frente a 58 mg/100 g)26; sin embargo, se ha observado que el consumo de verduras y legumbres ricas en purinas no aumentan el riesgo de gota 16,28. Tampoco una mayor ingesta de proteínas, en general, aumenta el riesgo de hiperuricemia y gota 17,27,28,30. Las diferencias en el riesgo de padecer hiperuricemia y gota entre los diferentes alimentos ricos en purinas podrían explicarse por diversos factores, como la variación en las cantidades ingeridas, el tipo de purinas, el hecho de que estén cocinadas o no y la diferente biodisponibilidad para la transformación de purinas a AU28. Por otra parte, los glicósidos flavonoides presentes en las legumbres tienen efecto inhibidor de la xantino oxidasa 31. Finalmente, las dietas altas en proteínas se asocian con disminución del AU y del riesgo de gota ya que producen un aumento de la excreción urinaria de AU 27,28,30.
Alcohol
La incidencia exacta de la artritis gotosa relacionada con el consumo de alcohol no se conoce, pero se estima que la mitad de los gotosos beben en exceso19. Diversos estudios han demostrado que el consumo de alcohol, tanto en hombres como en mujeres, se asocia con niveles más altos de uricemia32,33 y gota5,34,35. Así, el riesgo de desarrollar gota es 2,5 veces mayor entre los hombres que consumen 50 gramos o más de alcohol al día, comparados con los que no beben alcohol32. La magnitud de la asociación aumenta con el incremento en la ingesta de alcohol y varía según el tipo de bebida alcohólica. Dos o más cervezas al día confieren un mayor riesgo de gota (RR 2,51, IC del 95%, 1,77-3,55) que dos o más copas de licor al día (RR 1,60, IC del 95%, 1,19-2,16). El consumo moderado de vino (2 copas al día) no parece aumentar el riesgo de gota (RR 1,05, IC del 95%, 0,64-1,72)32. Por tanto, el riesgo de desarrollar gota depende del tipo y cantidad de la bebida alcohólica consumida, atribuyéndose a la cerveza el riesgo más alto. Además, el riesgo es mayor en las mujeres que en los hombres. En un estudio basado en los datos del Framingham Heart Study, el consumo elevado de cerveza se asoció con un riesgo relativo de gota de 7,10 (IC del 95%, 1,70-29,62) en las mujeres y de 2,00 (IC del 95%, 1,26-3,19) en los hombres, mientras que el consumo moderado-alto de vino se asociaba con un riesgo relativo de 1,46 (IC del 95%, 0,80-2,65) en las mujeres y de 1,24 (IC del 95%, 0,84-1,84) en los hombres5.
El alcohol ocasiona hiperuricemia por varios mecanismos (tabla II). Durante el consumo excesivo y agudo de alcohol, éste es convertido en ácido láctico, que reduce la excreción renal de AU inhibiendo competitivamente la secreción de AU por el túbulo proximal. El consumo crónico de alcohol incrementa la producción de purinas y de AU, acelerando la degradación de adenosina trifosfato (ATP) a adenosina monofosfato, un precursor de AU33. Los mayores efectos hiperuricémicos de la cerveza, en comparación con otras bebidas alcohólicas, se atribuyen a su gran contenido en purinas, predominantemente guanosina.
Fructosa y bebidas edulcoradas
El consumo de refrescos edulcorados, incluyendo refrescos de cola y otras bebidas gaseosas edulcoradas, conlleva incrementos significativos en las tasas de incidencia de hiperuricemia16,36 y de gota37. El riesgo de incidencia de gota se multiplica aproximadamente por dos entre los hombres y mujeres que consumen dos o más bebidas gaseosas edulcoradas al día, comparados con los que toman menos de una bebida al mes37,38 y se multiplica hasta por 6 en los que consumen cuatro bebidas edulcoradas cada día frente a los no consumidores, existiendo diferencias entre grupos raciales39. La odds ratio de desarrollar gota para los que tomaban cuatro o más bebidas azucaradas al día frente a cero fue de 6,89 (IC del 95%, 1,05-45,44), 5,19 (IC del 95%, 1,4818,17) y 2,84 (IC del 95%, 1,04-7,77), para europeos caucásicos, maoríes y oriundos de las islas del Pacífico respectivamente, estando influenciado el incremento del AU por polimorfismos del gen SLC2A939. Por el contrario, el consumo de bebidas bajas en calorías (colas bajas en calorías con cafeína o sin cafeína, otras bebidas bajas en calorías y bebidas light"), no parece asociarse con un aumento del riesgo de gota37.
Aunque las bebidas edulcoradas contienen bajos niveles de purinas, tienen grandes cantidades de fructosa. La fructosa es el único hidrato de carbono que se ha demostrado que ejerce un efecto directo sobre el metabolismo del AU. La fosforilación de la fructosa consume ATP, con depleción de ATP hepática y liberación de adenina, que finalmente se transforma en AU12,30,37. Además, la fructosa podría aumentar indirectamente los niveles de AU y el riesgo de gota incrementando la resistencia a la insulina y los niveles de insulina circulante, que reduce la excreción renal de AU37 (tabla II). Otros estudios, por el contrario, no avalan esta relación entre el consumo de fructosa y el aumento de los niveles de AU. Así, una revisión sistemática y metaanálisis reciente concluye que sólo la ingesta muy elevada de fructosa, en el contexto de dietas hipercalóricas, aumentan los niveles de AU, lo que no ocurre con ingestas isocalóricas de fructosa40. Por ello, es difícil determinar si el aumento de AU en relación con las bebidas edulcoradas se debe a la fructosa sola o a algún otro componente de las bebidas, o bien a que la fructosa pudiera tener efectos adversos sólo en dosis elevadas16. Alternativamente, el consumo de bebidas edulcoradas podría ser más bien un marcador de una dieta y estilo de vida poco saludables16.
La ingesta de otras fuentes de fructosa, como los zumos de frutas o las frutas ricas en fructosa, también se asocia significativamente con un mayor riesgo de gota37. Los hombres que consumen más de 2 vasos de zumo de frutas al día, comparados con los que consumen menos de un vaso al mes, tienen un riesgo relativo de gota de 1,81 (IC del 95%, 1,12-2,93). Datos similares se observan en relación con la ingesta de manzanas o naranjas: comparados con los que consumen menos de una manzana al mes, los que consumen una cada día tienen un riesgo relativo de 1,55 (IC del 95%, 1,02-2,36)37.
Lácteos desnatados
El consumo de lácteos, en especial lácteos desnatados, se asocia inversamente con los niveles de uricemia16,27. Quienes consumen leche una o más veces al día tienen unos niveles de AU más bajos que los que no consumen leche. Igualmente, los que comen yogur al menos cada dos días tienen también niveles más bajos que los que no consumen yogur27. Del mismo modo, en un ensayo clínico randomizado de 4 semanas de duración se observó un incremento en los niveles de AU con una dieta sin lácteos41.
Igualmente, se ha observado que una mayor ingesta de productos lácteos desnatados reducía el riesgo de padecer gota28. Así, el riesgo relativo de desarrollar gota de aquellos que beben 2 o más vasos de leche desnatada al día, comparado con el de quienes beben menos de un vaso al mes, es de 0,54 (IC del 95%, 0,40-0,73).
La leche contiene factores uricosúricos, como el ácido orótico. El transportador renal URAT1 transporta orotato, además de urato, lo que sugiere que la competencia entre ellos por el URAT1 puede originar uricosuria tras la ingesta de lácteos42. Además, tanto la lactosa como la galactosa activan el hUAT, otro transportador renal de urato43. Los lácteos tienen, asimismo, elevadas cantidades de calcio, que en algunos estudios se ha asociado con disminución del AU16, aunque en otro estudio se observó que la adición de suplementos de calcio no afectaba a los niveles de AU44. Por otra parte, Dalbeth y cols. demostraron que tanto la fracción lipídica como la proteica de los productos lácteos modulan las respuesta inflamatoria a los cristales de urato monosódico en modelos animales45, por lo que los lácteos podrían tener acciones semejantes a la colchicina43.
Verduras
Hay evidencias en sujetos sanos de que el consumo de verduras se asocia con menores niveles séricos de AU y menor riesgo de urolitiasis17,46. El consumo de verduras y alimentos ricos en fibra disminuye el riesgo de gota47. Las dietas ricas en verduras podrían actuar favoreciendo la eliminación renal de AU48.
Vitamina C
Una mayor ingesta de vitamina C se asocia a un menor riesgo de hiperuricemia y gota47,49,50. Dosis de 500 mg/día o mayores se asocian en algunos estudios con un menor riesgo de gota51. Sin embargo, un estudio reciente encuentra que la administración de 500 mg/día de vitamina C a pacientes gotosos tiene un efecto clínicamente insignificante sobre los niveles de AU52. La vitamina C, probablemente, modula las concentraciones séricas de AU por sus efectos uricosúricos50.
Café
Dos grandes estudios sugieren una relación inversa entre el consumo de 4 o más cafés al día y la uricemia. Este efecto beneficioso del café no parece ser debido a la cafeína, ya que se mantiene en el café descafeinado y no está presente en otras bebidas con cafeína, como el té o las colas53,54.
Fibra
Una mayor ingesta de fibra se asocia a niveles séricos significativamente más bajos de AU y reducción del riesgo de hiperuricemia33 y gota47. Este efecto podría deberse a la inhibición de la absorción de adenina o purinas en el aparato digestivo por la fibra de la dieta33.
Cerezas
El consumo de cerezas y extractos de cerezas se asocia con uricemias más bajas y con una disminución de los ataques de gota55,56. La ingesta de cerezas durante un período de dos días se asocia con una reducción del riesgo de gota del 35% y la de extractos de cerezas con una reducción del 45%. Estos efectos podrían deberse a un aumento de la excreción renal de urato y a cierta acción antiinflamatoria55.
Ácido úrico y patrones dietéticos
Además de la influencia de diversos alimentos o nutrientes, varios estudios han evaluado la influencia sobre los niveles de AU y gota de diferentes patrones dietéticos o dietas generales, con múltiples nutrientes.
Dietas bajas en purinas
Desde que se conoció que, en los humanos, el AU es el producto final de las purinas, la restricción de éstas en la dieta ha constituido el tratamiento dietético clásico de la hiperuricemia y gota. En estudios a corto plazo se demostró que dietas estrictas bajas en purinas logran reducir los niveles séricos de AU en una media de 1-2 mg/dl7,19,26,57. Sin embargo, estas dietas muy bajas en purinas están prácticamente olvidadas y no se consideran recomendables por varios motivos. Por un lado, estos estudios estaban basados en dietas experimentales, realizadas durante unos pocos días, siendo difícil su seguimiento a largo plazo para la mayoría de la gente. Por otra parte, como ya se ha indicado, las verduras y legumbres con altos contenidos en purinas y las dietas ricas en proteínas no se relacionan con el desarrollo de hiperuricemia y gota; al contrario, una mayor ingesta de proteínas parece disminuir su riesgo. Finalmente, estas dietas probablemente no sean sanas debido al incremento que conllevan en la ingesta de hidratos de carbono y grasas, que podrían empeorar la evolución de otras enfermedades relacionadas con la hiperuricemia y la gota.
Dietas de adelgazamiento
Más del 60% de los pacientes con gota padecen síndrome metabólico y un porcentaje similar obesidad21,22,29. Los adultos con sobrepeso y con obesidad tienen una mayor probabilidad de tener hiperuricemia que aquellos con un índice de masa corporal (IMC) normal19,33,58. En concreto, en el estudio Coronary Artery Risk Development in Young Adults se observó que el sobrepeso multiplicaba entre 3 y 9 veces la probabilidad de hiperuricemia, siendo el riesgo más acusado en las mujeres58. Otro tanto ocurre con el sobrepeso y la obesidad y el riesgo de gota5,17.
Zhu y cols, en un estudio sobre 12.379 varones con alto riesgo cardiovascular del Multiple Risk Factor Intervention Trial, seguidos durante 7 años, observaron la existencia de una relación gradual entre la pérdida de peso y la consecución de la normouricemia59. Al inicio del estudio, el 70% de los participantes tenían un AU sérico superior a 6 mg/dl y el 38% mayor de 7 mg/dl. El 74% de los participantes redujeron su peso durante los 7 años de seguimiento. Comparados con los que no habían cambiado de peso, las odds ratio de alcanzar la normouricemia para una pérdida de peso de entre 1-4,9 kg, 5-9,9 kg y más de 10 kg, fueron 1,43 (IC del 95%, 1,33-1,54), 2,17 (1,95-2,40) y 3,90 (3,31-4,61), respectivamente. La pérdida de peso mayor de 10 kg aumentaba casi 4 veces la probabilidad de conseguir un nivel sérico de AU de 6 mg/dl. En conjunto, la pérdida de 1 kg de peso se asociaba con un aumento del 11% en la probabilidad de conseguir el objetivo terapéutico. Estas asociaciones se mantenían independientemente de que los pacientes padecieran o no gota59. Igualmente, los datos obtenidos a partir del Health Professionals Follow-up Study subrayan la relación entre control del peso y gota60. En total, 47.150 hombres sin historia de gota, de edad entre 40 y 75 años, entraron en el estudio y fueron seguidos durante 12 años. En este tiempo, 730 pacientes desarrollaron gota, incrementándose el riesgo con el aumento del índice de masa corporal (IMC); por el contrario, los que habían reducido su peso también redujeron el riesgo de gota. Cuando se compararon los que habían mantenido su peso corporal con los que lo habían disminuido al menos 4,5 kg desde la entrada en el estudio, se observó que en éstos se redujo significativamente el riesgo relativo de desarrollar gota a 0,61 (IC del 95%, 0,40-0,92)60.
La eficacia del adelgazamiento también se ha puesto de manifiesto en estudios a corto plazo. Dessein y cols61 consiguieron en pacientes gotosos, sólo con la reducción de peso mediante una dieta moderadamente hipocalórica (1.600 kcal/día durante 16 semanas), con restricción de carbohidratos y aumento proporcional de proteínas y grasas no saturadas (nueces, aceites y pescados), una pérdida de peso media de 7,7 kg (rango 0-21), una disminución media del AU del 18% (de una media basal de 9,65 mg/dl a 7,83 mg/dl al final del estudio) y una disminución de los ataques de gota del 67%. Casi el 60% de los pacientes alcanzó el objetivo terapéutico (nivel sérico de AU de 6 mg/dl). Además, el 85% tenían un riesgo aterosclerótico elevado al inicio, frente al 23% al final del estudio. Otros estudios también han observado que dietas hipocalóricas en pacientes con sobrepeso y obesidad ayudan a mejorar los parámetros clínicos y analíticos de riesgo cardiovascular, además de mejorar los niveles séricos de AU62,63.
El efecto hipouricemiante del adelgazamiento depende del grado de la pérdida de peso59 y de la uricemia inicial. Así, en grupos de pacientes con sobrepeso y uricemia inicial media inferior a 7 mg/dl59,62, los descensos en los niveles séricos de AU son poco significativos clínicamente (adelgazamientos de hasta 5 kg consiguen reducciones de la uricemia menores de 0,2 mg/dl, y pérdidas de más de 10 kg consiguen descensos medios de sólo 0,6 mg/dl). Sin embargo, los efectos del adelgazamiento en pacientes con hiperuricemia y gota parecen ser muy superiores, con descensos en la uricemia de casi 2 mg/dl para una pérdida de peso de 7,7 kg61. Aunque el efecto hipouricemiante de la pérdida de peso es más débil que el de los fármacos, sus otros beneficios para la salud constituyen un valor añadido, lo que ha llevado a algunos autores a pensar que la hiperuricemia asociada a la obesidad podría ser tratada adecuadamente sólo con dieta en un buen número de casos64.
Finalmente, la eficacia del adelgazamiento en el tratamiento de la gota se hace patente a partir de algunos datos históricos, como la práctica desaparición de la gota en las épocas de penuria y hambre, como ocurrió en Alemania después de la Segunda Guerra Mundial26.
La obesidad podría aumentar la uricemia mediante el incremento del aporte exógeno, el aumento de la producción endógena de purinas y, sobre todo, por una disminución de la excreción renal de urato7 (tabla II). El incremento en los niveles de insulina asociado con la obesidad probablemente sea la causa principal de hiperuricemia en la obesidad y síndrome metabólico, ya que unos niveles más altos de insulina reducen la excreción renal de urato, como ya se ha indicado5. Además, el aumento de lactato en la obesidad acelera la reabsorción renal de urato y, por otra parte, la síntesis de ácidos grasos acelera la purinosíntesis de novo3.
Dieta mediterránea
En dos artículos recientes se observó que una mayor adherencia a la dieta mediterránea se asociaba con unos niveles séricos más bajos de AU y una menor probabilidad de hiperuricemia65,66. Además, la dieta mediterránea revertía la hiperuricemia, después de un seguimiento medio de 5 años, en el 43,8% de los individuos, siendo mayor la reversión en aquellos con mayor adherencia a la dieta66. Además de los efectos observados sobre la uricemia, una mayor adherencia a la dieta mediterránea se ha asociado con una reducción significativa de la prevalencia de síndrome metabólico67 y de enfermedad cardiovascular, así como de la mortalidad68-70. Igualmente, la dieta mediterránea ha demostrado su eficacia en la reducción de peso70, en especial cuando se asocia a restricción de calorías, actividad física y duración mayor de 6 meses71.
Dietas ricas en frutas, verduras y lácteos desnatados
Se ha observado que el pH urinario es más ácido con una dieta abundante en proteínas animales comparada con una dieta básicamente vegetariana (pH de 5,9 frente a 6,5), lo que dificultaría la excreción renal de AU48. Con modificaciones dietéticas de este tipo, con más proteínas de origen vegetal y menos de origen animal, se puede conseguir una mayor eliminación renal de urato48. Un aumento de la ingesta de frutas, verduras y lácteos desnatados es uno de los principales componentes del Dietary Approaches to Stop Hypertension (DASH diet). Estas dietas pueden reducir no sólo la presión arterial, sino también la incidencia de hiperuricemia y gota1. En un estudio reciente que comparaba diversos patrones dietéticos, los participantes con un mayor consumo de frutas y verduras tendían a tener menores niveles de AU que aquellos con patrones de alimentación teóricamente más propensos a elevar el AU, aunque no se encontraron diferencias significativas después de ajustar para factores de confusión adicionales72. Sin embargo, en otro trabajo, cuando se compararon individuos comedores de carne, comedores de pescado, vegetarianos y seguidores de una dieta vegana se observó que los niveles más altos de AU correspondían a la dieta vegana, seguidos de los comedores de carne, siendo los niveles más bajos en los vegetarianos73. Esta mayor concentración de AU en los consumidores de una dieta vegana es atribuida por los autores a la ausencia de productos lácteos y a la baja ingesta de calcio propios de la dieta vegana.
Transgresiones agudas: atracones y banquetes
Además de los efectos sobre los niveles de AU y gota de factores dietéticos a largo plazo, es conocido el efecto desencadenante de episodios de gota de los abusos puntuales en la comida y la bebida, debido a las fluctuaciones agudas en los niveles séricos de AU12. Sirva como ejemplo el experimento Rodnan, en el que siete pacientes gotosos fueron hospitalizados en el Clinical Research Center en la Universidad de Pittsburgh, donde fueron estabilizados con una dieta baja en purinas. Se les proporcionó entonces una cena festín con abundancia de carnes, lo que se tradujo en un incremento en los niveles séricos de AU entre 1,3 y 3,3 mg/dl. Cuando al mismo grupo, además del banquete abundante en carnes, se les proporcionó cantidades generosas de alcohol (83-198 g de etanol) los niveles séricos de urato se incrementaron aún más, entre 2,0 y 6,1 mg/dl. Seis de los siete pacientes desarrollaron ataques de gota, cuatro de ellos tras la fiesta que incluía alcohol12,74. Parece claro que una buena medida terapéutica en los pacientes gotosos es evitar los atracones o ingestas excesivas de comida y bebidas alcohólicas.
Recomendaciones dietéticas y de estilo de vida en hiperuricemia y gota
Aunque el hecho cardinal de la gota es la artritis, la gota es una enfermedad metabólica asociada a elevados niveles de AU. La hiperuricemia y la gota se asocian, como ya se ha dicho, con diversas entidades metabólicas y vasculares, incluyendo obesidad, hipertensión arterial, dislipemia, resistencia a la insulina, diabetes mellitus, litiasis renal, insuficiencia renal, arteriosclerosis y enfermedades cardiovasculares7,13,17,21,22. Estas comorbilidades de la gota y su asociación independiente con el riesgo de padecer enfermedad cardiovascular en el futuro, nos obligan a no conformarnos únicamente con un tratamiento adecuado de la gota, sino también a promover decididamente la adopción de hábitos dietéticos y estilos de vida más sanos, en especial en relación con la reducción del riesgo cardiovascular29. Al respecto, solo existen unas pequeñas potenciales contradicciones, o excepciones, relativas al consumo de pescado, frutas y bebidas alcohólicas, que son fácilmente salvables en una dieta globalmente más sana29. En la tabla III se recogen las recomendaciones prácticas más habituales según los conocimientos actuales y siguiendo los consejos de las principales guías de tratamiento.
Todas las guías terapéuticas recomiendan, como parte fundamental del tratamiento de la gota, la educación y los consejos sobre alimentación y estilo de vida23,75-80. Además, estas recomendaciones son la única alternativa terapéutica aceptada en la hiperuricemia asintomática y en los pacientes con ataques de gota esporádicos23,75-80,84. Frecuentemente, los pacientes preguntan a sus médicos sobre el papel de las modificaciones dietéticas en el tratamiento de la gota, ya que pertenece al acervo cultural general que el AU y la gota tienen algo que ver con la dieta. Aunque los médicos, según los resultados de encuestas, parecen ser conscientes de la conveniencia de instaurar medidas higiénico-dietéticas85, los datos indican que las medidas educativas relacionadas con la gota se proporcionan a un escaso número de pacientes, que en ocasiones las informaciones son contradictorias y que, a menudo, no son correctas a la luz de los conocimientos actuales86-88. Sólo se ofrecen consejos dietéticos al 30 % de los pacientes; además, frecuentemente estos consejos no están actualizados y, en ocasiones, son contradictorios16,89,90. Los errores más habituales suelen ser la restricción de verduras y legumbres ricas en purinas, la limitación de las proteínas de la dieta, no restringir el consumo de bebidas edulcoradas y no aconsejar un aumento en la ingesta de lácteos desnatados16. En un estudio reciente, la mayoría de los pacientes señalaban incorrectamente a las verduras (58%), al pollo (55%) y a las legumbres (39%) como alimentos que podían incrementar el riesgo de hiperuricemia y gota, comparados con los pescados (23%), carne de vacuno (22%) y carne de cerdo (7%). Sólo el 43% conocía que beber cerveza aumenta el riesgo de hiperuricemia y gota88. Esta falta de educación a los pacientes puede contribuir a la reconocida escasa adherencia de los gotosos al tratamiento farmacológico, que es peor que en otras enfermedades crónicas91-94. Aunque no hay datos al respecto, se supone que el cumplimiento de las recomendaciones no farmacológicas es aún peor que la adhesión al tratamiento con fármacos, pues según algunos estudios, menos del 20% de los pacientes que buscan servicios médicos en general están dispuestos a realizar cambios sostenidos en su estilo de vida95. Sin embargo, observaciones recientes indican que, si la información es adecuada y si los tratamientos se realizan siguiendo los consejos de las guías, se consigue una elevada adherencia al tratamiento en los pacientes gotosos y unos resultados óptimos en una mayoría de pacientes96. En un estudio sobre 106 gotosos que recibieron una intervención, que incluía educación sobre la enfermedad y los factores de riesgo, consejos sobre estilo de vida y tratamiento farmacológico adecuado hasta alcanzar el objetivo, a los 12 meses el 92% habían conseguido el objetivo terapéutico de AU < 6 mg/dl y el 85% tenían un AU sérico < 5 mg/dl96. En otro estudio, con intervenciones diversas (educación global del paciente, acceso telefónico, visitas frecuentes hasta la consecución del objetivo y ajustes progresivos, con incremento de la dosis de alopurinol) para conseguir un nivel de AU <6 mg/dl, el 8,1% de los pacientes habían alcanzado el objetivo terapéutico a los 3 meses, el 40,6% a los 6 meses y el 72% a los 12 meses97. Por tanto, el cumplimiento de las medidas terapéuticas en la gota parece mejorar notablemente cuando se incluyen información sobre la enfermedad y los factores de riesgo, consejos sobre estilo de vida, un seguimiento más frecuente e instauración de un tratamiento farmacológico adecuado.
Conclusiones
Investigaciones realizadas en la última década han definido con mayor claridad algunos factores de riesgo de hiperuricemia y gota candidatos desde la antigüedad, como el exceso en la ingesta de carnes y pescados, el abuso de alcohol -en especial, cervezas y licores- o la obesidad17. Se han descrito nuevos factores de riesgo, en especial las dietas con elevados contenidos de fructosa y las bebidas edulcoradas10,12,16,36. Otros factores que estaban señalados como culpables, como las legumbres y las verduras con alto contenido en purinas, el consumo moderado de vino o las dietas con elevado contenido proteico, en general han sido exculpados29. Finalmente, se ha observado que algunos alimentos tienen efecto protector frente a la hiperuricemia y gota, en especial los productos lácteos desnatados, las verduras, la fibra, el café y las cerezas29.
Las evidencias científicas de la asociación entre la gota y varios factores de riesgo alimentarios y de estilo de vida proceden fundamentalmente de grandes estudios epidemiológicos y observacionales98. Son escasos los ensayos controlados aleatorizados sobre la eficacia de la supresión o el aporte de un alimento específico, o el cambio de un hábito de estilo de vida, en la modificación de los niveles de AU y el control de la gota98. Por otra parte, los hábitos alimentarios, las comorbilidades y la respuesta a las modificaciones alimentarias pueden ser distintos en diferentes grupos de población39,99. La adopción de determinadas medidas dietéticas y de estilo de vida, no avaladas suficientemente por la evidencia científica86,98, en los pacientes con hiperuricemia y gota no debería ser motivo para olvidar o retrasar la implantación de medidas farmacológicas más eficaces en aquellos pacientes que lo precisen, de acuerdo con las recomendaciones de las guías terapéuticas99. Del mismo modo, el hecho de dar un comprimido muy eficaz para el control de la uricemia no debería hacer caer en el olvido la adopción de medidas dietéticas y de estilo de vida en aquellos pacientes con hábitos alimenticios poco saludables100.
La gota tiene en la actualidad un tratamiento farmacológico excelente, mejorado aún en los últimos años con el desarrollo de nuevos fármacos hipouricemiantes. Sin embargo, un tratamiento óptimo de la gota no se puede conformar con tratar únicamente los episodios agudos, ni con alcanzar y mantener una uricemia inferior a 6 mg/dl, sino que debe prestar también una atención especial al tratamiento de las enfermedades asociadas y al riesgo cardiovascular. La gota se asocia con obesidad, hipertensión, diabetes mellitus, dislipe-mia y síndrome metabólico, cuyas manifestaciones y complicaciones deberían ser minimizadas con medidas de control de peso, cambios en la alimentación y de estilo de vida. El tratamiento dietético en la gota puede no ser necesario para controlar los niveles de AU, lo que se puede conseguir en la mayoría de los casos con los fármacos; sin embargo, parece imprescindible para evitar y mejorar las comorbilidades y proporcionar a los pacientes una mejor calidad de vida. Así, es inexcusable no aconsejar un programa de adelgazamiento al paciente gotoso con sobrepeso, no restringir el consumo de bebidas alcohólicas y/o bebidas edulcoradas, a los que las consumen en exceso, y no estimular a todos a llevar una dieta más saludable, con más verduras, legumbres y productos lácteos desnatados.
Son necesarios más estudios que investiguen la utilidad clínica real de los consejos dietéticos y de modificación de estilo de vida en la reducción de los niveles de AU y en la mejor evolución de la gota; sin embargo, parece razonable mantener estas recomendaciones en los pacientes gotosos, en especial cuando se observen patrones alimentarios y estilos de vida claramente poco saludables y para la prevención y tratamiento de las comorbilidades. Estas intervenciones pueden proporcionar a la larga un beneficio neto muy superior al mero descenso de los niveles de AU, otorgando al paciente una mejor calidad de vida y salud general.
Referencias
1. Johnson RJ, Rideout BA. Uric acid and diet -insights into the epidemic of cardiovascular disease. N Engl J Med 2004; 350: 1071-3. [ Links ]
2. Fam AG. Gout, diet and the insulin resistance syndrome. J Rheumatol 2002; 29: 1350-5. [ Links ]
3. Doherty M. New insights into the epidemiology of gout. Rheumatology (Oxford). 2009; 48 Suppl 2: ii2-ii8. [ Links ]
4. Campion EW, Glynn RJ, DeLabry LO. Asymptomatic hyperuricemia. Risks and consequences in the Normative Aging Study. Am J Med 1987; 82: 421-6. [ Links ]
5. Bhole V, de Vera M, Rahman MM, Krishnan E, Choi H. Epidemiology of gout in women: Fifty-two-year follow up of a prospective cohort. Arthritis Rheum 2010; 62: 1069-76. [ Links ]
6. Pérez Ruiz F. Gout: past, present, and future. Reumatol Clin 2011; 7: 217-9. [ Links ]
7. Saag KG, Choi H. Epidemiology, risk factors, and lifestyle modifications for gout. Arthritis Res Ther 2006; 8 (Supl. 1): S2. [ Links ]
8. Baker JF, Schumacher HR. Update on gout and hyperuricemia. Int J Clin Pract 2010; 64: 371-7. [ Links ]
9. Zhu Y, Pandya BJ, Choi HK. Prevalence of gout and hyperuricemia in the US general population: the National Health and Nutrition Examination Survey 2007-2008. Arthritis Rheum 2011; 63:3136-41. [ Links ]
10. Rho YH, Zhu Y, Choi HK. The epidemiology of uric acid and fructose. Semin Nephrol 2011; 31: 410-9. [ Links ]
11. Robinson PC, Merriman TR, Herbison P, Highton J. Hospital admissions associated with gout and their co-morbidities in New Zealand and England 1999-2009. Rheumatology (Oxford) 2013; 52: 118-26. [ Links ]
12. Kedar E, Simkin PA. A perspective on diet and gout. Adv Chronic Kidney Dis 2012; 19: 392-7. [ Links ]
13. Alvarez-Lario B, Macarrón-Vicente J. Is there anything good in uric acid? QJM 2011; 104: 1015-24. [ Links ]
14. Alvarez-Lario B, Macarrón-Vicente J. Evolution of Uric Acid Metabolism in Humans. In: eLS 2013. John Wiley & Sons, Ltd: Chichester. DOI: 10.1002/9780470015902.a0024618 [ Links ]
15. Johnson RJ, Titte S, Cade JR, Rideout BA, Oliver WJ. Uric acid, evolution and primitive cultures. Semin Nephrol 2005; 25 (1): 3-8. [ Links ]
16. Zgaga L, Theodoratou E, Kyle J, Farrington SM, Agakov F, Tenesa A y cols.The association of dietary intake of purine-rich vegetables, sugar-sweetened beverages and dairy with plasma urate, in a cross-sectional study. PLoS One 2012; 7: e38123. [ Links ]
17. Singh JA, Reddy SG, Kundukulam J. Risk factors for gout and prevention: a systematic review of the literature. Curr Opin Rheumatol 2011; 23: 192-202. [ Links ]
18. Gil-Campos M, Aguilera CM, Cañete R, Gil A. Uric acid is associated with features of insulin resistance syndrome in obese children at prepubertal stage. Nutr Hosp 2009; 24: 607-13. [ Links ]
19. Fam AG. Gout: excess calories, purines, and alcohol intake and beyond. Response to a urate-lowering diet. J Rheumatol 2005; 32: 773-7. [ Links ]
20. Feig DI, Kang DH, Johnson RJ. Uric acid and cardiovascular risk. N Engl J Med 2008; 359: 1811-21. [ Links ]
21. Richette P, Clerson P, Périssin L, Flipo RM, Bardin T. Revisiting comorbidities in gout: a cluster analysis. Ann Rheum Dis 2013 Oct 9. DOI: 10.1136/annrheumdis-2013-203779. (Epub ahead of print). [ Links ]
22. Zhu Y, Pandya BJ, Choi HK. Comorbidities of gout and hyperuricemia in the US general population: NHANES 2007-2008. Am J Med 2012; 125: 679-87. [ Links ]
23. Khanna D, Fitzgerald JD, Khanna PP, Bae S, Singh MK, Neogi T y cols. 2012 American College of Rheumatology guidelines for management of gout. Part 1: Systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia. Arthritis Care Res (Hoboken) 2012; 64: 1431-46. [ Links ]
24. Emmerson BT. The management of gout. N Engl J Med 1996; 334: 445-51. [ Links ]
25. Clifford AJ, Riumallo JA, Young VR, Scrimshaw NS. Effect of oral purines on serum and urinary uric acid of normal, hyperuricemic and gouty humans. J Nutr 1976; 106: 428-34. [ Links ]
26. Zöllner N, Griebsch A. Diet and gout. Adv Exp Med Biol 1974; 41: 435-42. [ Links ]
27. Choi HK, Liu S, Curhan G. Intake of purine-rich foods, protein, and dairy products and relationship to serum levels of uric acid: the Third National Health and Nutrition Examination Survey. Arthritis Rheum 2005; 52: 283-9. [ Links ]
28. Choi HK, Atkinson K, Karlson EW, Willett W, Curhan G. Purine-rich foods, dairy and protein intake, and the risk of gout in men. N Engl J Med 2004; 350: 1093-103. [ Links ]
29. Choi HK. A prescription for lifestyle change in patients with hyperuricemia and gout. Curr Opin Rheumatol 2010; 22: 165-72. [ Links ]
30. Gibson T, Rodgers AV, Simmonds HA, Court-Brown F, Todd E, Meilton V. A controlled study of diet in patients with gout. Ann Rheum Dis 1983; 42: 123-7. [ Links ]
31. Spanou C, Veskoukis AS, Kerasioti T, Kontou M, Angelis A, Aligiannis N y cols. Flavonoid glycosides isolated from unique legume plant extracts as novel inhibitors of xanthine oxidase. PLoS One 2012; 7: e32214. [ Links ]
32. Choi HK, Curhan G. Beer, liquor, and wine consumption and serum uric acid level: the Third National Health and Nutrition Examination Survey. Arthritis Rheum 2004; 51: 1023-9. [ Links ]
33. Sun SZ, Flickinger BD, Williamson-Hughes PS, Empie MW. Lack of association between dietary fructose and hyperuricemia risk in adults. Nutr Metab (Lond) 2010; 7: 16. [ Links ]
34. Choi HK, Atkinson K, Karlson EW, Willett W, Curhan G. Alcohol intake and risk of incident gout in men: a prospective study. Lancet 2004; 363: 1277-81. [ Links ]
35. Zhang Y, Woods R, Chaisson CE, Neogi T, Niu J, McAlindon TE y cols. Alcohol consumption as a trigger of recurrent gout attacks. Am J Med 2006; 119: 800.e13-8. [ Links ]
36. Choi JW, Ford ES, Gao X, Choi HK. Sugar-sweetened soft drinks, diet soft drinks, and serum uric acid level: the Third National Health and Nutrition Examination Survey. Arthritis Rheum 2008; 59: 109-16. [ Links ]
37. Choi HK, Curhan G. Soft drinks, fructose consumption, and the risk of gout in men: prospective cohort study. BMJ 2008; 336: 309-12. [ Links ]
38. Choi HK, Willett W, Curhan G. Fructose-rich beverages and risk of gout in women. JAMA 2010; 304: 2270-8. [ Links ]
39. Batt C, Phipps-Green AJ, Black MA, Cadzow M, Merriman ME, Topless R, y cols. Sugar-sweetened beverage consumption: a risk factor for prevalent gout with SLC2A9 genotype-specific effects on serum urate and risk of gout. Ann Rheum Dis 2013 Sep 11. doi: 10.1136/annrheumdis-2013-203600. (Epub ahead of print). [ Links ]
40. Wang DD, Sievenpiper JL, de Souza RJ, Chiavaroli L, Ha V, Cozma AI y cols. The effects of fructose intake on serum uric acid vary among controlled dietary trials. J Nutr 2012; 142: 916-23. [ Links ]
41. Ghadirian P, Shatenstein B, Verdy M, Hamet P. The influence of dairy products on plasma uric acid in women. Eur J Epidemiol 1995;11:275-81. [ Links ]
42. Dalbeth N, Wong S, Gamble GD, Horne A, Mason B, Pool B y cols. Acute effect of milk on serum urate concentrations: a randomised controlled crossover trial. Ann Rheum Dis 2010; 69: 1677-82. [ Links ]
43. Lipkowitz MS. Regulation of uric acid excretion by the kidney. Curr Rheumatol Rep 2012; 14: 179-88. [ Links ]
44. Dalbeth N, Horne A, Gamble GD, Ames R, Mason B, McQueen FM y cols. The effect of calcium supplementation on serum urate: analysis of a randomized controlled trial. Rheumatology (Oxford) 2009; 48: 195-7. [ Links ]
45. Dalbeth N, Palmano K. Effects of dairy intake on hyperuricemia and gout. Curr Rheumatol Rep 2011; 13: 132-7. [ Links ]
46. Tsai YT, Liu JP, Tu YK, Lee MS, Chen PR, Hsu HC y cols. Relationship between dietary patterns and serum uric acid concentrations among ethnic Chinese adults in Taiwan. Asia Pac J Clin Nutr 2012; 21: 263-70. [ Links ]
47. Lyu LC, Hsu CY, Yeh CY, Lee MS, Huang SH, Chen CL. A case-control study of the association of diet and obesity with gout in Taiwan. Am J Clin Nutr 2003; 78: 690-701. [ Links ]
48. Kanbara A, Miura Y, Hyogo H, Chayama K, Seyama I. Effect of urine pH changed by dietary intervention on uric acid clearance mechanism of pH-dependent excretion of urinary uric acid. Nutr J 2012; 11: 39. [ Links ]
49. Choi HK, Gao X, Curhan G. Vitamin C intake and the risk of gout in men: a prospective study. Arch Intern Med 2009; 169: 502-7. [ Links ]
50. Gao X, Curhan G, Forman JP, Ascherio A, Choi HK. Vitamin C intake and serum uric acid concentration in men. J Rheumatol 2008;35: 1853-8. [ Links ]
51. Juraschek SP, Miller ER 3rd, Gelber AC. Effect of oral vitamin C supplementation on serum uric acid: a meta-analysis of randomized controlled trials. Arthritis Care Res (Hoboken) 2011; 63: 1295-306. [ Links ]
52. Stamp LK, O´Donnell JL, Frampton C, Drake JM, Zhang M, Chapman PT. Clinically insignificant effect of supplemental vitamin C on serum urate in patients with gout: a pilot randomized controlled trial. Arthritis Rheum 2013; 65: 1636-42. [ Links ]
53. Choi HK, Curhan G. Coffee, tea, and caffeine consumption and serum uric acid level: the third national health and nutrition examination survey. Arthritis Rheum 2007; 57: 816-21. [ Links ]
54. Choi HK, Curhan G. Coffee consumption and risk of incident gout in women: the Nurses´ Health Study. Am J Clin Nutr 2010; 92: 922-7. [ Links ]
55. Jacob RA, Spinozzi GM, Simon VA, Kelley DS, Prior RL, Hess-Pierce B y cols. Consumption of cherries lowers plasma urate in healthy women. J Nutr 2003; 133: 1826-9. [ Links ]
56. Zhang Y, Neogi T, Chen C, Chaisson C, Hunter D, Choi HK. Cherry consumption and the risk of recurrent gout attacks. Arthritis Rheum 2012; 64: 4004-11. [ Links ]
57. Yü T, Yu TF. Milestones in the treatment of gout. Am J Med 1974; 56: 676-85. [ Links ]
58. Rathmann W, Funkhouser E, Dyer AR, Roseman JM. Relations of hyperuricemia with the various components of the insulin resistance syndrome in young black and white adults: the CARDIA study. Coronary Artery Risk Development in Young Adults. Ann Epidemiol 1998; 8: 250-61. [ Links ]
59. Zhu Y, Zhang Y, Choi HK.The serum urate-lowering impact of weight loss among men with a high cardiovascular risk profile: the Multiple Risk Factor Intervention Trial. Rheumatology (Oxford) 2010; 49: 2391-9. [ Links ]
60. Choi HK, Atkinson K, Karlson EW, Curhan G. Obesity, weight change, hypertension, diuretic use, and risk of gout in men: the health professionals follow-up study. Arch Intern Med 2005; 165: 742-8. [ Links ]
61. Dessein PH, Shipton EA, Stanwix AE, Joffe BI, Ramokgadi J. Beneficial effects of weight loss associated with moderate calorie/carbohydrate restriction, and increased proportional intake of protein and unsaturated fat on serum urate and lipoprotein levels in gout: a pilot study. Ann Rheum Dis 2000; 59: 539-43. [ Links ]
62. Piñera MJ, Arrieta FJ, Alcaraz-Cebrián F, Botella-Carretero JI, Calañas A, Balsa JA y cols. Influence of weight loss in the clinical evolution, metabolic and psychological of the patients with overweight or obesity. Nutr Hosp 2012; 27: 1480-8. [ Links ]
63. Tsunoda S, Kamide K, Minami J, Kawano Y. Decreases in serum uric acid by amelioration of insulin resistance in overweight hypertensive patients: effect of a low-energy diet and an insulin-sensitizing agent. Am J Hypertens 2002 ; 15: 697-701. [ Links ]
64. Yamashita S, Matsuzawa Y, Tokunaga K, Fujioka S, Tarui S. Studies on the impaired metabolism of uric acid in obese subjects: marked reduction of renal urate excretion and its improvement by a low-calorie diet. Int J Obes 1986; 10: 255-64. [ Links ]
65. Kontogianni M, Chrysohoou C, Panagiotakos D, Tsetsekou E, Zeimbekis A, Pitsavos C y cols. Adherence to the Mediterranean diet and serum uric acid: the ATTICA study. Scand J Rheumatol 2012; 41: 442-9. [ Links ]
66. Guasch-Ferré M, Bulló M, Babio N, Martínez-González MA, Estruch R, Covas MI, y cols. Mediterranean diet and risk of hyperuricemia in elderly participants at high cardiovascular risk. J Gerontol A Biol Sci Med Sci 2013; 68: 1263-70. [ Links ]
67. Kastorini CM, Milionis HJ, Esposito K, Giugliano D, Goudevenos JA, Panagiotakos DB. The effect of Mediterranean diet on metabolic syndrome and its components: a meta-analysis of 50 studies and 534,906 individuals. J Am Coll Cardiol 2011; 57: 1299-313. [ Links ]
68. Sofi F, Abbate R, Gensini GF, Casini A. Accruing evidence on benefits of adherence to the Mediterranean diet on health: an updated systematic review and meta-analysis. Am J Clin Nutr 2010; 92: 1189-96. [ Links ]
69. Tognon G, Lissner L, Sæbye D, Walker KZ, Heitmann BL. The Mediterranean diet in relation to mortality and CVD: a Danish cohort study. Br J Nutr 2013 Jul 3: 1-9. [ Links ]
70. Varela-Moreiras G. Alguacil Merino LF, Alonso Aperte E, Aranceta Bartrina J, Ávila Torres JM, Aznar Lain S y cols. Documento de consenso y conclusiones. Obesidad y sedentarismo en el siglo XXI: ¿qué se puede y se debe hacer? Nutr Hosp 2013; 28 (Supl. 5): 128-37. [ Links ]
71. Esposito K, Kastorini CM, Panagiotakos DB, Giugliano D. Mediterranean diet and weight loss: meta-analysis of randomized controlled trials. Metab Syndr Relat Disord 2011; 9: 1-12. [ Links ]
72. Tsai YT, Liu JP, Tu YK, Lee MS, Chen PR, Hsu HC y cols. Relationship between dietary patterns and serum uric acid concentrations among ethnic Chinese adults in Taiwan. Asia Pac J Clin Nutr 2012; 21: 263-70. [ Links ]
73. Schmidt JA, Crowe FL, Appleby PN, Key TJ, Travis RC. Serum uric acid concentrations in meat eaters, fish eaters, vegetarians and vegans: a cross-sectional analysis in the EPIC-Oxford cohort. PLoS One 2013; 8: e56339. [ Links ]
74. Rodnan GP. The pathogenesis of aldermarnic gout: procatarctic role of fluctuations in serum concentration in gouty arthritis provoked by feast and alcohol (abstract). Arthritis Rheum 1980; 23 (Supl.): 737. [ Links ]
75. Jordan KM, Cameron JS, Snaith M, Zhang W, Doherty M, Seckl J y cols. British Society for Rheumatology and British Health Professionals in Rheumatology guideline for the management of gout. Rheumatology (Oxford) 2007; 46: 1372-4. [ Links ]
76. Hamburger M, Baraf HS, Adamson TC, Basile J, Bass L, Cole B y cols. 2011 recommendations for the diagnosis and management of gout and hyperuricemia. Phys Sportsmed 2011; 39: 98-123. [ Links ]
77. Yamanaka H. Japanese guideline for the management of hyperuricemia and gout: second edition. Nucleosides Nucleotides Nucleic Acids 2011; 30: 1018-29. [ Links ]
78. Manara M, Bortoluzzi A, Favero M, Prevete I, Scirè CA, Bianchi G y cols. Italian Society of Rheumatology recommendations for the management of gout. Reumatismo 2013; 65: 4-21. [ Links ]
79. Guia de práctica clínica para el manejo de la gota. Sociedad Española de Reumatología. 2013. http://www.ser.es/practicaClinica/GuipClinGot/ [ Links ]
80. Zhang W, Doherty M, Bardin T, Pascual E, Barskova V, Conag-han P y cols. EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis 2006; 65: 1312-4. [ Links ]
81. Carrero JJ, Martin-Bautista E, Barò L, Fonollá J, Jiménez J, Boza JJ y cols. Cardiovascular effects of omega-3-fatty acids and alternatives to increase their intake. Nutr Hosp 2005; 20: 63-9. [ Links ]
82. Silva Ton T, Gonsalves Alfenas RD. Dairy products consumption versus type 2 diabetes prevention and treatment; a review of recent findings from human studies. Nutr Hosp 2013; 28: 1384-95. [ Links ]
83. Bao Y, Wei Q. Water for preventing urinary stones. Cochrane Database Syst Rev 2012; 6: CD004292. [ Links ]
84. Sivera F, Andrés M, Carmona L, Kydd AS, Moi J, Seth R y cols. Multinational evidence-based recommendations for the diagnosis and management of gout: integrating systematic literature review and expert opinion of a broad panel of rheumatologists in the 3e initiative. Ann Rheum Dis 2014; 73: 328-35. [ Links ]
85. Fara N, Vázquez Mellado J, Sequeira G, Kerzberg E. A survey on the current evaluation and treatment of gout in Buenos Aires, Argentina. Reumatol Clin 2012; 8: 306-9. [ Links ]
86. Chiowchanwisawakit P, Taweesuk A, Katchamart W, Sri-nonprasert V. Prevalence and risk factors of symptomatic hyperuricemia; quality of care of patients with hyperuricemia in a university hospital. J Med Assoc Thai 2013; 96 (Supl. 2): S178-86. [ Links ]
87. Doherty M, Jansen TL, Nuki G, Pascual E, Pérez-Ruiz F, Punzi L y cols. Gout: why is this curable disease so seldom cured? Ann Rheum Dis 2012; 71: 1765-70. [ Links ]
88. Harrold LR, Mazor KM, Peterson D, Naz N, Firneno C, Yood R. Patients´ knowledge and beliefs concerning gout and its treatment: a population based study. BMC Musculoskelet Disord 2012; 13: 180. [ Links ]
89. Shulten P, Thomas J, Miller M, Smith M, Ahern M. The role of diet in the management of gout: a comparison of knowledge and attitudes to current evidence. J Hum Nutr Diet 2009; 22: 3-11. [ Links ]
90. Pal B, Foxall M, Dysart T, Carey F, Whittaker M. How is gout managed in primary care? A review of current practice and proposed guidelines. Clin Rheumatol 2000; 19: 21-5. [ Links ]
91. Briesacher BA, Andrade SE, Fouayzi H, Chan KA. Comparison of drug adherence rates among patients with seven different medical conditions. Pharmacotherapy 2008; 28: 437-43. [ Links ]
92. Riedel AA, Nelson M, Joseph-Ridge N, Wallace K, MacDonald P, Becker M. Compliance with allopurinol therapy among managed care enrollees with gout: a retrospective analysis of administrative claims. J Rheumatol 2004; 31: 1575-81. [ Links ]
93. Sarawate CA, Brewer KK, Yang W, Patel PA, Schumacher HR, Saag KG y cols. Gout medication treatment patterns and adherence to standards of care from a managed care perspective. Mayo Clin Proc 2006; 81: 925-34. [ Links ]
94. Reach G. Treatment adherence in patients with gout. Joint Bone Spine 2011; 78: 456-9. [ Links ]
95. Levinson W, Cohen MS, Brady D, Duffy FD. To change or not to change: "Sounds like you have a dilemma". Ann Intern Med 2001;135:386-91. [ Links ]
96. Rees F, Jenkins W, Doherty M. Patients with gout adhere to curative treatment if informed appropriately: proof-of-concept observational study. Ann Rheum Dis 2013; 72: 826-30. [ Links ]
97. Lim A, Shen L, Tan C, Lateef A, Lau T, Teng G. Achieving treat to target in gout: a clinical practice improvement project. Scand J Rheumatol 2012; 41: 450-7. [ Links ]
98. Moi JH, Sriranganathan MK, Edwards CJ, Buchbinder R. Lifestyle interventions for chronic gout. Cochrane Database SystRev 2013; 5: CD010039. [ Links ]
99. Pérez-Ruiz F, Herrero-Beites AM. Crystal arthritis: Environment and genetics in gout: a maze for clinicians? Nat Rev Rheumatol 2014; 10: 8-9. [ Links ]
100. Liote F, Choi H. Managing gout needs more than drugs: "Il faut le savoir-faire, l´Art et la maniere". Ann Rheum Dis 2013; 72: 791-3. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Bonifacio Álvarez Lario.
Sección de Reumatología.
Hospital Universitario de Burgos.
Avda. de Islas Baleares, s/n.
09006 Burgos.
E-mail: balario@hubu.es
Recibido: 4-XII-2013.
Aceptado: 18-XII-2013.