INTRODUCCIÓN
Los seres humanos tenemos el mismo número de bacterias que células propias en nuestro organismo, y están presentes en todas las partes del cuerpo, aunque la mayoría se localiza en la piel y aquellas cavidades del organismo que se comunican con el exterior y que son, fundamentalmente, la vagina y el aparato digestivo, sobre todo en el intestino grueso. Es lo que llamamos microbiota autóctona. La relación que mantenemos con ella es habitualmente mutualista, ya que sus microorganismos nos proporcionan una serie de ventajas que van desde la protección frente a la invasión por agentes patógenos y el desarrollo del sistema inmunitario a la colaboración en la digestión de componentes de la dieta y la provisión de vitaminas y otros nutrientes esenciales. Las funciones que ejerce la microbiota son esenciales para nuestra vida.
Aunque desde hace más de un siglo se conoce que la microbiota autóctona tiene efectos beneficiosos para el organismo, el interés por el microbioma humano y su relación con la salud ha aumentado notablemente en los últimos años. Las investigaciones del Proyecto Microbioma Humano estadounidense y del proyecto MetaHIT europeo han revolucionado el mundo de la ciencia y nos han confirmado que los humanos somos superorganismos, cuyo funcionamiento representa una amalgama de propiedades microbianas y humanas, y que muchas enfermedades son fruto de la pérdida de armonía entre nuestro genoma y el microbioma. Aunque todavía queda mucho camino por recorrer, el conocimiento y la modulación de la microbiota nos abren la puerta a un gran número de investigaciones para tratar y prevenir muchas enfermedades, lo que hace de ello una de las revoluciones científicas más importantes de la medicina 1.
La dieta aparece como elemento clave para la relación simbiótica entre los microorganismos del intestino y del animal hospedador. El anfitrión, huésped o sujeto proporciona hábitat y nutrición a las comunidades del tracto intestinal, y estas contribuyen a la salud del anfitrión. Además, como los alimentos suministran sustratos diversos y variables para el metabolismo microbiano, la dieta puede influir y modular la estructura y la composición de las comunidades microbianas 2.
ADQUISICIÓN DE LA MICROBIOTA
Cada individuo posee una comunidad microbiana peculiar que depende de su genotipo y de la exposición temprana a los microorganismos de su entorno, pero también de la dieta, los cambios de estilo de vida o la terapia frente a las infecciones. Esto implica que la colonización desde el nacimiento será diferente dependiendo de factores como el tipo de parto, el modelo de lactancia, el entorno en el que crecemos (rural o urbano), nacer en un país en vías de desarrollo o desarrollado, el uso de antibióticos, especialmente los utilizados para combatir infecciones durante el parto y en la primera infancia, etc. Un inadecuado desarrollo de nuestra microbiota intestinal durante los primeros meses de vida por el aumento del número de cesáreas, el abandono prematuro de la lactancia materna o, ya en la edad adulta, por el abuso de antibióticos, una dieta inadecuada o el proceso del envejecimiento, puede llevarnos a un estado de disbiosis con una alteración de la microbiota tanto cualitativa (predominio de especies distintas a las habituales) como cuantitativa (menor concentración de bacterias beneficiosas). La consecuencia será la disminución de sus efectos saludables y la aparición de enfermedades 3.
Está generalmente aceptado que un recién nacido a término por vía vaginal y alimentado con leche materna desarrolla una microbiota más competente y protectora frente a la aparición de algunas enfermedades. La leche materna es un alimento totalmente adaptado a la capacidad metabólica del neonato y aporta una serie de componentes muy importantes para el mantenimiento del estado de salud del lactante, como los oligosacáridos de leche materna (Human Milk Oligosaccharides -HMO-, en inglés), que favorecen el crecimiento de algunos microorganismos beneficiosos, como las bifidobacterias.
En la actualidad, se han identificado más de 250 especies diferentes en la leche humana, lo que contradice la antigua idea de que es un líquido estéril. Además, se ha demostrado la existencia de la circulación enteromamaria, una vía mediante la cual las bacterias intestinales beneficiosas de la madre pasarían a través de la glándula mamaria al intestino del lactante, lo que le otorga a este múltiples beneficios para su salud. Así, los lactantes alimentados con leche humana tienen una menor incidencia de infecciones, alergias, problemas digestivos, un mejor desarrollo neurológico y menor posibilidad de presentar enfermedad inflamatoria intestinal o diabetes en un futuro, beneficios atribuidos en parte a las bacterias beneficiosas y los componentes que las hacen crecer 4. Al comparar la influencia de la alimentación con leche materna con la de leche de fórmula, observamos un patrón de colonización diferente, caracterizado por una población más abundante de bifidobacterias en los niños alimentados al pecho.
Otro factor que condiciona el tipo de bacterias presentes en nuestro intestino es el paso de la lactancia a la alimentación sólida. Tras el destete, se producen importantes modificaciones en el perfil de nutrientes ingeridos por el niño, ya que se introducen por primera vez en la dieta los alimentos de origen vegetal, la carne y el pescado. Es en este momento cuando empiezan a producirse cambios en la comunidad microbiana que tendrán como resultado el establecimiento de una microbiota con un aumento de la diversidad, una disminución de las bifidobacterias y una transición hacia un microbiota madura, adaptada a una mayor ingesta de proteína animal y de polisacáridos de origen vegetal y dominada por los filos Bacteroidetes y Firmicutes. De hecho, hay una correlación entre la microbiota intestinal que va adquiriendo el lactante y la introducción paulatina de los alimentos durante los dos primeros años de vida (Fig. 1).

Figura 1 Correlación entre la microbiota intestinal del lactante y la introducción paulatina de los alimentos tras el destete. Cedido por el Prof. Evaristo Suárez.
En general, se estima que los grupos microbianos dominantes en la microbiota intestinal de los niños de 2-3 años son similares a los de los adultos, aunque todavía existen diferencias en cuanto a las especies presentes. Al final de la adolescencia se alcanza el clímax y, a partir de entonces, este ecosistema muestra una elevada estabilidad en los adultos sanos, aunque hay una serie de factores, fundamentalmente la dieta y el estilo de vida, que pueden modificarla a cualquier edad, incluso en la vejez. En cualquier caso, la microbiota intestinal del ser humano parece ser específica de cada individuo, aunque compartamos aproximadamente la mitad de los casi 600.000 genes que tenemos en ella.
IMPACTO DE LA DIETA EN LA COMPOSICIÓN DE LA MICROBIOTA
Lo que comemos influye mucho en la estructura y en la composición de las comunidades microbianas del intestino. La primera prueba de ello se obtuvo mediante la comparación de muestras de microbiota fecal de distintas especies de mamíferos. La microbiota de los herbívoros se diferencia claramente de la de los omnívoros o carnívoros exclusivos. Por tanto, la dieta habitual parece ser el principal determinante de la composición microbiana intestinal cuando se comparan muestras de distintas especies. Así, la microbiota fecal humana es similar a la de especies de primates omnívoros. La variedad de alimentos de la dieta omnívora y el estilo de vida libre de nuestra especie son probablemente los principales factores que afectan la composición de la microbiota intestinal humana 5.
Este dato cobra gran importancia cuando existen diferencias entre la dieta de distintas poblaciones humanas. En estudios realizados en la etnia hazda, en Tanzania, pueblo de cazadores y recolectores y con una dieta rica en fibra (frutas, raíces y tubérculos) y muy baja en grasas, presenta una microbiota mucho más diversa y rica en la que predomina el género Prevotella, modelo de bacterias adaptadas a recuperar la energía y nutrientes de alimentos ricos en fibra vegetal 6. Estudios similares se han observado en etnias amazónicas de Brasil y Perú. En cambio, las sociedades industrializadas tienen un predominio de Bacteroides, por el consumo de alimentos proteicos y grasa, que presentan un elevado contenido energético. Especial interés tiene el estudio de Di Filippo et al., que comparó la microbiota de niños africanos (de Burkina Faso) con la de niños europeos (de Italia). Los primeros tienen mayor presencia de especies del género Prevotella, menor abundancia de especies de Bacteroides, mayor diversidad microbiana y mayor producción de ácidos grasos de cadena corta. Es razonable especular que la dieta agraria de Burkina Faso (rica en carbohidratos complejos, fibra y proteína no animal) en comparación con la dieta occidental (rica en proteínas y grasas animales, azúcares, almidones y pobre en fibra) tiene un papel determinante en las diferencias observadas 7.
Por lo tanto, el incremento de la ingesta alimentaria con proteínas y grasa animal junto con la ausencia del consumo de fibra dietética aumenta la abundancia de microorganismos tolerantes de las sales biliares (Alistipes, Bilophila y Bacteroides) y disminuye los niveles de especies que metabolizan los carbohidratos complejos de los vegetales (Roseburia, Eubacterium rectale y Ruminococcus bromii). Por el contrario, el consumo abundante de fibra dietética, frutas, verduras y otros vegetales se asocia con incrementos importantes de las especies fermentativas. En conclusión, la mayor proporción de Prevotella en la microbiota intestinal del humano adulto es un marcador de regímenes dietéticos propios de áreas rurales y cultura agraria, mientras que una mayor proporción de Bacteroides se asocia con residencia en regiones industrializadas y hábitos dietéticos propios de la vida urbana 8 (Fig. 2).
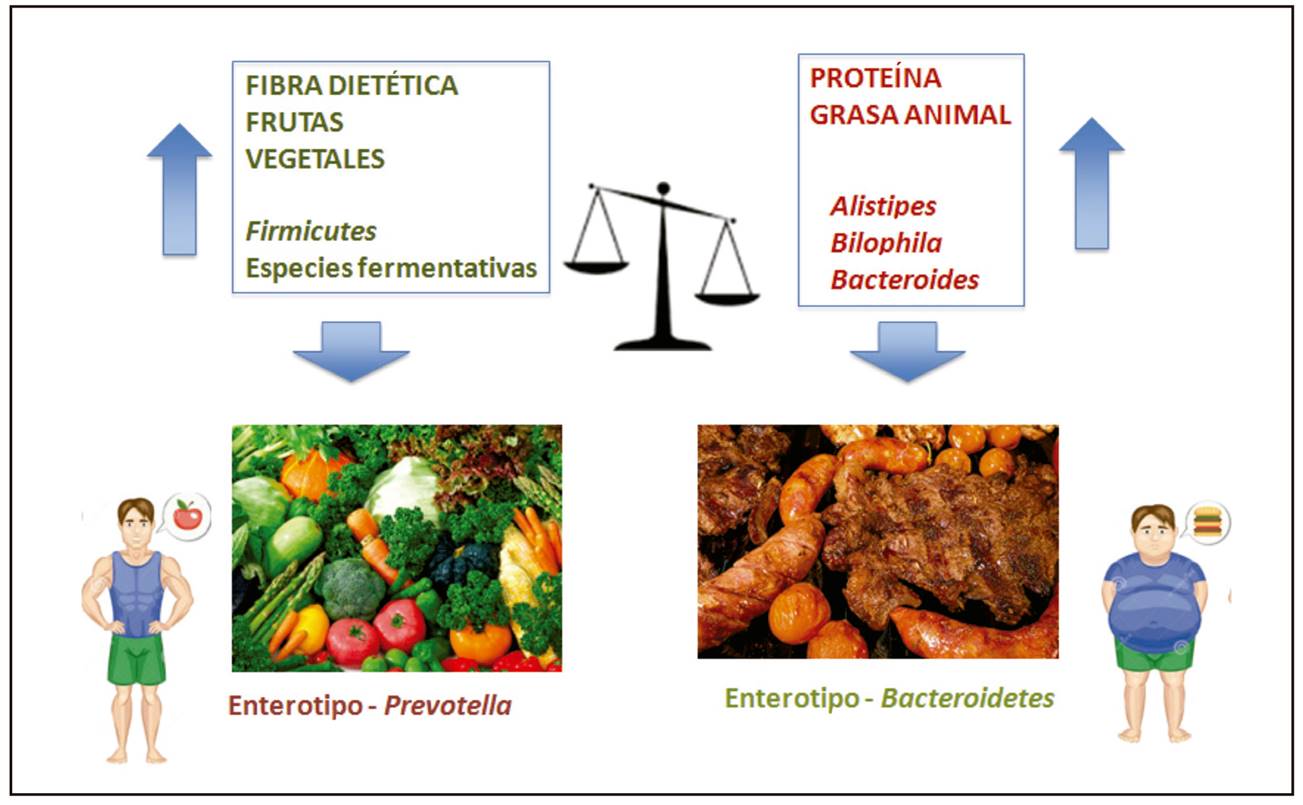
Figura 2 La relación inversa de los enterotipos Prevotella y Bacteroides debido a la dieta puede conducirnos a ser más propensos a padecer enfermedades cardiovasculares.
En personas de edad avanzada, se observan diferencias importantes entre las personas mayores residentes en la comunidad frente a las que viven de modo permanente en residencias de la tercera edad. Al analizar con detalle las dietas habituales en los distintos entornos, se detectó que los que viven de manera independiente en sus domicilios suelen consumir dietas altas en frutas, verduras y fibra y bajas en grasas. Por el contrario, los ancianos de las residencias consumen más grasas y menos fibra, por lo que tienen más cantidad de bacterias potencialmente perjudiciales (proteobacterias y clostridios) y menor de las beneficiosas (lactobacilos y bifidobacterias) 9. Estos datos se relacionaron con unos parámetros analíticos indicadores de mayor susceptibilidad a padecer enfermedad cardiovascular en estos últimos 10.
Un caso especial son las dietas de adelgazamiento, altas en proteínas y bajas en hidratos de carbono, puestas de moda en los últimos años y que siguen muchas personas sin control médico, lo que puede tener efectos indeseables sobre la microbiota, sobre todo si son prolongadas. La fibra dietética tiene efectos antioxidantes protectores sobre el intestino y es precursora de compuestos como el ácido butírico, mientras que el exceso de proteínas puede generar metabolitos asociados al cáncer. El ayuno prolongado o cambios en las rutinas de nuestras comidas (horarios, viajes transoceánicos, etc.) también afectan a nuestra microbiota y, consecuentemente, a nuestra salud 11.
La dieta puede alterar el metabolismo funcional del microbioma intestinal. Muchos ingredientes de los alimentos no son absorbidos por el organismo, sino que son sustratos para la actividad metabólica de la microbiota intestinal, que luego puede producir otras moléculas útiles para el hospedador. Por ejemplo, los hidratos de carbono no digeribles en la dieta son fermentados por la microbiota intestinal para producir ácidos grasos de cadena corta, con un número de funciones beneficiosas para el individuo 12.
ENFERMEDADES ASOCIADAS A LA DIETA
Se han relacionado los hábitos dietéticos y, sobre todo, la disminución del consumo de fibra dietética con determinados patrones de la composición de la microbiota. La pérdida progresiva de la diversidad microbiana durante generaciones en las sociedades industrializadas se ha asociado con el aumento emergente de enfermedades crónicas no transmisibles. La dieta tiene fuertes implicaciones en el desarrollo de enfermedades como la obesidad, el síndrome metabólico, la desnutrición, los trastornos alimenticios, la enfermedad inflamatoria intestinal y el cáncer colorrectal, entre otras. Por ese motivo, es necesario realizar estudios con el fin de identificar biomarcadores pronósticos relacionados con la microbiota para estos trastornos 13. A su vez, dietas saludables e intervenciones nutricionales específicas, incluyendo el aumento de la fibra dietética y el consumo de probióticos y prebióticos, podrían ser valiosas para la restauración de una microbiota con mayor diversidad y con capacidad para prevenir estas enfermedades. Sirvan como ejemplos, por un lado, un reciente metaanálisis que muestra que la administración de determinadas cepas probióticas reduce significativamente el peso corporal, el índice de masa corporal y el porcentaje de grasa en personas obesas 14, y, por otro, una propuesta de intervención dietética como modelo de la llamada "nueva medicina" y "nutrición de precisión" 15.
Como conclusión, hoy contamos con muchos datos científicos que refuerzan la importancia de la dieta para el establecimiento, la composición, la estructura y la actividad funcional de la microbiota intestinal humana. Los estudios que identifican asociaciones entre microbiota y salud en los seres humanos proporcionan pruebas que señalan el papel de la dieta en la patogenia de determinadas enfermedades a través de sus efectos sobre las comunidades microbianas del intestino. La modulación de esta microbiota disbiótica con la dieta o el empleo de probióticos y prebióticos seguramente nos ayude a prevenir enfermedades como la obesidad, el síndrome metabólico o el cáncer y, en general, muchos procesos inflamatorios.
Resumiendo, aunque hoy coincidamos con la frase escrita en 1850 por el antropólogo alemán Ludwig Feuerbach en su obra Enseñanza de la alimentación, "somos lo que comemos", más de un siglo y medio después los avances científicos nos hacen afirmar que también "somos las bacterias que nos colonizan".














